- 2021-05-14 发布 |
- 37.5 KB |
- 14页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
厦门双十中学高考模拟考试
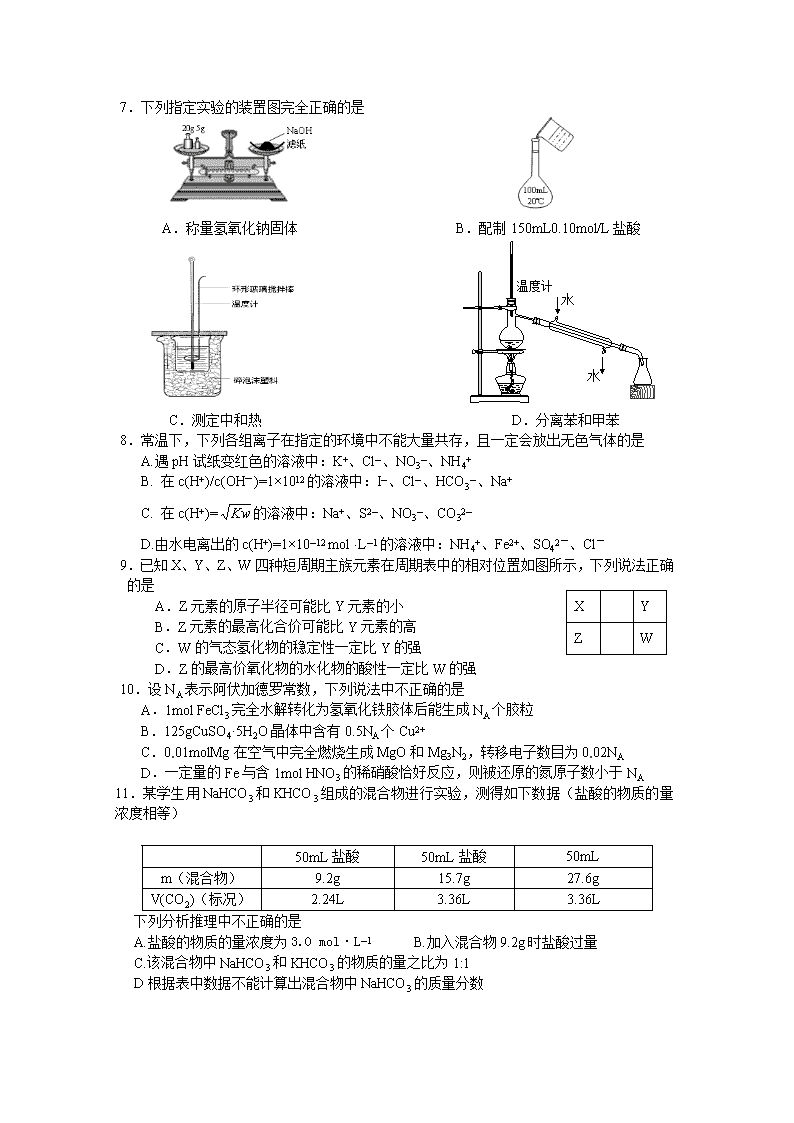
2008年厦门双十中学高考模拟考试 理科综合能力测试1 厦门市双十中学 李仁麒(物理) 王后已(化学) 林荣坤(生物) 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。共300分,考试时间150分钟。 第Ⅰ卷 (选择题 共21小题 每小题6分,共126分) 一、选择题(本题共13小题。在每小题给出的四个选项中,只有一项是符合题目要求的) 1.某动物的基因型AaBb,两对基因位于一对同源染色体上,位置关系如下图所示,正常情况下,由它的一个精原细胞形成的任意两个精子,不可能的基因组合是 A.aB和Ab B.AB和AB C.Ab和Ab D.Ab和ab 叶面积指数 强度 P 光合作用 呼吸作用 2. 一株自然条件下生长的成年果树,总叶面积(叶面积指数)与呼吸作用和光合作用强度的变化关系如图曲线所示。若使P点右移可达到增产目的,据图,使P点右移的最简便、有效的方法是 A.合理施肥,增加叶的光合面积。 B.降低温度,减少呼吸消耗。 C.增加光照强度,提高光能利用率。 D.修剪枝叶,降低叶面积指数。 3.我国的池塘养鱼历史悠久,其中,青、草、鲢、鳙为我国的四大家鱼,而我国将四大家鱼混合放养能充分利用鱼塘资源,被世界列为生态养鱼的典范。之所以能将四大家鱼混合放养,是因为 A.群落中的生物具有水平结构 B.四大家鱼的食性不同,分布在不同的水层 C.四大家鱼之间为共生关系 D.养鱼的种类越多,产量越高 4.下列有关基因工程的叙述,错误的是( ) A.目的基因与运载体结合的过程发生在细胞外 B.目的基因导入受体细胞不进行碱基互补配对 C.DNA连接酶的作用是将两个黏性末端的碱基连接起来 D.基因工程能定向改变生物的性状 5.下列关于人体在寒冷环境中体温调节的叙述中,不正确的是 ( ) A.寒冷时人体可通过骨骼肌不自主的颤抖来增加产热 B.受寒冷刺激,皮肤毛细血管收缩,这是一个非条件反射 C.寒冷环境中,人体代谢增强,产热增多与多种激素的分泌增多有关 D.寒冷环境中正常人的产热速率大于20℃时产热速率,散热速率则小于20℃时散热速率 6.生活中碰到的某些问题常涉及到化学知识,下列叙述中错误的是 A.凡含有食品添加剂的食物对人体健康均有害,不宜食用 B.废弃的塑料,金属、纸制品及玻璃都是可回收再利用的资源 C.大气污染物SO2、CO和NO2主要来源于煤的燃烧和汽车排放的尾气 D.变质的油脂有难闻的特殊气味,是由于油脂发生了化学变化 7.下列指定实验的装置图完全正确的是 A.称量氢氧化钠固体 B.配制150mL0.10mol/L盐酸 温度计 水 水 C.测定中和热 D.分离苯和甲苯 8.常温下,下列各组离子在指定的环境中不能大量共存,且一定会放出无色气体的是 A.遇pH试纸变红色的溶液中:K+、Cl─、NO3─、NH4+ B. 在c(H+)/c(OH-)=1×1012的溶液中:I─、Cl─、HCO3─、Na+ C. 在c(H+)=的溶液中:Na+、S2─、NO3─、CO32─ D.由水电离出的c(H+)=1×10─12 mol·L─1的溶液中:NH4+、Fe2+、SO42-、Cl- 9.X Y Z W 已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是 A.Z元素的原子半径可能比Y元素的小 B.Z元素的最高化合价可能比Y元素的高 C.W的气态氢化物的稳定性一定比Y的强 D.Z的最高价氧化物的水化物的酸性一定比W的强 10.设NA表示阿伏加德罗常数,下列说法中不正确的是 A.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 B.125gCuSO4·5H2O晶体中含有0.5NA个Cu2+ C.0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA D.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA 11.某学生用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等) 50mL盐酸 50mL盐酸 50mL m(混合物) 9.2g 15.7g 27.6g V(CO2)(标况) 2.24L 3.36L 3.36L 下列分析推理中不正确的是 A.盐酸的物质的量浓度为3.0 mol·L─1 B.加入混合物9.2g时盐酸过量 C.该混合物中NaHCO3和KHCO3的物质的量之比为1:1 D根据表中数据不能计算出混合物中NaHCO3的质量分数 放电 充电 12.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。 下列叙述不正确的是 A.放电时锌做负极 B.放电时每转移3mol电子,有2mol FeO42─被还原C.充电时溶液的碱性减弱 D.充电时氢氧化铁被氧化 13.环扁桃醋具有松弛血管平滑肌,扩张血管的功能,其结构简式如下图。下列对该物质叙述中,正确的是 A.该物质属于芳香烃 B.分子式为C17H23O3 C.该有机物难溶于水 D.1 mol 该物质最多可与2 molNaOH发生反应 二、选择题(本题包括8小题,每小题给出的四个选项中,有的小题只有一个选项正确,有的小题有多个选项正确,全部选对的得6分,选不全的得3分,有选错或不选的得0分) 14.下列说法正确的是 ( ) A.研制核武器的钚239由铀239经过4次衰变而产生 B.发现中子的核反应方程是 C.20g的经过两个半衰期后其质量变为15g D.在中子轰击下,生成和的核反应前后,原子核的核子总数减少 15.用a、b两束单色光分别照射到同一双缝干涉装置上,在距双缝恒定距离的屏上得到如图所示的干涉图样,其中图(a)是a光照射时形成的图样,图(b)是b光照射时形成的图样,则关于a、b两束单色光,下列说法正确的是( ) A.若a光照在某金属上恰好能发生光电 效应,则b光照在该金属上不能发生 光电效应 B.在水中a光传播的速度较大 C.在相同的环境下,b光更容易发生全反射 (a) (b) D.若a光是氢原子的核外电子从第三轨道向第 二轨道跃迁时产生的,则b光可能是氢原子 的核外电子从第四轨道向第二轨道跃迁时产生的 16.如图所示,甲分子固定在坐标原点O,乙分子沿x轴运动,两分子间的分子势能Ep与两分子间距离的变化关系如图中曲线所示.图中分子势能的最小值为-E0.若两分子所具有的总能量为0,则下列说法中正确的是 ( ) A.乙分子在P点(x=x2)时,加速度最大 B.乙分子在P点(x=x2)时,其动能为E0 C.乙分子在Q点(x=x1)时,处于平衡状态 D.乙分子的运动范围为x≥x1 0 x/m y/cm 10 5 20 40 60 80 b a c Q P 17..一列简谐横波沿x轴正方向传播,t时刻波形图如图中的实线所示,此时波刚好传到P点,t+0.6s时刻的波形如图中的虚线所示,a、b、c、P、Q是介质中的质点,则以下说法正确的是( ) A.这列波的波速可能为150m/s B.质点a在这段时间内通过的路程一定小于30cm C.质点c在这段时间内通过的路程可能为60cm D.如果T=0.8s,则当t+0.5s时刻,质点b、P的位移相同 P Q 18.2007年10月24日,我国第一颗探月卫星“嫦娥一号”成功发射,标志着我国航天事业取得巨大成就.卫星发射后,假设地—月转移轨道阶段可以简化为:绕地球做匀速圆周运动的卫星,在适当的位置P点火,进入Q点后被月球俘获绕月球做匀速圆周运动,已知月球表面重力加速度为g,月球半径为R,“嫦娥一号”绕月球做匀速圆周运动的轨道半径为r,从发射“嫦娥一号”到在绕月轨道上正常运行,其示意图如图所示,则下列说法正确的是( ) A.在P点启动火箭向运动方向喷气 B.在Q点启动火箭向运动方向喷气 C.“嫦娥一号”在绕月轨道上运行的速率为 D.“嫦娥一号”在绕月轨道上运行的速率为 O E P1 P2 19.竖直平面内,一带正电的小球,系于长为L的 不可伸长的轻线一端,线的另一端固定为O点,它 们处在匀强电场中,电场的方向水平向右,场强的 大小为E. 已知电场对小球的作用力的大小等于小 球的重力. 现先把小球拉到图中的P1处,使轻线 伸直,并与场强方向平行,然后由静止释放小球. 已知小球在经过最低点的瞬间,因受线的拉力作用, 其速度的竖直速度突变为零,水平分量没有变化,则 小球到达与P1点等高的P2时线上张力T为多少?( ) A.mg B.2mg C.3mg D.4mg 20.氧化锡传感器主要用于汽车尾气中 一氧化碳浓度的检测。它的电阻随 一氧化碳浓度的变化而变化,在右 图所示的电路中,不同的一氧化碳 浓度对应着传感器的不同电阻,这 样,显示仪表的指针就与一氧化碳 浓度有了对应关系,观察仪表指针 就能判断一氧化碳浓度是否超标。 有一种氧化锡传感器,其技术资料中给出的是电导(即电阻的倒数)——浓度曲线如图所示,请判断,电压表示数与一氧化碳浓度C之间的对应关系正确的是 ( ) 21. 为监测某化工厂的污水排放量,技术人员在该厂的排污管末端安装了如图所示的流量计.该装置由绝缘材料制成,长、宽、高分别为a、b、c,左右两端开口.在垂直于上下底面方向加磁感应强度大小为B的匀强磁场,在前后两个内侧面分别固定有金属板作为电极.污水充满管口从左向右流经该装置时,理想电压表将显示两个电极间的电压U.若用Q表示污水流量(单位时间内排出的污水体积),下列说法中正确的是 A、前表面电极比后表面电极电势高 B、后表面电极比前表面电极电势高 C、电压表的示数U与污水中离子浓度成正比 D、污水流量Q与电压表的示数U成正比,与a、b无关 第Ⅱ卷 (非选择题 共10题,共174分) 22.(18分) (1)现行高中物理教材的学生实验中,提供了重锤线的是( ) A、研究平抛物体的运动 B、验证机械能守恒定律 C、验证动量守恒定律 D、用单摆测定重力加速度 (2)测量一螺线管两接线柱之间金属丝的长度。 器材:A、待测螺线管L(符号):绕制螺线管金属丝的电阻率m,电阻 约为 B、螺旋测微器 C、电流表G:量程100μA,内阻=500Ω D、电压表V:量程6V,内阻=4kΩ E、定值电阻R0:R0=50Ω F、滑动变阻器:全电阻约1k G、电源E:电动势9V,内阻忽略不计 H、电键S一个,导线若干 ①实验中用螺旋测微器测得金属丝的直径如图甲所示,其示数为d= __________ ②按图乙所示电路测量金属丝的电阻,请在图丙的实物图上连线。 图乙 图丙 ③若测得的金属丝直径用d表示,电流表G的读数用I表示,电压表V的读数用U表示,则由已知量和测得量的符号表示金属丝的长度l= _____________ h v x M O′ O 第23题 23.(18分)如图所示,M是水平放置的圆盘,绕过其圆心的竖直轴匀速转动,以经过O水平向右的方向作为x轴的正方向。在圆心O正上方距盘面高为h处有一个正在间断滴水的容器,在t=0时刻开始随长传送带沿与x轴平行的方向做匀速直线运动,速度大小为v。已知容器在t=0时滴下第一滴水,以后每当前一滴水刚好落到盘面上时再滴一滴水。问: 1)每一滴水经多长时间滴落到盘面上? 2)要使盘面上只留下3个水滴,圆盘半径R应满足什么条件? 3)若圆盘半径R足够大,第二滴水和第三滴水在圆盘上可能相距的最远距离为多少?此时圆盘转动的角速度至少为多少? 24.(16分)矩形裸导线框长边的长度为2l,短边的长度为l,在两个短边上均接有阻值为R的电阻,其余部分电阻均不计.导线框的位置如图所示,线框内的磁场方向及分布情况如图,大小为.一电阻为R的光滑导体棒AB与短边平行且与长边始终接触良好.起初导体棒处于x=0处,从t=0时刻起,导体棒AB在沿x方向的外力F的作用下做速度为v的匀速运动.试求: (1)导体棒AB从x=0运动到x=2l的过程中外力F随时间t变化的规律; (2)导体棒AB从x=0运动到x=2l的过程中整个回路产生的热量. F A B O x y R R 2l v 25.(20分)如图所示,A为位于一定高度处的质量为m、带电荷量为+q的小球,B为位于水平地面上的质量为M的用特殊材料制成的长方形空心盒子,且M=2m,盒子与地面间的动摩擦因数=0.2,盒内存在着竖直向上的匀强电场,场强大小E=,盒外没有电场.盒子的上表面开有一系列略大于小球的小孔,孔间距满足一定的关系,使得小球进出盒子的过程中始终不与盒子接触.当小球A以1m/s的速度从孔1进入盒子的瞬间,盒子B恰以v1=6 m/s的速度向右滑行.已知盒子通过电场对小球施加的作用力与小球通过电场对盒子施加的作用力大小相等方向相反.设盒子足够长,取重力加速度g=10m/s2,小球恰能顺次从各个小孔进出盒子.试求: (1)小球A从第一次进入盒子到第二次进入盒子所经历的时间; (2)盒子上至少要开多少个小孔,才能保证小球始终不与盒子接触; (3)从小球第一次进入盒子至盒子停止运动的过程中,盒子通过的总路程. 1 2 3 n A B 26.(15分)氯及其化合物是中学化学中的重要研究对象。 (1)写出实验室中制取氯气的离子方程式 ; (2)某一反应体系存在以下五种物质:KC1O3 、KCl 、H2O、Cl2、浓盐酸。试用这五种物质组成一个合理的反应方程式,配平并标出电子转移的方向和数目: ; 若制取标准状况下的6.72L氯气,该反应中电子转移的物质的量为 ; (3)某同学用排空气法收集一瓶氯气,进行氯气与铁反应的实验:取一根细铁丝 ,然后立即伸入充满氯气的集气瓶中,观察到的现象是 。为观察生成的氯化铁溶液的颜色,向反应后的集气瓶中加入少量的蒸馏水,振荡,实际观察到的现象是 ,产生这种现象的原因是 ;为真正观察到氯化铁溶液的颜色,应向反应后的集气瓶中改加(填试剂名称) 。 27.(15分)如图,A为直流电源,B为电解槽,c、d为石墨电极,B中存放有100 mL NaCl和CuCl2的混合溶液,其中Cu2+的物质的量浓度为0.1 mol·L─1,闭合K,d极收集到标准状况下448 mL一种气体甲,该气体能使湿润的碘化钾淀粉试纸变蓝。气体体积均在标准状况下测定,假设溶液的体积变化忽略不计,不考虑电解产生的气体溶解和吸收。请回答下列问题。 (1)A电源的a极是 极,d极发生反应的电极反应式 是 。 (2)c极理论上收集到的气体的体积是 (标准状况下)。 (3)假设100 mL溶液中,c(Cu2+)= a mol·L─1,c(Na+)=b mol·L─1, Cu2+完全放电后,理论上d极产生甲气体的体积V范围是 (用带a、b的代数式表示)。 (4)若利用此装置在铁上镀铜,则d极材料为 ,应选用的电解质溶液是 , C极的电极反应式为 。当电路中通过0.04mol电子时,析出金属的质量为 。 28.(16分) 已知: (1) (2)△ △ (3) R—OH+HBr R—Br+H2O 苯酚是一种重要的化工原料,以下是利用苯酚为原料,生产阿司匹林、香料和高分子化合物的合成线路图。 (1)反应②属于 反应。 (2)写出下列有机物的结构简式:D ,G 。(3)完成下列反应的化学方程式:① ;② 。 (4)可以检验阿司匹林样品中含有水杨酸的试剂是 (填写字母)。 A.碳酸氢钠溶液 B.氯化铁溶液 C.红色石蕊试纸 D.新制氢氧化铜 (5)与阿司匹林互为同分异构体的物质有多种,请按以下要求写出阿司匹林的一种同分异 构体:①苯环上有两个对位的取代基;②能发生银镜反应;③属于羧酸和酯类的有机物 有 。 29.(14分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。 (1)写出Y2O2的电子式 ;其中含有的化学键是 (2)X、Z、W三种元素的最高氧化物对应的水化物酸性最强的是(填写化学式): ; (3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是(填写化学式); ; (4)与Z上下相邻的同主族元素M、N,原子电子层数M>Z>N,三种元素氢化物沸点由大到小的顺序是(填写化学式) > > (5)元素Y的单质在一定条件下,能与氢气化合生成一种固态氢化物YH,熔点为800℃。 ①YH晶体类型是 ②YH能与水反应放氢气,写出化学方程式 ③若将1molYH和1molAl混合加入足量水中,放出气体的体积是(标准状况下) L。 30.(22分)回答下列Ⅰ、Ⅱ小题: Ⅰ. (15分)人类的血型有多种类型,发现最早、应用最普遍的是ABO血型系统,该系统将人类的血型分为四类:A型、B型、AB型、O型,不同血型的人红细胞、血清中所含有的蛋白质见下表: A B AB O 红细胞 A凝集原 B凝集原 A、B凝集原 无 血清 抗B凝集素 抗A凝集素 无 抗A、抗B凝集素 控制血型的基因有:IA、IB、i,A型血基因型:IA IA、IAi ;B型血的基因型:IBIB、IBi;AB型血基因型:IAIB;O型血基因型:i i。根据以上信息及所学知识回答下列问题: (1)古人有“滴血认亲”的说法,即将两人的血各取一滴混在一起,如果不发生凝集反应,则为亲子关系,如果发生凝集反应,则不是亲子关系。你认为这种做法可靠吗?请举例说明 。 (2)有人说O型血的人为万能的献血者,请你根据上述的信息提出你自己的看法: 。凝集素的化学本质是 。 (3)现有A标准血清、B标准血清、载玻片、消毒酒精、取血针、牙签、棉签、显微镜等用具,请你设计一个实验为初一的学生鉴定血型。 实验原理: 。 实验步骤: 第一步: 。 第二步: 。 第三步: 。 预测实验结果: 1 2 3 4 A标准血清 B标准血清 结果 Ⅱ.(7分)激素分子周游全身,与各种细胞接触,在体液调节中,激素的调节作用最为重要。根据人体内某激素作用机理的图解(如下图)回答下列问题。 (1)若图中的①代表雄性激素,则它进入细胞的方式 是 。 (2)图中①和②组成的复合物可以作用于[ ] ,通过[ ] 和[ ] 合成特异蛋白,从而影响生命活动。 (3)若①表示肾上腺素分子,有人估计一个肾上腺素分子可以使肝细胞释放大约1010个葡萄糖分子,这说明激素与酶的相似特性是具有 。 (4)若要大量生产物质①,如胰岛素等,那么会涉及的主要生物工程技术是 ,物质①属于微生物 代谢产物。 31.(20分)一批经多代种植果实均为红色的柿子椒种子被带上太空,将遨游过太空的柿子椒种子种植后,第一年收获的柿子椒均为红色,用收获的种子再种,第二年发现有数株所结柿子椒均为黄色。 (1) ①根据已知,你认为柿子椒果色是细胞质遗传吗? 。请简要说明。 ②能否确定柿子椒果色的显隐性? 请简要说明推断过程(设控制果色的基因为A,a)。 (2)欲快速获得大量黄色柿子椒,最简便方法是 。 (3)由于太空试管植物种苗细胞十分珍贵有限,所以在科学研究之前需要诱导 ,以求获得更多的细胞团。之后,科研人员将调整培养基,使部分细胞团经 ,培养成新植株。 2008年厦门双十中学高考模拟考试 理科综合能力测试1参考答案及评分标准 生物部分 1.C 2.D 3.B 4.C 5.D 30.(22分) Ⅰ. (15分)(1)不可靠,例如AB型(IAIB)与O型(i i)的人婚配,后代的血型为A型或B型,与父母的血型都不相同,亲子之间也要发生凝集反应。(其他合理答案也可) (2)不对,因为O型献血者血清中的抗A、抗B凝集素要与A、B或AB血型的受血者的红细胞上的A、B凝集原发生凝集反应 球蛋白 (3)实验原理:B标准血清中的抗A凝集素要与A凝集原发生凝集反应,A标准血清中的抗B凝集素要与B凝集原发生凝集反应,从而根据凝集反应情况,判断出被检验者的红细胞上的凝集原而确定其血型。 实验步骤: 第一步:取两块载玻片,分别编号为A、B,在A装片上滴A标准血清、在B装片上滴B标准血清。 第二步:用棉签蘸取消毒酒精给被检测的学生手指消毒,用取血针刺破消毒手指的皮肤,再用牙签蘸取少量血液分别在A、B装片的血清中涂抹。 第三步:几分钟后,将A、B装片分别放在显微镜下观察 预测实验结果: 1 2 3 4 A装片 凝集 凝集 不凝集 不凝集 B装片 凝集 不凝集 凝集 不凝集 结果 AB型 B型 A型 O型 Ⅱ.(7分)(1)自由扩散 (2)[③]细胞核内的遗传物质(DNA) [④]转录 [⑤]翻译 (3)高效性 (4)基因工程、发酵工程 次级 31.(20分) (1) ①不是(1分)因为红果母本生出黄果后代(或不符合母系遗传的特点)(2分) ②能 (1分) 设红色对黄色为显性,则遨游太空的柿子椒(胚)基因型为AA(红色)。(2分) 若发生基因突变,可能结果是Aa或aa,(1分)其中aa种子种植在第一年不可能收获红色椒,所以突变结果只能是Aa。(1分)播种上述Aa种子,第一年收获的柿子椒,果色表现为红,胚基因型有的为aa,次年种植,aa种子长成的植株均结黄色果实。符合题意。(1分) 设红色对黄色为隐性,则遨游太空的柿子椒(胚)基因型为aa (红色)。(2分) 若发生基因突变,可能结果是Aa或AA,(1分)不论是AA还是Aa的突变株,在第一年都不可能收获红色椒,(1分)这不符合题意。 综上所述,红色对黄色为显性(1分)。 (2)自交(2分) (3) 细胞分裂(2分) 细胞分化(2分) 化学部分 6.A 7.C 8.B 9.B 10.A 11.D 12.B 13.C 26. (1)MnO2+4H++2C1- Mn2++C12↑+2H2O(2分) (2)KC1O3+6HC1(浓) KC1+3C12↑+3H2O (2分)电子转移方向从盐酸中氯元素转移至KC1O3中氯元素,数目为5mol;(2分)0.5mol(1分) (3)用砂纸将铁丝擦至光亮,用坩锅钳夹住,在酒精灯上烧至红热(2分);铁丝保持红热,产生棕褐色的烟(2分);产生红褐色的沉淀(1分)氯化铁发生水解,生成氢氧化铁沉淀(2分);稀盐酸溶液(1分) 27. (1)负极,2Cl--2e-=Cl2↑ (2)224 mL (3)2.24aL≤V≤(2.24a+1.12b)L (4)铜, 硫酸铜,Cu2+ + 2e- = Cu ;12.8g。 28.(1)取代 (2) (3)① ② (4)B (5) 29.(1)Na+[]2+Na2+;离子键、非极性键(每空1分,共2分) (2)HClO4(2分) (3)NH3(2分) (4)H2O>H2Se>H2S(2分) (5)①离子晶体(2分) ②NaH+H2O=NaOH+H2↑(2分) ③56(2分) 物理部分 14. B 15. BCD 16. BD 17 .BD 18. BD 19. C 20. B 21. BD 22.(1)AC (6分) (2)①0.384~0.386mm (4分) ②如图所示 (4分) ③ (4分) 23.解:1)……3分 2)第3滴水离开圆心,第4滴水离开圆心 ……4分 3)当第2滴与第3滴落在同一直线上,且在圆心两侧时,相距最远……2分 ……3分 两滴水落在盘面上的时间差t与圆盘周期T满足 (n=0,1,2,3……)……3分 当n=0时,……3分 24.(1)在t时刻AB棒的坐标为 2分 感应电动势 2分 回路总电阻 1分 回路感应电流 2分 棒匀速运动时有F=F安=Bil 解得: 2分 (2)导体棒AB在切割磁感线的过程中产生半个周期的正弦交流电 感应电动势的有效值为 2分 回路产生的电热 2分 通电时间 1分 联立解得 2分 25.(1)A在盒子内运动时, 由以上两式得 a=g 3分 A在盒子内运动的时间 A在盒子外运动的时间 A从第一次进入盒子到第二次进入盒子的时间 3分 (2)小球在盒子内运动时,盒子的加速度 小球在盒子外运动时,盒子的加速度 小球运动一个周期盒子减少的速度为 3分 从小球第一次进入盒子到盒子停下,小球运动的周期数为 故要保证小球始终不与盒子相碰,盒子上的小孔数至少为2n+1个,即11个. 4分 (3)小球第一次在盒内运动的过程中,盒子前进的距离为 小球第一次从盒子出来时,盒子的速度 小球第一次在盒外运动的过程中,盒子前进的距离为 小球第二次进入盒子时,盒子的速度 小球第二次在盒子内运动的过程中,盒子前进的距离为 小球第二次从盒子出来时,盒子的速度 小球第二次在盒外运动的过程中,盒子前进的距离为 4分 ………… 分析上述各组数据可知,盒子在每个周期内通过的距离为一等差数列,公差d=0.12m.且当盒子停下时,小球恰要进入盒内,最后0.2s内盒子通过的路程为0.04m. 所以从小球第一次进入盒子至盒子停止运动的过程中,盒子通过的总路程为 3分查看更多