- 2021-08-06 发布 |
- 37.5 KB |
- 12页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
江苏省泰州市2019-2020学年高二下学期期末考试化学(选修)试题 Word版含答案
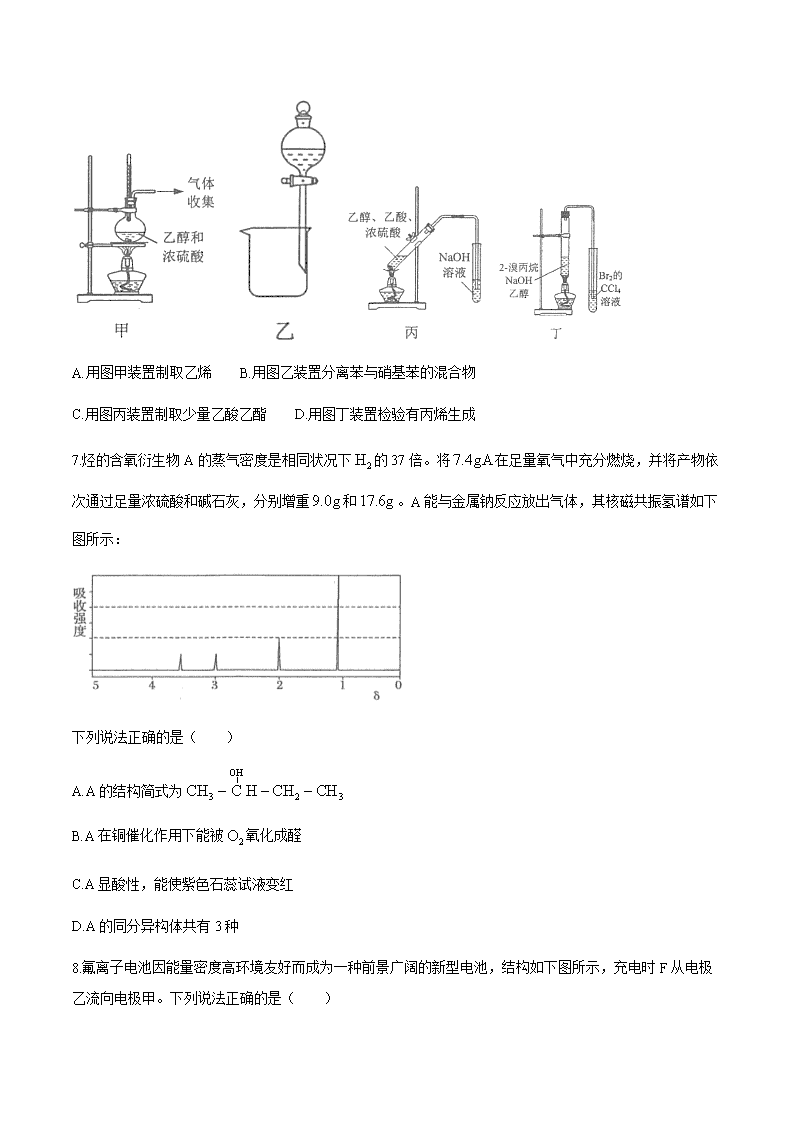
2019~2020学年度第二学期期末考试 高二化学(选修)试题 (考试时间:90分钟;总分:100分) 命题人: 审题人: 注意事项: 1.本试卷共分两部分,Ⅰ卷为选择题,Ⅱ卷为非选择题。 2.所有试题的答案均填写在答题纸上,答案写在试卷上的无效。 可能用到的相对原子质量:H—1 C—12 N—14 O—16 F—19 Mg—24 N—59 Ⅰ卷(选择题 40分) 单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。 1.标准医用口罩的中间过滤层一般使用聚丙烯纤维制成的熔喷布。下列说法正确的是( ) A.废弃口罩直接丢弃,不会造成环境污染 B.聚丙烯能使溴水和高锰酸钾酸性溶液褪色 C.等质量的丙烯和聚丙烯完全燃烧,消耗的量相等 D.聚丙烯纤维和光导纤维都属于有机高分子化合物 2.用化学用语表示反应中的相关微粒,其中正确的是( ) A.中子数为8的C原子: B.的电子式: C.乙烯的结构式: D.的原子结构示意图: 3.室温下,下列各组微粒在指定溶液中能大量共存的是( ) A.的溶液:、、、 B.溶液:、、、 C.加甲基橙变红的溶液:、、、 D.溶液:、、、 4.下列有关化学反应的叙述正确的是( ) A.油脂在酸性条件下水解生成甘油 B.与溴水反应得到 C.蛋白质在饱和溶液中发生变性 D.电解溶液得到金属 5.下列有机物的系统命名正确的是( ) A.:3,二甲基丁烷 B.:甲基,己二烯 C.:1,二甲苯 D.:环己酚 6.下列装置进行相应的实验,能达到实验目的的是( ) A.用图甲装置制取乙烯 B.用图乙装置分离苯与硝基苯的混合物 C.用图丙装置制取少量乙酸乙酯 D.用图丁装置检验有丙烯生成 7.烃的含氧衍生物A的蒸气密度是相同状况下的37倍。将在足量氧气中充分燃烧,并将产物依次通过足量浓硫酸和碱石灰,分别增重和。A能与金属钠反应放出气体,其核磁共振氢谱如下图所示: 下列说法正确的是( ) A.A的结构简式为 B.A在铜催化作用下能被氧化成醛 C.A显酸性,能使紫色石蕊试液变红 D.A的同分异构体共有3种 8.氟离子电池因能量密度高环境友好而成为一种前景广阔的新型电池,结构如下图所示,充电时F从电极乙流向电极甲。下列说法正确的是( ) A.放电时,电极乙为正极,发生还原反应 B.放电时,电极甲发生反应: C.充电时,电极甲与外加电源的正极相连 D.充电时,导线上每通过,乙电极质量减少 9.下列判断正确的是( ) A.图甲表示晶体的晶胞,晶胞中“○”代表 B.图乙表示晶体的晶胞,每个原子周围距离最近的原子有12个 C.图丙表示常温下,将等体积一定浓度的盐酸和醋酸分别加水稀释,溶液的导电能力随溶液体积变化的曲线 D.图丁表示其他条件不变时,只改变的起始浓度,反应的平衡体系中随交化的关系曲线 10.某科研组提出与在羟基磷灰石()表面催化氧化生成和的历程,该历程示意图如下(图中只画出了分结构)。 下列说法正确的是( ) A.产物分子中的氧原子全部来自 B.在反应过程中有碳氧之间的键发生断裂 C.和互为同系物 D.能降低与反应所需的活化能 不定项选择题:本题包括5小题,每小题4分,共计20分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。 11.下列说法正确的是( ) A.电解精炼铜时,粗铜作阴极 B.反应能自发进行,该反应的 C.氢氧燃料电池正极消耗气体时,电路中通过的电子数为 D.常温下,,欲使溶液中,需调节溶液的 2.有机物X的结构简式如右图所示,下列说法正确的是( ) A.X有1个手性碳原子 B.X中所有碳原子可能共平面 C.X可以发生取代、氧化、加成、消去反应 D.最多能与反应 13.根据下列实验操作和现象所得出的结论正确的是( ) 选项 实验操作和现象 结论 A 向苯酚溶液中滴加少量浓溴水,振荡,无白色沉淀 苯酚与浓溴水不反应 B 向肉桂醛()中加酸性溶液,振荡,酸性溶液褪色 醛基能被酸性溶液氧化 C 取少量与溶液共热,冷却后先加足量酸化,再滴加溶液,有淡黄色沉淀生成 已水解 D 向20%麦芽糖溶液中加入少量稀硫酸,加热一段时间后,加入溶液调节至碱性,再加入银氨溶液,水浴加热,出现银镜 麦芽糖的水解产物具有还原性 4.已知:。室温下,几种弱酸的如下表所示: 化学式 4.74 3.74 下列有关微粒浓度的说法正确的是( ) A.浓度均为和溶液中: B.浓度为溶液中: C.室温下,的和的混合溶液中: D.溶液与溶液等体积混合后: 15.向的密闭容器中充入和,发生反应。后,测得不同温度下转化率如下图所示。下列说法正确的是( ) A.400℃时,反应在内的平均速率 B.b点所示条件下延长反应时间,转化率将大于42% C.c、d两点,反应的化学平衡常数相等 D.600℃时达平衡后,保持其他条件不变,再充入和,达新平衡时转化率小于35% Ⅱ卷(非选择题 60分) 16.(10分)有机化合物M是一种重要的化工原料,以A和C合成M的路线如下图所示: 已知:①。 ②M分子中含2个六元环和1个八元环。 (1)A的一氯代物有_______种。 (2)M的结构简式为_______。 (3)D→E的化学方程式为_______。 (4)F与含有的悬浊液反应的化学方程式为_________。 (5)G通过缩聚反应得到高聚物L,L的结构简式为_______。 17.(12分)全氮类物质具有高密度、高生成焓、超高能量及爆轰产物清洁无污染等优点,成为新一代超高能含能材料的典型代表。 Ⅰ.高性能炸药的结构为。 (1)基态原子的核外电子排布式为_______;O基态原子核外电子占据最高能级的电子云轮廓图形状为_______(用文字描述,下同);的空间构型为_______。 (2)写出与互为等电子体的阳离子的化学式_______;中所含各元素第一电离能由大到小的顺序为_______(用元素符号表示)。 Ⅱ.作为新型高能含能材料,在炸药、推进剂和发射药等领域具有较高的应用价值。 (3)为平面结构,结构为,其中,原子的杂化方式是_______。 (4)的晶体结构与相似。的结构分为和,立方晶胞的示意图见图-1。图-2是晶胞正上方的俯视投影图,图中黑球(实心球)表示,请在题图-2中用白球(空心球)表示出的位置_______。 (5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。图-1中,原子1的坐标是,则原子2的坐标为_______。 18.(12分)研究氮氧化物等大气污染物的处理对建设美丽家乡、打造宜居环境具有重要意义。 (1)受热分解后能得到、和另一种气体,该气体为_______(写分子式)。 (2)现有以下反应: 查阅资料获得部分化学键的键能E数据如下表: 化学键 946 436 497 632 已知,则________。 (3)一石灰乳联合处理的方法是先将经氧化,再用石灰乳吸收氮的氧化物,发生的主要化学反应有: , , , ①为保证被充分吸收,至少为_______(填字母)。 A. B. C. D.1 ②其他条件相同时,石灰乳浆液中分别加入等物质的量的不同亚硫酸盐对去除效率的影响如图-1所示。内,对的去除效率明显高于的原因是_______。 ③图-2是环保工业中利用催化反硝化电解法降解水中的示意图,写出阴极的电极反应式_______。 (4)对于反应 ,有学者认为分两步完成,其反应历程如题图-3所示。已知第1步反应(是快反应,会快速建立平衡状态,第2步反应是慢反应。研究发现,在未使用催化剂的条件下,升高温度,总反应速率减慢,其原因可能是_______。 19.(14分)盐酸非那嗪奈是一种用于治疗缺氧性脑卒的新药,其合成路线如下: (1)G中含氧官能团的名称为_______和____________。 (2)E→F的反应类型为________。 (3)若不设计反应①和③,和反应生成D的同时,还会生成副产物X(分子式为),写出X的结构简式_______。 (4)写出同时满足下列条件的C的一种同分异构体的结构简式_______。 ①分子中有两个氨基直接与苯环相连,且能发生银镜反应 ②能发生水解反应,其水解产物之一可与溶液发生显色反应 ③分子中有4种不同化学环境的氢 (5)已知:,写出以和为原料制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)_________。 20.(12分)利用镍渣(含、、、等杂质)制备草酸镍晶体的工艺流程如下: (1)加入发生反应的离子方程式为_______。 (2)加入除去的离子是_______。 (3)下图为在空气中受热的固体残留率曲线和热流曲线(用于表示化学反应导致的热量变化),曲线中375℃以上所得固体为镍的氧化物。的常见化合价为、。() ①C点对应物质的化学式为_______。 ⑨A→B的过程_______(填“吸收”或“放出”)热量。 ③取一定质量的镍的氧化物,用的盐酸恰好完全溶解,生成黄绿色气体(已折算成标准状况),溶液中的全部是价。计算该氧化物中和O的物质的量之比(写出计算过程)。查看更多