- 2021-05-13 发布 |
- 37.5 KB |
- 4页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018中考专题复习之实验探究题
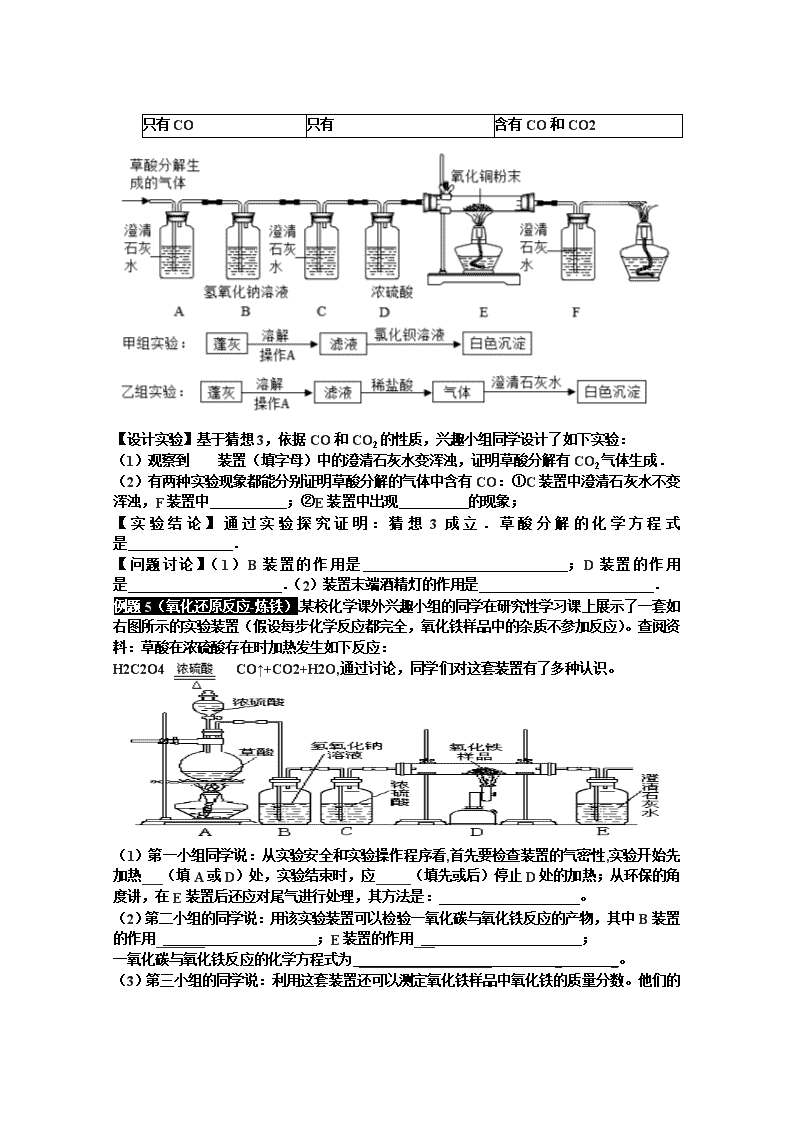
中考考专题复习——实 验 探 究 题 【近几年科学探究热点题型】 (1)氢氧化钠和氢氧化钙变质的探究; (2)有关化学反应及反应后成分的探究; (3)有关金属活动性及金属回收的探究; (4)催化剂对化学反应速率的影响的探究; (5)有关废水、废气(尾气)分析及处理的探究等。 【实验探究的基本环节】 提出问题→猜想与假设→制定计划→进行实验→收集证据→解释与结论→反思与评价→表达与交流。 【化学实验探究题解题注意事项】 (1)提出的猜想要合理,有利于方案的设计;合乎题意,不能信口开河。 (2)设计的实验方案要紧扣提出的猜想,设计方案要简单易行。 (3)结论一定是对假设的判定,反思评价一般是对实验方案、实验操作、 结论等方面的反思,是探究题中最难的地方。 【解题思路】 (1)认真读题:划出关键的语句,审清题意,明确要求; (2)找出题目中与教材相联系的知识点; (3)灵活应用基础知识解决探究题中的问题。 【教学过程】 例1、(金属性质)小新拿来一片黄色的金属向同学们炫耀说他捡 到了黄金。小宝说他曾在网上看到过,有一种铜锌合金外观与黄金相似,常被误认为是黄金。于是他与小新开始探究。 【提出问题】:这块黄色的金属是黄金?还是铜锌合金? 【提出猜想】:①小新认为是黄金 ②小宝认为是铜锌合金 【查阅资料】: 合金中的金属保持各自的化学性质,金在高温下不与氧气反应,铜在高温下与氧气反应生成黑色固体。 【设计实验】: ①小新设计的实验是:截取一小片黄色的金属放在石棉网上用酒精灯加热;②小宝设计的实验是:截取一小片黄色的金属放入硝酸银溶液中。 【现象与结论】①小新在实验中观察到黄色的金属变黑,则他的猜想对吗?黑色物质是_____ ②小宝在实验中能观察到的现象:_______________________________________ 写出反应的化学方程式:______________________________________ 【反思与应用】①假如你的观点和小宝的观点相同,你还可以设计一个实验是:截取一小片黄色的金属放入__________溶液中,你设计的实验中观察到的现象是____________________ 例题2:(氢氧化钠变质) (2017∙铜仁)某校化学兴趣小组的小王和小张两位同学根据已有知识经验。对敞口放置在实验室的NaOH溶液产生了兴趣。分别进行实验探究。 【提出问题】:这瓶NaOH溶液肯定变质了,其变质程度怎样呢? 【猜想与假设】:小王:NaOH溶液部分变质; 小张:NaOH溶液全部变质; 小王、小张认为NaOH溶液一定变质的理由(用化学方程式表示) : _。 【进行实验】 (1)小王设计好方案后,进行了如下实验来验证自己的猜想,请你协助小王完成实验现象的填写: 实验步骤 现象 结论 ①取一定量NaOH溶液样品于试管中,滴加足量BaCl2溶液 有 _产生 NaOH溶液样品部分变质 ②取经过①反应后的滤液,向其中滴加紫色石蕊溶液 溶液变成 _色 (2)小张用小王第①步反应后的滤液,滴加CuCl2溶液,有 _色沉淀产生,证明自己猜想错误。 【反思与评价】 (1)如果NaOH溶液中混有少量Na2CO3杂质,常加入适量 (填物质的化学式)。 (2)小王、小张通过以上探究分析推出,实验室保存Ba(OH)2溶液的方法应该是 。 例题3、中和反应((2017·临沂)某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动,请你和他们仪器完成以下实验探究. 【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,该反应的化学方程式是 . 【查阅资料】CaCl2溶液显中性 【提出问题】实验中未观察到明显显像,部分同学产生了疑问:反应后溶液中溶质的成分是什么? 【猜想与假设】针对疑问,甲组同学猜想如下: 猜想Ⅰ:只有CaCl2 猜想Ⅱ:有 ;猜想Ⅲ:有CaCl2和Ca(OH)2; 猜想Ⅳ:有CaCl2、HCl和Ca(OH)2 乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是 . 【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究. 实验方案 滴加紫色石蕊溶液 通入CO2 滴加Na2CO3溶液 实验操作 实验现象 产生白色沉淀 实验结论 溶液中含有Ca(OH)2 溶液中含有Ca(OH)2 溶液中含有Ca(OH)2 【得出结论】通过探究,全班同学一致确定猜想Ⅲ是正确的. 【评价反思】 (1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因 . (2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑 . 例题4、(气体的干燥与净化)(2016•德州)在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水,某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究:【提出问题】生成物中有哪种碳的氧化物?【猜测】 猜想1 猜想2 猜想3 只有CO 只有 含有CO和CO2 【设计实验】基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如下实验: (1)观察到 装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成. (2)有两种实验现象都能分别证明草酸分解的气体中含有CO:①C装置中澄清石灰水不变浑浊,F装置中 ;②E装置中出现 的现象; 【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是 . 【问题讨论】(1)B装置的作用是 ;D装置的作用是 .(2)装置末端酒精灯的作用是 . 例题5(氧化还原反应-炼铁).某校化学课外兴趣小组的同学在研究性学习课上展示了一套如右图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应)。查阅资料:草酸在浓硫酸存在时加热发生如下反应: H2C2O4 CO↑+CO2+H2O,通过讨论,同学们对这套装置有了多种认识。 (1)第一小组同学说:从实验安全和实验操作程序看,首先要检查装置的气密性,实验开始先加热___(填A或D)处,实验结束时,应_____(填先或后)停止D处的加热;从环保的角度讲,在E装置后还应对尾气进行处理,其方法是: 。 (2)第二小组的同学说:用该实验装置可以检验一氧化碳与氧化铁反应的产物,其中B装置的作用_______ ;E装置的作用___ ; 一氧化碳与氧化铁反应的化学方程式为 ___________________ _ _。 (3)第三小组的同学说:利用这套装置还可以测定氧化铁样品中氧化铁的质量分数。他们的测定方法是:称量氧化铁样品的质量10.0 g,样品与玻璃管的总质量为60.0 g,完全反应并冷却后再称量玻璃管与剩余固体的总质量为57.6 g。计算实验测得氧化铁样品中氧化铁的质量分数为 。 (4)第四小组同学说:利用这套装置还有另外测定样品中氧化铁的质量分数的方法:先称量氧化铁样品的质量,再分别称量E装置在反应前后的总质量,即可计算求得样品中氧化铁的质量分数。但按此方法实际实验测定结果却偏大,分析造成偏大的原因可能是 。 五.金属活动性顺序 例题6.催化剂: . (2017随州)课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。 【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何? 【实验探究】 实验步骤 实验现象 实验结论及解释 Ⅰ. A中无明显现象, B中产生大量能使带火星木条复燃的气体 产生的气体是 ② 红砖粉末能改变过氧化氢分解速率 Ⅱ. 向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag 红砖粉末的 在反应前后均没有发生变化,能作过氧化氢分解的催化剂 Ⅲ. 两试管中均产生气泡 且 红砖粉末的催化效果没有二氧化锰粉末好 【练习】2017长沙中考真题——实验探究 某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想: a.可能是二氧化碳; b.可能是一氧化碳。 并设计如图所示装置进行实验,预期的实验现象 及结论如下: Ⅰ.若澄清的石灰水变浑浊,则气体为二氧化碳; Ⅱ.若澄清的石灰水不变浑浊,则气体为一氧化碳. 请你分析并回答: ⑴该同学的猜想是否严谨?请你说明理由:_________ ;___________ ; ⑵设计一个实验,验证⑴中你的理由。请简述你的实验方案_____________________________________; ⑶该实验装置存在的缺陷是________________________; ⑷反应结束时,停止实验的操作步骤是________________________; ⑸实验后发现试管①内壁上附着不易用试管刷洗净的固体生成物,清洗试管①的方法是_______________________查看更多