- 2021-11-10 发布 |
- 37.5 KB |
- 6页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
九年级化学下册第十一单元盐化肥课题1生活中常见的盐第2课时复分解反应和盐的化学性质课堂练习(附解析新人教版)
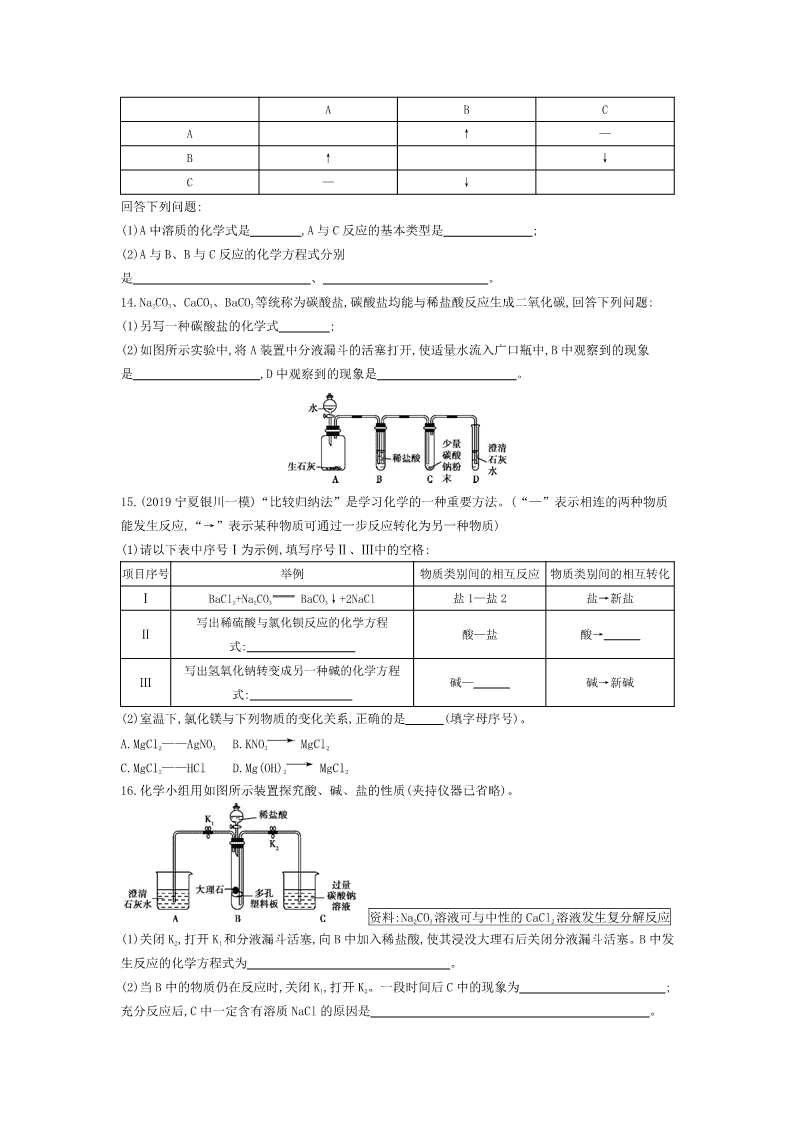
初中化学·人教版·九年级下册——第十一单元 盐 化肥 第 2 课时 复分解反应和盐的化学性质 测试时间:30 分钟 一、选择题 1.(2019 广东广州从化二模)下列各组物质能发生反应,且无明显现象的是( ) A.盐酸与大理石 B.硝酸钠溶液与氢氧化钾溶液 C.氢氧化钠溶液与盐酸 D.氯化钡溶液与稀硫酸 2.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是( ) A.HCl B.KNO3 C.K2CO3 D.FeCl3 3.(2019 河南邓州二模)下列各组物质中,能发生复分解反应且反应后溶液总质量变小的是( ) A.碳酸钠固体和稀硫酸 B.氢氧化钠溶液和盐酸 C.硫酸和氯化钡溶液 D.氯化钾溶液和硫酸钠溶液 4.(2019 江苏徐州月考)酸、碱、盐在溶液中发生复分解反应的条件是有沉淀析出,或有气体放出,或 有水生成。下列各组物质在水溶液中不能发生复分解反应的是( ) A.AgNO3 和 NaClB.NaCl 和 Ca(OH)2 C.Ba(OH)2 和 H2SO4 D.Na2CO3 和 HCl 5.(2019 湖南长沙二模)下列各组物质间能发生反应,且现象描述正确的是( ) A.BaCl2 溶液与 NaOH 溶液,产生白色沉淀 B.Ba(OH)2 溶液与稀 H2SO4,没有明显现象 C.CuO 与稀 H2SO4,黑色固体溶解且溶液呈蓝色 D.CuSO4 溶液与 MgCl2 溶液,产生蓝色沉淀 6.向盛有 NaOH 和 Na2CO3 混合溶液的烧杯中加入一定量的稀硫酸,看到产生大量气泡。则停止冒气泡后, 烧杯中有关溶质成分的推断,错误的是( ) A.可能只有 Na2SO4 B.可能是 Na2SO4 和 Na2CO3 C.可能是 Na2SO4 和 H2SO4 D.可能是 Na2SO4、Na2CO3 和 NaOH 7.(2019湖南湘西凤凰模拟)实验室有盐酸和BaCl2的混合溶液,小李同学向其中逐滴加入过量某物质X, 溶液的 pH 变化如图。你认为 X 是( ) A.纯碱溶液 B.水 C.稀盐酸 D.石灰水 8.已知 A、B、C、D 四种物质是含有同种金属元素的不同化合物,其中 B 是一种常见的建筑材料,A、D 含有两种元素,B、C 含有三种元素,反应④是放热反应,它们之间的转化关系如图所示,下列推理不正 确的是( ) A.反应③一定是中和反应 B.反应①属于分解反应 C.物质 C 可用于改良酸性土壤 D.反应②可以由多个化学反应实现 9.下列各组物质在 pH=12 的溶液中能大量共存并形成无色溶液的是( ) A.CuCl2 NaCl Ba(NO3)2 B.CaCl2 KNO3 HCl C.K2SO4 BaCl2 NaNO3 D.NaCl KOH KNO3 10.按下表进行实验,有关说法及分析错误的是( ) 实验 向少量 KOH 溶液中滴加 CuSO4 溶液 向少量 Ba(OH)2 溶液中滴加 MgSO4 现象 ① 白色沉淀 化学方程式 CuSO4+2KOH Cu(OH)2↓+K2SO4 ② A.①有蓝色沉淀生成 B.②反应的化学方程式为 Ba(OH)2+MgSO4 BaSO4↓+Mg(OH)2↓ C.复分解反应不可能同时生成两种沉淀 D.两个反应都属于复分解反应 11.下列各组物质的溶液,只需组内物质相互反应,就能区别的是( ) A.Cu(NO3)2 Na2SO4 MgCl2 HCl B.FeCl3 HNO3 NaCl NaOH C.BaCl2 K2SO4 Na2CO3 KOH D.H2SO4 KCl BaCl2 CuCl2 二、填空题 12.有一包白色固体,可能含有碳酸钾、硫酸钠、氯化钠、硝酸钡、氢氧化钾中的一种或几种。某化学 兴趣小组为探究其成分,进行如下实验: (1)取少量固体于烧杯中,逐渐加水并不断搅拌,待烧杯中的物质充分反应后过滤,得到白色沉淀和滤 液。 (2)取少量滤液于试管中,滴加酚酞溶液,酚酞溶液不变色。 (3)向白色沉淀中滴加过量稀硝酸并不断搅拌,沉淀不溶解。 请根据上述实验过程和发生的现象,回答问题: 原白色固体中一定含有 ,一定不含有 ,可能含有 。 13.有 A、B、C 三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种。为了 鉴别它们,各取少量溶液两两混合,实验结果如下表所示。表中“↓”表示有沉淀产生;“↑”表示有 气体产生;“—”表示观察不到明显的现象变化。 A B C A ↑ — B ↑ ↓ C — ↓ 回答下列问题: (1)A 中溶质的化学式是 ,A 与 C 反应的基本类型是 ; (2)A 与 B、B 与 C 反应的化学方程式分别 是 、 。 14.Na2CO3、CaCO3、BaCO3 等统称为碳酸盐,碳酸盐均能与稀盐酸反应生成二氧化碳,回答下列问题: (1)另写一种碳酸盐的化学式 ; (2)如图所示实验中,将 A 装置中分液漏斗的活塞打开,使适量水流入广口瓶中,B 中观察到的现象 是 ,D 中观察到的现象是 。 15.(2019 宁夏银川一模)“比较归纳法”是学习化学的一种重要方法。(“—”表示相连的两种物质 能发生反应,“→”表示某种物质可通过一步反应转化为另一种物质) (1)请以下表中序号Ⅰ为示例,填写序号Ⅱ、Ⅲ中的空格: 项目序号 举例 物质类别间的相互反应 物质类别间的相互转化 Ⅰ BaCl2+Na2CO3 BaCO3↓+2NaCl 盐 1—盐 2 盐→新盐 Ⅱ 写出稀硫酸与氯化钡反应的化学方程 式: 酸—盐 酸→ Ⅲ 写出氢氧化钠转变成另一种碱的化学方程 式: 碱— 碱→新碱 (2)室温下,氯化镁与下列物质的变化关系,正确的是 (填字母序号)。 A.MgCl2——AgNO3 B.KNO3 MgCl2 C.MgCl2——HCl D.Mg(OH)2 MgCl2 16.化学小组用如图所示装置探究酸、碱、盐的性质(夹持仪器已省略)。 资料:Na2CO3 溶液可与中性的 CaCl2 溶液发生复分解反应 (1)关闭 K2,打开 K1 和分液漏斗活塞,向 B 中加入稀盐酸,使其浸没大理石后关闭分液漏斗活塞。B 中发 生反应的化学方程式为 。 (2)当 B 中的物质仍在反应时,关闭 K1,打开 K2。一段时间后 C 中的现象为 ; 充分反应后,C 中一定含有溶质 NaCl 的原因是 。 (3)当实验结束后,将装置 A、B、C 上层清液全部倒入同一烧杯中,滴加无色酚酞溶液,发现溶液呈无色, 请选用一种试剂确定溶质成分有几种可能情况,写出所加试剂,预期现象和结论。 。 答案 一、选择题 1.答案 C 盐酸与大理石反应生成二氧化碳气体,有气泡产生;硝酸钠溶液与氢氧化钾溶液相互交换 成分没有沉淀、气体或水生成,不能发生反应;氢氧化钠溶液与盐酸相互交换成分生成氯化钠和水,能 发生反应,且无明显现象;氯化钡溶液与稀硫酸反应生成硫酸钡白色沉淀。 2.答案 C HCl 与两种物质反应都没有明显现象,不能鉴别;KNO3 与两种物质都不能反应,不能鉴 别;K2CO3 与氢氧化钠不反应,与氢氧化钙反应产生白色沉淀,能用于鉴别两种物质;FeCl3 与两种物质反 应都生成红褐色沉淀,不能鉴别。 3.答案 C 碳酸钠固体和稀硫酸反应生成硫酸钠、水和二氧化碳,参加反应的碳酸钠固体的质量大于 生成二氧化碳的质量,反应后溶液总质量增大;氢氧化钠溶液和盐酸反应生成氯化钠和水,没有气体或 沉淀生成,混合后溶液质量不变;稀硫酸和氯化钡溶液反应生成硫酸钡沉淀和盐酸,属于复分解反应, 由于生成了沉淀,则溶液的质量会减少;氯化钾溶液和硫酸钠溶液相互交换成分没有沉淀、气体或水生 成,不反应。 4.答案 B AgNO3 和 NaCl 能生成氯化银白色沉淀,反应能发生;NaCl 和 Ca(OH)2 混合后没有沉淀、气 体或水生成,反应不能发生;Ba(OH)2 和 H2SO4 能生成硫酸钡白色沉淀和水,反应能发生;Na2CO3 和 HCl 反 应生成氯化钠、水和二氧化碳,反应能发生。 5.答案 C BaCl2 溶液与 NaOH 溶液混合后没有沉淀、气体或水生成,不能发生复分解反应,故 A 错 误;Ba(OH)2 溶液与稀 H2SO4 反应生成硫酸钡沉淀和水,会观察到产生白色沉淀,故 B 错误;CuO 与稀 H2SO4 反应生成硫酸铜和水,会观察到黑色固体溶解且溶液呈蓝色,故 C 正确;CuSO4 溶液与 MgCl2 溶液混合后 没有沉淀、气体或水生成,不能发生复分解反应,故 D 错误。 6.答案 D 向盛有 NaOH 和 Na2CO3 混合溶液的烧杯中加入一定量的稀硫酸,硫酸先与氢氧化钠反应生 成硫酸钠和水,氢氧化钠反应完毕后,硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,看到产生大量气 泡,说明氢氧化钠已经反应完全,所以烧杯中溶液的溶质成分不可能含有氢氧化钠,当碳酸钠和硫酸恰 好反应时溶液中只有硫酸钠,硫酸过量时还可能含有硫酸,碳酸钠过量时还可能含有碳酸钠。 7.答案 A 向盐酸和 BaCl2 的混合溶液中加入纯碱溶液时,碳酸钠先和盐酸反应,随着反应的进行溶 液的酸性减弱,pH 升高,当恰好完全反应时溶液显中性;继续加入碳酸钠时,碳酸钠又和氯化钡反应生 成碳酸钡沉淀和显中性的氯化钠,在碳酸钠和氯化钡反应的过程中溶液的 pH 不变,当氯化钡完全反应 后,再加入碳酸钠时,溶液的 pH 又升高,故 A 正确。向盐酸和 BaCl2 的混合溶液中加入水时,溶液的酸性 减弱,pH 增大,但不可能等于 7、大于 7,故 B 错误。向盐酸和 BaCl2 的混合溶液中加入稀盐酸时,溶液 的酸性逐渐增强,溶液的 pH 减小,故 C 错误。向盐酸和 BaCl2 的混合溶液中加入石灰水时,氢氧化钙会 与盐酸反应使 pH 增大,但不会与氯化钡反应,曲线不会有一段水平的,故 D 错误。 8.答案 A A、B、C、D 四种物质是含有同种金属元素的不同化合物,其中 B 是一种常见的建筑材料, 则 B 为碳酸钙;A、D 含有两种元素,B、C 含有三种元素,反应④是放热反应,说明 A 为氧化钙,其能与水 反应放出热量生成氢氧化钙,C 为氢氧化钙;氢氧化钙能与盐酸反应生成氯化钙,D 可以为氯化钙。代入 题中验证,符合题意。氢氧化钙与氯化镁反应可以生成氯化钙,不是中和反应,故 A 错误;碳酸钙高温分 解生成氧化钙,属于分解反应,故 B 正确;物质 C 是氢氧化钙,可用于改良酸性土壤,故 C 正确;氢氧化钙 转化为碳酸钙,可以由多个化学反应实现,故 D 正确。 9.答案 D pH=12 的水溶液显碱性,水溶液中含有大量的 OH-。CuCl2 中的铜离子和 OH-在溶液中能结合 生成氢氧化铜沉淀,A 组不能大量共存;HCl 在溶液中解离出的氢离子和 OH-能结合生成水,B 组不能大 量共存;K2SO4 与 BaCl2 在溶液中相互交换成分生成硫酸钡白色沉淀,C 组不能大量共存;D 中三者之间不 反应,能在碱性溶液中共存,且不存在有色离子。 10.答案 C 向少量 KOH 溶液中滴加 CuSO4 溶液,生成氢氧化铜蓝色沉淀,会观察到有蓝色沉淀生成, 故选项 A 正确。②是氢氧化钡与硫酸镁溶液反应生成硫酸钡沉淀和氢氧化镁沉淀,故选项 B 正确。氢 氧化钡与硫酸镁溶液反应生成硫酸钡沉淀和氢氧化镁沉淀,属于复分解反应,复分解反应可以同时生 成两种沉淀,故选项 C 错误。两个反应都是两种化合物相互交换成分生成两种新的化合物的反应,均属 于复分解反应,故选项 D 正确。 11.答案 B A 项,呈蓝色的是 Cu(NO3)2 溶液,其余物质的溶液两两混合或分别与 Cu(NO3)2 溶液混合均 没有明显现象,故不加其他试剂无法鉴别。B 项,呈浅黄色的是 FeCl3 溶液,能与 FeCl3 溶液反应产生红 褐色沉淀的是 NaOH 溶液,再将剩余的两种物质的溶液分别滴加至红褐色沉淀中,能使沉淀消失的是 HNO3 溶液,无明显变化的是氯化钠溶液,故不加其他试剂可以鉴别。C 项,K2SO4、Na2CO3 溶液与 BaCl2 溶 液反应均能产生白色沉淀,不加其他试剂无法鉴别。D 项,呈蓝色的是 CuCl2 溶液,其余物质的溶液两 两混合,均没有明显现象的是 KCl 溶液,不加其他试剂无法鉴别 H2SO4 和 BaCl2 溶液。 二、填空题 12.答案 硫酸钠、硝酸钡 氢氧化钾、碳酸钾 氯化钠 解析 取少量固体于烧杯中,逐渐加水并不断搅拌,待烧杯中的物质充分反应后过滤,得到白色沉淀和 滤液,混合物中一定含有硝酸钡,且含有硫酸钠、碳酸钾中的一种或两种;取少量滤液于试管中,滴加酚 酞溶液,酚酞溶液不变色,混合物中一定不含氢氧化钾;向白色沉淀中滴加过量稀硝酸并不断搅拌,沉 淀不溶解,混合物中一定含有硫酸钠,不含碳酸钾,所以原白色固体中一定含有硫酸钠、硝酸钡,一定不 含有氢氧化钾、碳酸钾,可能含有氯化钠。 13.答案 (1)HCl 复分解反应 (2)Na2CO3+2HCl 2NaCl+H2O+CO2↑ Ca(OH)2+Na2CO3 CaCO3↓+2NaOH 解析 (1)盐酸与碳酸钠反应生成二氧化碳气体,盐酸和氢氧化钙反应没有明显现象,澄清石灰水会与 碳酸钠反应生成碳酸钙沉淀。B 和 A 会生成气体,B 和 C 会生成沉淀,所以 B 是碳酸钠,A 是 HCl,C 是氢 氧化钙,A 与 C 的反应是盐酸和氢氧化钙反应生成氯化钙和水,所以基本反应类型是复分解反应。(2)A 与 B 的反应是盐酸和碳酸钠反应生成氯化钠、水和二氧化碳;B 与 C 的反应是碳酸钠和氢氧化钙反应 生成碳酸钙沉淀和氢氧化钠。 14.答案 (1)K2CO3(合理即可) (2)B 中左边导管口产生气泡,稀盐酸被压入 C 中 澄清石灰水变浑浊 解析 (1)碳酸钾是一种常见的碳酸盐,其化学式为 K2CO3。(2)生石灰与水反应放出大量的热,A 装置中 空气受热膨胀,会观察到 B 中左边导管口产生气泡,稀盐酸被压入 C 中。稀盐酸与碳酸钠反应生成二氧 化碳气体,二氧化碳能使澄清石灰水变浑浊,会观察到 D 中澄清石灰水变浑浊。 15.答案 (1)BaCl2+H2SO4 BaSO4↓+2HCl 新酸 2NaOH+CuSO4 Na2SO4+Cu(OH)2↓ 盐 (2)AD 解析 (1)氯化钡和稀硫酸反应的化学方程式为 BaCl2+H2SO4 BaSO4↓+2HCl,酸与盐反应生成新酸 和新盐;氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为 2NaOH+CuSO4 Na2SO4+Cu(OH)2↓;碱与盐反应生成新碱和新盐。(2)MgCl2 能与 AgNO3 反应;KNO3 不能 通过化学反应转化为 MgCl2;MgCl2 不能与 HCl 反应;Mg(OH)2 与盐酸反应能生成 MgCl2。 16.答案 (1)CaCO3+2HCl CaCl2+H2O+CO2↑ (2)先有气泡冒出,后产生白色沉淀 B 中的稀盐酸和 生成的CaCl2溶液进入C中与碳酸钠反应生成了氯化钠 (3)向混合液中加入碳酸钠,若无现象,说明溶 质只有氯化钠;若产生沉淀,说明溶质有氯化钠和氯化钙;若先产生气泡后产生沉淀,说明溶质有氯化 钠、氯化钙、氯化氢 解析 (1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳。(2)当 B 中的物质仍在反应时,关闭 K1,二氧 化碳无法排出,B 中压强增大,打开 K2,则 B 中液体会被压入 C 中,盐酸和碳酸钠发生反应生成氯化钠、 二氧化碳和水,稀盐酸反应完后氯化钙与碳酸钠反应生成氯化钠和碳酸钙沉淀,所以,观察到 C 中先有 气泡冒出,后产生白色沉淀。(3)实验结束后,将 A、B、C 上层清液全部倒入同一烧杯中,滴加无色酚酞 溶液,发现溶液呈无色,说明氢氧化钙、碳酸钠已完全反应,混合后溶液中的溶质可能为氯化钠,氯化钠、 氯化钙,氯化钠、氯化钙、氯化氢。因此可向混合液中加入碳酸钠,若无现象,说明溶质只有氯化钠; 若产生沉淀,说明溶质有氯化钠和氯化钙;若先产生气泡后产生沉淀,说明溶质有氯化钠、氯化钙、氯 化氢。查看更多