- 2022-03-30 发布 |
- 37.5 KB |
- 42页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
16版 初级药师 练习题2
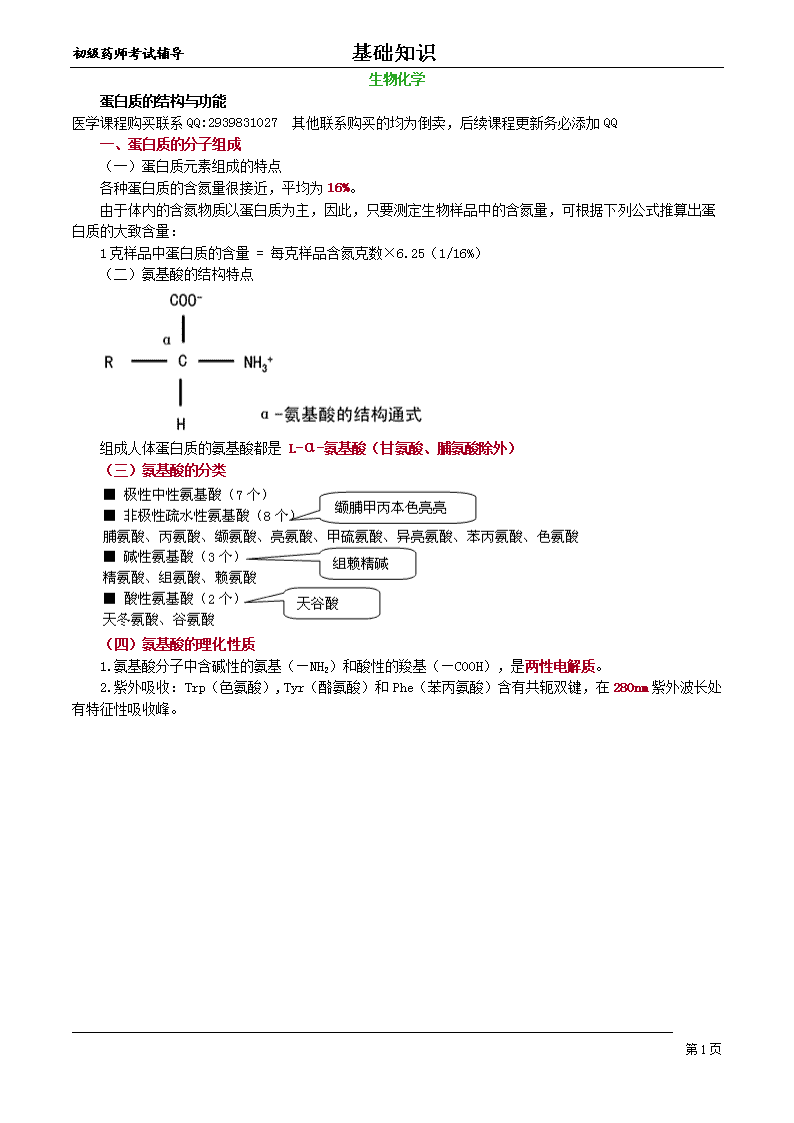
初级药师考试辅导 基础知识生物化学 蛋白质的结构与功能医学课程购买联系QQ:2939831027其他联系购买的均为倒卖,后续课程更新务必添加QQ 一、蛋白质的分子组成 (一)蛋白质元素组成的特点 各种蛋白质的含氮量很接近,平均为16%。 由于体内的含氮物质以蛋白质为主,因此,只要测定生物样品中的含氮量,可根据下列公式推算出蛋白质的大致含量: 1克样品中蛋白质的含量=每克样品含氮克数×6.25(1/16%) (二)氨基酸的结构特点 组成人体蛋白质的氨基酸都是L-α-氨基酸(甘氨酸、脯氨酸除外) (三)氨基酸的分类 (四)氨基酸的理化性质 1.氨基酸分子中含碱性的氨基(—NH2)和酸性的羧基(—COOH),是两性电解质。 2.紫外吸收:Trp(色氨酸),Tyr(酪氨酸)和Phe(苯丙氨酸)含有共轭双键,在280nm 第42页 初级药师考试辅导 基础知识紫外波长处有特征性吸收峰。 应用:对蛋白质溶液进行定量。 (五)肽与肽键 在蛋白质分子中,氨基酸通过肽键连接形成肽。 1.肽键(—CO—NH—,酰胺键) 一分子氨基酸的α-COOH与另一分子氨基酸的α-NH2脱水缩合生成二肽(氨基酰-氨基酸)。 —CO—NH—称为肽键。是多肽及蛋白质分子的主要化学键。 第42页 初级药师考试辅导 基础知识 肽键连接氨基酸形成的长链骨架——多肽主链 连接于Cα上的各氨基酸残基的R基团——多肽侧链 ◆由十个以内氨基酸相连而成的肽称为寡肽,由十个以上的氨基酸相连形成的肽称多肽。 ◆肽链都有 游离α-NH2端—N(末)端 游离α-COOH端—C(末)端 ◆编号、命名、书写:N→C 如:甘-丙-谷……组-蛋 二、蛋白质的分子结构 (一)蛋白质的一级结构 概念:蛋白质的一级结构指多肽链中氨基酸的排列顺序 第42页 初级药师考试辅导 基础知识。 基本化学键:肽键 (二)蛋白质的二级结构 概念:蛋白质分子中某一段肽链的局部空间结构,即该段肽链主链骨架原子的相对空间位置,并不涉及氨基酸残基侧链的构象。局部主链! 主要的化学键:氢键 基本结构形式:α-螺旋、β-折叠、β-转角、无规卷曲 1.α-螺旋 结构特点 ①右手螺旋; ②螺旋稳定的化学键为氢键; ③ 第42页 初级药师考试辅导 基础知识R基团伸向螺旋外侧; ④每3.6个氨基酸残基螺旋上升一圈。螺距为0.54nm,所以每个氨基酸残基上升的高度为0.15nm。 2.β-折叠 ①多肽链相邻肽键平面折叠成锯齿状,夹角为110°; ②氨基酸侧链交替地位于锯齿状结构的上、下方; ③两条以上肽链或一条肽链内的若干肽段平行排列,通过链间羰基氧和亚氨基氢形成氢键,从而稳固β-折叠结构; ④肽链有顺式平行和反式平行两种。 β-折叠 第42页 初级药师考试辅导 基础知识 平行式 反平行式 第42页 初级药师考试辅导 基础知识 3.β-转角 结构特点: ①常发生于肽链180°回折时的转角上; ②由四个连续的氨基酸残基组成。第一个氨基酸残基的CO与第四个氨基酸残基的NH形成氢键,以稳定转折的构象。 β-转角 4.无规卷曲 (三)蛋白质的三级结构 概念:一条多肽链内所有原子的空间排布,包括主链、侧链构象内容。一条所有 第42页 初级药师考试辅导 基础知识! 化学键:疏水作用力、离子键、氢键和范德华力 肌红蛋白三级结构 (四)蛋白质的四级结构 亚基:有些蛋白质由两条或两条以上具有独立三级结构的多肽链组成,其中每条多肽链称为一个亚基。亚基单独存在没有生物学功能。由亚基构成的蛋白质称为寡聚蛋白。 蛋白质四级结构:蛋白质分子中各亚基之间的空间排布及相互接触关系。 亚基之间的结合力主要是疏水作用,其次是氢键和离子键。 第42页 初级药师考试辅导 基础知识 (五)蛋白质的空间构象 1.分子伴侣 定义:是一类帮助新生多肽链正确折叠的蛋白质。 作用: ①可逆地与未折叠肽段结合防止错误的聚集发生,使肽链正确折叠; ②与错误聚集的肽段结合,使之解聚后,再诱导其正确折叠; ③对蛋白质分子中二硫键的正确形成起到重要作用。 伴侣蛋白在蛋白质折叠中的作用 2.肽单元 参与肽键的6个原子Cα1、C、O、N、H、Cα2位于同一平面,Cα1和Cα2 第42页 初级药师考试辅导 基础知识在平面上所处的位置为反式构型,此同一平面上的6个原子构成肽单元。 3.模体 二个或三个具有二级结构的肽段,在空间上相互接近,形成一个特殊的空间构象,称为模体。 钙结合蛋白中结合钙 锌指结构 离子的模体 4.结构域 分子量大的蛋白质三级结构常可分割成1个和数个球状或纤维状的区域,折叠得较为紧密,具有独立的生物学功能,称为结构域。如纤连蛋白含有6个结构域。 三、蛋白质的结构与功能的关系 (一)蛋白质一级结构与功能的关系 1.一级结构是空间构象的基础; 第42页 初级药师考试辅导 基础知识 2.蛋白质一级结构的改变与分子病 镰刀形红细胞贫血 HbAβ肽链 N-val·his·leu·thr·pro·glu·glu·····C(146) HbSβ肽链 N-val·his·leu·thr·pro·val·glu·····C(146) 六月,携镰刀割谷子 (二)蛋白质空间结构与功能的关系 1.血红蛋白(Hb)的构象 2.Hb有2种天然构象 (1)紧密型(tensestate,T型) 未结合O2时,紧凑,与O2亲和力小 (2)松弛型(relaxedstate,R型) 结合O2时,松弛,与O2亲和力大 3.Hb的运O2功能通过构象的互变实现 肺毛细血管: O2分压↑,O2作为变构剂使T→R, 利于结合O2。 组织毛细血管: O2分压↓,CO2和H+作为变构剂使R→T, 利于释放O2。 4.别构效应(变构效应) 一个蛋白质与它的配体(或其他蛋白质)结合后,蛋白质的构象发生变化,使它更适于功能需要,这一类变化称为别构效应。 例如Hb是别构蛋白,小分子O2是Hb的别构剂或称为效应剂。 5.协同效应 一个寡聚体亚基与其配体结合后,能影响此寡聚体中另一亚基与配体的结合能力,如果是促进作用,则称为正协同效应,反之则为负协同效应。 以血红蛋白为例,当Hb的第一个亚基与O2结合以后,促进了第二及第三个亚基与O2结合后,又大大促进了第四个亚基与O2结合,这种效应为正协同效应。 四、蛋白质的理化性质 (一)蛋白质的两性解离 第42页 初级药师考试辅导 基础知识 当蛋白质溶液处于某一pH时,蛋白质解离成正、负离子的趋势相等,即成为兼性离子,净电荷为零,此时溶液的pH称为蛋白质的等电点。 (二)蛋白质的胶体性质 分子量1万-100万 达到胶体颗粒范围(1-100nm) 不能透过半透膜 扩散速度慢、粘度大 —透析法纯化蛋白质的原理 1.水化膜和表面电荷是蛋白质维持亲水胶体的稳定因素 (1)水化膜 亲水的极性基团位于表面,可发生水合作用,形成水化膜,将蛋白质颗粒相互隔开,防止聚沉。 (2)表面电荷 亲水基团大都能解离,使蛋白质表面带相同电荷而相斥,防止蛋白质颗粒聚沉。 (三)蛋白质的变性 定义:在某些物理和化学因素(如加热、强酸、强碱、有机溶剂、重金属离子及生物碱等)作用下,其特定的空间构象被破坏,从而导致其理化性质的改变和生物活性的丧失,称为蛋白质的变性。 变性的实质: 空间结构的破坏,不涉及一级结构的改变 第42页 初级药师考试辅导 基础知识 (四)蛋白质的紫外吸收 由于蛋白质分子中含有色氨酸和络氨酸,因此在280nm波长处有特征性吸收峰,可作蛋白质定量测定。 【例题】 蛋白质的平均含氮量是( ) A.10% B.27% C.16% D.36% E.6% 【正确答案】C A.天冬氨酸 B.精氨酸 C.甲硫氨酸 D.苏氨酸 E.酪氨酸 1.碱性氨基酸 【正确答案】B 2.非极性疏水性氨基酸 【正确答案】C 3.酸性氨基酸 【正确答案】A A.氢键 B.肽键 C.疏水作用力 D.盐键 E.范德华力 1.维系蛋白质化学键一级结构的 【正确答案】B 2.维系蛋白质二级结构的主要化学键 【正确答案】A 组成人体蛋白质多肽链的基本单位是 A.L-α-氨基酸 B.D-α-氨基酸 C.L-β-氨基酸 D.D-β-氨基酸 E.L-ω-氨基酸 【正确答案】A 蛋白质的一级结构 A.亚集聚和 B.α-螺旋 C.β 第42页 初级药师考试辅导 基础知识-折叠 D.氨基酸序列 E.氨基酸含量 【正确答案】D 有关蛋白质变构,下列哪种叙述是错误的 A.氧对血红蛋白的作用属于正协同效应 B.氧对血红蛋白的作用属于负协同效应 C.氧是血红蛋白的变构剂 D.氧与血红蛋白结合呈S型曲线 E.蛋白质变构效应是生物体内重要的代谢调节方式之一 【正确答案】B A.二级结构 B.三级结构 C.四级结构 D.模序 E.结构域 1.β-转角是 【正确答案】A 2.血红蛋白是具有几级结构的蛋白质 【正确答案】C 3.亚基间的空间排布是 【正确答案】C 核酸的结构与功能 一、核酸的化学成分及一级结构 1.定义:核酸是以核苷酸作为基本组成单位的生物大分子,携带和传递遗传信息。 2.分类: (1)脱氧核糖核酸,DNA (2)核糖核酸,RNA 3.核苷酸 (1)碱基 第42页 初级药师考试辅导 基础知识 嘧啶嘌呤DNA胞嘧啶(C)、胸腺嘧啶(T)腺嘌呤(A)、鸟嘌呤(G)RNA胞嘧啶(C)、尿嘧啶(U)腺嘌呤(A)、鸟嘌呤(G) (2)戊糖 DNA:β-D-2-脱氧核糖 RNA:β-D-核糖 (3)核苷:戊糖的C1与嘌呤的N9或嘧啶的N1以糖苷键相连形成核苷。 (4)核苷酸: 核苷的戊糖羟基与磷酸结合形成。 第42页 初级药师考试辅导 基础知识 4.核酸的一级结构 (1)定义:核苷酸链中,核苷酸的排列顺序(也就是碱基排列顺序)。 (2)3’,5’-磷酸二酯键是核酸的基本结构键。 二、DNA的空间结构与功能 (一)DNA的二级结构——双螺旋结构模型整体右手双螺旋:两条链走向相反,长度相等。局部特点磷酸和脱氧核糖相连而成的亲水骨架位于外侧,疏水碱基位于内侧。结构参数直径2nm,每旋转一周包括10个脱氧核苷酸残基,螺距为3.4nm。稳定因素纵向—碱基堆积力(疏水力);横向—氢键(A-T,两个氢键;G-C,三个氢键)。 第42页 初级药师考试辅导 基础知识 (二)DNA的超螺旋结构 是指DNA在双螺旋结构的基础上,进一步旋转折叠,在蛋白质的参与下组装成的空间构象。 1.原核生物DNA形成超螺旋 原核生物DNA大多是闭合的环状双链DNA分子,在形成双螺旋结构后,进一步螺旋化形成超螺旋结构。 第42页 初级药师考试辅导 基础知识 2.真核生物核内DNA常为线状,在形成双螺旋结构后,与多种组蛋白构成核小体,最终组装成染色体。 (三)DNA的功能 作为生物遗传信息复制的模板和基因转录的模板,它是生命遗传繁殖的物质基础,也是个体生命活动的基础。 三、RNA的空间结构与功能 (一)概述 1.主要有三种RNA mRNA:携带遗传信息,蛋白质合成模板; tRNA:转运氨基酸; rRNA:和蛋白质一起构成核糖体。 2.单链,链的局部可形成双链结构。 第42页 初级药师考试辅导 基础知识 (二)信使RNA 真核细胞mRNA一级结构特点 1.5’末端有帽式结构(m7GpppNm); 2.3’末端有一段长度30-200腺苷酸构成的多聚腺苷酸的节段(polyA尾); 3.编码区中三个核苷酸构成一个密码子。 (三)转运RNA 1.一级结构特点: (1)分子量最小; (2)富含稀有碱基; (3)3’-末端是-CCA。 2.tRNA二级结构的特点—三叶草形 三叶草型结构含有四臂三环一附叉,其中的反密码环,能识别mRNA分子上的遗传密码;氨基酸臂可携带氨基酸。 第42页 初级药师考试辅导 基础知识 3.tRNA三级结构呈倒“L”字母形 (四)核蛋白体RNA(rRNA) 在细胞内含量最多,约占RNA总量的80%以上。 rRNA的功能是与核蛋白体蛋白组成核蛋白体,在细胞质作为蛋白质的合成场所。 rRNA二级结构的特点是含有大量茎环结构。可作为核蛋白体蛋白的结合和组装的结构基础。 (五)DNA与RNA在化学组成、结构与生物学功能方面的异同 比较项目DNARNA相同点分子组成含碱基A、G、C、磷酸和戊糖 分子结构基本单位为单核苷酸,由3’5’-磷酸二酯键连接不同点分子组成含脱氧核糖,含T含核糖,含U 分子结构一级结构是指脱氧核糖核苷酸的数量和排列顺序。二级结构为双螺旋结构。三级结构为超螺旋结构,真核细胞中为核小体结构。一级结构是指核糖核苷酸的数量和排列顺序。二级结构是发夹型的单链结构,tRNA的二级结构为三叶草型;tRNA的三级结构为倒L字母型。 功能是遗传物质的储存和携带者。参与蛋白质的合成。 四、核酸的理化性质 第42页 初级药师考试辅导 基础知识 (一)变性 1.概念:在某些理化因素作用下,DNA双链解开成两条单链的过程。 2.本质:DNA变性的是双链间氢键的断裂。 3.现象: 粘度降低 由于变性时双螺旋松解,碱基暴露,对260nm紫外吸收将增加,OD260值增高称之为增色效应。 (二)DNA解链曲线 通常将DNA分子达50%解链时的温度称为熔点或解链温度(Tm) (三)探针 一小段已知序列的单链核苷酸用放射性核素(如32P、35S)或生物素标记其末端或全链,可依碱基配对规律与具有互补序列的待测核酸进行杂交,以探测它们的同源程度,这段核苷酸链称为探针。 A.G、C、T、U B.G、A、C、T C.A、G、C、U D.G、A、T、U E.I、C、A、U 1.DNA分子中所含的碱基是 【正确答案】B 第42页 初级药师考试辅导 基础知识 2.RNA分子中所含的碱基是 【正确答案】C A.核苷酸在核酸长链上的排列顺序 B.三叶草结构 C.双螺旋结构 D.超螺旋结构 E.核小体结构 1.属于核酸一级结构的描述是: 【正确答案】A 2.属于tRNA二级结构的描述是: 【正确答案】B 3.属于DNA的二级结构的描述是: 【正确答案】C 有关DNA的二级结构,错误的描述为: A.DNA分子是由两条走向相反的多核苷酸链组成的右手双螺旋 B.DNA分子的二级结构上有大沟和小沟 C.A与T之间有三对氢键,而G与C之间有二对氢键 D.每10个碱基对旋转一周 E.氢键和碱基堆积力从横向与纵向稳定DNA双螺旋 【正确答案】C 酶 一、酶的分子结构与功能 (一)酶的分子组成 单纯酶:仅含氨基酸,多为水解酶 辅助因子可分为: 辅酶:以非共价键与酶蛋白疏松结合,透析方法可分。 辅基:与酶蛋白结合紧密,不易分开。 第42页 初级药师考试辅导 基础知识 (二)酶的活性中心 1.必需基团:与酶活性发挥有关的化学基团。 2.活性中心:这些必需基团在一级结构上可能相距很远,但在空间结构上彼此靠近,组成特定空间结构的区域,能与底物结合,并将其转变为产物,该区域称酶的活性中心。 二、酶促反应的特点 1.有极高的效率 2.高度的特异性 绝对专一性 相对专一性 立体异构专一性 3.活性可调节性 三、酶促反应动力学 第42页 初级药师考试辅导 基础知识 1、影响酶促反应速度的因素 酶浓度 底物浓度 温度 pH值 激活剂 抑制剂 底物浓度Km值—酶促反应速度为最大反应速度一半时的底物浓度; Vm是酶完全被底物饱和时的反应速度,与酶浓度成正比。温度酶的最适温度:酶催化活性最大时的环境温度。pH值酶的最适pH:酶催化活性最大时的环境PH值。竞争性抑制抑制剂与底物结构相似,可竞争非共价结合酶的活性中心,阻碍酶与底物结合; 例如:磺胺类药物竞争性抑制二氢叶酸合成酶活性。 与对氨基苯甲酸竞争二氢叶酸合成酶 细菌不能利用环境中的叶酸,要靠自己合成! 二氢蝶呤啶+对氨基苯甲酸+谷氨酸 四、酶的调节 (一)酶原与酶原的激活 1.酶原:有些酶在细胞内合成或初分泌时,没有催化活性,这种无活性的酶的前体称为酶原。 2.酶原的激活:酶原在特定条件下转变为有催化活性的酶的过程。 3.酶原激活的实质:酶的活性中心形成或暴露的过程。不可逆。 第42页 初级药师考试辅导 基础知识 (二)变构酶 1.酶活性的调节方式 2.变构调节 (1)定义:体内一些代谢物与某些酶活性中心外的调节部位非共价可逆地结合,使酶发生构象改变,引起催化活性改变。这一调节酶活性的方式称为变构调节。 这类受变构调节的酶称为变构酶。 引起变构效应的代谢物称变构效应剂。 变构调节 (三)同工酶 定义:催化相同的化学反应,但酶蛋白的分子结构、理化性质和免疫学性质有所不同的一组酶。 影响酶促反应速度的因素不包括 A.底物浓度 B.酶浓度 C.产物浓度 D.反应温度、pH E.激活剂、抑制剂 【正确答案】C Km值的概念 A.与酶的性质无关 B.与同一种酶的各种同工酶无关 C.与酶对底物的亲和力无关 D.与酶的浓度有关 E.是达到1/2Vmax时的底物浓度 【正确答案】E 第42页 初级药师考试辅导 基础知识 磺胺药的抑菌作用属于 A.不可逆抑制 B.竞争性抑制 C.非竞争性抑制 D.反竞争性抑制 E.抑制强弱不取决于底物与抑制剂浓度的相对比例 【正确答案】B 糖代谢 一、糖的无氧氧化 1.定义:葡萄糖在无氧或缺氧条件下分解形成乳酸的过程称无氧氧化,也被称为糖酵解。 2.主要过程: 第一阶段:1分子G→2分子磷酸丙糖 第二阶段:磷酸丙糖→丙酮酸 氧供应不足时,糖酵解途径生成的丙酮酸在乳酸脱氢酶催化下,由NADH+H+提供氢,还原成乳酸。 (二)糖酵解小结 1.反应部位:胞浆; 2.反应条件:不需氧; 3.三个关键酶:己糖激酶 磷酸果糖激酶-1 丙酮酸激酶 (三)关键酶及其调节 激活剂抑制剂己糖激酶胰岛素诱导其基因表达,合成增加6-磷酸葡萄糖6-磷酸果糖激酶-1(别构酶)AMP、ADP1,6-二磷酸果糖、2,6-二磷酸果糖ATP、柠檬酸丙酮酸激酶1,6-二磷酸果糖ATP (四)生理意义 1.是机体在缺氧情况下获取能量的有效方式,1mol葡萄糖经糖酵解途径氧化成2mol乳酸,净生成2molATP。 2.是某些细胞在氧供应正常情况下的重要供能途径。 ① 第42页 初级药师考试辅导 基础知识无线粒体的细胞,如:红细胞 ②代谢活跃的细胞,如:白细胞、骨髓细胞 二、糖的有氧氧化 (一)糖有氧氧化的概念 葡萄糖或糖原的葡萄糖单位在有氧情况下,彻底分解为CO2和H2O,生成大量ATP的过程称为有氧氧化。 (二)糖的有氧氧化过程 第一阶段:酵解途径 第二阶段:丙酮酸的氧化脱羧 第三阶段:三羧酸循环和氧化 磷酸化 (三)糖有氧氧化的关键酶 (四)三羧酸循环细胞定位线粒体底物乙酰CoA 第42页 初级药师考试辅导 基础知识反应过程4个脱氢反应,3个NADH,1个FADH2;3个关键酶:柠檬酸合酶、异柠檬酸脱氢酶、α-酮戊二酸脱氢酶系;2个脱羧反应,生成2分子CO2;能量生成10分子ATP (五)有氧氧化的生理意义 1.葡萄糖的有氧氧化是机体获得能量的主要方式。1mol葡萄糖经有氧氧化全过程,彻底氧化成CO2和H2O,总共生成30mol或32molATP; 2.TAC是糖、脂肪、氨基酸三大营养物质彻底氧化分解的共同途径。 3.TAC是三大营养物质代谢联系的枢纽。 三、磷酸戊糖途径 磷酸戊糖途径的生理意义 1.提供5-磷酸核糖,参与核苷酸和核酸合成。 2.提供还原型辅酶Ⅱ(NADPH+H+)。 是体内许多合成代谢的供氢体,如脂肪酸、胆固醇、非必需氨基酸的合成; 四、糖原的合成与分解 糖原合成糖原分解概念葡萄糖合成糖原肝糖原分解葡萄糖关键酶糖原合酶糖原磷酸化酶反应过程葡萄糖↓6-磷酸葡萄糖↓1-磷酸葡萄糖UTP→↓UDPG(活性葡萄糖)↓糖原分子上增加一个G单位供能物质:ATP、UTP糖原上的葡萄糖单位↓1-磷酸葡萄糖↓6-磷酸葡萄糖∣葡萄糖-6-磷酸酶(肝)↓葡萄糖肌糖原不能补充血糖 (二)糖原合成与分解的调节 糖原合成与分解的关键酶分别是糖原合酶和糖原磷酸化酶。 糖原磷酸化酶和糖原合酶磷酸化, 结果:糖原合酶活性↓ 第42页 初级药师考试辅导 基础知识; 糖原磷酸化酶活性↑。 五、糖异生 1.定义:由非糖物质转变为葡萄糖或糖原。 2.组织定位:肝脏(主要)、肾脏(少量) 3.原料:乳酸、甘油、氨基酸、三羧酸循环中的各酸等(没有脂肪酸)。 4.反应特点:不是糖酵解的逆反应,需要突破三个能障。糖异生糖酵解葡萄糖-6-磷酸酶果糖-1,6-二磷酸酶、丙酮酸羧化酶磷酸烯醇式丙酮酸羧激酶己糖激酶磷酸果糖激酶-1丙酮酸激酶 5.生理意义: ①空腹或饥饿时将非糖物质异生成糖,维持血糖浓度恒定; ②参与补充或恢复肝脏糖原储备; ③ 第42页 初级药师考试辅导 基础知识肾糖异生促进泌氨排酸维持酸碱平衡。 6.乳酸循环: 六、血糖及其调节 (一)血糖概念及正常血糖水平 1.定义:血液中的葡萄糖。是糖在体内的运输形式。为全身各组织提供G(尤其脑组织、红细胞等)。 2.正常人空腹血糖水平:3.89-6.11mmol/L (二)调节血糖水平的激素降血糖激素升血糖激素胰岛素1.促进葡萄糖进入肌肉、脂肪等组织细胞;2.加速葡萄糖在肝、肌肉内合成糖原;3.促进糖的有氧氧化4.促进糖转变为脂肪5.抑制糖异生肾上腺素1.促进糖原分解;2.促进肌糖原酵解3.促进糖异生胰高血糖素1.抑制肝糖原合成,促进肝糖原分解;2.促进糖异生糖皮质激素1.促进糖异生2.促进肝外组织蛋白质分解,生成氨基酸; 正常人血糖的浓度维持在(以mmol/L计): A.3.89~6.11 B.4.52~7.78 C.3.33~3.89 D.7.22~7.78 E.5.52~6.23 【正确答案】A 下列哪种激素不能使血糖浓度升高 A.糖皮质激素 B.胰高血糖素 C.肾上腺素 D.生长素 E.胰岛素 【正确答案】E 第42页 初级药师考试辅导 基础知识 三羧酸循环主要在哪一亚细胞区域中进行 A.内质网 B.线粒体 C.微粒体 D.细胞浆 E.高尔基复合体 【正确答案】B 下列哪个酶不是调控糖有氧氧化的关键酶 A.琥珀酸硫激酶 B.丙酮酸激酶 C.异柠檬酸脱氢酶 D.已糖激酶 E.丙酮酸脱氢酶 【正确答案】A 有氧氧化的主要生理意义是: A.清除物质代谢产生的乙酰CoA以防在体内堆积 B.机体大部分组织细胞获得能量的主要方式 C.是机体生成5-磷酸核糖的唯一途径 D.机体小部分组织细胞获得能量的主要方式 E.产生CO2供机体生物合成需要 【正确答案】B 磷酸戊糖途径: A.是体内CO2的主要来源 B.可生成NADH,后者通过电子传递链可产生ATP C.可生成NADPH,后者主要通过电子传递链产生ATP D.可生成NADPH,供合成代谢需要 E.饥饿时葡萄糖经此途径代谢增加 【正确答案】D 下列哪一项是胰岛素对糖代谢影响的错误论述 A.促进糖异生 B.促进糖变为脂肪 C.促进细胞膜对葡萄糖的通透性 D.促进肝葡萄糖激酶的活性 E.促进糖的氧化 【正确答案】A 脂类代谢 一、脂类的消化与吸收 第42页 初级药师考试辅导 基础知识 (一)胆汁酸盐及辅脂酶的作用 (二)乳糜微粒的形成 二、甘油三酯代谢 (一)脂肪动员 1.定义:脂肪组织中储存的TG被脂肪酶逐步水解为游离脂肪酸及甘油,并释放入血供全身各组织氧化利用的过程。 2.限速酶:甘油三酯脂肪酶。 3.脂解激素:能促进脂肪动员的激素,如肾上腺素、胰高血糖素等。 4.抗脂解激素:抑制脂肪动员的激素,如胰岛素。 第42页 初级药师考试辅导 基础知识 (二)甘油代谢 (三)脂肪酸分解代谢1.脂肪酸的活化生成脂酰CoA2.脂酰基由胞液进入线粒体载体:肉碱限速酶:肉碱脂酰转移酶Ⅰ3.脂肪酸的β氧化定义:脂酸的氧化分解从羧基端β-碳原子开始,每次断裂两个碳原子。过程:脱氢、水化、再脱氢、硫解。每轮循环生成1分子乙酰CoA及比原来少两个碳原子的脂酰CoA。最终全部产生乙酰CoA。乙酰CoA可通过三羧酸循环彻底氧化,产生能量;或在肝脏缩合成酮体而被肝外组织氧化利用。 (四)酮体的代谢 1.概念:乙酰乙酸,β-羟丁酸,丙酮的统称。 2.代谢特点:肝内合成,肝外分解 3.酮体代谢的意义: 酮体是脂肪酸在肝内正常的中间代谢产物,是肝输出能源的一种形式。 (五)脂肪酸的合成 1.原料及来源ATP提供能量乙酰CoA经乙酰辅酶A羧化酶催化生成其活性形式——丙二酰辅酶A 第42页 初级药师考试辅导 基础知识NADPH+H+提供氢 2.关键酶 乙酰CoA羧化酶 三、磷脂的代谢 (一)磷脂分类 磷脂是一类含磷酸的类脂。 (二)甘油磷脂的代谢 1.甘油磷脂的合成代谢 (1)合成部位:全身各组织细胞内质网,肝、肠、肾最活跃 (2)合成原料:脂酸、甘油由葡萄糖提供;C2多不饱和脂酸从植物油摄取;胆碱、乙醇胺、丝氨酸、肌醇、磷脂盐,ATP、CTP等。 2.甘油磷脂的分解代谢磷脂酶 四、胆固醇代谢 (一)胆固醇的合成 1.组织定位:除成年动物脑组织及成熟红细胞外的全身各组织,肝脏合成能力最强,小肠也比较旺盛。 2.细胞定位:内质网 3.原料:乙酰辅酶A、NADPH+H+、ATP等 4.限速酶:HMG-CoA还原酶 (二)胆固醇的转化与排泄 1.转化为胆汁酸—主要转化方式; 2.转化为类固醇激素; 3.转化为VD3; 4.在肠道,转变为粪固醇而排出体外。 第42页 初级药师考试辅导 基础知识 五、血浆脂蛋白代谢 (一)血浆脂蛋白的组成 (二)载脂蛋白 1.定义:脂蛋白中与脂类结合的蛋白质称载脂蛋白。主要有:ApoA、ApoB、ApoC、ApoD、ApoE等。 2.生理功能: (1)参与脂类物质的转运及稳定脂蛋白的结构; (2)调节脂蛋白代谢的关键酶活性; (3)识别脂蛋白受体; (4)参与脂蛋白间脂质交换: (二)血浆脂蛋白的分类及功能电泳法分类CM前β脂蛋白β脂蛋白α脂蛋白密度法分类CMVLDLLDLHDL合成部位小肠黏膜细胞肝细胞血液中由VLDL转变而来肝细胞主要功能转运外源性甘油三酯转运内源性甘油三酯转运胆固醇到肝外组织转运胆固醇由肝外组织回肝脏 参与将胆固醇逆向转运回肝脏的脂蛋白是 A.CM B.VLDL C.LDL D.IDL E.HDL 【正确答案】E 脂肪动员的限速酶是 A.组织细胞中的甘油一酯脂肪酶 B.脂肪细胞中的甘油二酯脂肪酶 C.组织细胞中的甘油三酯脂肪酶 D.脂肪细胞中的甘油一酯脂肪酶 E.脂肪细胞中的甘油三酯脂肪酶 【正确答案】E 第42页 初级药师考试辅导 基础知识 关于酮体叙述正确的是 A.酮体是不能为机体利用的代谢产物 B.脂肪动员减少时,肝内酮体生成和输出增多 C.酮体是甘油在肝脏的中间代谢产物 D.肝内生成的酮体主要为肝细胞本身利用 E.肝内生成的酮体主要为肝外组织细胞利用 【正确答案】E 脂肪酸合成的限速酶是 A.肉碱脂酰转移酶I B.脂酰转移酶 C.HMG-CoA合成酶 D.乙酰CoA羧化酶 E.脂肪酸合成酶系 【正确答案】D 胆固醇是下列哪种物质的前体 A.辅酶A B.维生素D C.维生素A D.辅酶Q E.维生素K 【正确答案】B 食物脂肪消化吸收后进入血液的主要方式是 A.脂肪酸和甘油 B.甘油二酯和脂肪酸 C.甘油三酯和脂肪酸 D.乳糜微粒 E.甘油一酯和脂肪酸 【正确答案】D 氨基酸代谢 一、蛋白质的营养作用 (一)氮平衡 1.概念:食物中的含氮物质绝大多数是蛋白质,体内蛋白质代谢的概况可根据氮平衡实验来确定,即测定尿与粪中的含氮量(排出氮)及摄入食物的含氮量(摄入氮)。 2.人体氮平衡有3种情况 (1)氮总平衡:摄入氮=排出氮正常人群 (2)氮正平衡:摄入氮>排出氮孕妇、乳母、康复期患者 (3)氮负平衡:摄入氮<排出氮饥饿、营养不良、衰老、消耗性疾病 (二)必需氨基酸 1.定义:体内需要但自身不能合成,必须由食物供应的氨基酸。 2.8种必需氨基酸:缬异亮亮苯蛋色苏赖 第42页 初级药师考试辅导 基础知识 (借一两本淡色书来) 二、氨基酸的一般代谢 1.氧化脱氨基:L-谷氨酸脱氢酶 2.转氨基作用: 重要的转氨酶:GPT(谷丙转氨酶) GOT(谷草转氨酶) 3.联合脱氨基:转氨酶和谷氨酸脱氢酶的联合。 体内主要的脱氨基方式 4.嘌呤核苷酸循环:主要发生在肌肉中 三、氨的代谢 (一)氨的来源、去路和转运形式 (二)尿素循环 1.组织定位:肝 2.细胞定位:线粒体、胞液 3.简要过程: ①氨基甲酰磷酸的生成,在线粒体内进行,消耗2分子ATP。 ②氨基甲酰磷酸与鸟氨酸缩合形成瓜氨酸,在线粒体内进行。 ③精氨酸的生成,在胞液中进行。 ④尿素的生成,精氨酸水解释放1分子尿素和鸟氨酸,完成鸟氨酸循环。鸟氨酸再重复上述反应。 第42页 初级药师考试辅导 基础知识 4.尿素分子的2个氮来自NH3和Asp(天冬氨酸) 5.生理意义:通过鸟氨酸循环将有毒的氨转变为无毒的尿素排出体外,降低了血氨的浓度,防止氨中毒的发生。 四、个别氨基酸的代谢 (一)一碳单位的代谢 1.定义:某些氨基酸分解代谢过程中产生的含有一个碳原子的基团。 2.载体:四氢叶酸 3.功能:作为嘌呤和嘧啶合成原料 【例题】 不是人体营养必需氨基酸的是 A.苯丙氨酸 B.异亮氨酸 C.瓜氨酸 D.亮氨酸 E.苏氨酸 【正确答案】C 氨在肝中合成的化合物是 A.尿素 B.糖原 C.血浆蛋白 D.胆固醇 E.酮体 【正确答案】A 第42页 初级药师考试辅导 基础知识 丙氨酸-葡萄糖循环由肌肉组织通过血液向肝转运的是 A.葡萄糖 B.氨基酸 C.氨 D.三脂酰甘油 E.胆固醇 【正确答案】B 携带一碳单位的载体是 A.叶酸 B.二氢叶酸 C.四氢叶酸 D.维生素B12 E.维生素B6 【正确答案】C 血氨的主要来源是 A.蛋白质腐败作用 B.体内胺类物质的代谢 C.氨基酸脱氨基作用 D.肾脏中谷氨酰胺的分解 E.氧化脱氨基作用 【正确答案】C 核苷酸代谢 一、嘌呤核苷酸合成代谢 (一)嘌呤核苷酸的从头合成合成途径 1.定位:胞液(肝脏为主,小肠和胸腺其次). 2.原料:天冬氨酸(Asp)、甘氨酸(Gly)、谷氨酰胺(Gln)、CO2、一碳单位、5-磷酸核糖 记忆:天河干,谷农叹气 3.合成特点:磷酸核糖为起始物,逐步加原料合成嘌呤环,形成重要中间产物IMP(次黄嘌呤核苷酸),再由它转变为AMP和GMP。 (二)嘌呤核苷酸的补救合成合成途径 定义:细胞利用现有嘌呤碱或嘌呤核苷重新合成嘌呤核苷酸。 部位:脑、骨髓 第42页 初级药师考试辅导 基础知识等组织 (三)脱氧核糖核苷酸的合成 在NDP(核苷二磷酸)水平上 (四)嘌呤核苷酸的分解代谢 (五)痛风的治疗 第42页 初级药师考试辅导 基础知识 二、嘧啶核苷酸的代谢 (一)嘧啶核苷酸的从头合成途径 1.从头合成途径的原料 *天冬氨酸(Asp) *谷氨酰胺(Gln) *CO2 (二)脱氧胸腺嘧啶核苷酸的合成 在核苷一磷酸水平进行 (三)核苷酸抗代谢物抗代谢物类似物作用6MPIMP抑制IMP转变为AMP、GMP氮杂丝氨酸谷氨酰胺 甲氨蝶呤叶酸抑制二氢叶酸还原酶别嘌呤醇次黄嘌呤抑制黄嘌呤氧化酶,治疗痛风5-氟尿嘧啶胸腺嘧啶抑制胸甘酸合酶阿糖胞苷核苷抑制CDP还原成dCDP 嘌呤、嘧啶核苷酸代谢比较 嘌呤核苷酸嘧啶核苷酸原料天冬氨酸,谷氨酰胺,甘氨酸、CO2,一碳单位天冬氨酸,谷氨酰胺,CO2程序在PRPP的基础上利用各种原料合成嘌呤环各种原料合成嘧啶环,再与PRPP相连抗代谢物6MP,氮杂丝氨酸等5-FU,氮杂丝氨酸代谢产物尿酸β-丙氨酸、β-氨基异丁酸 第42页 初级药师考试辅导 基础知识 【例题】 脱氧核糖核苷酸 A.体内不能合成,必须有食物供给 B.可由dPRPP从头合成 C.由相应核糖核苷酸直接还原合成 D.还原作用发生在二磷酸核苷的水平 E.只能通过补救途径合成 【正确答案】D 5-氟尿嘧啶是哪种化合物的类似物 A.胸腺嘧啶 B.胞嘧啶 C.尿嘧啶 D.二氢尿嘧啶 E.5-甲基胞嘧啶 【正确答案】A 嘌呤降解的终产物是 A.5-磷酸核糖 B.丙酮酸 C.乳清酸 D.尿酸 E.尿素 【正确答案】D 第42页查看更多