- 2021-11-06 发布 |
- 37.5 KB |
- 60页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
江西专版2020年中考化学复习方案第08单元金属和金属材料课件
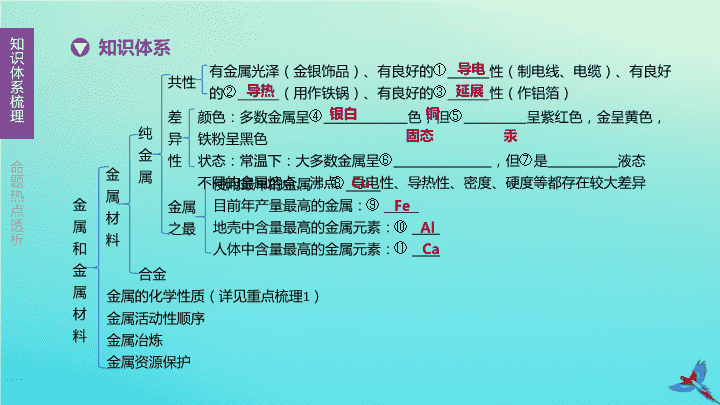
第 8 单元 金属和金属材料 第一篇 基础过关 命题热点透析 知识体系 知识体系梳理 金属和金属材料 金属材料 有金属光泽(金银饰品)、有良好的① ______ 性(制电线、电缆)、有良好的② ______ (用作铁锅)、有良好的③ ______ 性(作铝箔) 共性 颜色:多数金属呈④ 色,但⑤ 呈紫红色,金呈黄色,铁粉呈黑色 状态:常温下:大多数金属呈⑥ ,但⑦是 液态 不同的金属熔点、沸点、导电性、导热性、密度、硬度等都存在较大差异 差异性 使用最早的金属: ⑧ _____ 目前年产量最高的金属:⑨ _____ 地壳中含量最高的金属元素:⑩ ____ 人体中含量最高的金属元素:⑪ ____ 金属之最 纯金属 合金 金属的化学性质(详见重点梳理 1 ) 金属活动性顺序 金属冶炼 金属资源保护 导电 导热 延展 银白 铜 固态 汞 Cu Fe Al Ca 命题热点透析 知识体系 知识体系梳理 金属和金属材料 金属材料 纯金属 合金 金属的化学性质(详见重点梳理 1 ) 金属活动性顺序 金属冶炼 金属资源保护 定义:在金属中加热融合某些金属或非金属制成的具有金属特制的物资,属于⑫ (填物质类别) 特性:与组成合金的纯金属相比,合金硬度更⑬ (相互刻画)、熔点更⑭ 、 抗腐蚀性更⑮ _____ 铁合金:包括生铁(含碳量 2%~4.3% )和钢(含碳量 0.03%~2% ),含碳量不 同,硬度不同,生铁的硬度大于钢的硬度 铁合金:熔点高、密度小;与人体有很好的相容性,可制成人造骨等 常见金属 混合物 大 低 强 命题热点透析 知识体系 知识体系梳理 金属和金属材料 金属材料 金属的化学性质(详见重点梳理 1 ) 金属冶炼 金属资源保护 金属活动顺序 金属的位置越靠前,他的活动性就越⑱ ______ 位于氢前面的金属能置换出盐酸、稀硫酸中的氢 位于前面的金属能把位于后面的金属从其盐溶液中置换出来( K 、 Ca 、 Na 除外) 金属活动性顺序探究及应用(详见专题突破) 置换反应:由一种单质和一种化合物反应,生成⑲ 和⑳ _____________ 的反应。表达式为 A+BC→B+AC 金属活动性顺序 规律 Mg Cu 强 另一种单质 另一种化合物 命题热点透析 知识体系 知识体系梳理 金属和金属材料 金属材料 金属的化学性质(详见重点梳理 1 ) 金属活动性顺序 金属资源保护 金属资源的存在形式:地球上的金属资源广泛存在于地壳和海洋中,除少数不活泼的金 银等以㉑ 形式存在外,其他都以㉒ 形式存在 常见的矿石:赤铁矿(主要成分㉓ )、磁铁矿(主要成分 Fe 3 O 4 )、菱铁矿(主 要成分 FeCO 3 ) 实验室模拟炼铁(详见重点梳理 2 ) 工业炼铁 金属冶炼 单质 化合物 Fe 2 O 3 命题热点透析 知识体系 知识体系梳理 金属和金属材料 金属材料 金属的化学性质(详见重点梳理 1 ) 金属活动性顺序 金属资源保护 金属资源的存在形式 常见的矿石 实验室模拟炼铁(详见重点梳理 2 ) 原理:在高温下,用 CO 作还原剂把铁从其氧化物中还原出来 设备:高炉 原料:铁矿石、焦炭(作用 : ㉔ )、石灰石(除去 SiO2 )和空气 涉及化学方程式: C+O 2 CO 2 、 CO 2 +C 2CO 、 ㉕ ____________________ 工业炼得铁为 ㉖ ,属于 ㉗ (填物质类别) 金属冶炼 工业炼铁 提供热量,提供还原剂 CO 生铁 混合物 命题热点透析 知识体系 知识体系梳理 金属和金属材料 金属材料 金属的化学性质(详见重点梳理 1 ) 金属活动性顺序 金属冶炼 金属资源保护 铁锈蚀:铁与㉘ 和㉙ 发生化学反应生成铁锈;铁锈的主要成分为㉚ , 铁锈很㉛ 不能阻止里层的铁继续与氧气、水等反应,可用除㉜ ____________ 铁锈 铁制品锈蚀条件探究(详见重点梳理 3 ) 保持铁制品㉝ ,如用过的菜刀洗净擦干 在铁制品表面涂保护膜,如涂油、 ㉞ 、搪瓷等 改变内部结构制成合金,如制成㉟ 等 保护金属资源途径:㊱ 、回收利用废旧金属、合理开采矿物、㊲ __________ ___________ 防止铁锈的方法 O 2 H 2 O Fe 2 O 3 · x H 2 O 疏松 稀盐酸 ( 或稀 硫酸 ) 表面的清洁和干燥 刷漆 不锈钢 防止金属锈蚀 寻找金属 的替代品 命题热点透析 重点 梳理 1. 金属的化学性质 知识体系梳理 化学性质 条件及通式 化学方程式 现象及解释 注意 金属与氧 气反应 条件:多数金属能与氧气反应,但反应的难易和剧烈程度不同 通式:金属 + 氧气→金属氧化物 ( 属于 ① 反应 ) Al 与 O 2 反应: ②_________________ ___________________ 铝在常温下与氧 气反应,银白色表面逐渐变暗 铝的抗腐蚀性能好不是因为其化学性质稳定,而是因为铝在常温下与氧气反应生成了致密的 ⑤ Cu 与 O 2 反应: ③ _________________ ___________________ 铜在空气中加热时,生成 ④ 固体 化合 4Al+3O 2 2Al 2 O 3 2Cu+O 2 2CuO 黑色 氧化铝薄膜 命题热点透析 知识体系梳理 (续表) 化学性质 条件及通式 化学方程式 现象及解释 注意 活泼金 属与稀 酸反应 条件:氢前金属 (K 、 Ca 、 Na 除外 ) 通式:金属 + 酸→盐 + 氢气 ( 属于 ⑥_______ 反应 ) 镁与稀盐酸、稀硫酸反应: ⑦__________________________ ⑧ __________________________ 剧烈反应,产生大量 ⑨ ,放出大量热 铁与酸反应生成的盐为亚铁盐 ( 即铁的化合价为 +2) 金属与酸反应后,溶液的质量均增加 铁与稀盐酸、稀硫酸反应: ⑩ __________________________ ⑪ _________________________ 反应较缓慢,产生气泡,溶液由无色 变为 ⑫ _______ 色 置换 气泡 浅绿 命题热点透析 知识体系梳理 (续表) 化学性质 条件及通式 化学方程式 现象及解释 注意 金属与 某些可 溶性盐 溶液反应 条件:前置换后 (K 、 Ca 、 Na 除外 ) ,盐可溶 通式:金属 + 盐→新盐 + 新金属 ( 属于 ⑬ 反应 ) Fe 与 CuSO 4 溶液反应 : ⑭ _________________________ 铁表面 有 ⑮ 色固体生成,溶液 由 ⑯ 色 变为浅绿 色 铁与酸反应生成的盐为亚铁盐 ( 即铁的化合价为 +2) 金属与酸反应后,溶液的质量均增加 置换 红 蓝 命题热点透析 知识体系梳理 (续表) 化学性质 条件及通式 化学方程式 现象及解释 注意 金属与 某些可 溶性盐 溶液反应 条件:前置换后 (K 、 Ca 、 Na 除外 ) ,盐可溶 通式:金属 + 盐→新盐 + 新金属 ( 属于 ⑬ 反应 ) Cu 与 AgNO 3 溶液反应 : ⑰ ______________________ _________________________ 铜的表面 有 ⑱ 色 物质生成,溶液由无色 变为 ⑲ 色 铁与酸反应生成的盐为亚铁盐 ( 即铁的化合价为 +2) 金属与酸反应后,溶液的质量均增加 置换 银白 蓝 命题热点透析 知识体系梳理 (续表) 化学性质 条件及通式 化学方程式 现象及解释 注意 金属与 某些可 溶性盐 溶液反应 条件:前置换后 (K 、 Ca 、 Na 除外 ) ,盐可溶 通式:金属 + 盐→新盐 + 新金属 ( 属于 反应 ) Al 与 CuSO 4 溶液 反应: ⑳ __________________________________________________ 铝表面 有 ㉑ 色物质生成,溶液由蓝色 变为 ㉒ ____ 色 铁与酸反应生成的盐为亚铁盐 ( 即铁的化合价为 +2) 金属与酸反应后,溶液的质量均增加 置换 +3Cu 红 无 命题热点透析 知识体系梳理 2. 实验室模拟炼铁 实验装置 实验原理 ㉓_____________________________________ 命题热点透析 知识体系梳理 (续表) 实验步骤 (1) 先通纯净的 CO 一段时间——原因 : ㉔ _________________________________ ____________ (2) 再点燃酒精喷灯,给 Fe 2 O 3 加热——目的:使氧化铁和一氧化碳发生反应 (3) 实验结束,先停止加热再停止通入 CO(CO 早出晚归,酒精喷灯迟到早退 ) ——原因:一 是 ㉕ ;二 是 ㉖ ____________________________ 排尽玻璃管内的空气, 防止加热 时发生爆炸 防止液体倒吸 防止新生成的铁在较高温度 下被空气中的氧气再次氧化 命题热点透析 知识体系梳理 (续表) 实验现象 玻璃管内 : ㉗ 试管中 : ㉘ 最右端导管口: 有 ㉙ 色 火焰产生 实验反思 一氧化碳是有毒气体,本实验尾气处理方法 是 ㉚ , 还可以用气囊收集 该实验可验证 CO 的 ㉛ 、 ㉜ 的化学性质 红棕色粉末变为黑色 澄清石灰水变浑浊 蓝 点燃 还原性 可燃性 命题热点透析 知识体系梳理 3. 铁制品锈蚀条件探究 编号 Ⅰ Ⅱ Ⅲ 实验图示 生锈程度 ㉝________ ㉞_______ ㉟_______ 对比分析 实验 Ⅰ 、 Ⅲ 说明铁生锈一定 与 ㊱ 有关 实验 Ⅱ 、 Ⅲ 说明铁生锈一定 与 ㊲ 有关 实验 Ⅰ 蒸馏水煮沸后使用的原因 是 ㊳ 不生锈 不生锈 生锈 O 2 H 2 O 除去水中溶解的氧气 命题热点透析 知识体系梳理 (续表) 编号 Ⅰ Ⅱ Ⅲ 结论 分析对比实验 Ⅰ 、 Ⅱ 、 Ⅲ 可知,铁生锈的条件 是 ㊴____________________ Fe 与 O 2 、 H 2 O 同 时 接触 命题热点透析 易错判断 1. 合金一定是由两种或多种金属熔合而成 ( ) 2. 合金都是混合物,属于合成材料 ( ) 3. 金刚石、生铁、氧化铁、磁铁矿都是合金 ( ) 4. “真金不怕火炼”说明金的化学性质稳定 ( ) 5. 铝具有良好的抗腐蚀性是因为铝很难与氧气发生反应 ( ) 6. 铁丝在氧气中剧烈燃烧,火星四射,生成黑色的氧化铁 ( ) 7. 铁与稀盐酸反应: 2Fe+6HCl 2FeCl 3 +3H 2 ↑ ( ) 8. 经常用钢丝球擦洗铝锅表面以保持其清洁 ( ) 知识体系梳理 × × × √ × × × × 命题热点透析 9. 为防止铁生锈必须同时隔绝氧气和水 ( ) 10. 高炉炼铁得到的产物是纯铁 ( ) 11. 有一种单质和一种化合物生成的反应一定是置换反应 ( ) 12. 置换反应前后,一定存在元素化合价的变化 ( ) 知识体系梳理 × × × √ 命题热点透析 知识体系梳理 化学方程式网络构建 图 8-1 ( 答案不唯一,合理即可 ) ① ; ② ; 命题热点透析 ③ ; ④ ; ⑤ ; ⑥ ; ⑦ ; ⑧ ; ⑨ ; ⑩ 。 知识体系梳理 知识体系梳理 命题热点透析 考向一 金属材料 ( 6 年 2 考 ) 1. [2018· 江西 ] 常温下为液态的金属是 ( ) A. 汞 B. 金 C. 银 D. 铝 A 知识体系梳理 命题热点透析 2. [2012· 江西 ] 下列生活用品用金属材料制作而成的是 ( ) 图 8-2 [ 答案 ] B [ 解析 ] 陶瓷、玻璃属于无机非金属材料;塑料属于有机合成材料。 知识体系梳理 命题热点透析 3. [2017 ·江西 ] 如图 8-3 所示的自行车的材料中属于金属材料的是 ( 填序号,选一个即可,下同 ) ,属于有机合成材料的是 。 图 8-3 ②( 或 ③) ①( 或 ④) 知识体系梳理 命题热点透析 4. [2013 ·江西 ] 将黄铜片和纯铜片相互刻画,发现纯铜片表面留下较深的划痕,则它们的硬度大小关系是:黄铜 ( 填“ > ”“ < ”或“ = ” ) 纯铜。 > 知识体系梳理 命题热点透析 5. 拓展 [2019· 衡阳 ] 下列有关金属材料的说法中,正确的是 ( ) A. 地壳中含量最高的金属元素是铁 B. 钢的性能优良,所以钢是很纯的铁 C. 多数合金抗腐蚀性比组成它们的纯金属更好 D. 银的导电性最好,大多数电线都是用银作材料 [ 答案 ] C [ 解析 ] 地壳中含量最多的前五种元素:氧、硅、铝、铁、钙,地壳中含量最多的金属元素是铝;钢是铁的合金,含碳量为 0.03%~2% ,不是纯铁;多数合金的抗腐蚀性能比组成它们的纯金属更好;尽管银的导电性比铜强,但是由于银的价格较高,一般不用银作电线。 知识体系梳理 命题热点透析 考向二 金属的化学性质 ( 6 年 3 考 ) 6. [2011 ·江西 ] 有等质量的 A 、 B 两种金属,相对原子质量 A r (A)< A r (B) ,将 A 放入质量分数为 15% 的稀硫酸中, B 放入质量分数为 15% 的稀盐酸中,在反应中 A 、 B 均为正二价,产生氢气的质量随反应时间变化的曲线如图 8-4 所示。下列说法正确的是 ( ) 图 8-4 A. 产生氢气的速率 AFe>Zn B. 三种金属的相对原子质量: Mg查看更多