2020高考化学冲刺600分考前仿真冲刺卷五含解析
考前仿真冲刺卷(五)
1.本卷包括选择题和非选择题两部分,共100分,建议用时50分钟。
2.可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 Al-27 S-32 Cl-35.5 K-39 Fe-56 Cu-64 I-127
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
7.化学与生产和生活密切相关,下列有关说法正确的是( )
A.英文的“中国”一词又指“瓷器”,中国瓷器驰名世界,其主要成分SiO2
B.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
C.二氧化硫有毒,严禁将其添加到任何食品和饮料中
D.泡沫灭火器中用的是小苏打和硫酸铝
答案:D
解析:A项“瓷器”为硅酸盐产品,其主要成分不是SiO2,错误;B防止食品氧化变质应加还原剂,而生石灰为干燥剂,错误;C项葡萄酒中含有少量SO2,可起到杀菌作用,但含量较低,错误;D项中泡沫灭火器的工作原理为Al3++3HCO===Al(OH)3↓+3CO2↑,对应药品为NaHCO3和Al2(SO4)3,正确。
8.下列有关有机化合物的说法正确的是( )
A.乙酸乙酯和油脂互为同系物
B.油脂的皂化、硬化均为水解反应
C.C4H9Cl的同分异构体的数目为4
D. 属于不饱和烃,分子式均为C4H8
答案:C
解析:乙酸乙酯是乙酸和乙醇形成的酯,而油脂是高级脂肪酸和甘油形成的酯,二者不互为同系物,A项错误;油脂的皂化为水解反应,油脂的硬化为加成反应,B项错误;C4H10的同分异构体有CH3CH2CH2CH3、CH3CH(CH3)CH3,二者的一氯代物均有2种,故C4H9Cl的同分异构体的数目为4,C项正确; 属于饱和烃,D项错误。
9.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单气态氢化物的水溶液可使酚酞溶液变红,X是地壳中含量最大的元素,Y的族序数等于周期序数,Z的原子半径是同周期主族元素中最小的。下列说法正确的是( )
13
A.简单离子半径:W
Ka(HClO)>Ka2(H2CO3),少量CO2通入NaClO溶液中:CO2+H2O+2ClO-===2HClO+CO
正确;CO2少量时生成正盐
C
Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++2HCO+2OH-===MgCO3↓+CO+2H2O
正确;酸式盐与碱反应生成正盐和水
D
28 g Fe加入到含1.6 mol HNO3的稀硝酸中:5Fe+16H++4NO===2Fe3++3Fe2++4NO↑+8H2O
正确;Fe被氧化生成的Fe3+、Fe2+的物质的量之比为2:3
答案:D
解析:Fe3O4和氢碘酸发生氧化还原反应:Fe3O4+8H++2I-===3Fe2++I2+4H2O,A项错误;酸性:H2CO3>HClO>HCO,少量CO2通入NaClO溶液中:CO2+H2O+ClO-===HClO+HCO,B项错误;Mg(OH)2比MgCO3更难溶,Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++2HCO+4OH-===Mg(OH)2↓+2CO+2H2O,C项错误;0.5 mol Fe与1.6 mol HNO3反应,Fe被氧化为Fe3+、Fe2+,5Fe+16H++4NO===2Fe3++3Fe2++4NO↑+8H2
13
O符合得失电子守恒、电荷守恒和原子守恒,D项正确。
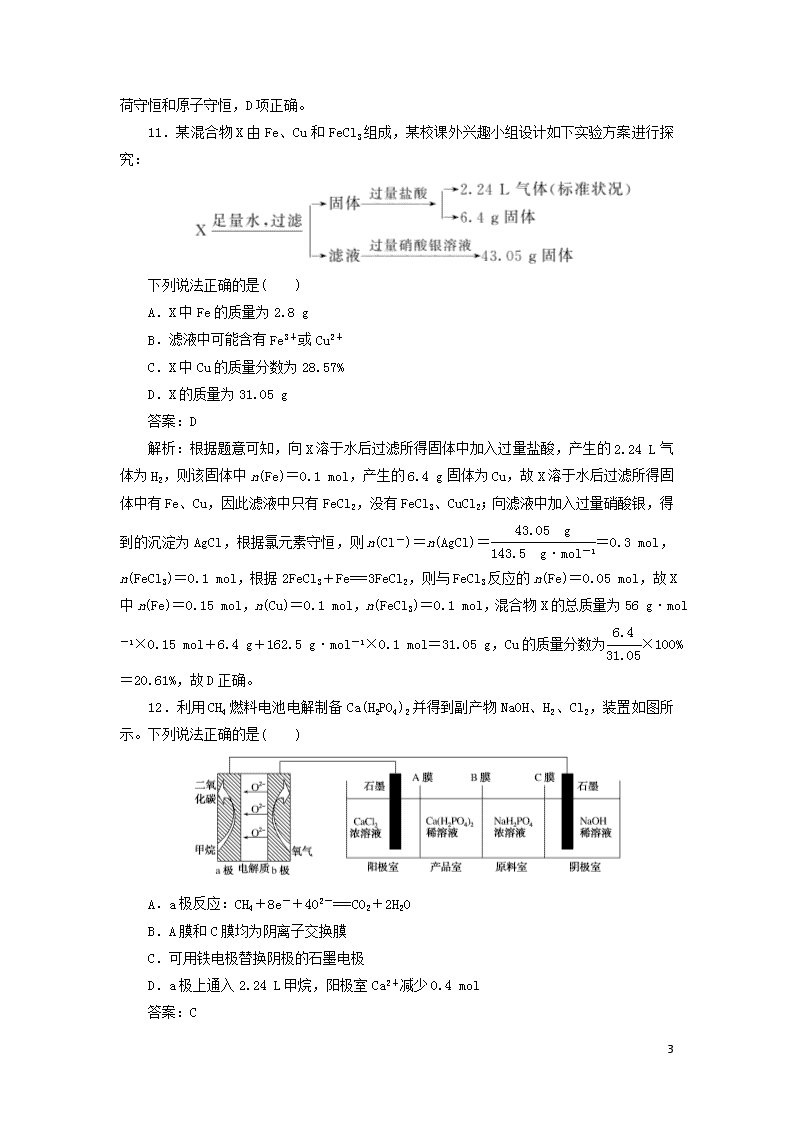
11.某混合物X由Fe、Cu和FeCl3组成,某校课外兴趣小组设计如下实验方案进行探究:
下列说法正确的是( )
A.X中Fe的质量为2.8 g
B.滤液中可能含有Fe3+或Cu2+
C.X中Cu的质量分数为28.57%
D.X的质量为31.05 g
答案:D
解析:根据题意可知,向X溶于水后过滤所得固体中加入过量盐酸,产生的2.24 L气体为H2,则该固体中n(Fe)=0.1 mol,产生的6.4 g固体为Cu,故X溶于水后过滤所得固体中有Fe、Cu,因此滤液中只有FeCl2,没有FeCl3、CuCl2;向滤液中加入过量硝酸银,得到的沉淀为AgCl,根据氯元素守恒,则n(Cl-)=n(AgCl)==0.3 mol,n(FeCl3)=0.1 mol,根据2FeCl3+Fe===3FeCl2,则与FeCl3反应的n(Fe)=0.05 mol,故X中n(Fe)=0.15 mol,n(Cu)=0.1 mol,n(FeCl3)=0.1 mol,混合物X的总质量为56 g·mol-1×0.15 mol+6.4 g+162.5 g·mol-1×0.1 mol=31.05 g,Cu的质量分数为×100%=20.61%,故D正确。
12.利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法正确的是( )
A.a极反应:CH4+8e-+4O2-===CO2+2H2O
B.A膜和C膜均为阴离子交换膜
C.可用铁电极替换阴极的石墨电极
D.a极上通入2.24 L甲烷,阳极室Ca2+减少0.4 mol
答案:C
13
解析:a极为负极,负极上甲烷发生氧化反应:CH4-8e-+4O2-===CO2+2H2O,A项错误;根据利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2和Cl2,可知阳极室的电极反应:2Cl--2e-===Cl2↑,则阳极室内Ca2+向产品室移动,A膜为阳离子交换膜,阴极室的电极反应:2H2O+2e-===2OH-+H2↑,则原料室内Na+向阴极室移动,C膜为阳离子交换膜,B项错误;阴极电极不参与反应,可用铁电极替换阴极的石墨电极,C项正确;没有指明标准状况下,无法计算,D项错误。
13.pC类似于pH,指极稀溶液中溶质浓度的负对数。如图为25 ℃时H2CO3溶液中各微粒的pC—pH图(若离子浓度小于10-5 mol·L-1,可认为该离子不存在)。下列说法错误的是( )
A.向Na2CO3溶液中滴加盐酸,溶液中总是存在:c(Na+)+c(H+)=2c(CO)+c(OH-)+c(HCO)+c(Cl-)
B.当c(HCO):c(H2CO3)=1:1时,此时溶液中H2CO3的电离程度小于HCO的水解程度
C.Kal(H2CO3)·Ka2(H2CO3)c(HCO)>c(CO)>c(OH-)>c(H+)
答案:B
解析:向Na2CO3溶液中滴加盐酸,溶液中始终存在电荷守恒的关系式:c(Na+)+c(H+)=2c(CO)+c(OH-)+c(HCO)+c(Cl-),A正确;由题图可知,当c(HCO):c(H2CO3)=1:1时,溶液的pH=6,溶液显酸性,H2CO3的电离使溶液显酸性,HCO的水解使溶液显碱性,所以此时H2CO3的电离程度大于HCO的水解程度,故B错误;由题图可知,溶液pH=6时,c(H2CO3)=c(HCO),则Kal(H2CO3)==1×10-6,溶液pH=10.5时,c(HCO)=c(CO),则Ka2(H2CO3)==1×10-10.5,Kal(H2CO3)·Ka2(H2CO3)=1×10-6×1×10-10.5<1×10-14=Kw,故C正确;25 ℃时,0.1 mol·L-1 Na2CO3和0.1 mol·L-1 NaHCO3的混合溶液呈碱性,由以上分析得到的H2CO3的Kal与Ka2可知,HCO的电离可忽略不计,又CO的水解程度大于HCO的水解程度,故离子浓度的大小关系为c(Na+)>c(HCO)>c(CO)>c(OH-)>c(H+),D正确。
13
二、非选择题:包括必考题和选考题两部分。第26~28题为必考题,每个试题考生都必须作答。第35~36题为选考题,考生根据要求作答。
(一)必考题(共43分)
26.(14分)硫代硫酸钠俗称大苏打,是一种重要的化工产品,某兴趣小组设计以下装置(部分夹持装置省略)制备硫代硫酸钠晶体(Na2S2O3·5H2O):
回答下列问题:
(1)仪器A的名称是____________,装置D的作用是____________。
(2)装置C中反应生成Na2S2O3和CO2,用化学方程式表示该反应________。
(3)以下实验步骤最合理的顺序是________(填序号)。
①按图示往各仪器中加入试剂
②打开C中分液漏斗旋塞,向三颈烧瓶内加入Na2S与Na2CO3的混合溶液
③连接装置并检查装置气密性
④向A中滴加70% H2SO4溶液
⑤取出C中混合物,经一系列操作得到产品
(4)装置E为尾气吸收装置,实验结束后装置E中的溶质有NaOH、Na2CO3、Na2SO3,还可能有________(填化学式),设计实验证明该物质的存在________。
答案:
(1)圆底烧瓶(2分) 作安全瓶(或防倒吸)(2分)
(2)4SO2+2Na2S+Na2CO3===3Na2S2O3+CO2(3分)
(3)③①④②⑤(2分)
(4)Na2SO4(2分) 先取少量E中溶液于试管中,加入足量稀盐酸,再滴加氯化钡溶液,若有白色沉淀生成,则含有硫酸钠(3分)
解析:(1)装置D作安全瓶,可以防止装置E中溶液倒吸入装置C。(2)依题意,Na2S和Na2CO3与通入的二氧化硫反应生成Na2S2O3和CO2,该反应的化学方程式为4SO2+2Na2S+Na2CO3===3Na2S2O3+CO2。(3)首先连接好实验装置,并检查装置的气密性,添加药品,先向A中滴加70%硫酸,产生的气体将装置中空气排尽后,再向C中加入Na2S和Na2CO3的混合溶液,取出C中反应得到的含产品的混合物,最后经一系列操作得到产品。(4)根据题图知,装置E中盛放的是氢氧化钠溶液,吸收二氧化碳和二氧化硫后,溶质有NaOH、Na2CO3、Na2SO3、Na2SO3在空气中易被氧化成Na2SO4,检验Na2SO4
13
的存在,可取少量装置E中的溶液于试管中,向其中加入足量稀盐酸,再滴加氯化钡溶液,若有白色沉淀生成,说明含有Na2SO4。
27.(14分)钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
已知:①还原性:Cl->Co2+;
②Fe3+和C2O结合生成较稳定的[Fe(C2O4)3]3-,在强酸性条件下分解重新生成Fe3+。回答下列问题:
(1)废旧电池初步处理为粉末状的目的是
________________________________________________________________________。
(2)从含铝废液得到Al(OH)3的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(3)滤液A中的溶质除HCl、LiCl外还有________(填化学式)。写出LiCoO2和盐酸反应的化学方程式
________________________________________________________________________
________________________________________________________________________。
(4)滤渣的主要成分为________________(填化学式)。
(5)在空气中加热一定质量的CoC2O4·2H2O固体样品时,其固体失重率数据见下表,请补充完整表中问题。
已知:①CoC2O4在空气中加热时的气体产物为CO2。
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
序号
温度范围/℃
化学方程式
固体失重率
Ⅰ
120~220
CoC2O4·2H2O CoC2O4+2H2O
19.67%
Ⅱ
300~350
______________
59.02%
(6)已知Li2CO3的溶度积常数Ksp=8.64×10-4,将浓度为0.02 mol·L-1的Li2SO4和浓度为0.02 mol·L-1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为________ mol·L-1。
13
(7)从FeCl3溶液得到FeCl3·6H2O固体的操作关键是
________________________________________________________________________。
答案:
(1)增大接触面积,加快反应速率,提高浸出率(2分)
(2)AlO+CO2+2H2O===Al(OH)3↓+HCO(2分)
(3)FeCl3、CoCl2 (1分) 2LiCoO2+8HCl===2CoCl2+Cl2↑+4H2O+2LiCl(2分) (4)C(1分) (5)2CoC2O4+O22CoO+ 4CO2(2分)
(6)0.02(2分)
(7)加入适量盐酸(或通入适量氯化氢气体)(2分)
解析:(1)废旧电池初步处理为粉末状是为了增大接触面积,加快反应速率,提高浸出率。(2)从含铝废液得到Al(OH)3的离子方程式为:AlO+CO2+2H2O===Al(OH)3↓+HCO。(3)滤液A中溶质除HCl、LiCl外还有FeCl3、CoCl2,LiCoO2与盐酸反应的化学方程式为:2LiCoO2+8HCl===2CoCl2+Cl2↑+4H2O+2LiCl。(4)滤渣主要成分为C。(5)CoC2O4在空气中加热生成CO2,反应化学方程式为:2CoC2O4+O22CoO+4CO2。(6)c(Li+)=0.02 mol/L,c(CO)=0.01 mol/L,Qc=c2(Li+)·c(CO)=4×10-6<8.64×10-4,无沉淀生成,因此c(Li+)=0.02 mol/L。(7)从FeCl3溶液得到FeCl3·6H2O固体过程中,由于HCl具有挥发性,因此要加入适量盐酸或通入适量氯化氢气体。
28.(15分)磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1)已知:25 ℃时,磷酸和氢氟酸的电离常数如下表所示。
物质
H3PO4
HF
电离常数
Ka1=7.1×10-3;
Ka2=6.3×10-8;
Ka3=4.2×10-13
Ka=6.6×10-4
向NaF溶液中滴加少量H3PO4溶液,反应的离子方程式为
________________________________________________________________________。
(2)已知:
Ⅰ.CaO(s)+H2SO4(l)CaSO4(s)+H2O(l) ΔH=-271 kJ·mol-1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1
则:
①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为____________。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率________(填“增大”“减小”或“不变”,下同);HF的平衡浓度________。
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物CO可用于制备H2
13
,原理为CO(g)+H2O(g)CO2(g)+H2(g) ΔH。
①一定温度下,向10 L密闭容器中充入0.5 mol CO和1 mol H2O(g),2 min达到平衡时,测得0~2 min内用CO2表示的反应速率v(CO2)=0.02 mol·L-1·min-1。则CO的平衡转化率α=________;该反应的平衡常数K=________。
②在压强不变的密闭容器中发生上述反应,设起始的=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH________0(填“>”“<”或“=”,下同)。a________1,理由为
________________________________________________________________________
________________________________________________________________________。
答案:
(1)H3PO4+F-===H2PO+HF(2分)
(2)①Ca5(PO4)3F(s)+5H2SO4(l)3H3PO4(l)+HF(g)+5CaSO4(s) ΔH=-418 kJ/mol(2分) ②增大(1分) 不变(1分)
(3)①80%(2分) 8/3(2分) ②<(1分) <(2分) 相同温度下,n(CO)/n(H2O)越小,CO的转化率越大,其平衡体积分数越小(2分)
解析:(1)由于Ka2Al>Na(2分)
(3)CaCl2(1分) sp2(2分) 平面三角形(1分)
(4)BaO2(2分) 6(2分) (3分)
解析:(1)该物质中铍元素化合价为+2,铍元素基态原子的价电子排布式为2s2。(2)镁原子的最外层能级为全充满状态,性质稳定,三者中镁的第一电离能最大。(3)CaCl2只含有离子键,CaCO3、CaSO4、Ca(OH)2中均含有离子键和极性共价键;CO中碳原子的成键电子对数为3,无孤电子对,采取sp2杂化,CO的空间构型为平面三角形。(4)晶胞中Ba2+位于晶胞的顶点和面心,晶胞中Ba2+的个数为8×1/8+6×1/2=4,阴离子位于晶胞的棱上和体心,晶胞中O的个数为12×1/4+1=4,所以晶胞中Ba2+与O的个数比为1:1,该化合物为BaO2。由晶胞结构可知,Ba2+的配位数为6。晶胞的体积为a3 cm3,一个晶胞中共含有4个BaO2,则晶体的密度为g·cm-3=g·cm-3。
13
36.[化学——选修5:有机化学基础](15分)
有机物J是合成药物格列卫的一种重要中间体,J的一种合成路线如下:
13
回答下列问题:
(1)B的名称为________。
(2)H→I和I→J的反应类型分别为________、________。
(3)G的结构简式为________。
(4)由E生成F的化学方程式为
________________________________________________________________________。
(5)芳香化合物X是E的同分异构体,X能发生银镜反应,并能发生水解反应,其核磁共振氢谱有4组峰,峰面积之比为1:4:2:1,写出符合条件的X的结构简式
________________________________________________________________________
________________________________________________________________________。
(6)写出用甲苯为原料制备聚合物的合成路线:
________________________________________________________________________
________________________________________________________________________。
答案:
(1)对硝基甲苯(或4硝基甲苯)(2分)
(2)还原反应(2分) 加成反应(2分)
(3) (2分)
(4) (2分)
(5) (2分)
13
(6) (3分)
解析:
(1)根据A、C的分子式、D的结构简式及转化关系可知,A为甲苯,B为对硝基甲苯,C为对氨基甲苯。
(2)H转化为I,发生了还原反应。I→J为加成反应。
(3)对比F与H的结构可知,F→H发生了取代反应,再结合G的分子式可推知G的结构简式为。
(5)X是E的同分异构体,能发生银镜反应,并能发生水解反应,说明含有“”,核磁共振氢谱显示有4组峰,峰面积之比为1:4:2:1,则符合条件的X为
13
13