2020届高考化学二轮复习专题十七电解池原理及应用含解析
专题十七 电解池原理及应用
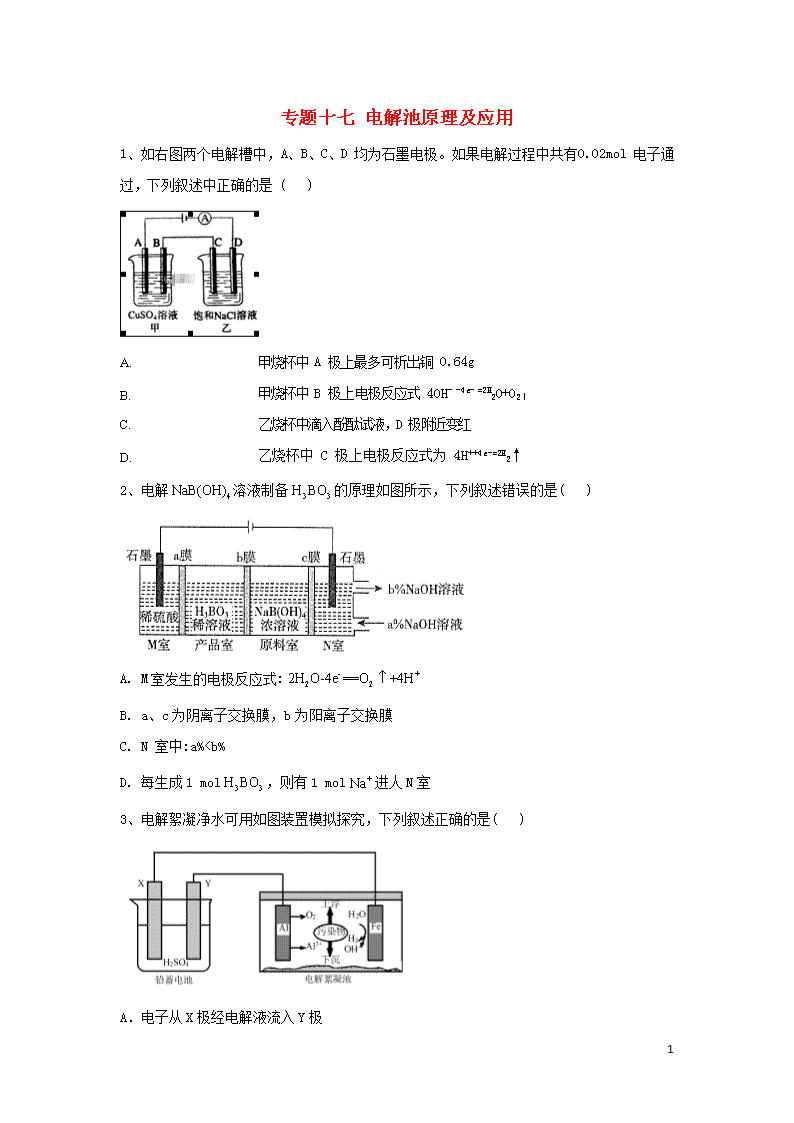
1、如右图两个电解槽中,A、B、C、D 均为石墨电极。如果电解过程中共有 0.02mol 电子通过,下列叙述中正确的是( )
A. 甲烧杯中 A 极上最多可析出铜 0.64g
B. 甲烧杯中 B 极上电极反应式 4OH- -4e- =2H2O+O2↑
C. 乙烧杯中滴入酚酞试液,D 极附近变红
D. 乙烧杯中 C 极上电极反应式为 4H++4e-=2H2↑
2、电解溶液制备的原理如图所示,下列叙述错误的是( )
A. M室发生的电极反应式:
B. a、c为阴离子交换膜,b为阳离子交换膜
C. N 室中:a%
a%>b%
D. 标准状况下,甲电极上每消耗22.4L气体时,理论上有4mol K+移入阴极区
7、电解法处理和混合污染气的原理如下图所示,电解质为熔融碳酸盐和硫酸盐,通电一段时间后,Ni电极表面形成掺杂硫的碳积层。下列说法错误的是( )
A. Ni电极表面发生了还原反应
B. 阳极的电极反应为:
C. 电解质中发生的离子反应有:
D. 该过程实现了电解质中碳酸盐和硫酸盐的自补充循环
8、铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图。若上端开口关闭,可得到强还原性的(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的(烃基自由基)。下列说法错误的是( )
15
A.无论是否鼓入空气,负极的电极反应式均为
B.不鼓入空气时,正极的电极反应式为
C.鼓入空气时,每生成1mol 有2 mol电子发生转移
D.处理含有草酸()的污水时,上端开口应打开并鼓入空气
9、用电解法处理含的废水,探究不同因素对含废水处理的影响,结果如表所示(的起始浓度、体积、电压、电解时间均相同)。下列说法错误的是( )
实验
i
ii
iii
iv
是否加入Fe2(SO4)3
否
否
加入30g
否
是否加入H2SO4
否
加入1mL
加入1mL
加入1mL
阴极村料
石墨
石墨
石墨
石墨
阳极材料
石墨
石墨
石墨
铁
的去除率
0.092%
12.7%
20.8%
57.3%
实验iii中Fe3+去除的机理
A. 实验ⅱ与实验i对比,其他条件不变,增加c(H+)有利于的去除
B. 实验ⅲ与实验ⅱ对比,其他条件不变,增加c(Fe3+)有利于的去除
C. 实验ⅳ中Fe2+循环利用提高了的去除率
D. 若实验ⅳ中去除0.01mol ,生成的阳离子全部转化成沉淀,则沉淀的质量是2.06g
15
10、如图为一定条件下采用多孔惰性电极的储氢电池充电装置(忽略其他有机物)。已知储氢装置的电流效率,下列说法不正确的是( )
A.若η=75%,则参加反应的苯为0.8mol
B.过程中通过C-H键断裂实现氢的储存
C.采用多孔电极增大了接触面积,可降低电池能量损失
D.生成目标产物的电极反应式为:
11、图甲是一种利用微生物将废水中的尿素[CO(NH2)2]转化为环境友好物质的原电池装置示意图,利用该电池在图乙装置中的铁上镀铜。下列说法正确的是( )
A. 图乙中Fe电极应与图甲中Y相连接
B. 图甲中H+透过质子交护膜由右向左移动
C. 图甲中M 电极反应式:CO(NH2)2+5H2O-14e=CO2+2NO2+14H+
D. 当图甲中M 电极消耗0.5mol尿素时,图乙中铁电极增重96g
12、某模拟"人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
15
A.该装置将化学能转化为光能和电能
B.该装置工作时,H+从b极区向a极区迁移
C.每生成1mol O2,有44g CO2被还原
D.a电极的反应为:3CO2 + 16H+-18e-= C3H8O+4H2O
13、某课外活动小组同学用如图装置进行实验,试回答下列问题:
(1)若开始时开关K与a连接,则B极的电极反应式为___________________。
(2)若开始时开关K与b连接,则B极的电极反应式为________________。
总反应的离子方程式为__________________________。
有关上述实验,下列说法正确的是(填序号)_________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生22.4L气体,则溶液中转移2mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
15
①该电解槽的阳极反应式为__________________________ 。
此时通过阴离子交换膜的离子数________(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数
②通电开始后,阴极附近溶液pH会增大,请简述原因:____________________________。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为_____________________。
14、电化学知识在物质制备领域的应用前景看好。
(1)从环境保护的角度看,制备一种新型多功能水处理剂高铁酸钠(Na2FeO4)较好的方法为电解法,其装置如图①所示:
①电解过程中阳极的电极反应式为______________________;
②“镁一次氯酸盐”燃料电池可为图①装置提供电能,该电池电极为镁合金和铂合金,其工作原理如图②所示。b为该燃料电池的______(填“正"或“负")极。当有16.6g Na2FeO4生成时消耗ClO-的物质的量为_____mol;
(2)电解Na2SO4溶液生产H2SO4和烧碱的装置如图③所示(已知:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过),其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1:2。则丁为_______;电解一段时间,当产生0.1mol气体甲时,通过离子交换膜f的离子的质量为_____g。
(3)用0.1032mol/L的NaOH溶液滴定未知浓度的稀盐酸,实验数据如下表:
实验序号
消耗NaOH溶液的体积/mL
待测稀盐酸的体积/mL
1
28.84
25.00
15
2
27.83
25.00
3
27.85
25.00
根据表格计算c(HCl)=_______。在上述滴定过程中,若滴定前碱式滴定管下端尖嘴中无气泡,滴定后有气泡,则测定结果将_______(填“偏大”、“偏小”或“不影响”)。
15、阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:
(1)电解饱和食盐水的化学方程式为 。
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是 (填字母序号)。
a. b. c.热空气吹出 d降低阳极区液面上方的气压
(3)食盐水中的若进入电解槽,可被电解产生的氧化为IC1,并进一步转化为,可继续被氧化为高碘酸根(),与结合生成溶解度较小的沉积于阳离子交换膜上,影响膜的寿命。
①从原子结构的角度解释IC1中碘元素的化合价为+ 1价的原因: 。
②,被氧化为,的化学方程式为 。
(4)在酸性条件下加入NaCIO溶液,可将食盐水中的转化为,再进一步除去。通过测定体系的吸光度,可以检测不同pH下的生成量随时间的变化,如图所示。已知:吸光度越高表明该体系中越大。
15
①结合化学用语解释10 min时pH体系吸光度不同的不同原因: 。
② pH = 4.0时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因
: 。
③研究表明食盐水中含量<0.2 mg • L -1时对离子交换膜影响可忽略。现将1 m3含浓度为1.47 mg. L-1的食盐水进行处理,为达到使用标准,理论上至少需要0.05 mol • L-1NaCIO溶液 L。(已知NaCIO的反应产物为NaCl,溶液体积变化忽略不计)
答案以及解析
1答案及解析:
答案:C
解析:
2答案及解析:
答案:B
15
解析:该装置有外加电源,因此该装置为电解池, 左端石墨为阳极,根据电解原理,阳极反应式为,产品室得到产品,因此a膜为 阳离子交换膜,右端石墨为阴极,根据电解原理,阴极反应式为,c膜为阳离 子交换膜;A. M室中石墨电极为阳极,电解时阳极上 水失电子生成和,电极反应式为,故A说法正确;B.原料室中的B通过b膜进入产品室,M室中氢离子通入a 膜进入产品室,原料室中的通过c膜进入N室, 则a、c为阳离子交换膜,b为阴离子交换膜,故B说法错误;C. N室中石墨为阴极,电解时阴极上水得电子生成原料室中的钠离子通过c膜进入 N室,溶液中c(NaOH)增大,所以N室:
a%
查看更多