- 2021-07-06 发布 |
- 37.5 KB |
- 15页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高二化学教案:第4讲-有机物性质梳理
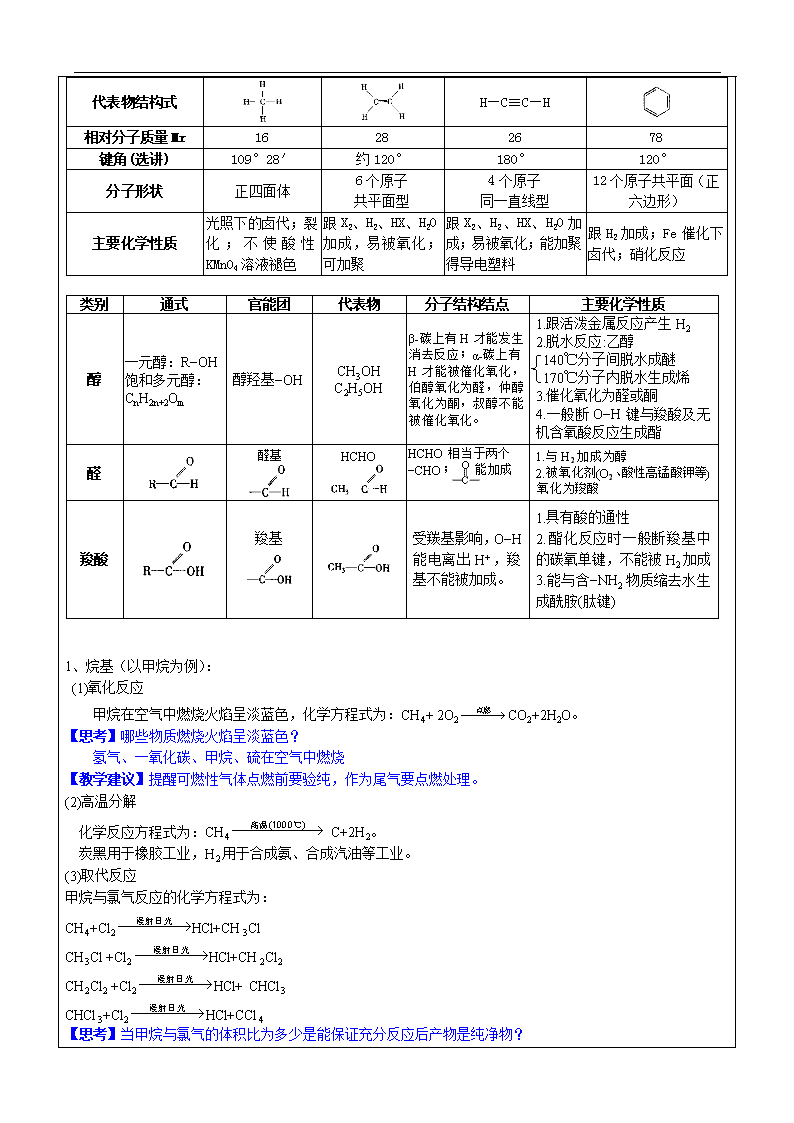
辅导教案 学员姓名: 学科教师: 年 级: 辅导科目: 授课日期 ××年××月××日 时 间 A / B / C / D / E / F段 主 题 有机物性质梳理 教学内容 本次课的重点、难点,需要掌握的方法技巧 1.复习官能团的性质; 2.复习官能团间的转换关系,理解官能团对分子化学性质的影响; 3.掌握同分异构体的书写技巧。 【预习作业】如何证明苯环不是单、双键交替的结构? ①苯的邻位二取代物只有一种 ②苯分子中碳碳键的长度均相等(即分子中两个碳碳原子的核间距离) ③苯不能使酸性KMnO4溶液、溴水褪色 ④苯在FeBr3存在的条件下同液溴发生取代反应 【教学建议】对于没有完成这部分内容的学生应该点名批评。可以深入讲解甲烷的空间结构证明方法,根据学生预习情况,给每位学生基准分5分、3分、1分。 【具体操作】独立思考+小组讨论。建议用时10分钟。学生先独立思考完成,可以采用由某一个学生分享他的答案,与其他两位同学比较,对于不同的选项让学生间相互分析、比较,教师负责正误的判断以及学生讨论过程中的引导,侧重引导学生相关探讨、共同分析问题的习惯。主动分享的学生加2分。补充的学生每次1分。 1、北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是 A.含有碳碳双键、苯环、羟基、羰基 B.含有苯环、羟基、羰基、羧基 C.能发生氧化,取代,加成,消去反应 D.能被氧化成醛 答案:C 2、下列区分苯和己烯的实验方法和判断中都正确的是( ) A.分别点燃,无黑烟生成的是苯 B.分别加入溴水振荡,静置后分层,下层红棕色消失的是己烯 C.分别加入溴水振荡,静置后分层,上、下两层红棕色消失的是己烯 D.分别加入酸性KMnO4溶液振荡,静置后紫色消失的是苯 答案:C 3、布洛芬的分子结构如图,则下列叙述正确的是( ) A.布洛芬的分子式是C13H20O2。 B.与布洛芬的官能团种类与数目都相同的同分异构体还有6个 C.布洛芬能发生取代、加成、氧化反应。 D.布洛芬的一氯取代物有6种 答案:C 【教学建议】整个教学过程可以对每个学生的表现进行统计,答题、方程式书写正确均记1分,得分最多的学生可以适当减少回家书面作业或给予其他小奖励。 在非金属元素硫以及硫化物的学习中,二氧化硫可以作为整个知识部分的中枢,通过对其氧化性和还原性的分析,可以将硫部分知识进行掌握。 一、官能团的性质与转化关系 决定有机化合物的化学特性的原子或原子团叫做官能团,如苯环、C=C、—OH等。 【教学建议】强调官能团不仅决定了有机物的化学性质,还决定了有机物的命名。 类别 烷烃 烯烃 炔烃 苯及同系物 通式 CnH2n+2(n≥1) CnH2n(n≥2) CnH2n-2(n≥2) CnH2n-6(n≥6) 代表物结构式 H—C≡C—H 相对分子质量Mr 16 28 26 78 键角(选讲) 109°28′ 约120° 180° 120° 分子形状 正四面体 6个原子 共平面型 4个原子 同一直线型 12个原子共平面(正六边形) 主要化学性质 光照下的卤代;裂化;不使酸性KMnO4溶液褪色 跟X2、H2、HX、H2O加成,易被氧化;可加聚 跟X2、H2、HX、H2O加成;易被氧化;能加聚得导电塑料 跟H2加成;Fe催化下卤代;硝化反应 类别 通式 官能团 代表物 分子结构结点 主要化学性质 醇 一元醇:R−OH 饱和多元醇: CnH2n+2Om 醇羟基−OH CH3OH C2H5OH β-碳上有H才能发生消去反应;α-碳上有H才能被催化氧化,伯醇氧化为醛,仲醇氧化为酮,叔醇不能被催化氧化。 1.跟活泼金属反应产生H2 2.脱水反应:乙醇 140℃分子间脱水成醚 170℃分子内脱水生成烯 3.催化氧化为醛或酮 4.一般断O−H键与羧酸及无机含氧酸反应生成酯 醛 醛基 HCHO HCHO相当于两个 −CHO; 能加成 1.与H2加成为醇 2.被氧化剂(O2、酸性高锰酸钾等)氧化为羧酸 羧酸 羧基 受羰基影响,O−H能电离出H+,羧基不能被加成。 1.具有酸的通性 2.酯化反应时一般断羧基中的碳氧单键,不能被H2加成 3.能与含−NH2物质缩去水生成酰胺(肽键) 1、烷基(以甲烷为例): (1)氧化反应 甲烷在空气中燃烧火焰呈淡蓝色,化学方程式为:CH4+ 2O2CO2+2H2O。 【思考】哪些物质燃烧火焰呈淡蓝色? 氢气、一氧化碳、甲烷、硫在空气中燃烧 【教学建议】提醒可燃性气体点燃前要验纯,作为尾气要点燃处理。 (2)高温分解 化学反应方程式为:CH4 C+2H2。 炭黑用于橡胶工业,H2用于合成氨、合成汽油等工业。 (3)取代反应 甲烷与氯气反应的化学方程式为: CH4+Cl2HCl+CH3Cl CH3Cl +Cl2HCl+CH2Cl2 CH2Cl2 +Cl2HCl+ CHCl3 CHCl3+Cl2HCl+CCl4 【思考】当甲烷与氯气的体积比为多少是能保证充分反应后产物是纯净物? 甲烷与氯气的反应,4个反应都有可能同时发生,因此只有能完全产生CCl4时,才能保证是纯净物,即体积比甲烷:氯气<1:4。 【教学建议】1.强调三个实验现象:量筒壁上出现油状液滴,量筒内水面上升。量筒内气体颜色变浅 2.取代反应的条件是用漫射阳光照射,而不用强光照射,是因为强光照射时反应过于剧烈,有可能引起爆炸。 【典型例题】下列反应属于取代反应的是 ( ) A.CH4C+ 2H2 B. 2HI+Cl2→I2+2HCl C.CH4 +O2CO2+ 2H2O D.C2H6+Cl2C2H5Cl+HCl 答案:D 2、碳碳双键(以乙烯为例): 乙烯的化学性质 :化学性质主要由其分子结构中C=C键所决定 (1) 氧化反应 ①可燃性 乙烯在空气中的燃烧现象为:火焰明亮并伴有黑烟,放出大量的热。 反应的化学方程式为:C2H4+3O2 2CO2+2H2O。 【思考】为什么乙烯燃烧相比甲烷燃烧会有黑烟? 乙烯分子中碳元素的质量分数较大,耗氧大,不完全燃烧而产生碳单质小颗粒,形成黑烟。 ②与强氧化剂反应 将乙烯通入酸性KMnO4溶液中,酸性KMnO4 溶液的紫色褪去。 本反应可以用来鉴别乙烷和乙烯,但不能用于除去乙烷中的乙烯。 【教学建议】说明乙烯被氧化为二氧化碳混入乙烷中。 (2) 加成反应 ①乙烯通入溴水中,溴水褪色,反应的化学方程式为: CH2 = CH2 +Br2 → CH2Br—CH2Br ; (可以用来鉴别乙烷与乙烯,也可以用来除去乙烷中的乙烯) ②与H2加成制乙烷,反应的化学方程式为: CH2 = CH2 +H2 CH3—CH3 ; ③乙烯水化法制乙醇,反应的化学方程式为: CH2 = CH2 +H2O CH3CH2OH ; ④与 HCl 加成制氯乙烷,反应的化学方程式为: CH2 = CH2 +HCl CH3CH2Cl 。 【典型例题1】可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( ) A.将气体通过盛有酸性KMnO4溶液的洗气瓶 B.将气体通过盛有适量溴水的洗气瓶 C.将气体通过盛有水的洗气瓶 D.将气体通过盛有澄清石灰水的洗气瓶 答案:B 【典型例题2】不可能是乙烯加成产物的是( ) A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br 答案:B (3) 加聚反应 化学方程式为: nCH2=CH2 [CH2—CH2]n ,产物为聚乙烯。 【教学建议】强调加聚反应的特点,含不饱和键的聚合链写在中间,其他基团都写在两侧。反推单体时,主链上的碳原子按每2个进行分解推敲。 【典型例题】乙烯和丙烯按1 : 1(物质的量)聚合时,生成高聚物乙丙树脂,该高聚物的结构式可能是 ( ) A. B. C. D. 答案:AD 3、碳碳叁键(以乙炔为例): 乙炔的化学性质 :化学性质主要由其分子结构中C≡C键所决定 (1)氧化反应 ①可燃性 燃烧现象:火焰明亮伴有浓烈的黑烟。 化学方程式:2C2H2+5O24CO2+2H2O。 ②氧化反应:乙炔能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色。 (2)加成反应 ①在150~160℃和用氯化汞(HgCl2)作催化剂的条件下,乙炔能跟氯化氢发生加成反应。 ②与卤素单质加成 ③与H2加成 用镍粉作催化剂并且加热,乙炔能跟氢气发生加成反应。 HCCH +H2 CH2=CH2 HCCH +2H2CH3—CH3 (3)加聚反应 n CHCH [CH2=CH2]n ,产物为聚乙炔,导电塑料。 【教学建议】比较碳碳叁键与双键的化学性质上有相似性 【典型例题】某烃1mol最多能和2 mol的HBr加成反应,其所得的产物又能跟6mol Br2发生取代反应,最后得到一种只含碳、溴两种元素的化合物,则原烃为 ( ) A.C2H2 B.C3H4 C.C3H6 D.C4H6 【教学建议】有2个不饱和键,可能是炔烃或双烯烃,取代反应后该分子中有8个Br原子,故按烷烃通式可知碳原子数为3,故为丙炔。强调区分加成反应与取代反应的不同点。 4、苯环 苯环并不是碳碳单、双键交替的结构,因此性质上与碳碳双、叁键不完全相同。 (1)取代反应 ①卤代反应: ②硝化反应: (2)加成反应: 苯和H2的加成反应的化学方程式为: 苯环不能与Br2发生加成反应,因此不能使溴水褪色。 (3)氧化反应: ①苯不能被酸性KMnO4溶液氧化,即不能使酸性KMnO4溶液褪色。 ②苯燃烧的反应的化学方程式为: 2C6H6+15O212CO2+6H2O 现象:火焰明亮,产生浓烈黑烟。 苯虽然不能被氧化,但苯的同系物能被酸性KMnO4溶液氧化,使之褪色。 【教学建议】这里需要说明①无论侧链有多长,最后氧化得到的都是羧基; ②只有与苯环相连的碳原子上有连氢原子才能被氧化; 各类烃与液溴、溴水、酸性KMnO4溶液反应的比较 液溴 溴水 酸性KMnO4溶液 烷烃 光照条件下取代 不反应,液态烷烃可将溴萃取褪色 不反应 烯烃 加成 加成褪色 氧化褪色 炔烃 加成 加成褪色 氧化褪色 苯 一般不反应,催化下可取代 不反应,苯可将溴萃取褪色 不反应 苯的同系物 一般不反应,催化下可取代苯环 光照情况下可取代烷基上的氢 不反应,苯的同系物可将溴萃取褪色 氧化褪色 【典型例题】下列两种物质,不能用酸性KMnO4鉴别是 ( ) A.乙烷和丙烯 B.Na2SO3和Na2SO4 C.苯和甲苯 D.SO2和H2S 答案:D 5、羟基(以乙醇为例) (1)与活泼金属的反应 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ (2)氧化反应 ①燃烧: C2H5OH+3O2 2CO2+ 3H2O ②催化氧化 2CH3CH2OH+O22CH3CHO+2H2O 【思考】是不是所有的醇类都可以被催化氧化成为醛? 不是,只有伯醇才能被氧化为醛,仲醇氧化为酮,而叔醇则不能发生氧化。 【教学建议】强调羟基相连的碳原子上有氢才能被氧化。 说明有机中的氧化还原反应不同与无机,得氧失氢为氧化,得氢失氧为还原。 (3)消去反应 在适当条件下,有机化合物分子内脱去小分子而生成不饱和(双键或叁键)化合物的反应,叫做消去反应。 如乙醇发生分子内消去反应:CH3CH2OHCH2=CH2↑+H2O。 【思考】醇能分子内消去反应的条件是什么? 与羟基碳原子相邻的(α位)碳原子上没有氢原子的醇类,不能发生消去反应,如2,2-二甲基-1-丙醇。 【教学建议】醇的氧化与消去反应条件容易混淆,讲解的时候需要重点说明,可以采用标示氢原子具体说明两种反应的机理。 (4)分子间脱水反应 乙醇发生分子间消去反应:CH3CH2OHC2H5—O—C2H5(乙醚) + H2O。 【教学建议】这里要注意反应类型的不同,同种醇分子间脱水是消去反应,但不同醇的分子间脱水是取代反应。 【典型例题1】乙醇分子中不同的化学键如图所示,下列关于乙醇在各种不同反应中断裂键的说法不正确的是 ( ) A.和金属钠反应键①断裂 B.在Ag催化下和O2反应键①③断裂 C.和浓H2SO4共热140℃时,键①或键②断裂 D.170℃时键②③断裂 答案:D 【典型例题2】某一元醇在红热的铜丝催化下,最多可被空气中的O2氧化成两种不同的醛。该一元醇的分子式可能是 ( ) A.C2H6O B.C3H8O C.C4H10O D.C5H12O 答案:C 【教学建议】只有—OH在链的末端即拥有—CH2OH组成时,才能被氧化成醛。所以本题也就转变为分子式改写成R—CH2OH的形式,而R—有几种结构,则氧化成的醛就有几种结构。这里要强调有机题答题时要注意所有符合要求的同分异构体可能性。 6、醛基(以甲醛为例) (1)氧化反应 ①醛与银氨溶液: HCHO + 2Ag(NH3)2OHHCOOH+2Ag↓+4NH3↑+H2O 而生成的甲酸与产物中的氨继续反应生成甲酸铵。故总反应化学方程式也可以为: HCHO + 2Ag(NH3)2OH HCOONH4+2Ag↓+3NH3↑+H2O 【教学建议】用图像描述氧化过程中原子的转移过程。 ②醛与新制氢氧化铜悬浊液反应 HCHO+2Cu(OH)2HCOOH+Cu2O↓+2H2O 【思考】银氨溶液和新制氢氧化铜悬浊液都是弱氧化剂,则在醛基在催化氧化反应中体现了说明性质? 醛基能被它们氧化,表明醛基具有强还原性。其他强氧化剂(如酸性高锰酸钾溶液等)也能氧化醛基。 【典型例题1】某3g饱和的一元醛和足量的银氨溶液反应,结果析出43.2 g Ag,则该醛为 ( ) A.甲醛 B.乙醛 C.丙醛 D.丁醛 答案:A 【教学建议】强调方程式书写要熟练,1份醛需要2份氧化剂,故产生0.4mol银,只反应了0.2mol醛基。再推醛的分子量,得到仅为15/mol,则为甲醛。 【典型例题2】下列物质中,不能发生银镜反应的是 ( ) A. B. C. D. 答案:A 【教学建议】说明能发生银镜反应的物质,不一定是醛,而是其分子结构中一定含有醛基—CHO结构。 (2)还原反应 HCHO+H2CH3OH 【教学建议】说明醇转化为醛是氧化反应,醛转化为醇是还原反应。 7、羧酸(以乙酸为例) (1)酸性 CH3COOHCH3COO-+H+ 具有酸的通性,酸性强于碳酸,弱于盐酸。 Cu(OH)2 +2CH3COOH→(CH3COO)2Cu + 2H2O CaCO3 +2CH3COOH→(CH3COO)2Ca+CO2↑+H2O Zn +2CH3COOH→(CH3COO)2Zn+H2↑ (2)酯化反应 酸和醇起作用,生成酯和水的反应叫做酯化反应。酯化反应一般是羧酸分子里的羟基与醇分子里的羟基上的氢原子结合成水,其余部分互相结合成酯。 CH3COOH +C2H5OHCH3COOC2H5+H2O 【思考】酯化反应属于什么反应类型? 取代反应 【典型例题】下列化合物中,既显酸性又能发生酯化反应和消去反应的是 ( ) A. B. C. D. 答案:C 二、同分异构体 【教学建议】同分异构体的判断与书写是高二有机学习中的难点,这部分讲解应侧重让学生多想、多练、多悟。对于这部分内容已较好掌握的学生,可以减少内容,侧重于有其他难点。 1、同分异构体概念 化合物具有相同的分子式,但结构不同的现象称为同分异构现象。具有同分异构现象的化合物互称为同分异构体。在中学阶段,引起同分异构的原因主要有三种:碳架异构、位置异构和官能团异构。识别两者是否是同分异构体,首先要查碳原子数,判别分子式是否相同,然后再看结构式。在分子式相同的情况下,若结构不同,则两者必为同分异构体。 【教学建议】强调分子式相同、结构相同是同种物质。判断两结构是否相同方法有二:(1) 将分子整体翻转或沿对称要素(面、线)旋转后能“重合”者;(2)用系统命名法命名,所得名称相同者。 【教学建议】对于需要进一步学习高三化学的学生,这里可以讲解“饱和度”及其用于分子式书写的技巧。 2、常见的同分异构体类型 (1)烃链的异构(碳骨架的异构) 熟记C1-C6的碳链异构: CH4、C2H6、C3H8 无异构体;C4H10 2种、C5H12 3种、C6H14 5种。 【教学建议】烃链的异构基本遵循先定主链长度再分支链的原则,即先将所有碳原子直连,再逐个减少碳原子数放为支链,注意①找对称点避免重复;②不能存在比主链长的碳链,常见问题如乙基连在第2个碳原子上等。 【典型例题】某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( ) A、C3H8 B、C4H10 C、C5H12 D、C6H14 答案:C (2)烯炔的异构(碳架的异构和双键或叁键官能团的位置异构) 如丁烯C4H8有两碳链形成三种异构体:、、。 【教学建议】稀炔的异构可以先确定含不饱和键的碳链长度(遵循烯烃的命名规则),再增加支链补足碳原子数。 (3)苯同系物的异构(侧链碳架异构及侧链位置的异构) 如C9H12有8种异构体:;;;;;;;。 【教学建议】苯的同系物异构书写上2侧链必有邻间对三种关系。如果侧链碳原子数较多,要注意侧链本身的同分异构体。 (4)烃的一元取代物的异构(等效氢取代法) 卤代烃、醇、醛、羧酸都可看着烃的一元取代物。确定它们异构体可用取代等效氢法。 等效氢概念:有机物分子中位置等同的氢叫等效氢,分子中等效氢原子有如下情况: ①分子中同一个碳原子上连接的氢原子等效。 ②同一个碳原子上所连接的甲基上的氢原子等效。如新戊烷(可以看作四个甲基取代了甲烷分子中的四个氢原子而得),其四个甲基等效,各甲基上的氢原子完全等效,也就是说新戊烷分子中的12个H原子是等效的。 ③分子中处于镜面对称位置(相当于平面镜成像时,物与像的关系)上的氢原子是等效的。如 分子中的18个H原子是等效的。 【教学建议】优先找对称轴,有时候有2个对称轴,斜向的对称轴需提示学生关注。 (5)烃的二元(或三元)取代物的异构有序法(定一议二) 有序法要求解决问题时遵循一定的特定线索和步骤去探索的一种思维方法。应用有序法解决烃的多元取代物异构体问题的步骤顺序是:先写出碳架异构,再在各碳架上依次先定一个官能团,接着在此基础上移动第二个官能团,依此类推 (6)酯的异构(拆分法) 酯可拆分为合成它的羧酸和醇(酚)。若已知酸有m种异构体,醇有n种异构体,则该酯的同分异构体有m×n种。而羧酸和醇的异构体可用取代有效氢法确定。 【典型例题】写出符合分子式C4H8O2且属于羧酸或酯的同分异构体 答案:属于羧酸的有、; 属于酯类的有 (7)类别异构 【教学建议】程度较好学生可以拓展这部分内容。 ①CnH2n:(n≥3)烯烃和环烷烃; ②CnH2n-2:(n≥3)二烯烃,炔烃,环烯烃; ③CnH2n+2O:(n≥2)饱和一元醇和饱和一元醚; ④CnH2nO:(n≥2)饱和一元醛、烯醇和环氧烷;(n≥3)饱和一元酮; ⑤CnH2nO2:(n≥2)饱和一元羧酸、饱和一元羧酸饱一元醇酯; 【教学建议】此环节教案预期时间20(练题)+15(互动讲解)分钟。 本单元综合检测,教案在提供基本练习题(简单+中档)之外,设置“附加题”环节,为本次知识的加深题型,供TR根据情况选择使用。通过竞赛的互动方式进行,并给予学生相应的鼓励与表扬,正确率高的学生可以适当减少回家作业或者按学生的情况,针对性安排回家作业。 选择题: 1、在光照条件下,将等物质的量的CH4与Cl2混合,所得产物的物质的量最多的是 ( ) A. CH3Cl B.CH2Cl2 C.CHCl3 D.HCl 2、下列反应不属于取代反应的是 ( ) A.C2H4+ Cl2 →C2H4Cl2 B.2C2H5OH→C2H5—O—C2H5 +H2O C.C2H5Cl+H2O→C2H5OH+HCl D.CH4+4Cl2→CCl4+4HCl 3、能证明乙烯里含有一个碳碳双键的事实是( ) A.乙烯能使酸性KMnO4溶液褪色 B.乙烯分子里碳、氢原子个数比为1∶2 C.乙烯完全燃烧生成的CO2和H2O的物质的量相等 D.乙烯容易与溴水发生反应,且1 mol乙烯完全加成消耗1 mol溴单质 4、在下列物质中,能使酸性KMnO4溶液褪色的是 ( ) A.聚乙烯 B.乙烷 C.聚乙炔 D.聚氯乙烯 5、有机物具有的性质是( ) ①能使酸性高锰酸钾溶液褪色 ②能发生取代反应 ③能发生加成反应 A.只有① B.只有①② C.只有②③ D.①②③ 6、下列物质能发生消去反应,但不能发生催化氧化反应的是( ) A. B. C. D. 7、现有组成为C2H5OH和C3H8O的混合物,在一定条件下进行脱水反应,可能生成的有机物的种数为( ) A.2 B.6 C.7 D.8 8、丙烯醇(CH2=CH—CH2OH)可发生的化学反应有 ( ) ①加成 ②氧化 ③燃烧 ④加聚 ⑤取代 A.①②③ B.①②③④ C.①②③④⑤ D.①③④ 9、下列物质可以直接由甲醛经过一步反应制得的是( ) A.二氧化碳 B.甲烷 C.氯仿 D.乙酸 10、甲醛在一定条件下发生如下反应:2HCHO+NaOH(浓)→HCOONa+CH3OH,在此反应中,甲醛发生的变化是 ( ) A.仅被氧化 B.仅被还原 C.既被氧化,又被还原 D.既未被氧化,也未被还原 11、下列5种有机物中,能够发生酯化、加成和氧化3种反应的是 ( ) ①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH ⑤CH3CH(OH)CH2CHO A.①③④ B.②④⑤ C.①③⑤ D.①②⑤ 12、芳香族化合物A的分子式为C7H6O2,将它与NaHCO3 溶液混合加热,有酸性气体产生,那么包括A在内,属于芳香族化合的同分异构体数目是( ) A.2 B.3 C.4 D.5 13、已知分子式为C12H12的物质A的结构简式为,A苯环上的二溴代物有九种同分异构体,由此推断A苯环上的四溴代物的同分异构体有 种。 14、某链烃分子中都含有下列基团:2个,2个,3个和1个,请写出该烃可能的结构简式。 15、乙炔是重要的有机化工原料,其化学性质活泼。完成下列填空 (1)乙炔能使溴水褪色,说明乙炔能发生 反应(填反应类型);乙炔能使酸性高锰酸钾褪色,说明乙炔容易被 。 (2)乙炔在一定条件下三聚得到CH2=CH—C≡C—CH=CH2,写出与该三聚物具有相同化学式且不易发生加成反应的物质的结构简式。 。 (3)乙炔聚合得到聚乙炔,聚乙炔 导电(选填“能”或“不能”)。 (4)乙炔在不同的催化条件下加氢可得到不同的产物。下列物质与乙炔加氢得到的某种产物互为同系物的 是 (选填编号)。 CH2 CH2 H2C a.C2H4 b.C2H6 c. d.CH2=CHCH3 16、羧酸A(C5H10O2)是由醇B氧化而成,A又可和B生成相对分子量为172的酯C,符合这种条件的酯有几种?写出这几种酯的结构简式。 答案:1~12 DADCD DDCAC CD 13、9 14、;;;;; 15、(1)加成;氧化 (2) (3) 能 (4) d 16、;; ;。 (此环节设计时间在10分钟内) (以学生自我总结为主,TR根据教案中的总结及学生的实际学习能力进行引导为辅,为本次课做一个总结回顾;总结方式可以多种多样,如画思维导图、默想回忆、抢答形式等。教案中给到重难点/易错点等的总结条目。) 1.可以采取选择性默写本次课上讲解过的有机物反应方程式; 2.给出一个简单烃类的分子式,要求学生书写同分异构体; 一、复习作业 1、1mol甲烷完全和氯气发生取代反应,生成四种取代产物的物质的量相同,则消耗氯气的物质的量为 A.0.5mol B.2mol C.2.5mol D.4mol 2、下列物质中,能发生银镜反应,其溶液呈酸性的是 ( ) A. B. C. D. 3、下列说法中,错误的是( ) A.不论乙烯与Br2的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关 B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷 C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同 D.利用燃烧的方法可以鉴别乙炔、乙烯、甲烷 4、据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:HC≡C-C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是( ) A.晶体的硬度与金刚石相当 B.可由乙炔和含氮化合物加聚制得 C.不能发生加成反应 D.能使酸性高锰酸钾溶液褪色 5、将浓硫酸和分子式为C4H10O的醇共热,所得到的有机产物有 ( ) A.14种 B.13种 C.8种 D.7种 6、下列反应中,属于消去反应的是 ( ) A.乙醇和浓硫酸加热到170℃ B.正丙醇与钠反应 C.甲醇在空气中燃烧 D.乙醇在催化剂存在下受热反应生成乙醛 7、等质量的下列醇与足量的金属钠反应,产生气体最多的是 ( ) A. B. C. D. 8、由乙醇制取乙二酸乙二酯时最简便的合成路线需经下列反应,其顺序正确的是 ( ) ①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应 A.①②③⑤⑥ B.⑤②①③⑥ C.⑥③①②⑤ D.①②⑤③⑥ 9、下列与有机物结构、性质相关的叙述错误的是( ) A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2 B.有机物都属于分子晶体,可以用化学式表示分子式 C.甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 D.苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 10、现有下列种物质:① ② ③ ④ ⑤ ⑥ (1)能发生消去反应的烯烃的是______(请填序号,下同),其消去产物依次是______; (2)能在铜的催化作用下氧化成醛的序号分别是______。 (1)②④⑤;、、CH3CH=CH2;(2)①③④ 11、乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出): 乙醇 氯乙烯 乙烯 二氯乙烷 聚乙烯 乙醛 乙酸 ① ⑤ ③ 500℃ (工业制法) ④ ② ⑥ 新制Cu(OH)2 按下列要求写出: (1)聚乙烯的结构简式是________________。乙酸中所含官能团的名称为___________基。 (2)乙醇能与乙酸反应生成有果香味的物质,其名称为___________,该反应类型是_______。 (3)反应②的化学方程式是 ,反应类型是 。 (4)反应⑥的化学方程式是_________________________________, 实验现象是____________________________________________。 12、某种苯的同系物蒸气a L,完全燃烧时,需相同状况下的O2 12a L,则此烃的分子式为_______。若已知此烃分子中有一个乙基,则此烃的结构简式可能为__________、_________、_________。 13、某化合物的分子式为C5H11Cl,结构分析表明,该分子中含有两个 —CH3、两个 —CH2—、一个和一个 —Cl。它的可能结构有4种,请写出这4种可能的结构简式。 14、已知某有机物的结构简式如右: 写出同时符合下列两项要求的同分异构体的结构简式。 ①化合物是1,3,5-三取代苯 ②苯环上的三个取代基分别是甲基、羟基和含有酯基结构的基团 二、预习作业 【预习建议】思考用甲苯合成苯甲酸苯甲酯的合成线路。 答案:1~9 CCBDB ABBB 10、(1)②④⑤;、、CH3CH=CH2;(2)①③④ 11、(1) 羧 (2)乙酸乙酯 取代(酯化)反应 (3)CH2=CH2+ Cl2 → CH2Cl-CH2Cl 加成反应 (4) CH3CHO +2Cu(OH) 2 CH3COOH+Cu2O↓+2H2O 产生红色沉淀 12、C9H12 13、;;;; 14、查看更多