- 2021-05-13 发布 |
- 37.5 KB |
- 4页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
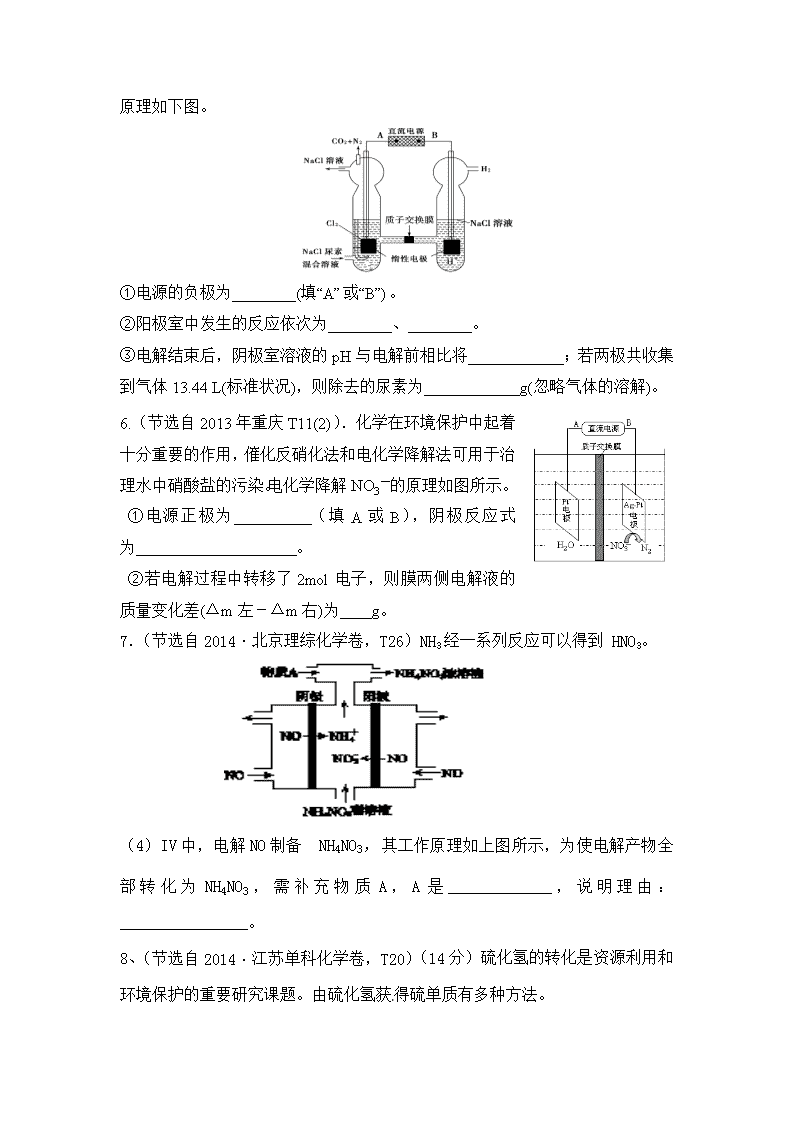
高考中有关离子交换膜的电化学试题
高考中有关离子交换膜的电化学试题 离子交换膜是一种对溶液里的离子具有选择透过能力的高分子膜。因在应用时主要是利用它的离子选择透过性,又称为离子选择透过性膜.离子交换膜法在电化学工业中应用十分广泛。教材中并未专门介绍,一般是在讲解氯碱工业时介绍阳离子交换膜的应用,但在近年考试中涉及离子交换膜原理的考题屡见不鲜. 一、交换膜的功能: 使离子选择性定向迁移(目的是平衡整个溶液的离子浓度或电荷)。 二、交换膜在中学电化学中的作用: 1.防止副反应的发生,避免影响所制取产品的质量;防止引发不安全因素。(如在电解饱和食盐水中,利用阳离子交换膜,防止阳极产生的氯气进入阴极室与氢氧化钠反应,导致所制产品不纯;防止与阴极产生的氢气混合发生爆炸)。 2.用于物质的制备、分离、提纯等。 三、离子交换膜的类型: 常见的离子交换膜为:阳离子交换膜、阴离子交换膜、特殊离子交换膜等。 四、试题赏析: 1.某同学按如图所示装置进行试验,A、B为常见金属,它们的硫酸盐可溶于水。当K闭合时,SO42-从右向左通过阴离子交换膜移向A极.下列分析正确的是 A.溶液中c(A2+)减小 B.B极的电极反应:B-2e- = B2+ C.Y电极上有H2产生,发生还原反应 D.反应初期,X电极周围出现白色胶状沉淀,不久沉淀溶解 2.(2014·全国大纲版理综化学卷,T9)右图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池)。下列有关说法不正确的是 A.放电时正极反应为:NiOOH+H2O+e-→Ni(OH)2+OH- B.电池的电解液可为KOH溶液 C.充电时负极反应为:MH+OH-→M+H2O+e- D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高 3.(2014·福建理综化学卷,T11)某原电池装置如右图所示,电池总反应为 2Ag+Cl2=2AgCl。下列说法正确的是 A.正极反应为AgCl +e-=Ag +Cl- B.放电时,交换膜右侧溶液中有大量白色沉淀生成 C.若用NaCl溶液代替盐酸,则电池总反应随之改变 D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 4.(2013·浙江高考·11)电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-=I+5I-+3H2O 下列说法不正确的是 ( ) A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH- B.电解结束时,右侧溶液中含有I C.电解槽内发生反应的总化学方程式:KI+3H2OKIO3+3H2↑ D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 5.(2012年重庆T29 (3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如下图。 ①电源的负极为________(填“A”或“B”)。 ②阳极室中发生的反应依次为________、________。 ③电解结束后,阴极室溶液的pH与电解前相比将____________;若两极共收集到气体13.44 L(标准状况),则除去的尿素为____________g(忽略气体的溶解)。 6.(节选自2013年重庆T11(2)).化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3-的原理如图所示。 ①电源正极为 (填A或B),阴极反应式为 。 ②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为 g。 7.(节选自2014·北京理综化学卷,T26)NH3经一系列反应可以得到 HNO3。 (4)IV中,电解NO制备 NH4NO3,其工作原理如上图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是_____________,说明理由:________________。 8、(节选自2014·江苏单科化学卷,T20)(14分)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。 (1)将烧碱吸收H2S后的溶液加入到如题20图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-—2e-S (n—1)S+ S2- Sn2①写出电解时阴极的电极反应式: 。 ②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成 。 9.(节选自2014·新课标全国卷Ⅰ)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。回答下列问题: (4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过): ①写出阳极的电极反应式: ________________________________。 ②分析产品室可得到H3PO2的原因是________________________________。 ③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有________杂质,该杂质产生的原因是________________________________。查看更多