- 2021-05-13 发布 |
- 37.5 KB |
- 4页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
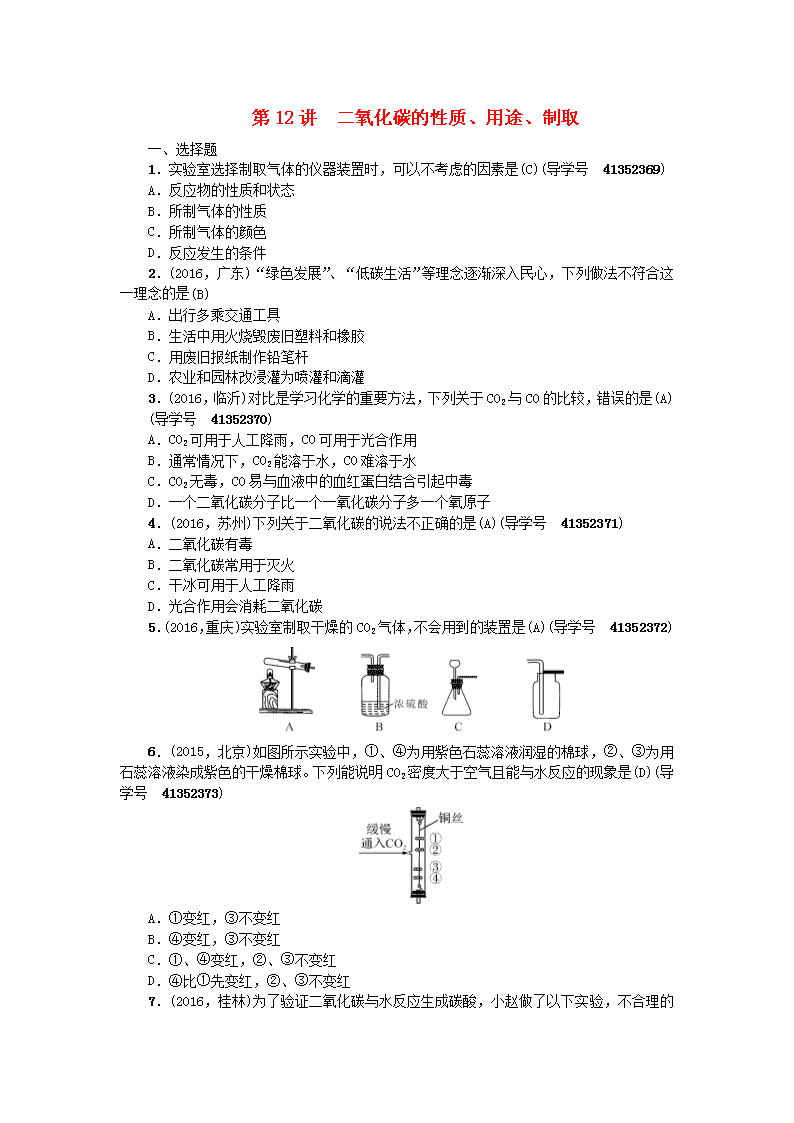
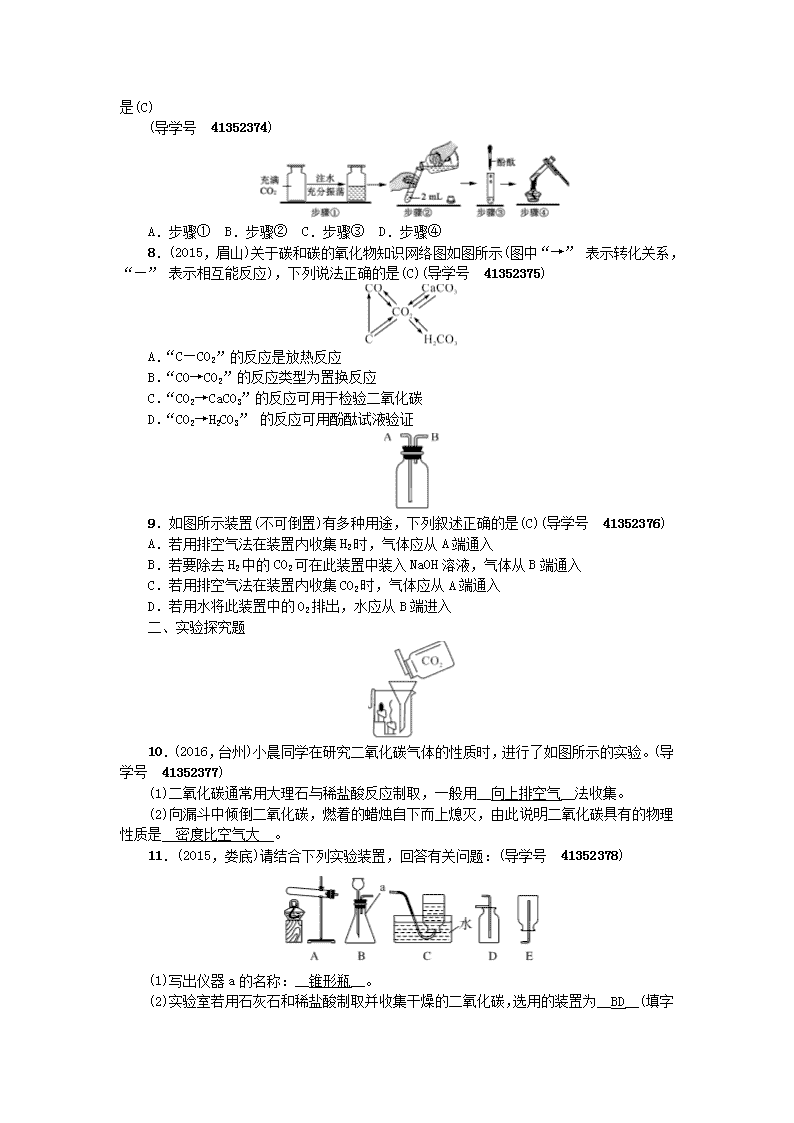
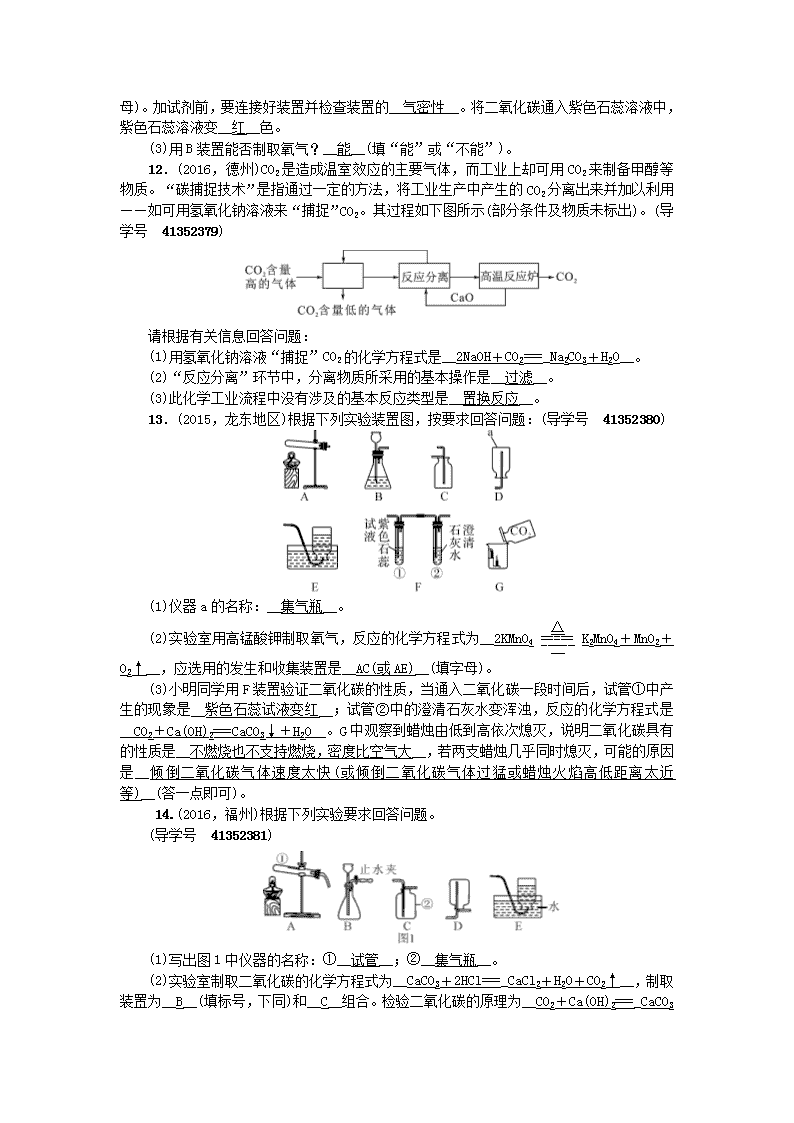
中考化学总复习 碳和碳的氧化物 二氧化碳的性质用途制取考点跟踪 新人教版
第12讲 二氧化碳的性质、用途、制取 一、选择题 1.实验室选择制取气体的仪器装置时,可以不考虑的因素是(C)(导学号 41352369) A.反应物的性质和状态 B.所制气体的性质 C.所制气体的颜色 D.反应发生的条件 2.(2016,广东)“绿色发展”、“低碳生活”等理念逐渐深入民心,下列做法不符合这一理念的是(B) A.出行多乘交通工具 B.生活中用火烧毁废旧塑料和橡胶 C.用废旧报纸制作铅笔杆 D.农业和园林改浸灌为喷灌和滴灌 3.(2016,临沂)对比是学习化学的重要方法,下列关于CO2与CO的比较,错误的是(A) (导学号 41352370) A.CO2可用于人工降雨,CO可用于光合作用 B.通常情况下,CO2能溶于水,CO难溶于水 C.CO2无毒,CO易与血液中的血红蛋白结合引起中毒 D.一个二氧化碳分子比一个一氧化碳分子多一个氧原子 4.(2016,苏州)下列关于二氧化碳的说法不正确的是(A)(导学号 41352371) A.二氧化碳有毒 B.二氧化碳常用于灭火 C.干冰可用于人工降雨 D.光合作用会消耗二氧化碳 5.(2016,重庆)实验室制取干燥的CO2气体,不会用到的装置是(A)(导学号 41352372) 6.(2015,北京)如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列能说明CO2密度大于空气且能与水反应的现象是(D)(导学号 41352373) A.①变红,③不变红 B.④变红,③不变红 C.①、④变红,②、③不变红 D.④比①先变红,②、③不变红 7.(2016,桂林)为了验证二氧化碳与水反应生成碳酸,小赵做了以下实验,不合理 的是(C) (导学号 41352374) A.步骤① B.步骤② C.步骤③ D.步骤④ 8.(2015,眉山)关于碳和碳的氧化物知识网络图如图所示(图中“→” 表示转化关系,“—” 表示相互能反应),下列说法正确的是(C)(导学号 41352375) A.“C—CO2”的反应是放热反应 B.“CO→CO2”的反应类型为置换反应 C.“CO2→CaCO3”的反应可用于检验二氧化碳 D.“CO2→H2CO3” 的反应可用酚酞试液验证 9.如图所示装置(不可倒置)有多种用途,下列叙述正确的是(C)(导学号 41352376) A.若用排空气法在装置内收集H2时,气体应从A端通入 B.若要除去H2中的CO2可在此装置中装入NaOH溶液,气体从B端通入 C.若用排空气法在装置内收集CO2时,气体应从A端通入 D.若用水将此装置中的O2排出,水应从B端进入 二、实验探究题 10.(2016,台州)小晨同学在研究二氧化碳气体的性质时,进行了如图所示的实验。(导学号 41352377) (1)二氧化碳通常用大理石与稀盐酸反应制取,一般用__向上排空气__法收集。 (2)向漏斗中倾倒二氧化碳,燃着的蜡烛自下而上熄灭,由此说明二氧化碳具有的物理性质是__密度比空气大__。 11.(2015,娄底)请结合下列实验装置,回答有关问题:(导学号 41352378) (1)写出仪器a的名称:__锥形瓶__。 (2)实验室若用石灰石和稀盐酸制取并收集干燥的二氧化碳,选用的装置为__BD __(填字母)。加试剂前,要连接好装置并检查装置的__气密性__。将二氧化碳通入紫色石蕊溶液中,紫色石蕊溶液变__红__色。 (3)用B装置能否制取氧气?__能__(填“能”或“不能”)。 12.(2016,德州)CO2是造成温室效应的主要气体,而工业上却可用CO2来制备甲醇等物质。“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并加以利用——如可用氢氧化钠溶液来“捕捉”CO2。其过程如下图所示(部分条件及物质未标出)。(导学号 41352379) 请根据有关信息回答问题: (1)用氢氧化钠溶液“捕捉”CO2的化学方程式是__2NaOH+CO2===_Na2CO3+H2O__。 (2)“反应分离”环节中,分离物质所采用的基本操作是__过滤__。 (3)此化学工业流程中没有涉及的基本反应类型是__置换反应__。 13.(2015,龙东地区)根据下列实验装置图,按要求回答问题:(导学号 41352380) (1)仪器a的名称:__集气瓶__。 (2)实验室用高锰酸钾制取氧气,反应的化学方程式为__2KMnO4K2MnO4+MnO2+O2↑__,应选用的发生和收集装置是__AC(或AE)__(填字母)。 (3)小明同学用F装置验证二氧化碳的性质,当通入二氧化碳一段时间后,试管①中产生的现象是__紫色石蕊试液变红__;试管②中的澄清石灰水变浑浊,反应的化学方程式是__CO2+Ca(OH)2===CaCO3↓+H2O__。G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是__不燃烧也不支持燃烧,密度比空气大__,若两支蜡烛几乎同时熄灭,可能的原因是__倾倒二氧化碳气体速度太快(或倾倒二氧化碳气体过猛或蜡烛火焰高低距离太近等)__(答一点即可)。 14.(2016,福州)根据下列实验要求回答问题。 (导学号 41352381) (1)写出图1中仪器的名称:①__试管__;②__集气瓶__。 (2)实验室制取二氧化碳的化学方程式为__CaCO3+2HCl===_CaCl2+H2O+CO2↑__ ,制取装置为__B__(填标号,下同)和__C__组合。检验二氧化碳的原理为__CO2+Ca(OH)2===_CaCO3 ↓+H2O__(用化学方程式表示)。 (3)实验室用高锰酸钾制取氧气的化学方程式为__2KMnO4K2MnO4+MnO2+O2↑__,可选用的发生装置为__A__(填标号)。 (4)若用水将图2所示的氧气从瓶内排出,水须从__b__(填“a”或“b”)端导管口通入。 (5)实验室用碘化氢溶液测定过氧化氢溶液中溶质的质量分数,反应原理:H2O2+2HI=== 2H2O+I2↓。取25.0 g过氧化氢溶液,加入足量的碘化氢溶液,充分反应后生成12.7 g碘。根据化学方程式计算该过氧化氢溶液中溶质的质量分数。 解:设该过氧化氢溶液中溶质过氧化氢的质量为x。 H2O2+2HI=== 2H2O+I2↓ 34 254 x 12.7 g = 解得:x=1.7 g 所以该过氧化氢溶液的溶质质量分数为×100%=6.8% 答:该过氧化氢溶液的溶质质量分数为6.8%。查看更多