- 2021-05-13 发布 |
- 37.5 KB |
- 5页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
淄博专版中考化学复习滚动检测卷一
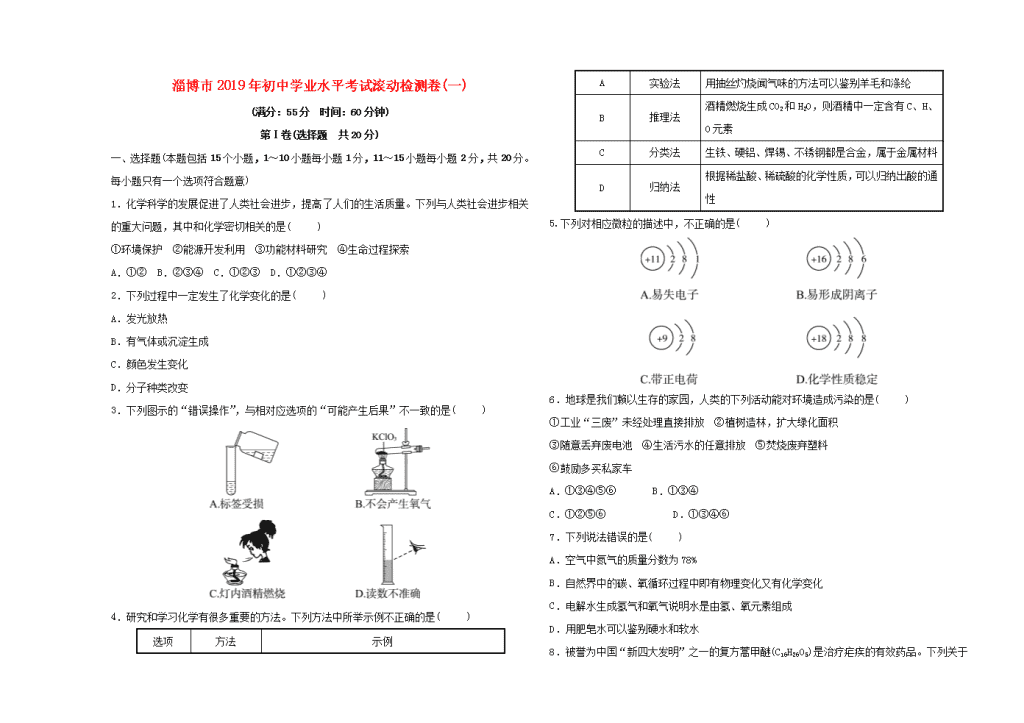
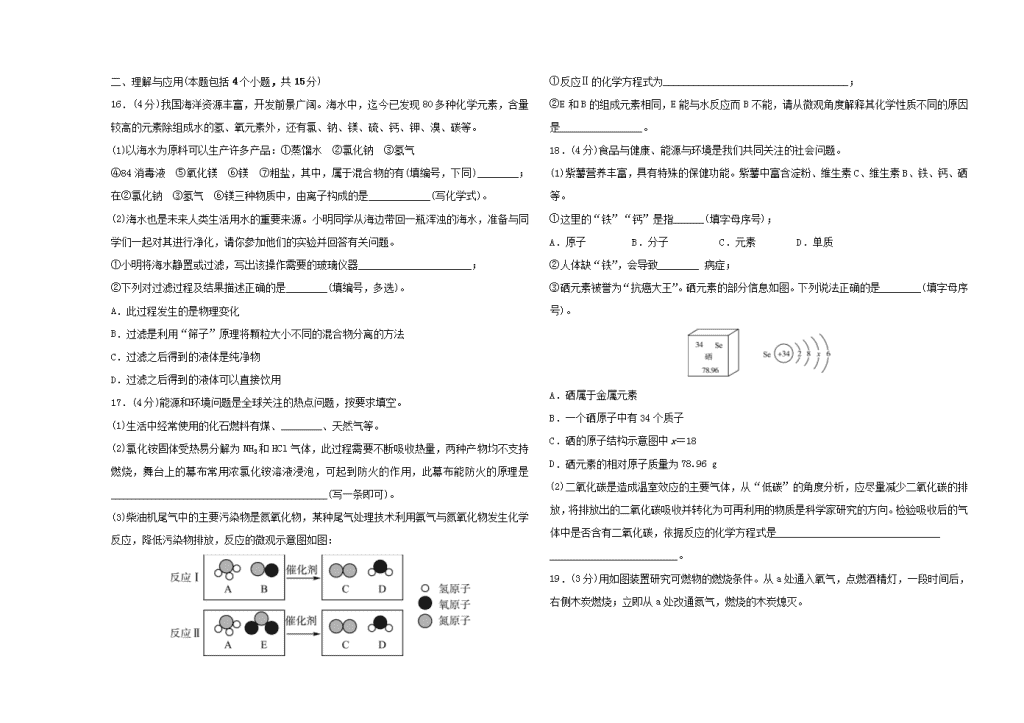
淄博市2019年初中学业水平考试滚动检测卷(一) (满分:55分 时间:60分钟) 第Ⅰ卷(选择题 共20分) 一、选择题(本题包括15个小题,1~10小题每小题1分,11~15小题每小题2分,共20分。每小题只有一个选项符合题意) 1.化学科学的发展促进了人类社会进步,提高了人们的生活质量。下列与人类社会进步相关的重大问题,其中和化学密切相关的是( ) ①环境保护 ②能源开发利用 ③功能材料研究 ④生命过程探索 A.①② B.②③④ C.①②③ D.①②③④ 2.下列过程中一定发生了化学变化的是( ) A.发光放热 B.有气体或沉淀生成 C.颜色发生变化 D.分子种类改变 3.下列图示的“错误操作”,与相对应选项的“可能产生后果”不一致的是( ) 4.研究和学习化学有很多重要的方法。下列方法中所举示例不正确的是( ) 选项 方法 示例 A 实验法 用抽丝灼烧闻气味的方法可以鉴别羊毛和涤纶 B 推理法 酒精燃烧生成CO2和H2O,则酒精中一定含有C、H、O元素 C 分类法 生铁、硬铝、焊锡、不锈钢都是合金,属于金属材料 D 归纳法 根据稀盐酸、稀硫酸的化学性质,可以归纳出酸的通性 5.下列对相应微粒的描述中,不正确的是( ) 6.地球是我们赖以生存的家园,人类的下列活动能对环境造成污染的是( ) ①工业“三废”未经处理直接排放 ②植树造林,扩大绿化面积 ③随意丢弃废电池 ④生活污水的任意排放 ⑤焚烧废弃塑料 ⑥鼓励多买私家车 A.①③④⑤⑥ B.①③④ C.①②⑤⑥ D.①③④⑥ 7.下列说法错误的是( ) A.空气中氮气的质量分数为78% B.自然界中的碳、氧循环过程中即有物理变化又有化学变化 C.电解水生成氢气和氧气说明水是由氢、氧元素组成 D.用肥皂水可以鉴别硬水和软水 8.被誉为中国“新四大发明”之一的复方蒿甲醚(C16H26O5 )是治疗疟疾的有效药品。下列关于复方蒿甲醚的说法错误的是( ) A.由C、H、O三种元素组成 B.一个分子由47个原子构成 C.属于化合物 D.C、H、O三种元素的质量比是16∶26∶5 9.下列关于空气成分的信息不正确的是( ) A.冬天清晨枯草上会结霜,说明空气中含水蒸气 B.木材能在空气中燃烧,说明空气中含氧气 C.正常的雨水呈酸性,是因为空气中含二氧化碳 D.利用空气成分可制取氨气,因为空气中含氨气 10.下列关于氧气的说法中,不正确的是( ) A.红磷在氧气中燃烧,产生浓厚的白烟 B.硫在氧气中燃烧发出明亮的蓝紫色火焰 C.氧气能支持燃烧,所以氧气可作燃料 D.铁在氧气中燃烧,火星四射、生成黑色固体 11.医务人员用3%的过氧化氢溶液为伤者处理伤口时,伤口处会看到大量泡沫。下列说法错误的是( ) A.生成的气体可能是过氧化氢分解产生的氧气 B.伤口处的生物酶可能对过氧化氢的分解起到催化作用 C.双氧水制取氧气时,若不加二氧化锰,则不能分解产生氧气 D.过氧化氢(H2O2)和水(H2O)的组成结构不同,所以它们的化学性质不同 12.下列有关溶液的叙述错误的是( ) A.长期放置后不会分层的液体一定是溶液 B.衣服上的油污用汽油或用加了洗涤剂的水可除去 C.一瓶合格的生理盐水密封一段时间,不会出现浑浊 D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率 13.下列涉及学科观点的有关说法正确的是( ) A.微粒观:水是由氢原子和氧原子构成的 B.转化观:O2和CO2在一定条件下可以相互转化 C.结构观:氦原子和镁原子最外层电子数相同,化学性质相同 D.守恒观:10 mL质量分数20%的硫酸,加10 mL水后体积为20 mL 14.小新同学在S+O2SO2中获得以下信息: ①该反应中反应物是硫和氧气 ②该反应发生的条件是点燃 ③反应前后元素种类和原子个数保持不变 ④反应前后分子总数保持不变 ⑤参加反应的硫和氧气的质量比为2∶1 其中正确的信息是( ) A.①②③④⑤ B.④⑤ C.①②③ D.①②③⑤ 15.在一个密闭容器内有四种物质,在一定条件下完全反应后,测得反应前后各物质的质量如下: 物质 X Y Z Q 反应前质量/g 4 10 1 21 反应后质量/g 0 12 15 待测 已知X的相对分子质量为N,Q的相对分子质量为2N,下列推理正确的是( ) A.反应后Q的质量为9 g B.反应中Y与Q发生改变的质量之比为1∶1 C.反应后生成15 g Z D.X与Q前的化学计量数之比为2∶1 第Ⅱ卷(非选择题 共35分) 二、理解与应用(本题包括4个小题,共15分) 16.(4分)我国海洋资源丰富,开发前景广阔。海水中,迄今已发现80多种化学元素,含量较高的元素除组成水的氢、氧元素外,还有氯、钠、镁、硫、钙、钾、溴、碳等。 (1)以海水为原料可以生产许多产品:①蒸馏水 ②氯化钠 ③氢气 ④84消毒液 ⑤氧化镁 ⑥镁 ⑦粗盐,其中,属于混合物的有(填编号,下同)________;在②氯化钠 ③氢气 ⑥镁三种物质中,由离子构成的是____________(写化学式)。 (2)海水也是未来人类生活用水的重要来源。小明同学从海边带回一瓶浑浊的海水,准备与同学们一起对其进行净化,请你参加他们的实验并回答有关问题。 ①小明将海水静置或过滤,写出该操作需要的玻璃仪器______________________; ②下列对过滤过程及结果描述正确的是________(填编号,多选)。 A.此过程发生的是物理变化 B.过滤是利用“筛子”原理将颗粒大小不同的混合物分离的方法 C.过滤之后得到的液体是纯净物 D.过滤之后得到的液体可以直接饮用 17.(4分)能源和环境问题是全球关注的热点问题,按要求填空。 (1)生活中经常使用的化石燃料有煤、________、天然气等。 (2)氯化铵固体受热易分解为NH3和HCl气体,此过程需要不断吸收热量,两种产物均不支持燃烧,舞台上的幕布常用浓氯化铵溶液浸泡,可起到防火的作用,此幕布能防火的原理是__________________________________________(写一条即可)。 (3)柴油机尾气中的主要污染物是氮氧化物,某种尾气处理技术利用氨气与氮氧化物发生化学反应,降低污染物排放,反应的微观示意图如图: ①反应Ⅱ的化学方程式为____________________________________; ②E和B的组成元素相同,E能与水反应而B不能,请从微观角度解释其化学性质不同的原因是________________。 18.(4分)食品与健康、能源与环境是我们共同关注的社会问题。 (1)紫薯营养丰富,具有特殊的保健功能。紫薯中富含淀粉、维生素C、维生素B、铁、钙、硒等。 ①这里的“铁”“钙”是指______(填字母序号); A.原子 B.分子 C.元素 D.单质 ②人体缺“铁”,会导致________ 病症; ③硒元素被誉为“抗癌大王”。硒元素的部分信息如图。下列说法正确的是________(填字母序号)。 A.硒属于金属元素 B.一个硒原子中有34个质子 C.硒的原子结构示意图中x=18 D.硒元素的相对原子质量为78.96 g (2)二氧化碳是造成温室效应的主要气体,从“低碳”的角度分析,应尽量减少二氧化碳的排放,将排放出的二氧化碳吸收并转化为可再利用的物质是科学家研究的方向。检验吸收后的气体中是否含有二氧化碳,依据反应的化学方程式是_________________________________ _________________________。 19.(3分)用如图装置研究可燃物的燃烧条件。从a处通入氧气,点燃酒精灯,一段时间后,右侧木炭燃烧;立即从a处改通氮气,燃烧的木炭熄灭。 (1)通入氧气时,左侧木炭未燃烧的原因是____________________。 (2)加热时,右侧木炭通氧气燃烧,改通氮气后熄灭,说明燃烧的条件之一是______________。 (3)实验结束时,应进行的操作依次是_________________________。 三、实验与探究(本题包括2个小题,共14分) 20.(5分)化学是一门以实验为基础的自然科学。依据实验目的设计切实可行的实验方案,是科学探究中的重要环节。 (1)实验1中发生反应的化学方程式为__________________________ _____________,做该实验时往溶液中加入硫酸钠的目的是____________________。 (2)通过实验2可以测定____________________。待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到烧杯中的水进入集气瓶中,液面约上升到刻度______处的现象时,可达到该实验目的。 (3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平________________。 21.(9分)根据下列装置图回答问题: (1)仪器①的名称是____________。 (2)实验室制取二氧化碳选用的发生装置是______(填装置序号),若将二氧化碳气体通入F装置,观察到现象为____________________。 (3)若用高锰酸钾制取氧气,应选用的发生装置为______(填序号),反应化学方程式是______________________________________________ ________________________;所选的发生装置中还缺少________。 (4)氨气(NH3)是一种无色有刺激性气味,极易溶于水的气体。实验室常用氯化铵晶体和氢氧化钙粉末混合加热来制取氨气。选取上述______(填字母)作为制取氨气的发生装置;收集氨气只能选用的装置为______(填字母),其原因是________________________________。 四、分析与计算(本题包括1个小题,共6分) 22.(6分)将3.2 g某红棕色粉末与足量的碳充分反应,将产生的二氧化碳气体全部通入足量的澄清石灰水中,得到3 g白色沉淀。计算: (1)生成二氧化碳的质量。 (2)红棕色粉末中氧元素的质量分数。 参考答案 1.D 2.D 3.B 4.B 5.C 6.A 7.A 8.D 9.D 10.C 11.C 12.A 13.B 14.C 15.A 16.(1)④⑦ NaCl (2)①烧杯、玻璃棒、漏斗 ②AB 17.(1)石油 (2)吸热使温度降到着火点以下(或隔绝氧气) (3)①8NH3+6NO27N2+12H2O ②分子结构不同 18.(1)①C ②贫血 ③BC (2)Ca(OH)2+CO2===CaCO3↓+H2O 19.(1)温度未达到着火点 (2)与氧气接触 (3)先熄灭酒精灯,后停止通氮气 20.(1)2H2O2H2↑+O2↑ 增强溶液的导电性 (2)空气中氧气的含量 1 (3)始终保持平衡 21.(1)长颈漏斗 (2)B 澄清石灰水变浑浊 (3)A 2KMnO4K2MnO4 +MnO2+O2↑ 棉花 (4)A D 氨气极易溶于水,密度比空气小 22.解:(1)设生成二氧化碳的质量为x。 Ca(OH)2+CO2===CaCO3↓+H2O, 44 100 x 3 g = x=1.32 g (2)红棕色粉末中的氧元素完全转化到反应生成的二氧化碳中,因此氧化铁中氧元素质量为1.32 g×=0.96 g, 红棕色粉末中氧元素的质量分数为×100%=30%。 答:(1)生成二氧化碳的质量是1.32 g。 (2)红棕色粉末中氧元素的质量分数为30%。查看更多