- 2021-05-11 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018南京市中考建邺区化学一模
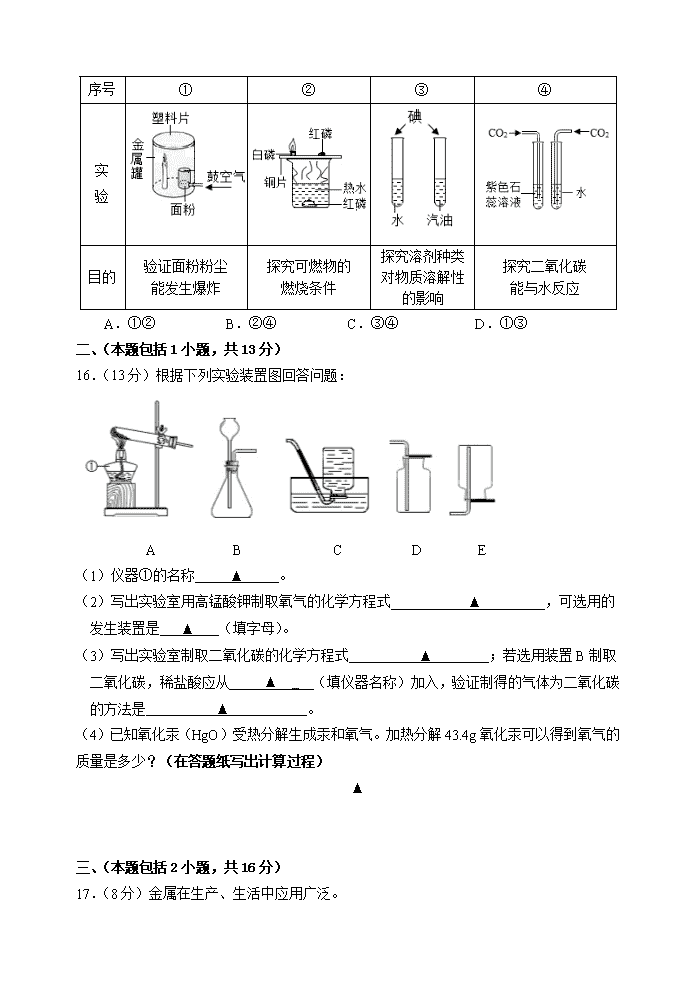
2018年中考第一次模拟调研 九年级化学学科 注意事项: 1.全卷满分80分。考试时间为60分钟。 2.考生答题全部答在答卷纸的指定位置上,在本试卷上或不在规定区域答题无效。 可能用到的相对原子质量:H-1、C-12、O-16、Ca-40、Hg-201 一、选择题(本题共15小题,每小题只有一个选项符合题意。每小题2分,共30分) 1.下列物质不是人体所需营养素的是 A.糖类 B.维生素 C.水 D.甲醛 2.下列化肥属于复合肥料的是 A.CO(NH2)2 B.KCl C.Ca3(PO4)2 D.(NH4)3PO4 3.物质的下列性质中,属于化学性质的是 A. 还原性 B.状态 C.硬度 D.导电性 4.人体内血浆的pH范围是7.35~7.45,说明血浆呈 A.强碱性 B.弱碱性 C.中性 D.弱酸性 5.下列材料中属于合成材料的是 A.玻璃 B.棉花 C.涤纶 D.锰钢 6.下列能源属于可再生能源的是 A.氢气 B.煤 C.石油 D. 天然气 7.下列图示实验操作中,正确的是 A B C D 8.下列做法中,不利于改善环境的是 A.严格监管化肥、农药的使用 B.燃放烟花爆竹 C.禁止工业污水超标排放 D.使用太阳能热水器 9.下列粒子在化学反应中容易得到电子的是 10.下列各组离子在溶液中一定能大量共存的是 A.Ba2+、Na+、SO42-、NO3- B.K+、NH4+、Cl-、OH- C.Ca2+、Mg2+、Cl-、NO3- D.Na+、H+、SO42-、HCO3- 11.罐装液化石油气中含有丙烯(C3H6)、丁烯(C4H8)等成分。下列说法不正确的是 A.丙烯、丁烯属于有机化合物 B.丙烯、丁烯中碳原子与氢原子的个数比均为1∶2 C.丁烯比丙烯多一个碳原子和两个氢原子 D.丙烯和丁烯中碳元素的质量分数相同 12.除去下列物质中的少量杂质(括号内为杂质),拟定实验方案可行的是 A.氨气(水蒸气) 通过足量的浓硫酸 B.C(CuO) 加入过量的稀盐酸,过滤,洗涤,干燥 C.K2CO3固体(KCl) 加入适量稀盐酸,蒸发结晶 D.FeCl2溶液(CuSO4) 加入过量的Fe粉,过滤 13.下列各组物质鉴别方案的描述,正确的是 A.H2、O2、CO、CH4四种气体,用燃着的木条就能将其鉴别出来 B.NH4NO3、NaOH、CaO、NaCl四种固体,只用水就能将其鉴别出来 C.MgCl2、NaOH、HCl、K2SO4四种溶液,只用酚酞溶液及相互反应不能将其鉴别出来 D.浓氨水、浓盐酸、稀硫酸、食盐水四种溶液,通过闻气味就能将其鉴别出来 14.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为50%,将50g该混合物高温煅 烧至固体质量不再改变,则最终固体质量是 A.35g B.25g C.15g D.5g 15.下列实验能达到实验目的的是 序号 ① ② ③ ④ 实 验 目的 验证面粉粉尘 能发生爆炸 探究可燃物的 燃烧条件 探究溶剂种类对物质溶解性的影响 探究二氧化碳 能与水反应 A.①② B.②④ C.③④ D.①③ 二、(本题包括1小题,共13分) 16.(13分)根据下列实验装置图回答问题: A B C D E (1)仪器①的名称 ▲ _ 酒精灯 。 (2)写出实验室用高锰酸钾制取氧气的化学方程式 ▲ _ ,可选用的发生装置是 ▲ _ (填字母)。 (3)写出实验室制取二氧化碳的化学方程式 ▲ ;若选用装置B制取二氧化碳,稀盐酸应从 ▲ _ (填仪器名称)加入,验证制得的气体为二氧化碳的方法是 ▲ _ 。 (4)已知氧化汞(HgO)受热分解生成汞和氧气。加热分解43.4g氧化汞可以得到氧气的质量是多少?(在答题纸写出计算过程) ▲ 三、(本题包括2小题,共16分) 17.(8分)金属在生产、生活中应用广泛。 (1)将铝块制成铝箔是利用了铝的 ▲ _ 。 (2)铁制品锈蚀的过程,实际上是铁与空气中的 ▲ _ 等发生化学反应的过程。请写出稀硫酸去除铁锈的化学方程式 ▲ _ 。而铝具有很好的抗腐蚀性,原因是 ▲ _ 。 (3)小明设计了右图的实验方案,通过观察到 ▲ 的现象,得出三种金属的活动性由强到弱的顺序为铝>铜>银。写出试管乙中反应的化学方程式 ▲ _ 。 18.(8分)水是地球上最常见的物质之一,人类的生活、生产离不开水。 (1)下图是自来水生产流程简化图。 ①上图中物质甲的名称是 ▲ _ ,自来水厂可用二氧化氯进行消毒,写出该物质的化学式并标出氯元素的化合价 ▲ _ 。 ②取少量自来水于试管中,加入肥皂水,振荡,若产生较多 ▲ _ ,则为硬水。 (2)右图是A、B、C三种固体物质(不含结晶水)的溶解度曲线,根据图示回答: ①a点表示t1℃时A物质的溶解度为 ▲ _ 。 ②若将b点的70gA溶液转化为c点的A溶液,则至少加入A的质量为 ▲ g。 ③若将t2℃三种物质的饱和溶液分别降温到t1℃时,三种溶液的溶质质量分数的大小关系是 ▲ _ 。 (3)把50g质量分数为40%的NaOH溶液稀释成10%的NaOH溶液,需要水的体积是 ▲ _ mL(水的密度近似为1g/cm3)。若采用右图所示的操作来量取水的体积(其他操作均正确),则所得溶液的溶质质量分数 ▲ _ (填“大于”、“小于”或“等于”)10%。 四、(本题包括2小题,共10分) NCl3 NH4Cl 反应Ⅲ 反应Ⅰ HCl N2 Cl2 NH3 反应Ⅱ H2 19.(4分)氮是一种地球上含量丰富的元素。下图表示氮及其化合物在一定条件下的转化关系: (1)氮元素在不同的物质中存在循环,体现了化学反应前后 ▲ _ (填“分子种类”、“原子种类”或“离子种类”)不变。 (2)反应Ⅰ所属的基本反应类型是 ▲ 。 (3)反应Ⅱ的化学方程式为__ _ ▲_ 。 20.(6分)下图中的A~J表示几种初中化学常见的物质,分别由H、C、O、S、Ca、Fe、Cu中的元素组成。B、C、G、H、J均属于单质;D、I均属于氧化物;农业上用E与F等配制波尔多液作为农药使用。图中“—”表示两端的物质间能发生化学反应;“ →”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。 D I B G C H A J E F (1)A属于 ▲ (填“酸”、“碱”或“盐”)。 (2)写出构成E的粒子的符号: ▲ 。 (3)写出D→C反应的化学方程式 ▲ 。 (4)写出J→G反应的化学方程式 ▲ 。 五、(本题包括1小题,共11分) 21.(11分)中国科学家屠呦呦因青蒿素和双氢青蒿素而荣获了诺贝尔奖。兴趣小组在老师的指导下对此进行了相关学习与探究。 【查阅资料】(1)青蒿素易溶于乙醚,在水中几乎不溶。 (2)双氢青蒿素是由碳、氢、氧元素组成的,且其相对分子质量不大于300。 【实验探究1】乙醚浸取法制青蒿素的主要工艺如下图所示: 残渣 乙醚 操作Ⅲ 青蒿 干燥、破碎 操作Ⅰ 精品 操作Ⅱ 粗品 蒸馏 提取液 乙醚 操作Ⅰ需要的玻璃仪器主要有:烧杯、漏斗、 ▲ ,操作Ⅱ的原理是利用物质的 ▲ 不同。 双氢 青蒿素 电炉 H2O2溶液 【实验探究2】小组同学设计如下图所示实验测定双氢青蒿素的组成,将7.1g的双氢青蒿素放在燃烧管C中燃烧,回答下列问题。 A B C D E F CuO MnO2 NaOH 无水CaCl2 (1)装置B中试剂名称为 ▲ ,请将装置B中的导管补画完整 ▲ 。 (2)写出E中发生反应的化学方程式 ▲ 。 装置(包括药品) 质量 实验前/g 实验后/g D 84.6 90.0 E 90.2 106.7 (3)实验测得数据如右表: 根据所给数据计算出双氢青蒿素中的碳元素和氢元素的质量比为 ▲ 。 (4)写出双氢青蒿素充分燃烧的化学方程式 ▲ 。 【反思拓展】对“实验探究2”的分析,下列说法正确的是 ▲ 。 A.若缺少装置B,则测出的双氢青蒿素中氢元素的质量偏大 B.若缺少氧化铜,则测出的双氢青蒿素中碳、氧元素的质量比偏小 C.若缺少装置F,则测出的双氢青蒿素中碳元素质量偏小 2018年中考第一次模拟调研 九年级化学参考答案及评分标准 一、选择题(每小题2分,本题共30分。每小题只有一个选项符合题意。) 题号 1 2 3 4 5 6 7 8 答案 D D A B C A C B 题号 9 10 11 12 13 14 15 答案 A C C B B A D 二、(本题包括1小题,化学方程式每个2分,16题(4)5分,其余每空1分,共13分) 16.(14分)(1)酒精灯(2)2KMnO4K2MnO4+MnO2+O2↑ A (3)CaCO3+2HCl CaCl2+H2O+CO2↑ 长颈漏斗 把气体通入澄清石灰水中,澄清石灰水变浑浊 (4)解:设加热分解43.4g氧化汞可得到氧气的质量为x。 2HgO 2Hg + O2↑ 434 32 43.4g x 43432g=43.4gx x=3.2g 答:加热分解43.4g氧化汞可得到氧气的质量为3.2g。 三、(本题包括2小题,化学方程式每个2分,其余每空1分,共16分) 17.(8分)(1)延展性(2)氧气、水蒸气(或水)Fe2O3+3H2SO4 Fe2(SO4)3+3H2O 铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化 (3)甲试管中无明显现象;乙试管中的铜丝表面有银白色固体析出,溶液变为蓝色 Cu+2AgNO3 Cu(NO3)2+2Ag 18.(8分)(1)①活性炭 ②浮渣(或沉淀) (2)① 40g ② 20 ③ B>C>A(3)150 小于 四、(本题包括2小题,化学方程式每个2分,其余每空1分,共10分) 19.(4分)(1)原子种类(2)化合反应(3)3Cl2+8NH3 6NH4C1+N2 20.(6分)(1)酸(2)Cu2+、SO42- (3)2H2O 2H2↑+O2↑ (4)C+2CuO 2Cu+CO2↑ 五、(本题包括1小题,化学方程式每个2分,其余每空1分,【反思拓展】每空2分,共11分) 21.(11分)【实验探究1】玻璃棒 沸点 【实验探究2】(1)浓硫酸 (2)2NaOH+CO2 Na2CO3+H2O (3)15∶2 (4)2C15H24O5+37O2 30CO2+ 24H2O 【反思拓展】AB 查看更多