- 2021-05-10 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
上海中考化学试题含答案精校
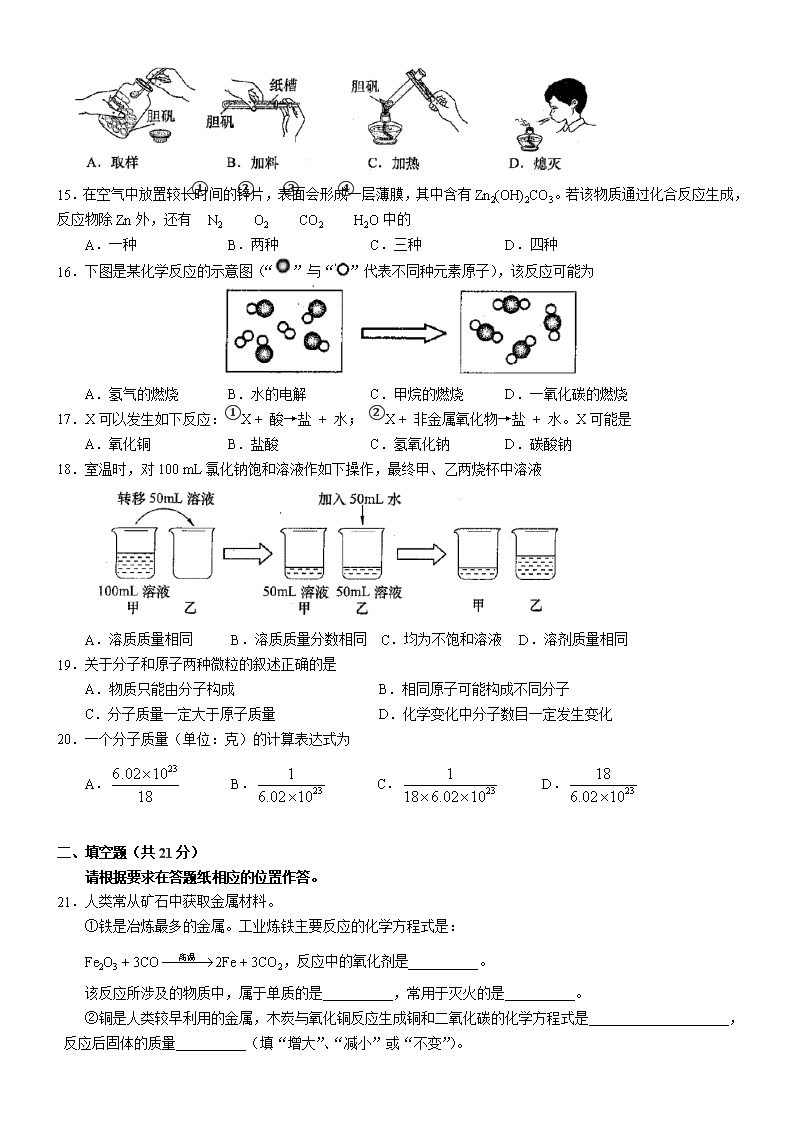
2013年中考卷 可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5 Ca-40 Zn-65 一、选择题(共20分) 下列各题均只有一个正确选项,请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。 1.氦是太阳中含量较多的元素,其元素符号为 A.H B.He C.N D.Cl 2.厨房中的物质放入足量水中,充分搅拌,不能形成溶液的是 A.食用油 B.白醋 C.白糖 D.食盐 3.属于有机物的是 A.C60 B.CO C.H2CO3 D.C2H6O 4.互为同素异形体的一组物质是 A.氢气与液氢 B.水银与银 C.干冰与冰 D.氧气与臭氧 5.Cr2O3可作某些化学反应的催化剂,其中Cr元素的化合价为 A.+2 B.+3 C.+5 D.+6 6.pH是水质检测的重要指标之一,下列水样酸性最强的是 A.pH=1.3的工业废水 B.pH=4.5的雨水 C.pH= 7.0的蒸馏水 D.pH=7.3的矿泉水 7.在充满氧气的集气瓶中燃烧,产生明亮蓝紫色火焰的物质是 A.硫粉 B.铁丝 C.木炭 D.红磷 8.物质的俗名与化学式相对应正确的是 A.天然气:CO B.烧碱:Na2CO3 C.熟石灰:Ca(OH)2 D.纯碱:KOH 9.镁在二氧化碳中燃烧的化学方程式为2Mg+CO2C+2MgO。该反应属于 A.化合反应 B.分解反应 C.置换反应 D.复分解反应 10.用稀硫酸除铁锈的原理是 A.FeO + H2SO4 → FeSO4 + H2O B.Fe2O3 + 3H2SO4 → Fe2(SO4)3+ 3H2↑ C.Fe2O3 + 2H2SO4 → 2FeSO4+ 2H2O D.Fe2O3 + 3H2SO4 → Fe2(SO4)3+ 3H2O 11.自来水厂对天然水进行人工净化的过程中,通常不会采用 A.电解 B.吸附 C.过滤 D.消毒 技术条件 HCl含量 36.0% ~ 38.0% 外观 合格 12.右图为市售盐酸标签的部分内容,其中36.0% ~ 38.0%表示该盐酸中 A.氯元素含量 B.溶质溶解度 C.溶质质量分数 D.溶质式量 13.物质不需要通过化学变化就能体现的性质是 A.可燃性 B.挥发性 C.不稳定性 D.还原性 14.加热胆矾的实验过程中,相关实验操作正确的是 15.在空气中放置较长时间的锌片,表面会形成一层薄膜,其中含有Zn2(OH)2CO3。若该物质通过化合反应生成,反应物除Zn外,还有①N2 ②O2 ③CO2 ④H2O中的 A.一种 B.两种 C.三种 D.四种 16.下图是某化学反应的示意图(“”与“”代表不同种元素原子),该反应可能为 A.氢气的燃烧 B.水的电解 C.甲烷的燃烧 D.一氧化碳的燃烧 17.X可以发生如下反应:①X + 酸→盐 + 水; ②X + 非金属氧化物→盐 + 水。X可能是 A.氧化铜 B.盐酸 C.氢氧化钠 D.碳酸钠 18.室温时,对100 mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液 A.溶质质量相同 B.溶质质量分数相同 C.均为不饱和溶液 D.溶剂质量相同 19.关于分子和原子两种微粒的叙述正确的是 A.物质只能由分子构成 B.相同原子可能构成不同分子 C.分子质量一定大于原子质量 D.化学变化中分子数目一定发生变化 20.一个分子质量(单位:克)的计算表达式为 A. B. C. D. 二、填空题(共21分) 请根据要求在答题纸相应的位置作答。 21.人类常从矿石中获取金属材料。 ①铁是冶炼最多的金属。工业炼铁主要反应的化学方程式是: Fe2O3 + 3CO2Fe + 3CO2,反应中的氧化剂是__________。 该反应所涉及的物质中,属于单质的是__________,常用于灭火的是__________。 ②铜是人类较早利用的金属,木炭与氧化铜反应生成铜和二氧化碳的化学方程式是____________________, 反应后固体的质量__________(填“增大”、“减小”或“不变”)。 ③铝在现代生活中得到广泛应用。炼铝原料水铝石的主要成分是Al(OH)3,Al(OH)3由 种元素组成, 2 mol Al(OH)3中含有__________g氧元素。 ④金属冶炼通常使矿石中金属元素转变为_______(填“化合”或“游离”)态。 22.某实验小组对不同条件下硝酸钾的溶解情况进行了以下实验。 在甲、乙、丙三个烧杯中各放入20.0 g硝酸钾晶体,再分别加入50.0 g冷水、热水与酒精,充分搅拌后(保 持各自温度不变),结果如下图所示。 ①甲烧杯中溶液是__________(填“饱和”或“不饱和”)溶液。 ②由以上实验可得出结论:影响物质溶解性的因素有__________、__________。 ③将乙烧杯中的溶液缓缓降温至t1℃时,溶液恰好达到饱和状态。则t1℃时,硝酸钾的溶解度是________g/100g水。再往乙烧杯中加入10 g 水,改变温度至t2℃时,溶液又恰好达到饱和状态,则t1______t2(填“>”、“<”或“=”)。 ④经实验测定,获得不同温度时硝酸钾的溶解度数据。 温度(℃) 溶解度(g/100g水) 20 31.6 40 63.9 50 145 60 110 70 140 80 169 分析上述数据,某温度时的硝酸钾溶解度数据可能存在较大的误差,该温度是__________℃。 请根据表中数据,在坐标图中描点、绘制符合硝酸钾溶液溶解度变化规律的曲线。__________ 23.如下图所示进行实验,同时将针筒内全部液体迅速注入容器中。实验内容如下表所示。 实验 编号 容器I 针筒I 容器II 针筒II 红墨水 液面位置 A 二氧化碳(充满) 10 mL 澄清石灰水 二氧化碳(充满) 10 mL 水 保持 左高右低 B 0.65 g 锌 15 mL 盐酸 0.24 g 镁 15 mL 盐酸 实验开始前红墨水左右两端液面保持相平,容器I、II体积相同,装置气密性良好。 ①实验a中,容器I内产生的现象是__________________。 红墨水液面位置发生变化的原因是____________________________________(用化学方程式表示)。 ②实验b中,针筒I、II内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器________(填“I”或“II”)。红墨水液面位置变化情况是__________________。 三、简答题(共19分) 请根据要求在答题纸相应的位置作答。 24.某大理石样品(所含杂质不溶于水且不与酸反应)与足量的盐酸充分反应,过滤后将滤液蒸干,冷却后称量所得氯化钙固体。相关实验数据如下图所示(不计损耗): ①氯化钙的质量为__________g。 ②计算该大理石样品中碳酸钙的物质的量(根据化学方程式列式计算)。__________ 25.气体制取是重要的化学实验活动。 ①实验室用双氧水与二氧化锰制取氧气。该方法制取氧气的化学方程式是________________。能收集氧气的装置是________(填编号)。 要得到干燥的氧气,可将制得的气体通过填充有一种氧化物的干燥装置。该氧化物是________。 ②实验室制备二氧化碳时,要求能随时控制反应进行或停止,以下符合该条件的发生装置是________(填编号)。 用所选装置制备二氧化碳,能用于添加液体的仪器名称是________,能使反应暂停的实验操作是________。实验室不适宜用排水集气法收集二氧化碳的理由是________________________。 26.某溶液中可能含有碳酸钠、硫酸钠、氯化钾、盐酸中的一种或几种。为测定其成分,进行如下实验。 第一步:取样,进行焰色反应,透过蓝色钴玻璃片观察到火焰呈紫色。 第二步:另取样,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的物质的量与时间关系如下图所示。 ①由上述实验可知,原溶液中一定含有碳酸钠、硫酸钠和________。 ②第二步实验中,AB之间图象所对应的溶液中的溶质一定有________________。 BC段减少的沉淀是________________。 ③C点沉淀的物质的量为B点沉淀的物质的量的三分之一。原溶液中碳酸钠的物质的量(n1)与硫酸钠的物质的量(n2)的关系为n1=________。 参考答案 六、选择题(每小题1分,共20分) 题号 27 28 29 30 31 32 33 34 35 36 答案 B A D D B A A C C D 题号 37 38 39 40 41 42 43 44 45 46 答案 A C B B C D C A B D 七、填空题 47.(1) Fe2O3或氧化铁 (2) Fe或铁 (3) CO2或二氧化碳 (4) C+2CuO2Cu+CO2↑ (5)减少 (6)3或三 (7) 96 (8)游离 48.(9)饱和 (10)温度 (11)溶剂种类 (12) 40.0 (13)> (14) 50 (15)答案如图。 49.(16)石灰水变浑浊,产生白色沉淀 (17) CO2+Ca(OH)2→CaCO3↓+H2O (18) II (19)开始时左高右低,最终左右相平。 八、简答题(共19分) 50.(1) 11.1 (2) 0.l mol 51.(3) 2H2O22H2O+O2↑ (4)d (5) CaO或氧化钙或生石灰 (6) ad (7)长颈漏斗 (8)在乳胶管处夹紧弹簧夹 (9) CO2可溶于水 52.(10) KC1或氯化钾 (11) NaCl、BaCl2、KC1或氯化钠、氯化钡、氯化钾 (12) BaCO3或碳酸钡 (13) 2n2查看更多