- 2021-08-24 发布 |
- 37.5 KB |
- 9页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019-2020学年湖南省郴州市湘南中学高一上学期期中考试化学试题
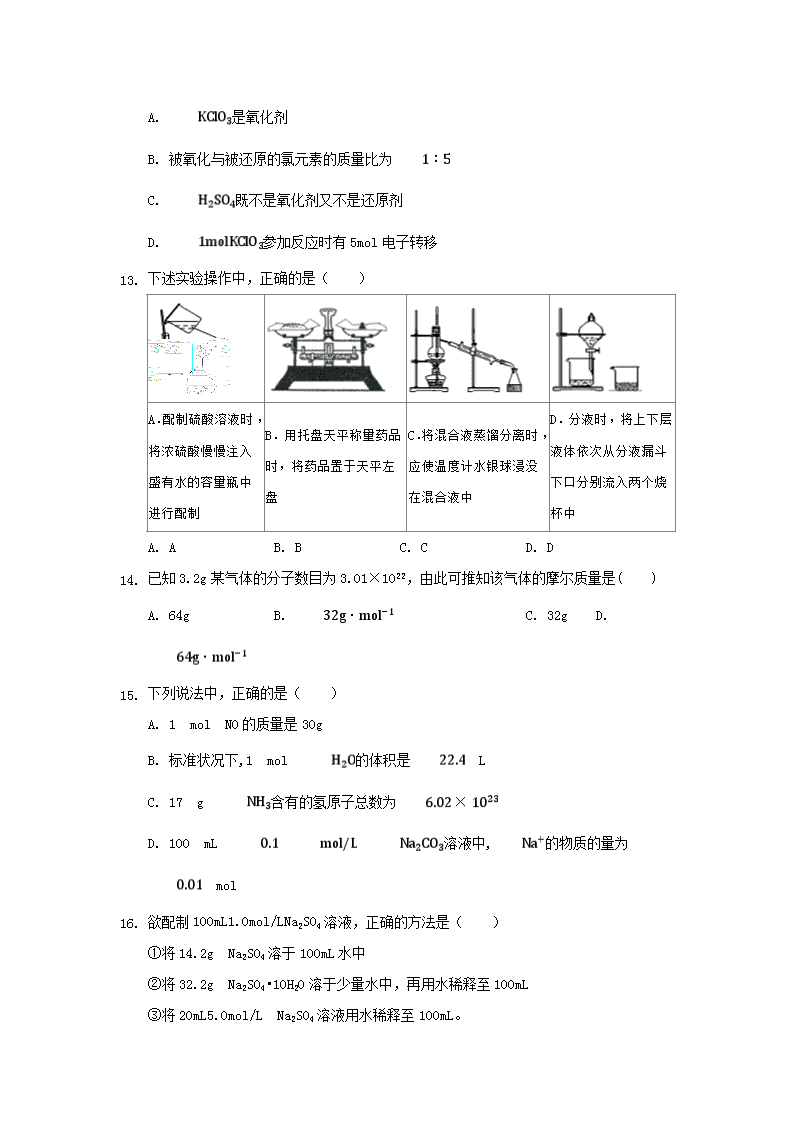
湘南中学2019年下期高一年级期中考试化学学科试卷 时间:90分钟 分值:100分 可能用到的相对原子质量:C-12 H-1 O-16 N-14 Na-23 S-32 一、单选题(共22小题,每小题2分,共44.0分) 1. 下列物质属于纯净物的是( ) A. 氮气 B. 氨水 C. 碘酒 D. 空气 2. 下列反应属于氧化还原反应的是( ) A. B. C. D. 2O 3. 下列化合物依次属于酸、碱、盐、氧化物的一组是 A. NaOH NaCl MgO B. C. CaO D. HBr KOH CuO 4. 我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人。这种做法的化学原因是( ) A. 胶体的电泳 B. 胶体的丁达尔效应 C. 胶体的布朗运动 D. 胶体的聚沉 5. 下列说法正确的是( ) A. 将放入水中不能导电,所以硫酸钡不是电解质 B. NaCl溶液能导电,所以NaCl溶液是电解质 C. 氯化氢溶于水能导电,所以盐酸是电解质 D. 固态的NaCl不导电,熔融态NaCl可以导电 6. 下列离子方程式,书写正确的是( ) A. 盐酸与石灰石反应 B. 硫酸铜溶液中滴加氢氧化钡溶液 C. 氢氧化镁和盐酸反应: D. 氯化铝溶液中加入过量氨水: 1. 某无色透明的酸性溶液中能大量共存的是( ) A. 、、、 B. 、、、 C. 、、、 D. 、、、 2. 下列物质能够导电且属于电解质的是( ) A. 稀盐酸 B. 蔗糖 C. 硝酸钾晶体 D. 熔融氯化钠 3. 在反应中,被氧化与被还原的硫原子数之比为( ) A. 1:2 B. 2:1 C. 1:1 D. 3:2 4. 已知有如下反应: ①ClO3-+5Cl-+6H+=3Cl2+3H2O, ②2FeCl3+2KI=2FeCl2+2KCl+I2, ③2FeCl2+Cl2=2FeCl3,判断下列各微粒氧化能力由强到弱的顺序正确的是( ) A. B. C. D. 5. 下列变化,加入还原剂可以实现的是( ) A. B. C. D. 6. 已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( ) A. 是氧化剂 B. 被氧化与被还原的氯元素的质量比为 C. 既不是氧化剂又不是还原剂 D. 参加反应时有5mol电子转移 1. 下述实验操作中,正确的是( ) A.配制硫酸溶液时,将浓硫酸慢慢注入盛有水的容量瓶中进行配制 B.用托盘天平称量药品时,将药品置于天平左盘 C.将混合液蒸馏分离时,应使温度计水银球浸没在混合液中 D.分液时,将上下层液体依次从分液漏斗下口分别流入两个烧杯中 A. A B. B C. C D. D 2. 已知3.2g某气体的分子数目为3.01×1022,由此可推知该气体的摩尔质量是( ) A. 64g B. C. 32g D. 3. 下列说法中,正确的是( ) A. 1 mol NO的质量是30g B. 标准状况下,1 mol 的体积是 L C. 17 g 含有的氢原子总数为 D. 100 mL 溶液中,的物质的量为 mol 4. 欲配制100mL1.0mol/LNa2SO4溶液,正确的方法是( ) ①将14.2g Na2SO4溶于100mL水中 ②将32.2g Na2SO4•10H2O溶于少量水中,再用水稀释至100mL ③将20mL5.0mol/L Na2SO4溶液用水稀释至100mL。 A. B. C. D. 1. 如果家中的食用花生油不小心混入了大量的水,最简便的分离方法是( ) A. B. C. D. 2. 我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和槽人甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指( ) A. 萃取 B. 渗析 C. 蒸馏 D. 干馏 3. 进行化学实验时应强化安全意识.下列做法正确的是( ) A. 金属钠着火时使用泡沫灭火器灭火 B. 用试管加热碳酸氢钠固体时使试管口竖直向上 C. 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 D. 稀释浓硫酸时应将浓硫酸沿着烧杯内壁慢慢加入水中,并不断搅拌 4. 实验室检验溶液中是否存在SO42―,可选用的化学试剂依次为( ) A. KCl溶液,稀盐酸 B. 稀硝酸,溶液 C. 溶液 ,稀硝酸 D. 稀盐酸,溶液 5. 下列离子方程式的书写中正确的是( ) A. 氢氧化铁与盐酸反应: B. 铁与盐酸反应: C. 氧化铜溶于稀硫酸: D. 向沸水中滴加溶液制备胶体: 1. 能够直接鉴别BaCl2、NaCl、Na2CO3三种溶液的试剂是( ) A. 溶液 B. 稀硫酸 C. 稀盐酸 D. 稀硝酸 二、填空题(共5小题,每空2分,共56分) 2. 用于提纯或分离物质的方法有:A、萃取分液 B、加热分解 C、蒸发结晶 D、分液 E、蒸馏 F、过滤 G、渗析等,请将提纯或分离的序号填在后面横线上。 分离饱和食盐水与泥沙的混合物____________, 精制胶体含有NaCl溶液____________, 分离相溶的沸点为和甲苯的混合物____________, 从碘水里提取碘____________。 3. 实验室用NaOH固体配制250mL 2mol/L的NaOH溶液,填空并请回答下列问题: (1)配制250mL 2mol/L的NaOH溶液 应称取NaOH的质量/g 应选用容量瓶的规格/mL 除容量瓶外还需要的其它仪器 量筒、烧杯、玻璃棒、 ______ (2)容量瓶上需标有以下四项中的______; ①温度、②浓度、③容量、④压强 (3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)______; A、用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡 B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中 D、将容量瓶盖紧,颠倒摇匀 E、改用胶头滴管加水,使溶液凹面恰好与刻度相切 F、继续往容量瓶内小心加水,直到液面接近刻度1-2cm 处 (4)下列配制的溶液浓度偏低的是______ A、定容时俯视刻线 B、向容量瓶中转移溶液时(实验步骤②)不慎有液滴洒在容量瓶外面 C、颠倒摇匀后发现液面低于刻线 D、配制前,容量瓶中有少量蒸馏水 1. 利用相关知识填空。 (1)标准状况下 11.2L NH3 中含_______个氨分子。 (2)物质的量相等的SO2 和 SO3 所含的氧原子数目之比为__________。 (3)4.8g CH4 中所含氢原子的物质的量为______________。 (4)12.4 g Na2R 含 Na+0.4 mol,则 Na2R 的摩尔质量为为_________________。 (5)标况下,一定量的 N2 与 22.4L CO 所含的分子数相等,则 N2 的质量为______。 2. 实验室中用二氧化锰和浓盐酸反应制取氯气的化学方程式为MnO2+4HCl(浓)MnCl2+2H2O+Cl2,请回答下列问题: (1)上述反应中______ 元素的化合价降低,被 ______ (填“氧化”或“还原”)。 (2)若消耗0.1mol MnO2,则还原剂的物质的量是 ______ mol,反应过程中转移电子的物质的量为 ______ mol。 (3)上述反应中浓盐酸表现出的化学性质是 ______ 。 3. 无机化合物可根据其组成和性质进行分类: (1)上述所示的物质分类方法名称是 ______ . (2)①CO2 ②Cu ③FeCl3溶液 ④H2SO4 ⑤氢氧化铁体胶体 ⑥Al2(SO4)3固体 ⑦酒精 ⑧BaSO4固体 属于电解质的是 ______ ; 属于非电解质的是 ______ (填序号)。 ( 3 )请写出⑥的电离方程式 (4)下列关于③和⑤的说法正确的是____________。 a.都不稳定,密封静置会产生沉淀 b.⑤能产生丁达尔效应,而③不能 c.加入盐酸都会产生沉淀 (5)按要求写出下列反应的离子方程式: ①锌跟稀硫酸反应 。 ②氢氧化钡溶液和稀硫酸反应 。 ③MgO滴加稀盐酸 。 湘南中学2019年下学期高一期中考试化学答案 1.【答案】A 2.【答案】C 3.【答案】D 4.【答案】D 5.【答案】D 6.【答案】D 7.【答案】B 8.【答案】D 9.【答案】A 10.【答案】C 11.【答案】C 12.【答案】B 13.【答案】B 14.【答案】D 15.【答案】A 16.【答案】B 17.【答案】B 18.【答案】C 19.【答案】D 20.【答案】D 21.【答案】C 22.【答案】B 23.【答案】(1)F;(2)G;(3)E;(4)A 24.【答案】 20.0g 250mL 胶头滴管 ①③ B、C、A、F、E、D B 25.【答案】(1)0.5NA (2)2:3 (3)1.2 mol (4)62g/mol (5)28g 26.【答案】(1)Mn;还原; (2)0.2;0.2; (3)还原性、酸性。 27.【答案】 (1)树状分类法;(2)④⑥⑧;①⑦; (3)Al2(SO4)3 = 2Al3+ + 3SO42- (4)b; (5)①Zn+2H+=Zn2++H2↑;②Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O; ③MgO+2H+=Mg2++H2O 查看更多