- 2021-07-03 发布 |
- 37.5 KB |
- 44页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
通用版五年2016_2020高考化学真题专题点拨专题11化学工艺流程含解析
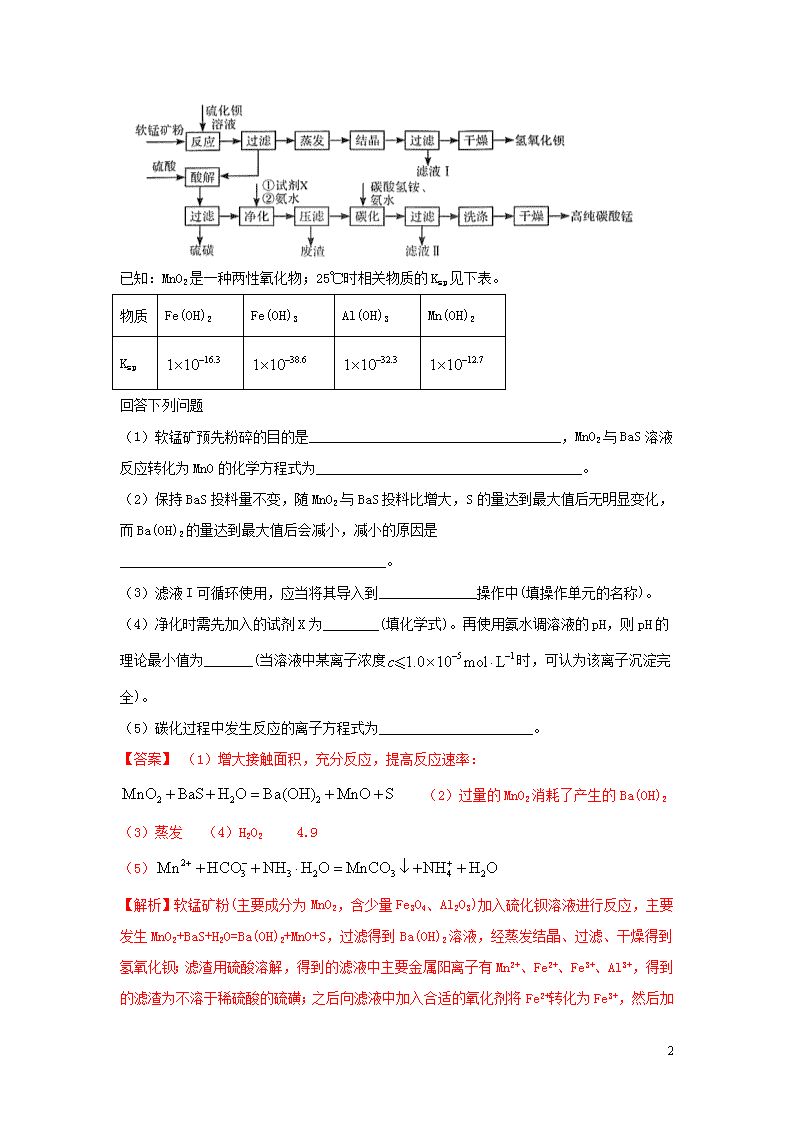
专题11 化学工艺流程 【2020年】 1.(2020·山东卷)以菱镁矿(主要成分为MgCO3,含少量SiO2,Fe2O3和A12O3)为原料制备高纯镁砂的工艺流程如下: 已知浸出时产生的废渣中有SiO2,Fe(OH)3和Al(OH)3。下列说法错误的是 A. 浸出镁的反应为 B. 浸出和沉镁的操作均应在较高温度下进行 C. 流程中可循环使用的物质有NH3、NH4Cl D. 分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物Ksp的不同 【答案】B 【解析】菱镁矿煅烧后得到轻烧粉,MgCO3转化为MgO,加入氯化铵溶液浸取,浸出的废渣有SiO2、Fe(OH)3、Al(OH)3,同时产生氨气,则此时浸出液中主要含有Mg2+,加入氨水得到Mg(OH)2沉淀,煅烧得到高纯镁砂。高温煅烧后Mg元素主要以MgO的形式存在,MgO可以与铵根水解产生的氢离子反应,促进铵根的水解,所以得到氯化镁、氨气和水,化学方程式为MgO+2NH4Cl=MgCl2+2NH3↑+H2O,故A正确;一水合氨受热易分解,沉镁时在较高温度下进行会造成一水合氨大量分解,挥发出氨气,降低利用率,故B错误;浸出过程产生的氨气可以回收制备氨水,沉镁时氯化镁与氨水反应生成的氯化铵又可以利用到浸出过程中,故C正确;Fe(OH)3、Al(OH)3的Ksp远小于Mg(OH)2的Ksp,所以当pH达到一定值时Fe3+、Al3+产生沉淀,而Mg2+不沉淀,从而将其分离,故D正确;故答案为B。 2.(2020·山东卷)用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下: 44 已知:MnO2是一种两性氧化物;25℃时相关物质的Ksp见下表。 物质 Fe(OH)2 Fe(OH)3 Al(OH)3 Mn(OH)2 Ksp 回答下列问题 (1)软锰矿预先粉碎的目的是____________________________________,MnO2与BaS溶液反应转化为MnO的化学方程式为______________________________________。 (2)保持BaS投料量不变,随MnO2与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是______________________________________。 (3)滤液I可循环使用,应当将其导入到______________操作中(填操作单元的名称)。 (4)净化时需先加入的试剂X为________(填化学式)。再使用氨水调溶液的pH,则pH的理论最小值为_______(当溶液中某离子浓度时,可认为该离子沉淀完全)。 (5)碳化过程中发生反应的离子方程式为______________________。 【答案】 (1)增大接触面积,充分反应,提高反应速率: (2)过量的MnO2消耗了产生的Ba(OH)2 (3)蒸发 (4)H2O2 4.9 (5) 【解析】软锰矿粉(主要成分为MnO2,含少量Fe3O4、Al2O3)加入硫化钡溶液进行反应,主要发生MnO2+BaS+H2O=Ba(OH)2+MnO+S,过滤得到Ba(OH)2溶液,经蒸发结晶、过滤、干燥得到氢氧化钡;滤渣用硫酸溶解,得到的滤液中主要金属阳离子有Mn2+、Fe2+、Fe3+、Al3+,得到的滤渣为不溶于稀硫酸的硫磺;之后向滤液中加入合适的氧化剂将Fe2+转化为Fe3+ 44 ,然后加入氨水调节pH,使Fe3+、Al3+转化为沉淀除去,压滤得到的废渣为Fe(OH)3和Al(OH)3,此时滤液中的金属阳离子只有Mn2+,向滤液中加入碳酸氢铵、氨水,Mn2+和碳酸氢根电离出的碳酸根结合生成碳酸锰沉淀,过滤、洗涤、干燥得到高纯碳酸锰。 (1)软锰矿预先粉碎可以增大反应物的接触面积,使反应更充分,提高反应速率;MnO2与BaS反应转化为MnO,Mn元素的化合价由+4价降低为+2价,根据元素价态规律可知-2价的S元素应被氧化得到S单质,则MnO2与BaS的系数比应为1:1,根据后续流程可知产物还有Ba(OH)2,结合元素守恒可得化学方程式为:MnO2+BaS+H2O=Ba(OH)2+MnO+S; (2)根据题目信息可知MnO2为两性氧化物,所以当MnO2过量时,会消耗反应产生的Ba(OH)2,从而使Ba(OH)2的量达到最大值或会减小; (3)滤液I为结晶后剩余的Ba(OH)2饱和溶液,所以可以导入到蒸发操作中循环使用; (4)净化时更好的除去Fe元素需要将Fe2+氧化为Fe3+,为了不引入新的杂质,且不将Mn元素氧化,加入的试剂X可以是H2O2;根据表格数据可知,Fe(OH)3和Al(OH)3为同种沉淀,而Al(OH)3的Ksp稍大,所以当Al3+完全沉淀时,Fe3+也一定完全沉淀,当c(Al3+)=1.0×10-5mol/L时,c(OHˉ)==10-9.1mol/L,所以c(H+)=10-4.9mol/L,pH=4.9,即pH的理论最小值为4.9; (5)碳化过程Mn2+和碳酸氢根电离出的碳酸根结合生成碳酸锰沉淀,促进碳酸氢根的电离,产生的氢离子和一水合氨反应生成铵根和水,所以离子方程式为Mn2++HCO+NH3·H2O=MnCO3↓+NH+H2O。 3.(2020·新课标Ⅰ)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。 该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示: 金属离子 Fe3+ Fe2+ Al3+ Mn2+ 开始沉淀pH 1.9 7.0 3.0 8.1 44 完全沉淀pH 3.2 9.0 4.7 10.1 回答下列问题: (1)“酸浸氧化”需要加热,其原因是______________________________________。 (2)“酸浸氧化”中,VO+和VO2+被氧化成,同时还有___________离子被氧化。写出VO+转化为反应的离子方程式_____________________________。 (3)“中和沉淀”中,钒水解并沉淀为,随滤液②可除去金属离子K+、Mg2+、Na+、___________,以及部分的_____________________________。 (4)“沉淀转溶”中,转化为钒酸盐溶解。滤渣③的主要成分是___________。 (5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是___________。 (6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是___________。 【答案】(1)加快酸浸和氧化反应速率(促进氧化完全) (2)Fe2+ VO++MnO2+2H+=+Mn2++H2O (3) Mn2+ Fe3+、Al3+ (4)Fe(OH)3 (5)NaAlO2+HCl+H2O=NaCl+Al(OH)3↓或Na[Al(OH)4]+HCl= NaCl+Al(OH)3↓+H2O (6)利用同离子效应,促进NH4VO3尽可能析出完全 【解析】黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4,用30%H2SO4和MnO2“酸浸氧化”时VO+和VO2+被氧化成,Fe3O4与硫酸反应生成的Fe2+被氧化成Fe3+,SiO2此过程中不反应,滤液①中含有、K+、Mg2+、Al3+、Fe3+、Mn2+、;滤液①中加入NaOH调节pH=3.0~3.1,钒水解并沉淀为V2O5·xH2O,根据表中提供的溶液中金属离子开始沉淀和完全沉淀的pH,此过程中Fe3+部分转化为Fe(OH)3沉淀,部分Al3+转化为Al(OH)3沉淀,滤液②中含有K+、Na+、Mg2+、Al3+、Fe3+、Mn2+、,滤饼②中含V2O5·xH2O、Fe(OH)3、Al(OH)3,滤饼②中加入NaOH使pH>13,V2O5·xH2O转化为钒酸盐溶解,Al(OH)3转化为NaAlO2,则滤渣③的主要成分为Fe(OH)3;滤液③中含钒酸盐、偏铝酸钠,加入HCl调pH=8.5,NaAlO2转化为Al(OH)3沉淀而除去;最后向滤液④中加入NH4Cl“沉钒”得到NH4VO3。 44 (1)“酸浸氧化”需要加热,其原因是:升高温度,加快酸浸和氧化反应速率(促进氧化完全); (2) “酸浸氧化”中,钒矿粉中的Fe3O4与硫酸反应生成FeSO4、Fe2(SO4)3和水,MnO2具有氧化性,Fe2+具有还原性,则VO+和VO2+被氧化成的同时还有Fe2+被氧化,反应的离子方程式为MnO2+2Fe2++4H+= Mn2++2Fe3++2H2O;VO+转化为时,钒元素的化合价由+3价升至+5价,1molVO+失去2mol电子,MnO2被还原为Mn2+,Mn元素的化合价由+4价降至+2价,1molMnO2得到2mol电子,根据得失电子守恒、原子守恒和电荷守恒,VO+转化为反应的离子方程式为VO++MnO2+2H+=+Mn2++H2O; (3)根据分析,“中和沉淀”中,钒水解并沉淀为V2O5·xH2O,随滤液②可除去金属离子K+、Mg2+、Na+、Mn2+,以及部分的Fe3+、Al3+; (4)根据分析,滤渣③的主要成分是Fe(OH)3; (5)“调pH”中有沉淀生成,是NaAlO2与HCl反应生成Al(OH)3沉淀,生成沉淀反应的化学方程式是NaAlO2+HCl+H2O=NaCl+Al(OH)3↓或Na[Al(OH)4]+HCl= NaCl+Al(OH)3↓+H2O。 (6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是:增大NH4+离子浓度,利用同离子效应,促进NH4VO3尽可能析出完全。 4.(2020·新课标Ⅲ)某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O): 溶液中金属离子开始沉淀和完全沉淀的pH如下表所示: 金属离子 Ni2+ Al3+ Fe3+ Fe2+ 开始沉淀时(c=0.01 mol·L−1)的pH 沉淀完全时(c=1.0×10−5 mol·L−1)的pH 7.2 8.7 3.7 4.7 2.2 3.2 7.5 9.0 回答下列问题: (1)“碱浸”中NaOH的两个作用分别是_________________________________ 44 ___。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式_________________________。 (2)“滤液②”中含有的金属离子是_________________________。 (3)“转化”中可替代H2O2的物质是_________________________。若工艺流程改为先“调pH”后“转化”,即 “滤液③”中可能含有的杂质离子为_________________________。 (4)利用上述表格数据,计算Ni(OH)2的Ksp=______________(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L−1,则“调pH”应控制的pH范围是_________________________。 (5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_________________________。 (6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是_________________________。 【答案】(1)除去油脂、溶解铝及其氧化物 +H++H2O=Al(OH)3↓或+H+=Al(OH)3↓+H2O (2)Ni2+、Fe2+、Fe3+ (3)O2或空气 Fe3+ (4) 3.2~6.2 (5)2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H2O (6)提高镍回收率 【解析】由工艺流程分析可得,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,并发生反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑、2Al2O3+4NaOH=4NaAlO2+2H2O将Al及其氧化物溶解,得到的滤液①含有NaAlO2,滤饼①为Ni、Fe及其氧化物和少量其他不溶性杂质,加稀H2SO4酸浸后得到含有Ni2+、Fe2+、Fe3+的滤液②,Fe2+经H2O2氧化为Fe3+后,加入NaOH调节pH使Fe3+转化为Fe(OH)3沉淀除去,再控制pH浓缩结晶得到硫酸镍的晶体,据此分析解答问题。 (1)根据分析可知,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,并将Al及其氧化物溶解,滤液①中含有NaAlO2(或Na[Al(OH)4]),加入稀硫酸可发生反应 44 +H++H2O=Al(OH)3↓或+H+=Al(OH)3↓+H2O; (2)加入稀硫酸酸浸,Ni、Fe及其氧化物溶解,所以“滤液②”中含有的金属离子是Ni2+、Fe2+、Fe3+; (3)“转化”在H2O2的作用是将Fe2+氧化为Fe3+,可用O2或空气替代;若将工艺流程改为先“调pH”后“转化”,会使调pH过滤后的溶液中含有Fe2+,则滤液③中可能含有转化生成的Fe3+; (4)由上述表格可知,Ni2+完全沉淀时的pH=8.7,此时c(Ni2+)=1.0×10-5mol·L-1,c(H+)=1.0×10-8.7mol·L-1,则c(OH-)=,则Ni(OH)2的;或者当Ni2+开始沉淀时pH=7.2,此时c(Ni2+)=0.01mol·L-1,c(H+)=1.0×10-7.2mol·L-1,则c(OH-)=,则Ni(OH)2的;如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,为避免镍离子沉淀,此时,则,即pH=6.2;Fe3+完全沉淀的pH为3.2,因此“调节pH”应控制的pH范围是3.2~6.2; (5)由题干信息,硫酸镍在强碱中被NaClO氧化得到NiOOH沉淀,即反应中Ni2+被氧化为NiOOH沉淀,ClOˉ被还原为Clˉ,则根据氧化还原得失电子守恒可得离子方程式为2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H2O; (6)分离出硫酸镍晶体后的母液中还含有Ni2+,可将其收集、循环使用,从而提高镍的回收率。 5.(2020·江苏卷)实验室由炼钢污泥(简称铁泥,主要成份为铁的氧化物)制备软磁性材料α-Fe2O3。 其主要实验流程如下: (1)酸浸:用一定浓度的H2SO4 44 溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能提高铁元素浸出率的有___________(填序号)。 A.适当升高酸浸温度 B.适当加快搅拌速度 C.适当缩短酸浸时间 (2)还原:向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中除生成Fe2+外,还会生成___________(填化学式);检验Fe3+是否还原完全的实验操作是______________。 (3)除杂:向“还原”后的滤液中加入NH4F溶液,使Ca2+转化为CaF2沉淀除去。若溶液的pH偏低、将会导致CaF2沉淀不完全,其原因是___________[,]。 (4)沉铁:将提纯后的FeSO4溶液与氨水-NH4HCO3混合溶液反应,生成FeCO3沉淀。 ①生成FeCO3沉淀的离子方程式为____________________________________。 ②设计以FeSO4溶液、氨水- NH4HCO3混合溶液为原料,制备FeCO3的实验方案:______________。 【FeCO3沉淀需“洗涤完全”,Fe(OH)2开始沉淀的pH=6.5】。 【答案】(1)AB H2 (2)取少量清液,向其中滴加几滴KSCN溶液,观察溶液颜色是否呈血红色 (3) pH偏低形成HF,导致溶液中F-浓度减小,CaF2沉淀不完全 (4)或 在搅拌下向FeSO4溶液中缓慢加入氨水-NH4HCO3混合溶液,控制溶液pH不大于6.5;静置后过滤,所得沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后的滤液,滴加盐酸酸化的BaCl2溶液,不出现白色沉淀 【解析】铁泥的主要成份为铁的氧化物,铁泥用H2SO4溶液“酸浸”得到相应硫酸盐溶液,向“酸浸”后的滤液中加入过量铁粉将Fe3+还原为Fe2+;向“还原”后的滤液中加入NH4F使Ca2+转化为CaF2沉淀而除去;然后进行“沉铁”生成FeCO3,将FeCO3沉淀经过系列操作制得α—Fe2O3;据此分析作答。 44 (1)适当升高酸浸温度,加快酸浸速率,能提高铁元素的浸出率,A选;适当加快搅拌速率,增大铁泥与硫酸溶液的接触,加快酸浸速率,能提高铁元素的浸出率,B选;适当缩短酸浸时间,铁元素的浸出率会降低,C不选; (2)为了提高铁元素的浸出率,“酸浸”过程中硫酸溶液要适当过量,故向“酸浸”后的滤液中加入过量的铁粉发生的反应有:Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑,“还原”过程中除生成Fe2+外,还有H2生成;通常用KSCN溶液检验Fe3+,故检验Fe3+是否还原完全的实验操作是:取少量清液,向其中滴加几滴KSCN溶液,观察溶液颜色是否呈血红色,若不呈血红色,则Fe3+还原完全,若溶液呈血红色,则Fe3+没有还原完全。 (3)向“还原”后的滤液中加入NH4F溶液,使Ca2+转化为CaF2沉淀,Ksp(CaF2)=c(Ca2+)·c2(F-),当Ca2+完全沉淀(某离子浓度小于1×10-5mol/L表明该离子沉淀完全)时,溶液中c(F-)至少为mol/L=×10-2mol/L;若溶液的pH偏低,即溶液中H+浓度较大,H+与F-形成弱酸HF,导致溶液中c(F-)减小,CaF2沉淀不完全。 (4)①将提纯后的FeSO4溶液与氨水—NH4HCO3混合溶液反应生成FeCO3沉淀,生成FeCO3的化学方程式为FeSO4+NH3·H2O+NH4HCO3=FeCO3↓+(NH4)2SO4+H2O[或FeSO4+NH3+NH4HCO3=FeCO3↓+(NH4)2SO4],离子方程式为Fe2+++NH3·H2O=FeCO3↓++H2O(或Fe2+++NH3=FeCO3↓+)。 ②根据题意Fe(OH)2开始沉淀的pH=6.5,为防止产生Fe(OH)2沉淀,所以将FeSO4溶液与氨水—NH4HCO3混合溶液反应制备FeCO3沉淀的过程中要控制溶液的pH不大于6.5;FeCO3沉淀需“洗涤完全”,所以设计的实验方案中要用盐酸酸化的BaCl2溶液检验最后的洗涤液中不含 。 【2019年】 1.[2019·新课标Ⅰ]硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下: 44 回答下列问题: (1)在95 ℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。 (2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。 (3)根据H3BO3的解离反应:H3BO3+H2O===H++B(OH)−4,Ka=5.81×10−10,可判断H3BO3是______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。 (4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为__________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。 【答案】(1)NH4HCO3+NH3== (NH4)2CO3 (2)SiO2、Fe2O3、Al2O3 KSCN (3)一元弱 转化为H3BO3,促进析出 (4)2Mg2++3 CO32-+2H2O==Mg(OH)2·MgCO3↓+2 HCO3- (或2Mg2++2 CO32-+H2O==Mg(OH)2·MgCO3↓+CO2↑) 溶浸 高温焙烧 【解析】(1)根据流程图知硼镁矿粉中加入硫酸铵溶液产生的气体为氨气,用碳酸氢铵溶液吸收,反应方程式为:NH3+NH4HCO3== (NH4)2CO3。 (2)滤渣I为不与硫酸铵溶液反应的Fe2O3、Al2O3、SiO2;检验Fe3+,可选用的化学试剂为KSCN, (3)由硼酸的离解方程式知,硼酸在水溶液中是通过与水分子的配位作用产生氢离子,而三价硼原子最多只能再形成一个配位键,且硼酸不能完全解离,所以硼酸为一元弱酸;在“过滤2”前,将溶液pH调节至3.5,目的是将B(OH)−4转化为H3BO3,并促进H3BO3析出, (4)沉镁过程中用碳酸铵溶液与Mg2+反应生成Mg(OH)2∙MgCO3,沉镁过程的离子反应为:2Mg2++2H2O+3CO32-==Mg(OH)2∙MgCO3↓+2HCO3-;母液加热分解后生成硫酸铵溶液,可以返回“溶浸”工序循环使用;碱式碳酸镁不稳定,高温下可以分解,故由碱式碳酸镁制备轻质氧化镁的方法是高温焙烧。 2.[2019·新课标Ⅱ]立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。回答下列问题: (1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为__________(填标号)。 A.黄色 B.红色 C.紫色 D.绿色 44 (2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉: ①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为______________________。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为______________________。 ②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差。其原因是“还原料”表面生成了难溶于水的___________(填化学式)。 ③沉淀器中反应的离子方程式为______________________。 (3)成品中S2−的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol·L−1的I2−KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉为指示剂,过量的I2用0.1000 mol·L−1Na2S2O3溶液滴定,反应式为I2+2==2I−+。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为_________________,样品中S2−的含量为______________(写出表达式)。 【答案】(1)D (2)①BaSO4+4C==BaS+4CO↑ CO+H2O==CO2+H2 ②BaCO3 ③S2−+Ba2++Zn2++== BaSO4·ZnS↓ (3)浅蓝色至无色 【解析】 (1)焰色反应不是化学变化,常用来检验金属元素存在,常见金属元素焰色:A.钠的焰色为黄色,故A错误;B.钙的焰色为红色,故B错误;C.钾的焰色为紫色,故C错误;D.钡的焰色为绿色,故D正确;故选D。 (2)①注意焦炭过量生成CO,反应物为硫酸钡与焦炭,产物为BaS与CO,写出方程式BaSO4+4C==BaS+4CO↑;CO与水蒸气反应生成CO2与H2,写出方程式:CO+H2O==CO2+H2。 ②根据信息臭鸡蛋气味气体为硫化氢气体,由强酸制弱酸原理,还原料硫化钡与空气中水,二氧化碳反应生成了碳酸钡与硫化氢气体。 44 ③硫化钡与硫酸锌为可溶性强电解质,写成离子形式,产物硫酸钡与硫化锌为沉淀,不可电离,写出离子方程式:S2−+Ba2++Zn2++ SO42-==BaSO4·ZnS↓。 (3)碘单质与硫离子的反应:S2-+I2==S+2I-;碘单质与淀粉混合为蓝色,用硫代硫酸钠滴定过量的I2,故终点颜色变化为浅蓝色至无色;根据氧化还原反应得失电子数相等,利用关系式法解题;根据化合价升降相等列关系式,设硫离子物质的量为n mol: S2- ~ I2 2S2O32- ~ I2 1 mol 1 mol 2 mol 1 mol n mol n mol 0.1V×10-3mol 0.1V×10-3mol n+0.1V×10-3mol=250.1V×10-3mol,得n=(25-V)0.1×10-3mol 则样品中硫离子含量为:×100%= ×100%。 3.[2019·新课标Ⅲ] 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题: 相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下: 金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+ 开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9 沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9 (1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。 (2)“氧化”中添加适量的MnO2的作用是________________________。 (3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。 (4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。 44 (5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。 (6)写出“沉锰”的离子方程式___________________________________________________。 (7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=时,z=___________。 【答案】(1)SiO2(不溶性硅酸盐) MnO2+MnS+2H2SO4==2MnSO4+S+2H2O (2)将Fe2+氧化为Fe3+ (3)4.7 (4)NiS和ZnS (5)F−与H+结合形成弱电解质HF,MgF2Mg2++2F−平衡向右移动 (6)Mn2++2 HCO3-==MnCO3↓+CO2↑+H2O (7) 【解析】(1)Si元素以SiO2或不溶性硅盐存在,SiO2与硫酸不反应,所以滤渣I中除了S还有SiO2;在硫酸的溶浸过程中,二氧化锰和硫化锰发生了氧化还原反应,二氧化锰作氧化剂,硫化锰作还原剂,方程式为:MnO2+MnS+2H2SO4==2MnSO4+S+2H2O。 (2)二氧化锰作为氧化剂,使得MnS反应完全,且将溶液中Fe2+氧化为Fe3+。 (3)由表中数据知pH在4.7时,Fe3+和Al3+沉淀完全,所以应该控制pH在4.7~6之间。 (4)根据题干信息,加入Na2S除杂为了除去锌离子和镍离子,所以滤渣3是生成的沉淀ZnS和NiS。 (5)由HFH++F-知,酸度过大,F-浓度减低,使得MgF2Mg2++2F-平衡向沉淀溶解方向移动,Mg2+沉淀不完全。 (6)根据题干信息沉锰的过程是生成了MnCO3沉淀,所以反应离子方程式为:Mn2++2HCO3-==MnCO3↓+CO2↑+H2O。 (7)根据化合物中各元素化合价代数和为0的规律得:1+2x+3y+4z=6,已知,x=y=1/3,带入计算得:z=1/3。 4.[2019·江苏卷]实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下: 44 (1)室温下,反应CaSO4(s)+ CO32- (aq)CaCO3(s)+ SO42- (aq)达到平衡,则溶液中= ▲ [Ksp(CaSO4)=4.8×10−5,Ksp(CaCO3)=3×10−9]。 (2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为 ▲ ;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是 ▲ 。 (3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是 ▲ ;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有 ▲ 。 (4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案: ▲ [已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。实验中必须使用的试剂:盐酸和Ca(OH)2]。 【答案】(1)1.6×104 (2)HCO3-+NH3·H2O== NH4++ CO32-+H2O(或HCO3-+NH3·H2O NH4++ CO32-+H2O) 增加溶液中CO32-的浓度,促进CaSO4的转化 (3)温度过高,(NH4)2CO3分解 加快搅拌速率 (4)在搅拌下向足量稀盐酸中分批加入滤渣,待观察不到气泡产生后,过滤,向滤液中分批加入少量Ca(OH)2,用pH试纸测量溶液pH,当pH介于5~8.5时,过滤 【解析】 (1)反应CaSO4(s)+CO32-(aq)CaCO3(s)+SO42-(aq)达到平衡时,溶液中 44 ====1.6×104。 (2)NH4HCO3属于酸式盐,与氨水反应生成(NH4)2CO3,反应的化学方程式为NH4HCO3+NH3·H2O=(NH4)2CO3+H2O[或NH4HCO3+NH3·H2O(NH4)2CO3+H2O],离子方程式为HCO3-+NH3·H2O=NH4++CO32-+H2O(或HCO3-+NH3·H2ONH4++CO32-+H2O);浸取废渣时,加入的(NH4)2CO3属于弱酸弱碱盐,溶液中存在水解平衡:CO32-+NH4++H2OHCO3-+NH3·H2O,加入适量浓氨水,水解平衡逆向移动,溶液中CO32-的浓度增大,反应CaSO4(s)+CO32-(aq)CaCO3(s)+SO42-(aq)正向移动,促进CaSO4的转化。 (3)由于铵盐具有不稳定性,受热易分解,所以温度过高,(NH4)2CO3分解,从而使CaSO4转化率下降;由于浸取过程中的反应属于固体与溶液的反应(或发生沉淀的转化),保持温度、反应时间、反应物和溶剂的量不变,提高CaSO4转化率即提高反应速率,结合外界条件对化学反应速率的影响,实验过程中提高CaSO4转化率的操作为加快搅拌速率(即增大接触面积,加快反应速率,提高浸取率)。 (4)工业废渣主要含CaSO4·2H2O,还含有少量SiO2、Al2O3和Fe2O3,加入(NH4)2CO3溶液浸取,其中CaSO4与(NH4)2CO3反应生成CaCO3和(NH4)2SO4,SiO2、Al2O3和Fe2O3都不反应,过滤后所得滤渣中含CaCO3、SiO2、Al2O3和Fe2O3;若以水洗后的滤渣为原料制取CaCl2溶液,根据题给试剂,首先要加入足量盐酸将CaCO3完全转化为CaCl2,发生的反应为CaCO3+2HCl=CaCl2+H2O+CO2↑,与此同时发生反应Al2O3+6HCl=2AlCl3+3H2O、Fe2O3+6HCl=2FeCl3+3H2O,SiO2不反应,经过滤除去SiO2;得到的滤液中含CaCl2、AlCl3、FeCl3,根据“pH=5时Fe(OH)3和Al(OH)3沉淀完全,pH=8.5时Al(OH)3开始溶解”,为了将滤液中Al3+、Fe3+完全除去,应加入Ca(OH)2调节溶液的pH介于5~8.5[加入Ca(OH)2的过程中要边加边测定溶液的pH],然后过滤即可制得CaCl2溶液。 【2018年】 1. (2018·全国卷Ⅰ)焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题: (1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式__________。 (2)利用烟道气中的SO2生产Na2S2O5的工艺为: 44 ①pH=4.1时,Ⅰ中为__________溶液(写化学式)。 ②工艺中加入Na2CO3固体、并再次充入SO2的目的是__________。 (3)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为_____________。电解后,__________室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。 (4)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.01000 mol·L−1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为_____________,该样品中Na2S2O5的残留量为____________g·L−1(以SO2计)。 【答案】 (1). 2NaHSO3=Na2S2O5+H2O (2). ①NaHSO3 ② 得到NaHSO3过饱和溶液 (3). 2H2O-4e-=4H++O2↑ a (4). S2O52-+2I2+3H2O=2SO42-+4I-+6H+ 0.128 【解析】 (1)亚硫酸氢钠过饱和溶液脱水生成焦亚硫酸钠,根据原子守恒可知反应的方程式为2NaHSO3=Na2S2O5+H2O; (2)①碳酸钠饱和溶液吸收SO2后的溶液显酸性,说明生成物是酸式盐,即Ⅰ中为NaHSO3; ②要制备焦亚硫酸钠,需要制备亚硫酸氢钠过饱和溶液,因此工艺中加入碳酸钠固体、并再次充入二氧化硫的目的是得到NaHSO3过饱和溶液; (3)阳极发生失去电子的氧化反应,阳极区是稀硫酸,氢氧根放电,则电极反应式为2H2O-4e-=4H++O2↑。阳极区氢离子增大,通过阳离子交换膜进入a室与亚硫酸钠结合生成亚硫酸钠。阴极是氢离子放电,氢氧根浓度增大,与亚硫酸氢钠反应生成亚硫酸钠,所以电解后a室中亚硫酸氢钠的浓度增大。 44 (4)单质碘具有氧化性,能把焦亚硫酸钠氧化为硫酸钠,反应的方程式为S2O52-+2I2+3H2O=2SO42-+4I-+6H+;消耗碘的物质的量是0.0001mol,所以焦亚硫酸钠的残留量(以SO2计)是。 2. (2018·全国卷II)我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示: 相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下: 金属离子 Fe3+ Fe2+ Zn2+ Cd2+ 开始沉淀的pH 1.5 6.3 6.2 7.4 沉淀完全的pH 2.8 8.3 8.2 9.4 回答下列问题: (1)焙烧过程中主要反应的化学方程式为_______________________。 (2)滤渣1的主要成分除SiO2外还有___________;氧化除杂工序中ZnO的作用是____________,若不通入氧气,其后果是________________。 (3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。 (4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返回_______工序继续使用。 【答案】 (1). ZnS+O2ZnO+SO2 (2). PbSO4 (3). 调节溶液的pH (4). 无法除去杂质Fe2+ (5). Zn+Cd2+Zn2++Cd (6). Zn2++2e-Zn (7). 溶浸 【解析】焙烧时硫元素转化为SO2 44 ,然后用稀硫酸溶浸,生成硫酸锌、硫酸亚铁和硫酸镉,二氧化硅与稀硫酸不反应转化为滤渣,由于硫酸铅不溶于水,因此滤渣1中还含有硫酸铅。由于沉淀亚铁离子的pH较大,需要将其氧化为铁离子,通过控制pH得到氢氧化铁沉淀;滤液中加入锌粉置换出Cd,最后将滤液电解得到金属锌,据此将解答。 (1)由于闪锌矿的主要成分是ZnS,因此焙烧过程中主要反应的化学方程式为2ZnS+3O22ZnO+2SO2。 (2)由于硫酸铅不溶于水,因此滤渣1的主要成分除SiO2外还有PbSO4;要测定铁离子,需要调节溶液的pH,又因为不能引入新杂质,所以需要利用氧化锌调节pH,即氧化除杂工序中ZnO的作用是调节溶液的pH。根据表中数据可知沉淀亚铁离子的pH较大,所以若不通入氧气,其后果是无法除去杂质Fe2+。 (3)溶液中的Cd2+可用锌粉除去,反应的离子方程式为Zn+Cd2+=Zn2++Cd。 (4)电解硫酸锌溶液制备单质锌时,阴极发生得到电子的还原反应,因此阴极是锌离子放电,则阴极的电极反应式为Zn2++2e-=Zn;阳极是氢氧根放电,破坏水的电离平衡,产生氢离子,所以电解后还有硫酸产生,因此沉积锌后的电解液可返回溶浸工序继续使用。 3. (2018·全国卷Ⅲ)KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题: (1)KIO3的化学名称是_______。 (2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示: “酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是________。“滤液”中的溶质主要是_______。“调pH”中发生反应的化学方程式为__________。 (3)KIO3也可采用“电解法”制备,装置如图所示。 ①写出电解时阴极的电极反应式______。 ②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。 ③与“电解法”相比,“KClO3氧化法”的主要不足之处有______________(写出一点)。 44 【答案】(1). 碘酸钾 (2). 加热 (3). KCl (4). KH(IO3)2+KOH==2KIO3+H2O或(HIO3+KOH==KIO3+H2O) (5). 2H2O+2e-==2OH-+H2↑ (6). K+ (7). a到b (8). 产生Cl2易污染环境 【解析】 (1)根据氯酸钾(KClO3)可以推测KIO3为碘酸钾。 (2)将溶解在溶液中的气体排出的一般方法是将溶液加热,原因是气体的溶解度是随温度上升而下减小。第一步反应得到的产品中氯气在“逐Cl2”时除去,根据图示,碘酸钾在最后得到,所以过滤时KH(IO3)2应该在滤渣中,所以滤液中主要为KCl。“调pH”的主要目的是将KH(IO3)2转化为KIO3,所以方程式为:KH(IO3)2+KOH=2KIO3+H2O。 (3)①由图示,阴极为氢氧化钾溶液,所以反应为水电离的氢离子得电子,反应为2H2O + 2e- = 2OH- + H2↑。 ②电解时,溶液中的阳离子应该向阴极迁移,明显是溶液中大量存在的钾离子迁移,方向为由左向右,即由a到b。 ③KClO3氧化法的最大不足之处在于,生产中会产生污染环境的氯气。 4. (2018·江苏卷)以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下: (1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为______________________。 (2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题16图所示。 44 已知:多数金属硫酸盐的分解温度都高于600 ℃ 硫去除率=(1—)×100% ①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于__________________。 ②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是______________________________________________________。 (3)向“过滤”得到的滤液中通入过量CO2,铝元素存在的形式由_______________(填化学式)转化为_______________(填化学式)。 (4)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=__________________。 【答案】(12分) (1)SO2+OH−HSO3− (2)①FeS2 ②硫元素转化为CaSO4而留在矿粉中 (3)NaAlO2 Al(OH)3 (4)1∶16 【解析】根据流程,矿粉焙烧时FeS2与O2反应生成Fe2O3和SO2,在空气中CaO可将SO2转化为CaSO4;“碱浸”时Al2O3、SiO2转化为溶于水的NaAlO2、Na2SiO3;Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2, (1)过量SO2与NaOH反应生成NaHSO3和H2O,反应的化学方程式为SO2+NaOH=NaHSO3,离子方程式为SO2+OH-=HSO3-。 (2)①根据题给已知,多数金属硫酸盐的分解温度高于600℃,不添加CaO的矿粉低于500℃焙烧时,去除的硫元素主要来源于FeS2。 ②添加CaO,CaO起固硫作用,添加CaO发生的反应为2CaO+2SO2+O2=2CaSO4 44 ,根据硫去除率的含义,700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低的原因是:硫元素转化为CaSO4留在矿粉中。 (3)“碱浸”时Al2O3、SiO2转化为溶于水的NaAlO2、Na2SiO3,向“过滤”得到的滤液中通入过量CO2,CO2与NaAlO2反应生成NaHCO3和Al(OH)3,反应的离子方程式为CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-,即Al元素存在的形式由NaAlO2转化为Al(OH)3。 (4)Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,反应的化学方程式为FeS2+16Fe2O311Fe3O4+2SO2↑,理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16。 5. (2018·江苏卷)以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下: 已知:①Cl2+2OH−ClO−+Cl−+H2O是放热反应。 ②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。 (1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。 (2)步骤Ⅱ合成N2H4·H2O的装置如题19图−1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。 (3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、HSO3-、SO32-随pH的分布如题19图−2所示,Na2SO3的溶解度曲线如题19图−3所示)。 44 ①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。 ②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。 【答案】(15分) (1)3Cl2+6OH−5Cl−+ClO3−+3H2O 缓慢通入Cl2 (2)NaClO碱性溶液 减少水合肼的挥发 (3)①测量溶液的pH,若pH约为4,停止通SO2 ②边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,在高于34℃条件下趁热过滤 【解析】步骤I中Cl2与NaOH溶液反应制备NaClO;步骤II中的反应为NaClO碱性溶液与尿素水溶液反应制备水合肼,;步骤III分离出水合肼溶液;步骤IV由SO2与Na2CO3反应制备Na2SO3。 (1)温度超过40℃,Cl2与NaOH溶液发生歧化反应生成NaClO3、NaCl和H2O,反应的化学方程式为3Cl2+6NaOH5NaCl+NaClO3+3H2O,离子方程式为3Cl2+6OH-5Cl-+ClO3-+3H2O。由于Cl2与NaOH溶液的反应为放热反应,为了减少NaClO3的生成,应控制温度不超过40℃、减慢反应速率;实验中控制温度除用冰水浴外,还需采取的措施是:缓慢通入Cl2。 (2)步骤II中的反应为NaClO碱性溶液与尿素水溶液反应制备水合肼,由于水合肼具有强还原性、能与NaClO剧烈反应生成N2,为了防止水合肼被氧化,应逐滴滴加NaClO碱性溶液,所以通过滴液漏斗滴加的溶液是NaClO碱性溶液。NaClO碱性溶液与尿素水溶液在110℃继续反应,N2H4·H2O沸点约118 ℃,使用冷凝管的目的:减少水合肼的挥发。 (3)①向Na2CO3溶液中通入SO2制备NaHSO3溶液,根据图示溶液pH约为4时,HSO3- 44 的摩尔分数最大,则溶液的pH约为4时停止通入SO2;实验中确定何时停止通入SO2的实验操作为:测量溶液的pH,若pH约为4,停止通SO2。 ②由NaHSO3溶液制备无水Na2SO3,首先要加入NaOH将NaHSO3转化为Na2SO3,根据含硫微粒与pH的关系,加入NaOH应调节溶液的pH约为10;根据Na2SO3的溶解度曲线,温度高于34℃析出Na2SO3,低于34℃析出Na2SO3·7H2O,所以从Na2SO3溶液中获得无水Na2SO3应控制温度高于34℃。由NaHSO3溶液制备无水Na2SO3的实验方案为:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,在高于34℃条件下趁热过滤,用少量无水乙醇洗涤,干燥,密封包装。 6.(2018·北京卷)磷精矿湿法制备磷酸的一种工艺流程如下: 已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。 溶解度:Ca5(PO4)3(OH)查看更多