- 2021-07-02 发布 |
- 37.5 KB |
- 12页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020届二轮复习化学工艺流程试题的突破方略学案(全国通用)
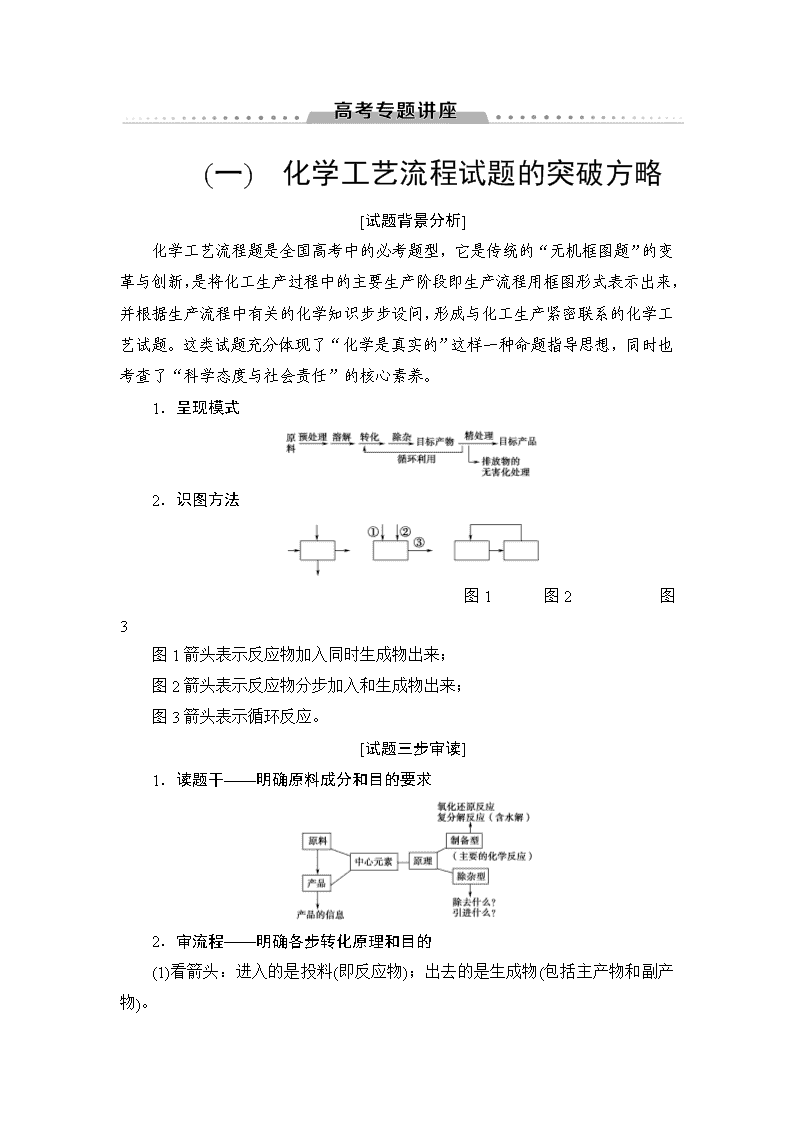
(一) 化学工艺流程试题的突破方略 [试题背景分析] 化学工艺流程题是全国高考中的必考题型,它是传统的“无机框图题”的变革与创新,是将化工生产过程中的主要生产阶段即生产流程用框图形式表示出来,并根据生产流程中有关的化学知识步步设问,形成与化工生产紧密联系的化学工艺试题。这类试题充分体现了“化学是真实的”这样一种命题指导思想,同时也考查了“科学态度与社会责任”的核心素养。 1.呈现模式 2.识图方法 图1 图2 图3 图1箭头表示反应物加入同时生成物出来; 图2箭头表示反应物分步加入和生成物出来; 图3箭头表示循环反应。 [试题三步审读] 1.读题干——明确原料成分和目的要求 2.审流程——明确各步转化原理和目的 (1)看箭头:进入的是投料(即反应物);出去的是生成物(包括主产物和副产物)。 (2)看三线:主线主产品、分支副产品、回头为循环。 (3)找信息:明确反应条件控制和分离提纯方法。 (4)关注所加物质的可能作用:参与反应、提供反应氛围、满足定量要求。 3.审问题——明确答什么 (1)答非所问:要看清题目要求,按要求答题,防止答非所问。 (2)规范答题:回答问题要准确全面,注意语言表达的规范性,特别是化学用语的书写与表示要准确、规范。 [试题分类探究] 以除杂、分离、提纯为主体的化工流程题 1.物质分离提纯的原则 (1)不增:不引入新的杂质。 (2)不减:不减少被提纯的物质。 (3)易分离:被提纯物与杂质易于分离。 (4)易复原:被提纯的物质易恢复原来的组成、状态。 2.常用的提纯方法 水溶法 除去可溶性杂质 酸溶法 除去碱性杂质 碱溶法 除去酸性杂质 氧化剂或还原剂法 除去还原性或氧化性杂质 加热灼烧法 除去受热易分解或易挥发的杂质 调节溶液的pH法 如除去酸性Cu2+溶液中的Fe3+等 3.常用的分离方法 过滤 分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法 萃取和 分液 利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用CCl4或苯萃取溴水中的溴 蒸发结晶 提取溶解度随温度变化不大的溶质,如NaCl 冷却结晶 提取溶解度随温度变化较大的溶质、易水解的溶质或结晶水合物,如KNO3、FeCl3、CuCl2、CuSO4·5H2O、FeSO4·7H2O等 蒸馏或 分馏 分离沸点不同且互溶的液体混合物,如分离乙醇和甘油 冷却法 利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中的氨气 [补短板] 1.增大原料浸出率(离子在溶液中被浸出的百分率)的措施:搅拌、升高温度、延长浸出时间、增大气体的流速(浓度、压强)、增大气液或固液接触面积。根据物质的具体性质,原料浸泡可分为水浸、酸浸、碱浸、醇浸等。 2.过滤问题 (1)3个基本操作 ①检验溶液中离子是否沉淀完全的方法:将溶液静置一段时间后,用胶头滴管取上层清液少许放入小试管中,向其中滴入沉淀剂,若无沉淀生成,则说明离子沉淀完全。 ②洗涤沉淀:沿玻璃棒往漏斗中加蒸馏水至液面浸没沉淀,待水自然流下后,重复操作2~3次。 ③检验沉淀是否洗涤干净的方法:取少量最后一次的洗涤液于试管中,向其中滴入某试剂,若没有特征现象出现,则证明沉淀已洗涤干净。 (2)特定洗涤目的 ①冰水洗涤的目的:洗去晶体表面的杂质离子并降低被洗涤物质的溶解度,减少其在洗涤过程中的溶解损耗。 ②乙醇洗涤的目的:降低被洗涤物质的溶解度,减少其在洗涤过程中的溶解损耗,得到较干燥的产物。 3.结晶方式 (1)蒸发浓缩、冷却结晶:适用于杂质的溶解度随温度变化不大的物质分离提纯,如除去KNO3中的少量NaCl或受热易分解的物质,如晶体水合物、铵盐等。 (2)蒸发结晶、趁热过滤:适用于杂质的溶解度随温度变化较大物质的分离提纯,可减少杂质晶体的析出,如除去NaCl中的少量KNO3。趁热过滤的方法:漏斗预热,用少量热蒸馏水通过过滤器,带加热装置的漏斗、抽滤。 提醒:晶体的干燥:要得到干燥的晶体,常见的干燥方法有自然晾干、滤纸吸干、在干燥器中干燥、烘干(适用于热稳定性较好的物质)。 4.调节溶液pH分离提纯 (1)控制溶液的酸碱性使其中某些金属离子形成氢氧化物沉淀。例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示: 物质 开始沉淀 沉淀完全 Fe(OH)3 1.5 3.7 Fe(OH)2 7.6 9.6 Mn(OH)2 8.3 9.8 若要除去Mn2+溶液中含有的Fe2+,可先用氧化剂把Fe2+氧化为Fe3+,再调节溶液的pH在3.7≤pH<8.3。 (2)调节pH所需的物质应满足两点:能与H+反应,使溶液pH增大;不引入新杂质。例如:要除去Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等物质来调节溶液的pH。 [典例导航] (2018·全国卷Ⅱ,T26)我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示: 相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下: 金属离子 Fe3+ Fe2+ Zn2+ Cd2+ 开始沉淀的pH 1.5 6.3 6.2 7.4 沉淀完全的pH 2.8 8.3 8.2 9.4 回答下列问题: (1)焙烧过程中主要反应的化学方程式为___________________________ _________________________________________________________________。 (2)滤渣1的主要成分除SiO2外还有________;氧化除杂工序中ZnO的作用是________,若不通入氧气,其后果是________。 (3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为___________________________________________________________________。 (4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为 __________________________________________________________________; 沉积锌后的电解液可返回________工序继续使用。 [三步审读] [解析] (1)在焙烧过程中ZnS和O2反应生成ZnO和SO2。(2)溶液中的Pb2+与SO不能共存,生成PbSO4沉淀,SiO2不溶于H2SO4,即滤渣1中含SiO2和PbSO4。氧化除杂过程中O2能将溶液中Fe2+氧化生成Fe3+,加入ZnO能调节溶液的pH,促进Fe3+完全水解。由题表知Fe2+、Zn2+开始沉淀和沉淀完全时的pH非常接近,若不通入O2使Fe2+氧化为Fe3+,加入ZnO后无法除去Fe2+,会影响Zn的纯度。(3)根据题中信息可知还原除杂工序中涉及的离子反应式为Cd2++Zn===Cd+Zn2+。(4)结合图示可知电解ZnSO4溶液时生成Zn,即电解时Zn2+在阴极被还原,电极反应式为Zn2++2e-===Zn。沉积Zn后的电解液中主要含有H2SO4,可返回溶浸工序中继续使用。 [答案] (1)2ZnS+3O22ZnO+2SO2 (2)PbSO4 调节溶液的pH 无法除去杂质Fe2+ (3)Cd2++Zn===Cd+Zn2+ (4)Zn2++2e-===Zn 溶浸 (1)“氧化除杂”过程除了加ZnO外还可以加________________________, O2的作用是__________________________________________________。 (2)滤渣洗涤的操作为_____________________________________________ _______________________________________________________________。 (3)“电解”制备Zn的阳极反应为__________________________________。 [答案] (1)Zn(OH)2或ZnCO3 把Fe2+氧化为Fe3+ (2)沿玻璃棒向漏斗中加蒸馏水至浸没沉淀,待蒸馏水自然流尽后,再重复操作2~3次 (3)4OH--4e-===2H2O+O2↑或2H2O-4e-===4H++O2↑ [对点训练] 1.(2019·全国卷Ⅲ)高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题: 相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下: 金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+ 开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9 沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9 (1)“滤渣1”含有S和______________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式___________________________________________ __________________________________________________________________。 (2)“氧化”中添加适量的MnO2的作用是___________________________。 (3)“调pH”除铁和铝,溶液的pH范围应调节为______~6之间。 (4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是________。 (5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是____________________________________________________ ___________________________________________________________________。 (6)写出“沉锰”的离子方程式______________________________________ ___________________________________________________________________。 (7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=时,z=________。 [解析] (1)硫化锰矿及二氧化锰粉末中加入硫酸后,发生氧化还原反应:MnO2+MnS+2H2SO4===2MnSO4+S+2H2O,故滤渣1的主要成分为S和SiO2(不溶性硅酸盐)。 (2)Fe2+沉淀完全时,Mn2+已经开始沉淀,故加入MnO2是为了将溶液中的Fe2+氧化为Fe3+,便于除去。 (3)除去Fe3+及Al3+,应使二者沉淀完全,故pH应大于4.7。 (4)锌和镍的硫化物都难溶于水,故“滤渣3”的主要成分为ZnS、NiS。 (5)“除杂1”步骤结束后,杂质金属阳离子只有Mg2+,加入MnF2形成MgF2沉淀而除去Mg2+,若溶液酸度过高,H+浓度偏大,则F-与H+结合形成HF,使MgF2沉淀溶解平衡正向移动而重新溶解。 (6)“沉锰”时加入NH4HCO3发生反应:Mn2++2HCO=== MnCO3↓+CO2↑+H2O。 (7)根据化合物中各元素化合价代数和为0的原则,求得z=。 [答案] (1)SiO2(不溶性硅酸盐) MnO2+MnS+2H2SO4 ===2MnSO4+S+2H2O (2)将Fe2+氧化为Fe3+ (3)4.7 (4)NiS和ZnS (5)F-与H+结合形成弱电解质HF,MgF2Mg2++2F-平衡向右移动 (6)Mn2++2HCO===MnCO3↓+CO2↑+H2O (7) 以物质制备为主体的化工流程题 1.物质制备过程的条件控制 (1)控制体系的环境氛围 ①需要在酸性气流中干燥FeCl3、AlCl3、MgCl2等含水晶体,抑制水解并带走因分解产生的水汽。 ②营造还原性氛围,防止还原性物质被氧化。如加入铁粉防止Fe2+被氧化。 ③加入氧化剂进行氧化。如加入绿色氧化剂H2O2将Fe2+氧化转化为Fe3+,绿色氧化剂H2O2的优点:不引入新杂质,对环境无污染。 (2)控制反应温度 ①加热:加速溶解、加快反应速率或促进平衡向某个方向移动(如促进水解生成沉淀)。 ②降温:防止某物质在某温度时会溶解或分解,或促进平衡向某个方向移动。 ③控制温度在一定范围内:综合多方面因素考虑。如使反应速率不至于太慢、抑制或促进平衡移动、防止反应物分解、防止副反应发生、使催化剂的催化活性最高等。 ④如题目中出现了包括产物在内的各种物质的溶解度信息,则要根据它们溶解度随温度升高而改变的情况,寻找合适的结晶分离方法。 2.在流程题中,常会看到压强、温度等外界条件的出现,不同的工艺对化学反应的温度或压强有不同的要求,其所起的作用也不一样,但都是能否达到实验目的的关键所在,也是命题专家们经常考查的地方。对外界条件的分析主要从对反应速率和平衡转化率的影响这两个方面着手。如 (1)使催化剂的活性达到最高:如工业合成氨或SO2的催化氧化反应,选择的温度是500 ℃左右,原因之一就是这样可使催化剂的活性达到最高。 (2)对于一些工艺来说,降温或减压都可以减少能源成本,降低对设备的要求,达到绿色化学的目的。 [典例导航] (2019·全国卷Ⅰ)硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工业。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下: 回答下列问题: (1)在95 ℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_____________________________________________________________。 (2)“滤渣1”的主要成分有________________。为检验“过滤1”后的滤液中是否含有Fe3+,可选用的化学试剂是________。 (3)根据H3BO3的解离反应:H3BO3+H2OH++B(OH),Ka=5.81×10-10,可判断H3BO3是________酸;在“过滤2”前,将溶液pH调节至3.5,目的是___________________________________________________________________ __________________________________________________________________。 (4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为______________ __________________________________________________________________, 母液经加热后可返回________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是____________________________________________________________。 [三步审读] [答案] (1)NH4HCO3+NH3===(NH4)2CO3 (2)SiO2、Fe2O3、Al2O3 KSCN (3)一元弱 转化为H3BO3,促进析出 (4)2Mg2++3CO+2H2O===Mg(OH)2·MgCO3↓+2HCO或2Mg2++2CO+H2O===Mg(OH)2·MgCO3↓+CO2↑ 溶浸 高温焙烧 (1)Mg(OH)2·MgCO3属于________(填“正盐”“酸式盐”或“碱式盐”)。 (2)H3BO3与足量NaOH溶液反应的离子方程式为______________________ __________________________________________________________________。 (3)常温下,B(OH)的水解常数为___________________________________ _______________________________________________________(列出计算式)。 [答案] (1)碱式盐 (2)H3BO3+OH-===B(OH) (3) [对点训练] 2.(2019·全国卷Ⅱ,T26节选)立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。以重晶石(BaSO4)为原料,可按如下工艺生产立德粉: (1)在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原料”表面生成了难溶于水的________(填化学式)。 (2)沉淀器中反应的离子方程式为___________________________________ __________________________________________________________________。 [解析] (1)潮湿空气中的CO2和水蒸气跟“还原料”中的硫化钡反应生成的臭鸡蛋气味的气体为H2S,水溶性变差是因为发生了反应BaS+CO2+H2O===H2S+BaCO3↓,由此可知难溶于水的物质为BaCO3。 (2)硫化钡溶液与硫酸锌反应生成难溶于水的立德粉(ZnS·BaSO4),因此离子反应方程式为S2-+Ba2++Zn2++SO===ZnS·BaSO4↓。 [答案] (1)BaCO3 (2)S2-+Ba2++Zn2++SO=== ZnS·BaSO4↓ 3.(2019·甘肃重点中学联考)溴酸镉[Cd(BrO3)2]常用于生产颜料和荧光粉。以镉铁矿(成分为CdO2、Fe2O3、FeO及少量的Al2O3和SiO2)为原料制备Cd(BrO3)2的流程如下: 已知:CdSO4溶于水。 (1)Cd(BrO3)2中Cd的化合价为________。 (2)酸浸时,为了提高镉的浸取率,可以采取的措施有__________________ _____________________________________________________(写出两种即可)。 (3)还原镉时,产生能使澄清石灰水变浑浊的气体,其发生反应的离子方程式为________________________________________________________________ __________________________________________________________________。 (4)用H2O2溶液氧化时,氧化剂与还原剂的物质的量之比为______________________。 (5)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,调pH时,应调整的pH范围为____________________,滤渣2的主要成分为________________(填化学式)。 金属离子 开始沉淀的pH 完全沉淀的pH Fe3+ 1.5 2.8 Al3+ 3.0 5.0 Fe2+ 6.3 8.3 Cd2+ 7.4 9.4 (6)实际工业生产中,有时还采用阳离子交换树脂法来测定Cd(OH)2悬浊液中Cd2+的含量,其原理是Cd2++2NaR===2Na++CdR2,其中NaR为阳离子交换树脂。常温下,将Cd(OH)2悬浊液(此时溶液pH=6)经过阳离子交换树脂后,测得溶液中的Na+比交换前增加了0.046 g·L-1,则该条件下Cd(OH)2的Ksp值为________。 (7)已知镉铁矿中CdO2的含量为72%,整个流程中镉元素的损耗率为8%,则2 t该镉铁矿可制得Cd(BrO3)2(相对分子质量为368)______ kg。 [解析] (4)加入H2O2溶液时Fe2+被氧化,发生的离子反应为H2O2+2Fe2++2H+===2Fe3++2H2O,则氧化剂与还原剂的物质的量之比为1∶ 2。(5)结合流程梳理和制备的目标产物知,调节pH的目的是使Fe3+和Al3+完全沉淀,而Cd2+不沉淀,由表中数据可知,pH应调节的范围为5.0≤pH<7.4,滤渣2的主要成分为Fe(OH)3、Al(OH)3。(6)根据溶液中Na+增加了0.046 g·L-1,结合反应原理知,溶液中c(Cd2+)=× mol·L-1=10-3 mol·L-1,pH=6时,c(OH-)=10-8 mol·L-1,则Ksp[Cd(OH)2]=c(Cd2+)·c2(OH-)=10-3×(10-8)2=10-19。(7)根据元素守恒知,n[Cd(BrO3)2]=92%×n(CdO2)= mol,则m[Cd(BrO3)2]=×368 g=3 385 600 g=3 385.6 kg。 [答案] (1)+2 (2)将矿石粉碎、适当升高浸取时的温度、延长浸取的时间、增大浸取液的浓度、充分搅拌等(任写两种) (3)3Cd4++CH3OH+H2O===3Cd2++CO2↑+6H+ (4)1∶2 (5)5.0≤pH<7.4或5.0~7.4 Fe(OH)3和Al(OH)3 (6)10-19 (7)3 385.6查看更多