2019届高考一轮复习鲁科版第五章物质结构 元素周期律学案
第五章 物质结构 元素周期律
第一节 原子结构
[教材基础——自热身]
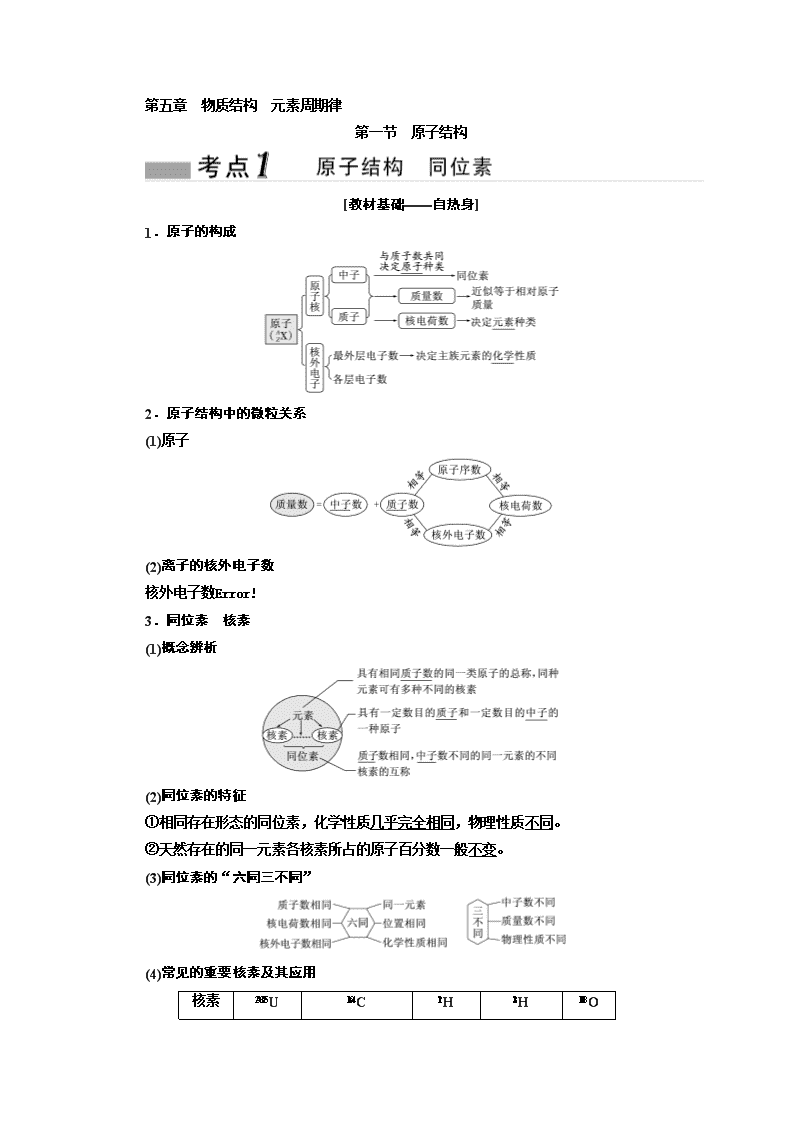
1.原子的构成
2.原子结构中的微粒关系
(1)原子
(2)离子的核外电子数
核外电子数
3.同位素 核素
(1)概念辨析
(2)同位素的特征
①相同存在形态的同位素,化学性质几乎完全相同,物理性质不同。
②天然存在的同一元素各核素所占的原子百分数一般不变。
(3)同位素的“六同三不同”
(4)常见的重要核素及其应用
核素
U
C
H
H
O
用途
核燃料
用于考古断代
制氢弹
示踪原子
4.同位素、同素异形体、同分异构体、同系物
同位素
同素异形体
同分异构体
同系物
概念
质子数相同,中子数不同的同一种元素的不同原子之间互为同位素
同种元素组成的结构不同的单质之间互为同素异形体
分子式相同,结构不同的化合物互为同分异构体
结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物
对象
原子之间
单质之间
一般为有机
化合物之间
有机化合物之间
化学
性质
几乎完全相同
相似,一定条件下可以相互转变
可能相似也可能不同
相似
实例
H、H、H
金刚石与石墨、C60;红磷与白磷
CH3COOH
与HCOOCH3
甲烷、乙烷、丙烷;乙烯、丙烯;甲酸、乙酸
[知能深化——扫盲点]
(1)任何粒子中,质量数=质子数+中子数,但质子数与电子数不一定相等,如阴、阳离子。
(2)有质子的粒子不一定有中子,如 H;有质子的粒子不一定有电子,如H+。
(3)质子数相同的粒子不一定属于同一种元素,如F-与OH-。
(4)核外电子数相同的粒子,其质子数不一定相同,如Al3+和Na+、F-等,NH与OH-等。
[对点练]
1.有以下六种原子:Li、Li、Na、Mg、6C、7N,下列相关说法不正确的是( )
A.Li和 Li在元素周期表中所处的位置相同
B.6C和 7N质量数相等,二者互为同位素
C.Na和 Mg的中子数相同但不属于同种元素
D.Li的质量数和 7N的中子数相等
解析:选B Li和 Li互为同位素,A正确;6C和 7N的质子数不相等,二者不互为同位素,B错误;Na和 Mg质子数不相同,属于不同种元素,C正确;Li的质量数为7,7N的中子数也为7,D正确。
提能点(二) 理解元素、核素、同位素、同素异形体的易错点
(1)一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子。
(2)同位素的化学性质几乎完全相同,原因是核外电子排布相同。
(3)同位素之间的转化,既不是物理变化也不是化学变化,是核反应。
(4)同位素是指同一元素的不同“原子”间的关系,同素异形体是指同一元素的不同“单质”间的关系。
(5)同位素之间可形成不同的同位素单质。如氢分子有六种:H2、D2、T2、HD、HT、DT。同位素之间可形成不同的同位素化合物。如水分子有:H2O(普通的水)、D2O(重水)、T2O(超重水)等。H、D、T与16O、17O、18O可形成3×6=18种水分子,相对分子质量不同。它们的物理性质(如密度)有所不同,但化学性质几乎完全相同。
[对点练]
2.下列说法正确的是( )
A.由H、D、T与16O、17O、18O构成的过氧化氢分子的相对分子质量有36种
B.H2、D2、T2互为同素异形体
C.H2、D2、T2在相同条件下的密度比为1∶2∶3
D.氕、氘发生核聚变生成其他元素,属于化学变化
解析:选C H、D、T组合H2、D2、T2、HD、HT、DT共6种;16O、17O、18O组合16O2、17O2、18O2、16O17O、16O18O、17O18O 共6种,所以构成的过氧化氢分子共有6×6=36种,但其中有相对分子质量相同的分子,故构成的过氧化氢分子的相对分子质量种数小于36种,故A错误;H2、D2、T2均为氢气单质,属于一种物质,故B错误;H2、D2、T2在相同条件下的密度比等于气体相对分子质量之比为2∶4∶6=1∶2∶3,故C正确;氕、氘发生核聚变生成其他元素,属于核反应,不是化学变化,故D错误。
[题点全练——过高考]
题点一 原子结构的概念辨析
1.下列说法不正确的是( )
①质子数相同的粒子一定属于同种元素
②同位素的物理性质有较大差别而化学性质几乎完全相同
③元素种类由质子数决定,原子种类由质子数和中子数共同决定,元素主要化学性质由最外层电子数决定
④电子数相同的粒子不一定是同一种元素
⑤每种元素都有两种或两种以上的核素
A.①②④⑤ B.③④⑤
C.②③⑤ D.①⑤
解析:选D 对于元素而言,大部分元素都有同位素原子,但是也有元素没有同位素,如Na和F,故⑤错误;质子数相同的粒子不一定属于同种元素,如OH-和F-的质子数都为9,但很明显不属于同种元素,故①错误。
2.中国科学技术名词审定委员会已确定第116号元素Lv的名称为。关于 Lv的叙述错误的是( )
A.原子序数116 B.中子数177
C.核外电子数116 D.相对原子质量293
解析:选D 由 Lv知,该原子的原子序数为116,核外电子数为116,中子数为293-116=177,293是其质量数,不是相对原子质量,D项错误。
题点二 各种粒子之间的相互关系
3.某元素的一种同位素X的原子质量数为A,含N个中子,它与 1H原子组成HmX分子,在a g HmX中所含质子的物质的量是( )
A.(A-N+m)mol B.(A-N)mol
C.(A-N)mol D.(A-N+m)mol
解析:选A X原子的质子数为(A-N),一个HmX分子中所含的质子数为(A-N+m),HmX的摩尔质量为(A+m)g·mol-1,所以a g HmX中所含质子的物质的量为(A-N+m)mol。
4.某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w g这种原子的原子核内中子数为( )
A. B.
C. D.
解析:选C X原子的中子数为A-(x-n),w g X的物质的量为 mol,则中子的物质的量为 mol,中子数为。
[教材基础——自热身]
1.核外电子排布规律
2.原子结构示意图
如镁离子结构示意图为,
氯离子结构示意图为。
3.常见的“10电子”“18电子”微粒
(1)常见的“10电子”微粒
(2)常见的“18电子”微粒
4.短周期常见原子的核外电子排布规律
(1)原子核中无中子的原子:H。
(2)最外层有1个电子的元素:H、Li、Na。
(3)最外层有2个电子的元素:Be、Mg、He。
(4)最外层电子数等于次外层电子数的元素:Be、Ar。
(5)最外层电子数是次外层电子数2倍的元素:;是次外层电子数3倍的元素:;是次外层电子数4倍的元素:。
(6)电子层数与最外层电子数相等的元素:H、Be、Al。
(7)电子总数为最外层电子数2倍的元素:。
(8)次外层电子数是最外层电子数2倍的元素:Li、Si。
(9)内层电子总数是最外层电子数2倍的元素:Li、P。
[题点全练——过高考]
题点一 核外电子排布规律
1.在元素周期表的前18号元素中,最外层电子数是其电子层数的2倍的元素共有( )
A.1种 B.2种
C.3种 D.4种
解析:选C He、C、S符合题意。
2.两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有( )
A.1对 B.2对
C.3对 D.4对
解析:选B 前10号元素的核外电子层数与最外层电子数分别为:1H:1,1;2He:1,2;3Li:2,1;4Be:2,2;5B:2,3;6C:2,4;7N:2,5;8O:2,6;9F:2,7;10Ne:2,8。核外电子层数之比与最外层电子数之比相同的为H和Be与He和C,共2对,B项符合题意。
题点二 依据核外电子排布特点推断元素
3.某元素X,其原子的电子层数为(n-1),最外层电子数为(2n-1)。下列有关元素X的说法中正确的是( )
A.X可能是金属元素
B.由X形成的含氧酸均为强酸
C.X不能形成化学式为KXO4的含氧酸盐
D.元素X的气态氢化物一定极易溶于水
解析:选D 由X原子的最外层电子数为(2n-1)可以推知n≤4,则X的电子层数≤3,X为短周期元素。当n=4时,X为Cl元素;当n=3时,X为N元素;当n=2时,不符合题意。HNO2和HClO均为弱酸,B项错误;Cl元素能形成KClO4,C错误;NH3和HCl均极易溶于水,D正确。
4.X和Y均为短周期元素,X原子的最外层电子数是次外层电子数的2.5倍,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的分子式可表示为 ( )
A.XY B.XY2
C.XY3 D.XY4
解析:选C 由题意知X是N,Y是H,C正确。
5.A、B、C、D 4种元素的核电荷数依次增大,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。则4种元素的元素符号依次是
A__________,B__________,C_________,D________。
解析:A原子的L层电子数与K、M层电子数之和相等,所以A的核电荷数为2×8=16,A为S元素;D原子的K、L层电子数之和等于电子总数的一半,所以D的核电荷数是(2+8)×2=20,D为Ca元素。根据核电荷数依次增大,它们的离子的电子层数相同且最外层电子数均为8,可以判断出B为Cl元素,C为K元素。
答案:S Cl K Ca
题点三 “10电子”、“18电子”微粒的应用
6.A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C-===D+E↑;②B++C-===2D。
请回答:
(1)C-的电子式是______________。
(2)分别写出A+和D反应、B+和E反应的离子方程式:________________________、________________________________________________________________________。
(3)除D、E外,请再写出两种含10个电子的分子的分子式__________________。
解析:因A+、C-、D、E均为10电子微粒,且A++C-===D+E↑,则A+为NH,C-为OH-,E为NH3,D为H2O,进而推知B+为H3O+。
答案:(1)[H]-
(2)NH+H2ONH3·H2O+H+
H3O++NH3===NH+H2O
(3)CH4、Ne(其他合理答案也可)
7.用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答下列问题:
(1)A元素是________、B元素是________、C元素是________(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是________,含有的化学键是________。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是________,其与水反应的化学方程式为_________________________________________________________
________________________________________________________________________。
(4)F是由两种元素组成的三原子分子,其分子式是________,其电子式和电离方程式为______________、_____________________________________________________
________________________________________________________________________。
(5)G分子中含有4个原子,其分子式是______________________________________。
(6)H分子中含有8个原子,其分子式是________________________________________。
答案:(1)K Cl S
(2)HCl 共价键
(3)F2 2F2+2H2O===4HF+O2
(4)H2S HH
H2SH++HS-,HS-H++S2-
(5)H2O2(或PH3) (6)C2H6
[课堂真题集训——明考向]
1.(2017·全国卷Ⅱ)a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同;c所在周期数与族数相同;d与a同族。下列叙述正确的是( )
A.原子半径:d>c>b>a
B.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱
D.d单质的氧化性比a单质的氧化性强
解析:选B 由题意可推出a为O,b为Na或Mg,c为Al,d为S。原子半径:Na(或Mg)>Al>S>O,A项错误;同周期主族元素从左到右,金属性逐渐减弱,即金属性:Na(或Mg)>Al,B项正确;Al2O3对应的水化物为Al(OH)3,Al(OH)3是两性氢氧化物,C项错误;同主族元素自上而下,非金属性逐渐减弱,则对应单质的氧化性逐渐减弱,即氧化性:O2>S,D项错误。
2.(2017·北京高考)2016年IUPAC命名117号元素为Ts(中文名“石田”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是( )
A.Ts是第七周期ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是 Ts
解析:选D 0族元素从上往下,原子序数依次为2、10、18、36、54、86、118,则可推断117号元素位于第七周期第ⅦA族,A项正确;互为同位素的不同原子具有相同的质子数,质子数等于核外电子数,B项正确;同主族元素从上往下,非金属性逐渐减弱,C项正确;中子数为176的Ts核素符号是 Ts,D项错误。
3.(2017·江苏高考)下列有关化学用语表示正确的是( )
A.质量数为31的磷原子:P
B.氟原子的结构示意图:
C.CaCl2的电子式:
D.明矾的化学式:Al2(SO4)3
解析:选A P的左上角标质量数,左下角标质子数,A项正确;F原子的最外层有7个电子,B项错误;两个Cl-应放在Ca2+的两侧,其电子式为,C项错误;明矾的化学式为KAl(SO4)2·12H2O,D项错误。
4.(2013·海南高考)重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1HO与DO的相对分子质量相同
解析:选C 同种元素形成的不同单质称为同素异形体。
[课下能力测评——查缺漏]
1.具有广泛用途的 Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如 Co、Co、Co和 Co。下列关于钴原子的说法正确的是( )
A.Co、Co、Co、Co和 Co是摩尔质量不同的五种同素异形体
B.Co放射源可以用来治疗癌症,其中子数与电子数之差等于6
C.Co、Co、Co、Co和 Co互为同位素,物理性质几乎相同,化学性质不同
D.Co、Co、Co、Co和 Co互为同分异构体
解析:选B Co、Co、Co、Co和 Co互为同位素,物理性质不同,化学性质几乎完全相同,A、C、D错误;Co 的中子数为60-27=33,与电子数之差为33-27=6,B正确。
2.据报道,俄罗斯科学家再次合成117号元素,其中有5个 X,1个 X。下列关于 X和 X的说法,不正确的是( )
A.是两种核素 B.互为同位素
C.中子数分别为176和177 D.电子数相差1
解析:选D X和 X的质子数都是117,中子数分别是176、177,是两种核素,A项、C项叙述正确;X和 X具有相同的质子数,不同的中子数,二者互为同位素,B项叙述正确;原子核外电子数等于质子数等于117,故两种核素的电子数相等,D项叙述错误。
3.由德国重离子研究中心人工合成的第112号元素的正式名称为“Copemicium”,相应的元素符号为“Cn”,该元素的名称是为了纪念天文学家哥白尼而得名。该中心人工合成Cn的过程可表示为 Zn+Pb===Cn+n。下列叙述中正确的是( )
A.上述合成过程属于化学变化
B.Cn元素的相对原子质量为277
C.Cn 的原子核内中子数比质子数多53
D.Cn元素位于元素周期表的第六周期,是副族元素
解析:选C A项,化学变化的最小粒子为原子,该反应中原子类型发生了变化,不属于化学变化,错误;B项,该Cn原子的相对原子质量为277,元素的相对原子量与该元素不同核素的相对原子量和在自然界中的含量有关,错误;C项,该原子的中子数=277-112,中子数比质子数多的数目为277-112-112=53,正确;D项,第118号元素位于周期表中第七周期0族,则112号元素位于第七周期ⅡB族,错误。
4.现有下列几组粒子:①N2、CO、C2H2;②NH、H3O+、OH-;③C、O、CN-;④PO、SO、ClO。对上述四组粒子归类正确的是( )
A.质子数相等,电子数和原子数不相等:①
B.质子数和电子数相等,原子数不相等:②
C.电子数相等,质子数和原子数不相等:③
D.原子数和电子数相等,质子数不相等:④
解析:选D ①中质子数和电子数均相等,A错误;②中质子数不相等,B错误;③中原子数相等,C错误。
5.某元素的一个原子形成的离子可表示为 Xn-,下列说法正确的是( )
A.Xn-含有的中子数为a+b
B.Xn-含有的电子数为a-n
C.X原子的质量数为a+b+n
D.1个X原子的质量约为 g
解析:选D Xn-中a表示质子数,b表示质量数,“n-”表示X得到n个电子,则其含有的中子数为b-a,电子数为a+n。1 mol Xn-的质量约为b g,则1个X原子的质量约为 g。
6.短周期元素X和元素Y,元素X原子的最外层电子数为a,次外层电子数为b;元素Y原子的M层电子数为(a-b),L层电子数为(a+b),则X、Y两元素形成的化合物可能具有的性质是( )
A.和水反应 B.和硫酸反应
C.和氢氧化钠反应 D.和氯气反应
解析:选C 根据Y原子的L层电子数为(a+b),M层电子数为(a-b)知a+b=8,再根据X原子次外层电子数为b,可知b=2,则a=6,进而确定X为氧(O),Y为硅(Si)。两元素形成SiO2,SiO2为酸性氧化物,可与NaOH反应。
7.X是第三周期非金属元素,该原子如果要达到8电子稳定结构,需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是( )
A.X最高价氧化物对应的水化物一定是强酸
B.X元素的氢化物化学式一定为H2X
C.X的单质一定是良好的半导体材料
D.X元素的氧化物一定能与烧碱反应
解析:选D A项,根据已知位、构、性方面的信息推断,X为Si或S,最高价氧化物对应的水化物为H2SiO3或H2SO4,前者是弱酸,后者是强酸,错误;B项,气态氢化物为SiH4或H2
S,错误;C项,单质为Si或S,前者是半导体材料,后者是绝缘体材料,错误;D项,氧化物为SiO2或SO2、SO3,都是酸性氧化物,正确。
8.X、Y、Z均为短周期主族元素,其核电荷数依次增大,且它们的原子最外层电子数之比为1∶4∶2。下列叙述中正确的是( )
A.X一定是碱金属元素
B.Y元素能形成化合物NaHYO3,且其水溶液呈碱性
C.Z元素形成的最高价氧化物熔点较低
D.X的单质一定能通过电解Z的盐酸盐溶液制备
解析:选B X、Y、Z均为短周期主族元素,其核电荷数依次增大,且它们的原子最外层电子数之比为1∶4∶2,应分别是ⅠA族、ⅣA族、ⅡA族,其可能是H或Li、C和Mg元素。A项,X不一定是碱金属元素,错误;C项,氧化镁的熔点较高,错误;D项,H2可以通过电解MgCl2溶液制取,但Li不可以,错误。
9.设X、Y、Z代表元素周期表中前四周期的三种元素,已知X+和Y-具有相同的电子层结构;Z元素的原子核内质子数比Y元素的原子核内质子数少9;Y和Z两种元素可形成含4个原子核、42个电子的负一价阴离子。下列说法不正确的是( )
A.元素Z的气态氢化物分子中含有10个电子
B.元素Y的气态氢化物分子中含有18个电子
C.元素Z与元素X形成的化合物X2Z中离子都达到稳定结构
D.元素Y、Z组成的化合物属于离子化合物
解析:选D 由“X+和Y-具有相同的电子层结构”知X+和Y-的最外层都是8电子,推知X为ⅠA族元素、Y为ⅦA族元素;又因“Z元素的原子核内质子数比Y元素的原子核内质子数少9”,故Y为Cl、Z为O、X为K。水分子中含有10个电子,氯化氢分子中含有18个电子,K2O中的K+、O2-均达到最外层8电子稳定结构。氯、氧组成的化合物为共价化合物。
10.A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子化合物。D元素的最外层电子数与核外电子层数相等。已知:甲+E2===丙+B2,甲+丙===丁,下列说法正确的是( )
A.离子半径:D>C>B
B.A与C两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置可以是第二周期ⅡA族
D.丁物质均由非金属元素构成,只含共价键
解析:选B 由题目信息可判断出A为氢元素;10电子化合物可能为甲烷、氨气、水、HF,已知甲+E2===丙+B2,甲+丙===丁,则E为氯元素,B为氮元素;由B、C相邻知C为氧元素,故甲为NH3、乙为H2O、丙为HCl、丁为NH4
Cl;D元素的最外层电子数与核外电子层数相等,原子序数大于氧元素,处于第三周期,最外层电子数为3,故D为铝元素。A项,N3-、O2-、Al3+电子层结构相同,核电荷数越大离子半径越小,故离子半径:N3->O2->Al3+,错误;B项,H与O两种元素可形成的10电子粒子有H2O、H3O+、OH-三种,正确;C项,Al元素位于第三周期ⅢA 族,错误;D项,NH4Cl含有离子键、共价键,错误。
11.现有部分短周期主族元素的性质或原子结构如下表所示:
元素编号
元素性质或原子结构
X
周期序数=主族序数=原子序数
Y
原子最外层电子数为a,次外层电子数为b
Z
原子L层电子数为a+b,M层电子数为a-b
M
单质在自然界中的硬度最大
N
位于第三周期,最外层电子数是电子层数的2倍
(1)写出X、Y、Z、N四种元素的名称:
X________,Y________,Z________,N________。
(2)由X、Y、Z、M、N五种元素两两组成的分子中,许多分子含有的电子数相等,写出符合下列要求的分子式:
①含10e-且呈正四面体结构的分子________;
②含14e-的双原子分子________;
③含16e-且能使溴水退色的分子________;
④含18e-且常温下呈液态的分子________。
解析:(1)根据周期序数=主族序数=原子序数,推知X为氢元素;根据电子数L层=a+b,M层=a-b,最外层为a,次外层为b,得出b=2,a=6,从而推得Y、Z分别为氧元素、硅元素;金刚石在自然界中的硬度最大,故M为碳元素,N的最外层电子数是电子层数的2倍,则推得N为硫元素。(2)①CH4为正四面体分子,②CO为双原子14e-分子,③乙烯能和溴水发生加成反应,使溴水退色,④H2O2 在常温下为18e-的液态分子。
答案:(1)氢 氧 硅 硫
(2)①CH4 ②CO ③C2H4 ④H2O2
12.现有部分元素的原子结构特点如表:
X
L层电子数是K层电子数的3倍
Y
核外电子层数等于原子序数
Z
L层电子数是K层和M层电子数之和
W
最外层电子数是次外层电子数的2.5倍
(1)画出W原子结构示意图________________________。
(2)元素X与元素Z相比,非金属性较强的是________(填元素名称),写出一个能表示X、Z非金属性强弱关系的化学反应方程式:___________________________________。
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为____________________。
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的、且在自然界中稳定存在的物质,写出该反应的化学方程式:________________________________________________________________________。
解析:X元素原子的L层电子数是K层电子数的3倍可知,L层为6个电子,X为氧元素;Y元素原子的核外电子层数等于原子序数,Y只能是氢元素;Z元素原子的L层电子数是K层和M层电子数之和,L层有8个电子,则其M层电子数为6,Z是硫元素;W元素原子的最外层电子数是次外层电子数的2.5倍,其次外层只能是K层,有2个电子,W为氮元素。(1)W(N)原子结构示意图为。(2)O2可置换H2S中的S,能说明氧元素比硫元素非金属性强。(3)H、N、O、S四种非金属元素形成离子化合物只能是铵盐,其水溶液显强酸性应是强酸的酸式盐,因为铵盐水解酸性不如其酸式盐溶液酸性强,故应为NH4HSO4。(4)H和O按原子个数比1∶1化合形成的化合物为H2O2,共有18个电子,则H和N形成的18电子微粒只能是N2H4,H2O2与N2H4反应生成无毒且在自然界中稳定存在的物质为N2和H2O,反应的化学方程式为N2H4+2H2O2N2+4H2O。
答案:(1)
(2)氧 2H2S+O2===2H2O+2S↓(其他合理答案亦可)
(3)NH4HSO4 (4)N2H4+2H2O2N2+4H2O
13.A、B、C、D、E、F、G、L、I九种主族元素分别位于三个不同的短周期,它们的原子序数依次增大,其中B、C、D位于同一周期,A与E、B与G、D与L分别位于同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)________________,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)____________________。
(2)L、I两元素可按原子个数比1∶1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为________________________。
(3)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的离子方程式:___________________________________________
________________________________________________________________________。
(4)由A、B、C、D按原子个数比4∶1∶1∶
2形成一种化合物Y,则Y的化学式为________________,向Y中加足量稀硫酸后,再加高锰酸钾溶液,高锰酸钾溶液退色。写出使高锰酸钾溶液退色的反应的离子方程式:_______________________________________
________________________________________________________________________。
解析:由于九种主族元素位于三个不同的周期,而B、C、D位于同一周期,可以知道A为氢元素,B、C、D位于第二周期,E、F、G、L、I则位于第三周期;由A与E为同一主族元素,可确定E为钠元素;由F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,可推知D、F为氧元素和铝元素;由C、D、F三种元素的原子序数之和为28,可推知C元素为氮元素;由D与L位于同一主族,可推知L为硫元素;由其原子序数关系和B与G位于同一主族可知,I只能是氯元素,B、G分别为碳元素和硅元素。即A、B、C、D、E、F、G、L、I分别对应H、C(碳)、N、O、Na、Al、Si、S、Cl。(1)题述非金属元素除H外,C(碳)、N、O、Si、S、Cl中硅元素的非金属性最弱,故形成的最简单的气态氢化物中SiH4的稳定性最弱。E、F、L所形成的简单离子中S2-与氩原子的核外电子排布相同,而Na+和Al3+则与氖原子核外电子排布相同,故离子半径大小顺序为S2->Na+>Al3+。(2)L、I 两元素按原子个数比1∶1组成的化合物应该是S2Cl2,其中硫原子和硫原子之间、硫原子和氯原子之间均以共价单键的形式结合。(3)Na2O2和Na2S的水溶液发生氧化还原反应,生成NaOH,同时有S沉淀析出。(4)由A、B、C、D按原子个数比4∶1∶1∶2形成的化合物为(NH4)2C2O4。C2O具有还原性,能够被酸性KMnO4溶液氧化,反应的离子方程式为2MnO+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O。
答案:(1)SiH4 S2->Na+>Al3+
(2)
(3)Na2O2+S2-+2H2O===S↓+2Na++4OH-
(4)(NH4)2C2O4
2MnO+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
第二节 元素周期表和元素周期律
[教材基础——自热身]
1.编排原则
2.元素周期表的结构
(1)周期(7个横行,7个周期)
短周期
长周期
序号
1
2
3
4
5
6
7
元素种数
18
32
32
0族元素原子序数
36
54
86
118
(2)族(18个纵行,16个族)
主族
列
1
2
13
14
15
16
17
族
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
副族
列
3
4
5
6
7
11
12
族
ⅢB
ⅣB
ⅤB
ⅥB
ⅦB
ⅠB
ⅡB
Ⅷ族
第8、9、10,共3个纵行
0族
第18纵行
(3)元素周期表中元素的分区
①分界线:如图所示,沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,即为金属元素区和非金属元素区分界线(氢元素除外)。
②各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
[注意] (1)从元素周期表的分区中可以看出,非金属性最强的是F,金属性最强的是Cs(放射性元素除外)。
(2)金属元素和非金属元素分界线右侧都是非金属,但左侧的并不都是金属元素,如氢元素。
(3)过渡元素都是金属元素,金属元素只有正价,没有负价。
(4)处在金属元素和非金属元素分界线上下的元素单质并不一定是半导体,如Al是导体,B(硼)不导电。
(4)元素周期表中的特殊位置
①过渡元素:元素周期表中从ⅢB族到ⅡB族10个纵列共60多种元素,这些元素都是金属元素。
②镧系:元素周期表第周期中,57号元素镧到71号元素镥共15种元素。
③锕系:元素周期表第周期中,89号元素锕到103号元素铹共15种元素。
④超铀元素:在锕系元素中,92号元素铀(U)以后的各种元素。
[注意] (1)第一张元素周期表是由俄国化学家门捷列夫绘制完成的。
(2)含元素种类最多的族是ⅢB族,共有32种元素。
(3)过渡元素包括7个副族和Ⅷ族,全部是金属元素,原子最外层电子数不超过2个(1~2个)。
(4)最外层电子数为3~7个的原子一定属于主族元素,且最外层电子数即为主族的族序数。
3.元素周期表的三大应用
(1)科学预测
为新元素的发现及预测他们的原子结构和性质提供了线索。
(2)寻找新材料
(3)用于工农业生产
对探矿有指导意义的是地球化学元素的分布与它们在元素周期表中的位置关系,研制农药材料等。
[知能深化——扫盲点]
1.常见的四组等量关系
(1)核电荷数=质子数=原子序数。
(2)核外电子层数=周期序数。
(3)主族序数=最外层电子数=最高正价。
(4)非金属元素:最低负价=最高正价-。
2.同主族元素的原子序数差的关系
(1)位于过渡元素左侧的主族元素,即ⅠA、ⅡA族,同主族、邻周期元素原子序数之差为上一周期元素所在周期所含元素种数。如钠、钾的原子序数之差为19-11=8。
(2)位于过渡元素右侧的主族元素,即ⅢA~ⅦA族,同主族、邻周期元素原子序数之差为下一周期元素所在周期所含元素种数。如氯和溴的原子序数之差为35-17=18(溴所在第四周期所含元素的种数)。
3.同周期ⅡA族和ⅢA族元素原子序数差的关系
周期序数
1
2
3
4
5
6
7
原子序数差
无
1
1
11
11
25
25
原因
—
增加了
过渡元素
增加了过渡元素和镧系或锕系元素
4.奇偶关系
(1)原子序数是奇数的主族元素,其所在主族序数必为奇数。
(2)原子序数是偶数的主族元素,其所在主族序数必为偶数。
[对点练]
1.(1)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是______________________。
(2)若甲、乙分别是同一周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为________________________。
解析:(1)因前六周期中元素的数目分别为2、8、8、18、18、32;同一主族中乙的原子序数可以是x+2、x+8、x+18、x+32。(2)对于第一、二、三周期,同一周期的ⅡA族和ⅦA族元素的原子序数只相差5,而对于第四、五周期来说,由于存在过渡元素,同一周期的ⅡA族和ⅢA族元素的原子序数则相差15;而对于第六、七周期来说,由于存在镧系和锕系元素,同一周期的ⅡA族和ⅦA族元素的原子序数则相差29。
答案:(1)x+2、x+8、x+18、x+32 (2)n=m+5、n=m+15、n=m+29
第一~第七周期稀有气体元素的原子序数依次为2、10、18、36、54、86、118。
确定主族元素在周期表中位置的方法:原子序数-最邻近的稀有气体元素的原子序数=x。
例如:①35号元素(相邻近的是 36Kr),则35-36=-1,故周期数为四,族序数为8-|-1|=7,即第四周期ⅦA族,即溴元素;②87号元素(相邻近的是 86Rn),则87-86=1,故周期数为七,族序数为1,即第七周期ⅠA族,即钫元素。
[对点练]
2.试推算原子序数为6、13、34、53、88、115的元素在周期表中的位置:
原子序数
6
13
34
53
88
115
周期
族
解析
:6号元素比Ne(10)少4个电子,有2个电子层,最外层电子数为4,位于第二周期ⅣA族,13号元素比Ne(10)多3个电子,有3个电子层,最外层电子数为3,位于第三周期ⅢA族;34号元素比Kr(36)少2个电子,共有4个电子层,最外层电子数为6,位于第四周期ⅥA族;53号元素比Xe(54)少1个电子,共有5个电子层,最外层电子数为7,位于第五周期ⅦA族;88号元素比Rn(86)多2个电子,共有7个电子层,最外层电子数为2,位于第七周期ⅡA 族;115号元素比118号元素少3个电子,共有7个电子层,最外层电子数为5,位于第七周期ⅤA族。
答案:
原子序数
6
13
34
53
88
115
周期
二
三
四
五
七
七
族
ⅣA
ⅢA
ⅥA
ⅦA
ⅡA
ⅤA
[题点全练——过高考]
1.下列说法正确的是( )
A.原子序数为7的元素的最高化合价为+4价
B.114号元素位于第七周期ⅣA族
C.位于同一主族的甲、乙两种元素,甲的原子序数为m,则乙的原子序数可能为m+4
D.位于同一周期的甲乙两种元素,甲位于ⅠA族,原子序数为m,乙位于ⅢA族,则乙原子序数可能为m+19
解析:选B 原子序数为7的元素为氮元素,其最高化合价为+5价,A错误;118号元素位于第七周期0族,114号元素位于第七周期ⅣA族,B正确;同一主族的元素相差2、8、18、32或上述数字间的和,C错误;同一周期ⅠA族与ⅢA族之间的差可能为2、12、26,D错误。
2.已知X、Y、Z三种主族元素在元素周期表中的位置如图所示,设X的原子序数为a。则下列说法不正确的是( )
A.Y与Z的原子序数之和可能为2a
B.Y的原子序数可能为a-17
C.Z的原子序数可能为a+31
D.X、Y、Z一定为短周期元素
解析:选D 由题给信息可知,X、Y、Z只能位于元素周期表中过渡元素区域的右边,则:若X、Y、Z同为短周期元素,由X的原子序数为a可知,Y的原子序数为a-8+1=a-7,Z的原子序数为a+8-1=a+7,A正确;若X为长周期非金属元素,Y为短周期非金属元素,则Y的原子序数可能为a-18+1=a-17,B正确;若Z为第六或第七周期元素,因存在镧系和锕系元素,则Z的原子序数可能为a+32-1=a+31,C正确。
[教材基础——自热身]
1.元素周期律
2.主族元素的周期性变化规律
项目
同周期(左→右)
同主族(上→下)
原子结构
电子层数
相同
逐渐增多
原子半径
逐渐减小
逐渐增大
离子半径
阳离子逐渐减小
阴离子逐渐减小
r(阴离子)>r(阳离子)
逐渐增大
性质
化合价
最高正化合价由+1→+7(O、F除外),负化合价=主族序数-8
相同,最高正化合价=主族序数(O、F除外)
元素的金属性和非金属性
金属性逐渐减弱
非金属性逐渐增强
金属性逐渐增强
非金属性逐渐减弱
离子的氧化性、还原性
阳离子氧化性逐渐增强
阴离子还原性逐渐减弱
阳离子氧化性逐渐减弱
阴离子还原性逐渐增强
气态氢化物稳定性
逐渐增强
逐渐减弱
最高价氧化物对应水化物的酸碱性
碱性逐渐减弱
酸性逐渐增强
碱性逐渐增强
酸性逐渐减弱
3.元素周期表、元素周期律的应用
(1)为新元素的发现及预测它们的原子结构和性质提供线索。
(2)预测元素的性质(由递变规律推测)
①比较不同周期、不同主族元素的性质
如金属性Mg>Al,Ca>Mg,则碱性Mg(OH)2Al(OH)3,Ca(OH)2Mg(OH)2(填“>”“<”或“=”)。
②推测未知元素的某些性质
如,已知Ca(OH)2微溶,Mg(OH)2难溶,可推知Be(OH)2溶。
又如,已知卤族元素的性质递变规律,可推知元素砹(At)应为色固体,与氢气化合,HAt稳定,水溶液呈酸性,AgAt溶于水等。
(3)启发人们在一定区域内寻找新物质
①制作半导体材料的元素在金属与非金属分界线附近,如Si、Ge、Ga等。
②农药中常用元素在周期表右上方,如F、Cl、S、P、As等。
③催化剂和耐高温、耐腐蚀合金材料主要在过渡元素中找,如Fe、Ni、Rh、Pt、Pd等。
[知能深化——扫盲点]
1.结构比较法
最外层电子数越少,电子层数越多,元素金属性越强;最外层电子数越多,电子层数越少,元素非金属性越强。
2.位置比较法
元素周期表
金属性从左向右,由强变弱,从上到下,由弱变强
非金属性从左向右,由弱变强,从上到下,由强变弱
金属活动性顺序
按 K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、Cu、Hg、Ag、Pt、Au的顺序,金属性减弱
非金属活动性顺序
按 F、O、Cl、Br、I、S 的顺序,非金属性减弱
3.实验比较法
[对点练]
1.将甲、乙两种金属的性质相比较,已知:①甲与H2O反应比乙与H2O反应剧烈;②甲单质能从乙的盐溶液中置换出乙单质;③甲的最高价氧化物对应的水化物碱性比乙的最高价氧化物对应的水化物碱性强;④与某非金属反应时甲原子得电子数目比乙原子得电子数目多;⑤甲单质的熔、沸点比乙的低。能说明甲的金属性比乙强的是( )
A.①④ B.①②③
C.③⑤ D.①②③④⑤
解析:选B 比较金属性强弱的一般方法是看与酸(或水)反应的剧烈程度、最高价氧化物对应的水化物碱性强弱、置换反应,而不能根据其与非金属反应时失电子数目的多少、熔沸点的高低进行比较。
2.(2018·辽宁沈阳二中期末)根据元素周期律,由下列事实进行推测,不合理的是( )
选项
事实
推测
A
12Mg与水反应缓慢,20Ca与水反应较快
56Ba(ⅡA族)与水反应会更快
B
Si是半导体材料,同族的Ge也是半导体材料
ⅣA族的元素的单质都可作半导体材料
C
HCl在1 500 ℃时分解,HI在230 ℃时分解
HBr的分解温度介于二者之间
D
Si与H2高温时反应,S与H2加热能反应
P与H2在高温时能反应
解析:选B 同主族元素由上至下金属性逐渐增强,与水反应的剧烈程度也逐渐增强,金属性:Ba>Ca>Mg,故Ba与水反应更快,A项正确;Pb不能作半导体材料,所以ⅣA族的元素的单质并不都是半导体材料,B项错误;同主族元素由上至下非金属性逐渐减弱,气态氢化物的热稳定性也逐渐减弱,非金属性:Cl>Br>I,所以HBr的分解温度介于HCl和HI之间,C项正确;同周期主族元素从左到右非金属性逐渐增强,与氢气化合的难度逐渐减小,非金属性:S>P>Si,所以P与H2在高温时能反应,D项正确。
[对点练]
3.已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙述中正确的是( )
A.原子序数:D>C>B>A
B.原子半径:B>A>C>D
C.离子半径:C3->D->A2+>B+
D.氧化性:A2+>B+,还原性:C3-<D-
解析:选B 由于四种离子具有相同的电子层结构,离子所对应的元素应位于相邻两个周期,根据阴阳离子所带的电荷数,得出元素在周期表中的位置关系:。原子序数大小应为A>B>D>C,A项错误;根据原子半径的递变规律,可以判断B正确;C项应为C3->D->B+>A2+;还原性:C3->D-,D错误。
[题点全练——过高考]
题点一 元素金属性、非金属性强弱的比较
1.下列实验不能达到实验目的的是( )
选项
实验操作
实验目的
A
Cl2、Br2分别与H2反应
比较氯、溴的非金属性强弱
B
向MgCl2、AlCl3溶液中分别通入氨
比较镁、铝的金属性强弱
C
测定相同物质的量浓度的Na2CO3、Na2SO4溶液的pH
比较碳、硫的非金属性强弱
D
Fe、Cu分别与稀盐酸反应
比较铁、铜的金属性强弱
解析:选B A项,Cl2、Br2分别与H2反应,根据反应条件的难易和反应剧烈程度可判断出氯、溴的非金属性强弱;B项,向MgCl2、AlCl3溶液中分别通入氨,MgCl2与AlCl3均生成相应的沉淀,不能比较二者的金属性强弱;C项,测定相同物质的量浓度的Na2CO3、Na2SO4溶液的pH,根据pH可判断出Na2CO3与Na2SO4水解程度的大小,即判断出酸性:H2CO3
X
B.离子半径:W3+>Y2-
C.非金属性:X>Y
D.最高价氧化物对应水化物的碱性:ZC,A正确;根据核外电子排布相同的离子,核电荷数小的半径大,离子半径:O2->Al3+,B错误;非金属性:O>C,C错误;根据元素的金属性越强最高价氧化物对应水化物的碱性越强,碱性:NaOH>Al(OH)3,D错误。
题点三 元素周期律的应用
5.(2018·四川德阳模拟)以下事实不能用元素周期律解释的是( )
A.F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应
B.“NO2球”在冷水中颜色变浅,在热水中颜色加深
C.氯原子与钠原子形成离子键,与硅原子形成共价键
D.H2O在4 000 ℃以上开始明显分解,H2S用酒精灯加热即可完全分解
解析:选B A项,非金属性:F>I,故F2与H2化合较容易,可以利用元素周期律解释; B项,NO2转化为N2O4是放热反应,升高温度,平衡左移,即NO2浓度增大,与元素周期律无关;C项,Cl最外层7个电子,容易得到,Na最外层1个电子,容易失去,Si最外层4个电子,不易失去也不易得到,所以钠、硅与氯气形成的化合物不同,可以利用元素周期律解释;D项,非金属性:O>S,故氢化物稳定性:H2O>H2S,能用元素周期律解释。
6.(2018·黑龙江五常模拟)元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y
B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
C.硅、锗都位于金属与非金属的交界处,都可以作半导体材料
D.Cs和Ba分别位于第六周期ⅠA和ⅡA族,碱性:CsOH>Ba(OH)2
解析:选B A项,X+和Y2-的核外电子层结构相同,则核外电子数相同,原子失去电子形成阳离子,原子获得电子形成阴离子,故原子序数:X>Y,正确;
B项,气态氢化物水溶液的酸性强弱,不能比较元素非金属性强弱,应利用最高价氧化物对应水化物的酸性比较,错误;C项,硅、锗处于金属与非金属的交界处,元素既表现一定的金属性又表现一定的非金属性,都可以作半导体材料,正确;D项,Cs、Ba同周期,自左而右金属性减弱,最高价氧化物对应水化物的碱性减弱,故碱性:CsOH>Ba(OH)2,正确。
[知能深化——扫盲点]
元素推断题是高考的热点题型,命题落脚点是借助元素周期表的片段、短周期元素的结构特点及这些元素形成重要化合物的特性推断元素。利用“位—构—性”关系综合考查元素及其化合物的性质和化学反应原理的相关内容。
(一)此类试题的基本特点
(二)“两步”快速突破元素推断题
(三)元素推断题的3类题型
(1)最外层电子规律
最外层电子数(N)
3≤N<8
N=1或2
N>次外层电子数
元素在周期表中的位置
主族
ⅠA族、ⅡA族、Ⅷ族、副族、0族元素氦
第二周期
(2)“阴三、阳四”规律
某元素阴离子最外层电子数与次外层相同,该元素位于第三周期;若为阳离子,则位于第四周期。
(3)“阴上、阳下”规律
电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期。
[对点练]
1.a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。下列叙述错误的是( )
A.d元素的非金属性最强
B.它们均存在两种或两种以上的氧化物
C.只有a与其他元素生成的化合物都是离子化合物
D.b、c、d分别与氢形成的化合物中化学键均为极性共价键
解析:选D 短周期元素中M层电子数是1,则a的核外电子排布是2、8、1,a是Na元素;b的最外层电子数为内层电子数的2倍,则b核外电子排布是2、4,b是C元素;c的最高化合价为最低化合价绝对值的3倍,则c是S元素;c、d的原子处于同一周期,d的原子半径小于c,根据元素周期律可知d是Cl元素。A.在上述元素中非金属性最强的元素是Cl元素,正确;B.Na可以形成Na2O、Na2O2两种氧化物,C可以形成CO、CO2两种氧化物,S可以形成SO2、SO3两种氧化物,而Cl元素则可以形成Cl2O、ClO2、ClO3等多种价态的氧化物,正确;C.Na是金属元素,可以与非金属元素C、S、Cl形成离子化合物,正确;D.C元素可以与H元素形成乙烷,该分子中含有非极性键,错误。
1.元素周期表中短周期的特殊结构的应用
(1)元素周期表中第一周期只有两种元素H和He,H元素所在的ⅠA族为元素周期表的左侧边界,ⅠA族左侧无元素分布。
(2)He为0族元素,0族元素为元素周期表的右侧边界,0族元素右侧没有元素分布。
利用这个关系可以确定元素所在的周期和族。
2.元素的位置关系和原子序数关系的应用
(1)同一周期中元素的原子序数比左边元素原子序数大1,比右边元素的原子序数小1。
(2)同主族上下周期元素的原子序数关系
①若在ⅠA族或ⅡA族,原子序数之差为上周期所包含的元素种数。
②若在ⅢA~ⅦA族,原子序数之差为下周期所包含的元素种数。如第三和第四周期的同族相邻元素,若在ⅠA或ⅡA族,原子序数之差为8,若在ⅢA~ⅦA族,原子序数之差为18。
3.熟悉主族元素在周期表中的特殊位置
(1)族序数等于周期数的元素:H、Be、Al。
(2)族序数等于周期数2倍的元素:C、S。
(3)族序数等于周期数3倍的元素:O。
(4)周期数是族序数2倍的元素:Li、Ca。
(5)周期数是族序数3倍的元素:Na、Ba。
(6)最高正价与最低负价代数和为零的短周期元素:H、C、Si。
(7)最高正价是最低负价绝对值3倍的短周期元素:S。
(8)除H外,原子半径最小的元素:F。
(9)最高正价不等于族序数的短周期元素:O(F无正价)。
[对点练]
2.甲~庚等元素在周期表中的相对位置如下表,己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
A.丙与戊的原子序数相差18
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丁的最高价氧化物可用于制造光导纤维
解析:选D 己的最高价氧化物对应水化物有强脱水性,则己为S;由元素在周期表中的相对位置可推断:丙为B、丁为Si、庚为F;因甲和丁在同一周期,且甲原子最外层与最内层具有相同电子数,则甲为Mg,乙为Ca。A.丙为B,原子序数为5,而戊位于P的下方,其原子序数比P的原子序数大18,即戊的原子序数为33,则丙与戊的原子序数相差28,错误;B.同周期元素自左向右,元素的非金属性逐渐增强,同主族元素自上而下,元素的非金属性逐渐减弱,因此元素的非金属性:庚>己>戊,元素的非金属性越强,其气态氢化物的稳定性越强,故氢化物稳定性:庚>己>戊;C.常温下,甲(Mg)与水反应缓慢,加热时反应较快;D.丁(Si)的最高价氧化物为SiO2,可用于制造光导纤维,正确。
常见元素及其化合物的特性
(1)形成化合物种类最多、单质是自然界中硬度最大、气态氢化物中氢的质量分数最大的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
(3)地壳中含量最多的元素或气态氢化物的沸点最高的元素或氢化物在通常情况下呈液态的元素:O。
(4)地壳中含量最多的金属元素:Al。
(5)最活泼的非金属元素或无正价的元素或无含氧酸的非金属元素或无氧酸(气态氢化物)可腐蚀玻璃的元素或气态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(6)最活泼的金属元素或最高价氧化物对应水化物碱性最强的元素或阳离子的氧化性最弱的元素:Cs(放射性元素除外)。
(7)最易着火的非金属元素的单质,其元素是P。
(8)焰色反应呈黄色的元素:Na。
(9)焰色反应呈紫色(透过蓝色钴玻璃观察)的元素:K。
(10)单质密度最小的元素:H,密度最小的金属元素:Li。
(11)常温下单质呈液态的非金属元素:Br;金属元素:Hg。
(12)最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素:Al。
(13)元素的气态氢化物和它的最高价氧化物对应水化物发生化合反应的元素:N,能发生氧化还原反应的元素:S。
(14)元素的气态氢化物能和它的氧化物在常温下反应生成该元素单质的元素:S。
(15)元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
(16)常见的一种元素存在几种单质的元素:C、P、O、S,其中一种同素异形体易着火的元素:P。
[对点练]
3.已知a、b、c、d、e是短周期中原子序数依次增大的5种主族元素,其中元素a、e的单质在常温下呈气态,元素b的原子最外层电子数是其电子层数的2倍,元素c在同周期的主族元素中原子半径最大,元素d是地壳中含量最多的金属元素。下列说法正确的是( )
A.b元素在自然界只有一种核素
B.元素c、d、e的简单离子的半径依次减小
C.在5种元素中e元素的单质氧化性最强
D.化合物ae与ce含有相同类型的化学键
解析:选C a、b、c、d、e是短周期中原子序数依次增大的5种主族元素,b原子最外层电子数是其电子层数的2倍,结合原子序数可知b是碳元素,c在同周期的主族元素中原子半径最大,c是钠元素,d是地壳中含量最多的金属元素,d是铝元素,元素a、e的单质在常温下呈气态,则a是氢元素,e是氯元素。A项, b元素(C)在自然界有3种核素12C、13C、14C,错误;B项,元素c、d、e的简单离子的半径大小关系为Cl->Na+>Al3+,错误;C项,在5种元素中,e(Cl)的非金属性最强,其单质的氧化性最强,正确;D项,HCl含有共价键,NaCl含有离子键,错误。
[题点全练——过高考]
1.X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
A.X的最常见气态氢化物的水溶液显酸性
B.最高价氧化物对应水化物的酸性W比Z强
C.Z的单质与氢气反应比Y单质与氢气反应剧烈
D.X的原子半径小于Y
解析:
选B 根据图示元素的位置关系,结合Z原子的最外层电子数是第一层电子数的3倍,可以推出Z为S,从而可以确定X为N,Y为O,W为Cl。N的最常见气态氢化物NH3的水溶液显碱性,A错误;非金属性Cl强于S,因此最高价氧化物对应水化物的酸性:HClO4>H2SO4,B正确;非金属性O强于S,因此O2与H2反应比S与H2反应剧烈,C错误;同周期元素从左到右原子半径逐渐减小,因此N的原子半径大于O,D错误。
2.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍,X、Y的核电荷数之比为3∶4。W-的最外层为8电子结构。金属单质Z在空气中燃烧生成的化合物可与水发生氧化还原反应。下列说法正确的是( )
A.X与Y能形成多种化合物,一般条件下都能与Z的最高价氧化物的水化物发生反应
B.原子半径大小:X<Y,Z>W
C.化合物Z2Y和ZWY3都只存在离子键
D.Y、W的某些单质或两元素之间形成的某些化合物可作水的消毒剂
解析:选D 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍,则X是C,由题意推知Y的核电荷数是8,则Y是O,Z的单质在氧气中燃烧生成的化合物可与水发生氧化还原反应,则Z是Na,W-最外层为8电子结构,且X、Y、Z、W的原子序数依次增大,则W是Cl。X与Y形成的化合物有CO、CO2,但CO不与NaOH反应,A项错误;原子半径大小:C>O,Na>Cl,B项错误;化合物Na2O中只含离子键,NaClO3中既有离子键也有共价键,C项错误;O3、Cl2、ClO2等有强氧化性的物质可作水的消毒剂,D项正确。
3.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有6个电子,Y是至今发现的非金属性最强的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料。下列叙述正确的是( )
A.原子最外层电子数由多到少的顺序:Y、X、W、Z
B.原子半径由大到小的顺序:W、Z、Y、X
C.元素非金属性由强到弱的顺序:Z、W、X
D.简单气态氢化物的稳定性由强到弱的顺序:X、Y、W
解析:选A A选项,由“Y是至今发现的非金属性最强的元素”可知,Y为F;由X原子序数小于Y且“X原子最外层有6个电子”可知,X为O;由“Z在周期表中处于周期序数等于族序数的位置”可知,Z为Al;由“W的单质广泛用作半导体材料”可知,W是Si。A选项,原子最外层电子数由多到少的顺序是F、O、Si、Al,所以正确;B选项,原子半径由大到小的顺序:Al、Si、O、F,所以错误;C选项,元素非金属性由强到弱的顺序:F、O、Si,所以错误;D选项,简单气态氢化物的稳定性HF的最强,所以错误。
4.现有五种短周期元素的性质、用途或原子结构信息如下表:
元素
元素的性质、用途或原子结构信息
Q
形成化合物的种类最多
R
最外层电子数是次外层电子数的3倍
X
气态氢化物的水溶液常用作肥料,呈弱碱性
Y
第三周期元素的简单阴离子中离子半径最小
Z
单质为银白色固体,在空气中燃烧发出黄色火焰
请根据表中信息回答下列问题:
(1)Q最简单的气态氢化物分子的空间构型为_____________________________。
(2)R单质与X单质在雷电条件下反应产物为________化合物(填“共价”或“离子”)。
(3)写出R与Z组成仅含离子键的化合物的化学式:________________________。
(4)工业上用电解Y与Z形成化合物的水溶液制取Y单质,写出该反应的离子方程式:________________________________________________________________________。
解析:形成化合物种类最多的元素为C,即Q为碳元素;最外层电子数是次外层电子数3倍的元素是氧,即R为氧元素;气态氢化物的水溶液呈碱性的为NH3,即X为氮元素;第三周期元素简单阴离子中离子半径最小的是Cl-,即Y为氯元素;焰色反应是黄色的是钠元素,即Z为钠元素。
答案:(1)正四面体形 (2)共价 (3)Na2O
(4)2Cl-+2H2OH2↑+Cl2↑+2OH-
[课堂真题集训——明考向]
1.(2017·全国卷Ⅰ)短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是( )
A.X的简单氢化物的热稳定性比W的强
B.Y的简单离子与X的具有相同的电子层结构
C.Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红
D.Z与X属于同一主族,与Y属于同一周期
解析:选C 由题知,W为氮,X为氧,Y为钠,Z为硫。同周期元素从左至右,简单氢化物的热稳定性逐渐增强,H2O的热稳定性比NH3的强,A项正确;O2-和Na+核外都有10个电子,B项正确;钠和硫形成的化合物为硫化钠,它是强碱弱酸盐,其水溶液呈碱性,能使红色石蕊试纸变蓝色,C项错误;氧、硫位于同主族,钠与硫同属于第三周期,D项正确。
2.(2017·全国卷Ⅲ)短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是( )
A.氢化物沸点:WW
C.化合物熔点:Y2X3NH3>SiH4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.如图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“”(ào)命名的第118号元素在周期表中位于第七周期0族
解析:选C 非金属性:O>N>C>Si,故气态氢化物的稳定性:H2O>NH3>SiH4,A项正确;H与C、N、O、F等非金属元素形成共价化合物,与Na、Mg等金属元素形成离子化合物,B项正确;题图所示实验可证明酸性:HCl>H2CO3>H2SiO3,但元素非金属性的强弱与元素的最高价氧化物对应的水化物的酸性强弱有关,HCl不是氯元素的最高价氧化物对应的水化物,故不能根据其酸性强弱判断Cl的非金属性强弱,C项错误;118号元素在元素周期表中位于第七周期0族,D项正确。
4.(2016·全国卷Ⅰ)短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L-1r溶液的pH为2, s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
解析:选C n是元素Z的单质,通常为黄绿色气体,则n为Cl2,Z为Cl元素。Cl2(n)与二元化合物p在光照条件下反应生成r和s,0.01 mol·L-1r溶液的pH为2,s通常是难溶于水的混合物,则p为CH4,r为HCl,s为CH3Cl、CH2Cl2、CHCl3和CCl4的混合物。二元化合物m与n反应生成q和r,q的水溶液具有漂白性,其中n为Cl2,r为HCl,从而推知m为H2O,q为HClO。结合四种短周期元素的原子序数关系及形成的二元化合物之间的转化推知,W、X、Y、Z元素分别为H、C、O、Cl。A项同周期主族元素的原子半径,随原子序数的递增而逐渐减小,则原子半径的大小关系为H<O<C;B项由ClO2、CCl4可以得出元素的非金属性:O>Cl,Cl>C,则元素的非金属性强弱关系为O>Cl>C;C项Y(O)的氢化物有H2O、H2O2,常温常压下均为液态;D项X(C)的最高价氧化物的水化物为H2CO3,是一种二元弱酸。
5.(2016·全国卷Ⅱ)a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,d和b同族。下列叙述错误的是( )
A.a与其他三种元素形成的二元化合物中其化合价均为+1
B.b与其他三种元素均可形成至少两种二元化合物
C.c的原子半径是这些元素中最大的
D.d与a形成的化合物的溶液呈弱酸性
解析:选A 由题中所给的信息可知,a为H,b为O,c 为Na,d为S。A项中,H与Na可以形成化合物NaH,H的化合价为-1;B项中,O与其他三种元素可以形成H2O、H2O2、Na2O、Na2O2、SO2、SO3等二元化合物;C项中,四种元素原子半径大小顺序为Na>S>O>H; D项中,H与S形成化合物H2S,其水溶液呈弱酸性。
6.(2016·全国卷Ⅲ)四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
A.简单离子半径:W<X<Z
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y
D.最高价氧化物的水化物的酸性:Y>Z
解析:选B 四种短周期主族元素的原子序数依次增大,X的原子半径是短周期主族元素原子中最大的,则X为Na元素;Z与X(Na)形成的离子化合物的水溶液呈中性,则Z为Cl元素;因W与X的简单离子电子层结构相同,且W与Y同族,则W可能为N(或O)元素、Y可能为P(或S)元素。A项,Na+与N3-(或O2-)电子层结构相同,核电荷数越大,离子半径越小,电子层数越多离子半径越大,故离子半径:Na+<N3-(或O2-)<Cl-;B项,W与X形成的化合物Na2O、Na2O2(或Na3N)溶于水后的溶液均为NaOH溶液(或NaOH和NH3的混合溶液),呈碱性;C项,元素的非金属性越强,其气态氢化物的热稳定性越强,故热稳定性:W>Y;D项,最高价氧化物对应的水化物中HClO4是酸性最强的无机酸。
7.(2016·江苏高考)短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于ⅠA族,W与X属于同一主族,下列说法正确的是( )
A.元素X、W的简单阴离子具有相同的电子层结构
B.由Y、Z两种元素组成的化合物是离子化合物
C.W的简单气态氢化物的热稳定性比Y的强
D.原子半径:r(X)<r(Y)<r(Z)<r(W)
解析:选B Y是迄今发现的非金属性最强的元素,则Y是F元素,X原子的最外层有6个电子,且原子序数比F小,则X是O元素,Z位于ⅠA族,原子序数比F大,则Z为Na元素,W与O属于同一主族且原子序数比O大,则W是S元素。A项中,O2-的结构示意图为,S2-的结构示意图为,错误;B项中,Y与Z形成的化合物NaF是离子化合物,正确;C项中,HF的热稳定性比H2S强,错误;D项中,原子半径大小顺序为r(Na)>r(S)>r(O)>r(F),错误。
8.(2015·全国卷Ⅰ)W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18。下列说法正确的是( )
A.单质的沸点:W>X
B.阴离子的还原性:W>Z
C.氧化物的水化物的酸性:YH2,A不正确;B.Cl元素的非金属性强于H元素,元素得电子能力越强,其对应阴离子越不容易失去电子,故对应阴离子的还原性:Cl-弱于H-,B正确;C.P元素的非金属性弱于Cl元素的非金属性,元素非金属性越弱,其最高价氧化物对应水化物的酸性越弱,故酸性:H3PO4M
解析:选B 非金属性:BBe,则碱性:Mg(OH)2>Be(OH)2,B正确;同周期自左向右原子半径逐渐减小,则C、N、O原子半径依次减小,C错误;原子序数:M>R,D错误。
2.下列结论错误的是( )
①微粒半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
A.只有① B.①③⑤
C.②④⑤⑥ D.①③
解析:选D ①K+、S2-、Cl-原子核外电子排布相同,核电荷数:S2-<Cl-<K+,则半径:S2->Cl->K+,离子的原子核外电子层数越多,半径越大,核外电子层数越少,则半径越小,则有S2->Cl->K+>Al3+,故①错误;②非金属性:F>Cl>S>P>Si,元素的非金属性越强,对应的氢化物越稳定,则氢化物的稳定性:HF>HCl>H2S>PH3>SiH4,故②正确;③非金属性:Cl>Br>I>S,元素的非金属性越强,对应阴离子的还原性越弱,则还原性:Cl-<Br-<I-<S2-,故③错误;④非金属性:Cl>S>Se>Te,元素的非金属性越强,对应单质的氧化性越强,则氧化性:Cl2>S>Se>Te,故④正确;⑤非金属性:S>P>C,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性:H2SO4
>H3PO4>H2CO3,又H2CO3酸性大于HClO,则有酸性:H2SO4>H3PO4>H2CO3>HClO,故⑤正确;⑥因同周期元素从左到右元素的非金属性逐渐增强,则有非金属性:O>N、P>Si,同主族元素从上到下元素的非金属性逐渐减弱,则N>P,所以有非金属性:O>N>P>Si,故⑥正确。
3.(2018·烟台模拟)氮化镓材料属于第三代半导体,在光电子、高温大功率器件和高温微波器件应用方面有着广阔的前景。MOCVD法是制备氮化镓的方法之一,通常以Ga(CH3)3作为镓源,NH3作为氮源,在一定条件下反应制取氮化镓。下列相关说法错误的是( )
A.氮化镓的化学式为GaN
B.该反应除生成氮化镓外,还生成CH4
C.Ga(CH3)3共价化合物
D.镓位于元素周期表第四周期ⅡA族
解析:选D A项,氮位于ⅤA族,镓位于ⅢA族,根据化合价代数和等于零的原则,氮化镓的化学式为GaN,正确;B项,甲基镓与氨气反应时除生成氮化镓外,根据元素守恒知,还生成CH4,正确; C项, Ga(CH3)3为甲基与Ga原子以共价键组成的共价化合物,正确; D项,镓位于元素周期表第四周期ⅢA族,错误。
4.几种短周期元素的原子半径及主要化合价如下表:
元素代号
X
Y
Z
M
R
Q
原子半径(×10-10 m)
1.86
0.99
1.43
1.60
0.75
0.74
主要化合价
最高正价
+1
+7
+3
+2
+5
—
最低负价
—
-1
—
—
-3
-2
下列说法中正确的是( )
A.X、Z、R的最高价氧化物的水化物之间可两两相互反应
B.元素X和Q形成的化合物中不可能含有共价键
C.X、Y、M的单质分别与水反应,Y最剧烈
D.Y的氢化物的水溶液可用于雕刻玻璃
解析:选A 由化合价可知X、Y、Z、M、R、Q分别位于ⅠA族、ⅦA族、ⅢA族、ⅡA族、ⅤA族、ⅥA族,由原子半径Q<R<Y(Cl)知,R、Q只能为第二周期元素,分别为N、O;同理结合原子半径可知X、Z、M分别为Na、Al、Mg。NaOH、Al(OH)3、HNO3之间可以两两相互反应,A选项正确;Na2O2中含共价键,B选项错误;Na、Cl2、Mg分别与水反应,Na最剧烈,C选项错误;HCl不与SiO2反应,D选项错误。
5.X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X原子的最外层电子数是电子层数的3倍,X、M同主族,Y原子在短周期主族元素中原子半径最大。下列说法正确的是( )
A.Y2X和Y2X2中化学键类型相同,阴、阳离子的个数比相同
B.气态氢化物的热稳定性:M>N
C.M与X的化合物对应的水化物一定是强酸
D.离子半径:r(X2-)>r(Y+)
解析:选D X最外层电子是电子层数的3倍可知X是O;X和M同主族可知M是S;短周期主族元素中原子半径最大的是Na(Y);因原子序数依次增大且均为主族元素,N为Cl。Na2O中只含离子键、Na2O2中既有离子键又有非极性共价键,Na2O2和Na2O中阴、阳离子个数比均为1∶2,A错误;非金属性:Cl>S,气态氢化物的稳定性:HCl>H2S,B错误;H2SO3是弱酸、H2SO4是强酸,C错误;电子层结构相同的离子,核电荷数越大,离子半径越小,D正确。
6.(2018·石家庄模拟)2017年5月9日,中国科学院、国家语言文字工作委员会、全国科学技术名词审定委员会联合召开发布会,向社会正式公布了四个新元素的中文定名。113号元素为(Nh);115号元素为镆(Mc);117号元素为(Ts);118号元素为(Og)。这4个新元素的合成与确认,填满了元素周期表的第7周期,形成了一张完整规范的元素周期表。关于这四种元素,下列说法正确的是( )
A.Al的金属性强于Nh
B.Mc所在族的某种元素是一种优良的半导体,并在芯片产业中应用广泛
C.气态氢化物的稳定性:HF>HTs
D.Og所在族的所有元素都达到了最外层8电子稳定结构
解析:选C 根据原子序数可知,四种元素在周期表中的位置分别为113号元素Nh:第7周期ⅢA族;115号元素Mc:第7周期ⅤA族;117号元素Ts:第7周期ⅦA族;118号元素Og:第7周期0族。A项, Al的金属性弱于Nh,错误;B项,在芯片产业中应用广泛的优良的半导体材料是硅,错误;C项,气态氢化物的稳定性:HF>HTs,正确;D项,Og所在族中He元素最外层为2电子稳定结构,错误。
7.如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
A.原子半径:Z>Y>X
B.气态氢化物的稳定性:RAl>O(或Y>Z>X);B项,气态氢化物的稳定性:HCl>H2S;C项,SO3(WX3)和水反应生成的H2SO4为共价化合物;D项,Al(OH)3和NaOH能反应。
8.(2018·长沙模拟)已知X、Y、Z、W为短周期元素,在周期表中的相对位置如图所示,下列说法正确的是( )
X
Y
Z
W
A.若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n为正整数)
B.若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
C.若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
D.若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应
解析:选A A项,若HmXOn为强酸,则X可能为N,NH3溶于水呈碱性,错误;B项,若四种元素均为金属,则X为Li、Y为Be、Z为Na、W为Mg,Na的最高价氧化物对应的水化物为NaOH,为强碱,正确;C项,若四种元素均为非金属,则W可能为P,P的最高价氧化物对应的水化物为磷酸,为弱酸,错误;D项,若四种元素中只有一种为金属,则X为B、Y为C、Z为Al、W为Si,则Al与C两者的最高价氧化物对应的水化物分别为氢氧化铝和碳酸,二者不能发生反应,错误。
9.a、b、c、d都是短周期元素,原子半径:d>c>a>b。已知:a、b同周期,a、c处于同一主族;c原子核内的质子数等于a、b原子核内的质子数之和;c原子最外层电子数是d原子最外层电子数的3倍,下列说法正确的是( )
A.a的元素符号为Be
B.b和d两种元素形成的化合物中只能含有离子键
C.c和d两元素的最高价氧化物的水化物相互反应生成盐和水
D.d2b和d2b2阴、阳离子个数比分别为1∶2和1∶1
解析:选C a、b、c、d都是短周期元素,原子半径:d>c>a>b。a、b同周期,a、c处于同一主族,可推知a、b、c、d在周期表中的大致相对位置为,c的原子核内的质子数等于a、b原子核内的质子数之和,c质子数等于A的质子数+8,故b为8号元素氧。因a、c为主族元素,且c最外层电子数为d的3倍,则d最外层电子数只能为1,故d为钠,c为Al,a为B元素,故A错误;O、Na形成的Na2O2既含有离子键又含有共价键,故B错误;c和d两元素的最高价氧化物对应的水化物分别为Al(OH)3、NaOH,二者反应生成NaAlO2和H2O,故C正确;Na2O和Na2O2中阴、阳离子个数比都是1∶2,故D错误。
10.X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2;Y和Z最外层电子数之和与W的最外层电子数相同;25 ℃时,0.1 mol·L-1X和W形成化合物的水溶液pH为1。下列说法正确的是( )
A.Y和其他四种元素均可形成至少两种化合物(两种元素组成)
B.R元素的最高价氧化物的水化物酸性最强
C.原子半径:X<Y<Z<R<W
D.由Y、Z、W三种元素组成化合物的水溶液一定显碱性
解析:选A 由“Y和R同主族,可组成共价化合物RY2”推出Y是O,R是S;由“25 ℃时,0.1 mol·L-1X和W形成化合物的水溶液pH为1”及五种短周期元素原子序数大小关系推出X是H,W是Cl;再根据Y、Z、W最外层电子数的关系可推出Z为Na。O和H可形成H2O、H2O2,O和Na可形成Na2O、Na2O2,O和S可形成SO2和SO3,O和Cl可形成Cl2O、ClO2、Cl2O7等,A项正确;短周期元素的最高价含氧酸中HClO4的酸性最强,B项错误;原子半径:Na>S>Cl>O>H,C项错误;NaClO4是强酸强碱盐,溶液呈中性,D项错误。
11.已知A、B、C、D、E、F、G为七种短周期主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。根据以上信息回答下列问题:
(1)B、C、G的氢化物中稳定性最强的是__________(填化学式),G的某种氧化物能使溴水退色,写出该反应的化学方程式__________________________________________。
(2)B、C、D、E、F形成的简单离子半径由大到小的顺序为__________________(用离子符号表示)。
(3)D、A、C和碳元素组成的化合物的水溶液呈______性,用离子方程式解释其原因________________________________________________________________________。
解析:A、B、C、D、E、F、G都为短周期主族元素,原子序数依次增大,由A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体,可知A为H,F为Al。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31,其内层电子数之和为14,必有两种元素(B、C)为第二周期,一种元素为第三周期(G),且C、G同主族,所以B为N,C为O,G为S。D与F同周期且在该周期中D元素的原子半径最大,可知D为Na,则E为Mg。
答案:(1)H2O SO2+Br2+2H2O===H2SO4+2HBr
(2)N3->O2->Na+>Mg2+>Al3+
(3)碱 HCO+H2OH2CO3+OH-
12.X、Y、Z、W、M、N为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与N分别同主族,在周期表中X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,Z、W的最外层电子数之和与M的核外电子总数相等。试回答下列问题:
(1)N元素在周期表中的位置为_____________________;Y的简单氢化物的稳定性________(填“>”“<”或“=”)W的简单氢化物的稳定性。
(2)X、Z形成的含18电子的化合物的电子式为________________________。
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式_______________________________
________________________________________________________________________。
(4)X和W组成的化合物中,既含有极性共价键又含有非极性共价键的是________(填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为________________________________________________________________________。
解析:H的原子半径最小,所以X为H;X和M同主族,由M在题述元素中的排序知,M是Na。Y、Z、W位于第二周期,它们与H可形成等电子分子,结合Z、W的最外层电子数之和与Na的核外电子总数相等知,Y、Z、W依次为C、N、O,W与N同主族,则N为S。(1)C的非金属性弱于O的非金属性,故CH4的稳定性比H2O弱。(2)H、N形成的含18电子的化合物是N2H4,N2H4的电子式为。(3)由H、N、O、S组成的既能与盐酸反应又能与氯水反应的离子化合物为NH4HSO3或(NH4)2SO3,其分别与足量盐酸反应的离子方程式为HSO+H+===H2O+SO2↑、SO+2H+===H2O+SO2↑。(4)H2O2中含有极性共价键和非极性共价键,H2O2氧化碱性工业废水中CN-的离子方程式为OH-+CN-+H2O2===CO+NH3↑。
答案:(1)第三周期ⅥA族 < (2)
(3)SO+2H+===H2O+SO2↑
(或HSO+H+===H2O+SO2↑)
(4)H2O2 OH-+CN-+H2O2===CO+NH3↑
13.X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1∶2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为______________;元素Z的离子结构示意图为____________。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(3)元素W位于周期表的________族,其非金属性比R弱,用原子结构的知识解释原因:________________________________________________________________________
________________________________________________________________________。
(4)R的一种氧化物能使品红溶液退色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:_____________________。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为 1∶3,则该反应的化学方程式为_____________________________________________________________。
解析:由X原子核外各层电子数之比为1∶2,推出X为C;由Y的氧化物和R的氧化物均能形成酸雨且R的原子序数大于Y,推出Y和R分别为N和S;由W和R是同周期相邻元素且R的原子序数大于W,推出W为P;由Y原子和Z原子的核外电子数之和为20,推出Z为Al。(4)氨水与足量SO2反应生成NH4HSO3。
答案:(1)
(2)3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
(3)ⅤA P原子和S原子的电子层数相同,P原子半径较大,得电子能力较弱
(4)SO2+NH3·H2O===HSO+NH
(5)Al2O3+3C+N22AlN+3CO
第三节 化学键
[教材基础——自热身]
1.离子键和共价键
(1)化学键的分类
(2)化学反应的本质
反应物生成物
(3)离子键与共价键
①概念
离子键:阴、阳离子通过静电作用形成的化学键。
共价键:原子间通过共用电子对所形成的化学键。
②对比
项目
离子键
共价键
成键粒子
阴、阳离子
原子
成键方式
得失电子形成阴、阳离子
形成共用电子对
成键条件
活泼金属元素与活泼非金属元素
一般在非金属原子之间
作用力
实质
静电作用
共用电子对
存在举例
存在于离子化合物中,如 NaCl、KCl、MgCl2、CaCl2、ZnSO4、NaOH等
(1)非金属单质,如H2、O2等;
(2)共价化合物,如HCl、CO2、CH4等;
(3)某些离子化合物,如NaOH、Na2O2等
2.电子式
(1)概念:在元素符号周围用“·”或“×”来代表原子的最外层电子的式子。
(2)书写方法
(3)用电子式表示化合物的形成过程
①离子化合物:左边是原子的电子式,右边是离子化合物的电子式,中间用“―→”连接,相同的原子或离子不合并。
如NaCl:。
②共价化合物:左边是原子的电子式,右边是共价化合物的电子式,中间用“―→”连接。
如HCl:。
[题点全练——过高考]
题点一 化学键类型的判断
1.下列关于化学键的叙述正确的是( )
A.非金属元素组成的化合物中只含共价键
B.C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键
C.不同元素的原子构成的分子只含极性共价键
D.CH4中所有的最外层电子都参与形成共价键
解析:选D A项,在铵盐中含有离子键;B项,C、N、O、H形成的氨基酸只含共价键;C项,C2H6、C2H4等烃中除极性键外,还含有非极性键。
2.下列化合物中,含有非极性共价键的离子化合物是( )
A.CaC2 B.N2H4
C.Na2O D.NH4NO3
解析:选A CaC2是离子化合物,C中C、C之间为非极性共价键,A项正确;N2H4是共价化合物,B项错误;Na2O中仅含离子键,C项错误;NH4NO3是离子化合物,但不含非极性共价键,D项错误。
题点二 电子式的书写
3.判断正误(正确的打“√”,错误的打“×”)。
答案:(1)× (2)× (3)× (4)× (5)× (6)× (7)×
(8)× (9)× (10)× (11)× (12)×
[误区警示] 电子式书写常见的6大误区
题点三 8电子结构的判断
4.下列物质中所有原子均满足最外层8电子稳定结构的化合物是( )
A.H2S B.P4 C.CCl4 D.NH3
解析:选C 判断原子满足最外层8电子结构的方法为最外层电子数+所成价键数=8,A、D项错误;P4为单质,而非化合物,B项错误;C项中5原子最外层均为8电子稳定结构,C项正确。
5.含有极性键且分子中各原子都满足8电子稳定结构的化合物是( )
A.CH4 B.CH2===CH2
C.CO2 D.N2
解析:选C A、B两项中的氢原子都只满足2电子稳定结构;D项,N2是单质而不是化合物。
[规律方法] 8电子结构的判断方法
(1)经验规律法
凡符合最外层电子数+|化合价|=8的皆为8电子结构。
(2)试写结构法
判断某化合物中的某原子最外层是否达到8电子稳定结构,应从其结构式或电子式结合原子最外层电子数进行判断,如①H2O中O最外层有8个电子,而H最外层只有2个电子,②N2中N原子最外层有5个电子,N与N之间形成3个共价键,所以N2中的N原子最外层达到8电子稳定结构。
[教材基础——自热身]
1.离子化合物与共价化合物的比较
项目
离子化合物
共价化合物
定义
含有离子键的化合物
只含有共价键的化合物
构成微粒
阴、阳离子
分子
化学键类型
一定含有离子键,
可能含有共价键
只含有共价键
与物质类
别的关系
①强碱、②绝大多数盐、③活泼金属氧化物
①酸、②弱碱、③气态氢化物、④非金属氧化物、⑤极少数盐
2.化学键与物质类别的关系
(1)只含有极性共价键的物质一般是由两种非金属元素形成的共价化合物,如SiO2、HCl、CH4等。
(2)只含有非极性共价键的物质是同种非金属元素形成的单质,如Cl2、P4、金刚石等。
(3)既有极性键又有非极性键的共价化合物一般由多个原子组成,如H2O2、C2H4等。
(4)只含离子键的物质主要是由活泼非金属元素与活泼金属元素形成的化合物,如Na2S、CaCl2、NaCl等。
(5)既有离子键又有极性共价键的物质,如NaOH、K2SO4等;既有离子键又有非极性共价键的物质,如Na2O2等。
(6)仅由非金属元素形成的离子化合物,如NH4Cl、NH4NO3等。
(7)金属元素和非金属元素间可能存在共价键,如AlCl3等。
3.物质的溶解或熔化与化学键变化
(1)离子化合物的溶解或熔化过程
离子化合物溶于水或熔化后均电离成自由移动的阴、阳离子,离子键被破坏。
(2)共价化合物的溶解过程
①有些共价化合物溶于水后,能与水反应,其分子内共价键被(填“被”或“不被”,下同)破坏,如CO2和SO2等。
②有些共价化合物溶于水后,与水分子作用形成水合离子,从而发生电离,形成阴、阳离子,其分子内的共价键被破坏,如HCl、H2SO4等。
③某些共价化合物溶于水后,其分子内的共价键不被破坏,如蔗糖(C12H22O11)、酒精(C2H5OH)等。
(3)单质的溶解过程
某些活泼的非金属单质溶于水后,能与水反应,其分子内的共价键被破坏,如Cl2、F2等。
4.分子间作用力和氢键
(1)分子间作用力
定义
把分子聚集在一起的作用力,又称范德华力
特点
①分子间作用力比化学键弱得多,它主要影响物质的熔点、沸点等物理性质,而化学键主要影响物质的化学性质;
②分子间作用力存在于由共价键形成的多数共价化合物和绝大多数气态、液态、固态非金属单质分子之间。但像二氧化硅、金刚石等由共价键形成的物质,微粒之间不存在分子间作用力
变化规律
一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔、沸点也越高。例如,熔、沸点:I2>Br2>Cl2>F2
(2)氢键
定义
分子间存在的一种比分子间作用力稍强的相互作用
形成条件
除H外,形成氢键的原子通常是O、F、N
存在
氢键存在广泛,如蛋白质分子、醇、羧酸分子、H2O、NH3、HF等分子之间。分子间氢键会使物质的熔点和沸点升高
[题点全练——过高考]
题点一 化学键的断裂与形成
1.在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )
A.将SO2通入水中 B.烧碱溶于水
C.将HCl通入水中 D.硫酸氢钠溶于水
解析:选D SO2、HCl不含有离子键,所以通入水中不会有离子键的破坏,A、C错误;烧碱在水溶液中电离产生Na+和OH-,没有共价键的破坏,B错误;硫酸氢钠既含有离子键又含有共价键,溶于水时电离出Na+、H+和SO,既有离子键被破坏,也有共价键被破坏。
2.下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
A.2Na2O2+2H2O===4NaOH+O2↑
B.Mg3N2+6H2O===3Mg(OH)2↓+2NH3↑
C.Cl2+H2O===HClO+HCl
D.NH4Cl+NaOH===NaCl+NH3↑+H2O
解析:选A A项,反应中有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成,正确;B项,该反应中没有非极性键的断裂和形成,错误;C项,该反应中没有离子键的断裂和形成,也没有非极性键的形成,错误;D项,该反应中没有非极性键的断裂和形成,错误。
题点二 化学键与物质类别
3.下列关于离子键、共价键的叙述中,正确的是( )
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如Cl2)中
C.在共价化合物分子内,一定不存在离子键
D.由多种元素组成的多原子分子里,一定只存在极性键
解析:选C A项,NH4Cl中存在共价键;B项,如H2O2、CH3CH3等分子中存在非极性键;C项,共价化合物一定不含离子键;D项,H2O2、C2H6等分子中存在非极性键。
4.有以下9种物质:①Ne ②HCl ③P4 ④H2O2
⑤Na2S ⑥NaOH ⑦Na2O2 ⑧NH4Cl ⑨AlCl3
请用上述物质的序号填空:
(1)不存在化学键的是______________________________________________________。
(2)只存在极性共价键的是__________________________________________________。
(3)只存在非极性共价键的是________________________________________________。
(4)既存在非极性共价键又存在极性共价键的是_______________________________。
(5)只存在离子键的是_______________________________________________。
(6)既存在离子键又存在共价键的是_________________________________________。
答案:(1)① (2)②⑨ (3)③ (4)④ (5)⑤ (6)⑥⑦⑧
题点三 分子间作用力与氢键
5.下列变化需克服相同类型作用力的是( )
A.碘和干冰的升华 B.硅和C60的熔化
C.氯化氢和氯化钾的溶解 D.溴和汞的汽化
解析:选A A项变化克服的都是分子间作用力,正确;硅和C60的熔化分别克服的是共价键、分子间作用力,
B项错误;氯化氢和氯化钾的溶解分别克服的是共价键、离子键,C项错误;溴和汞的汽化分别克服的是分子间作用力、金属键,D项错误。
6.下列现象与氢键有关的是( )
①NH3的熔、沸点比第ⅤA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶 ③冰的密度比液态水的密度小 ④水分子高温下很稳定
A.①②③④ B.①②③
C.①② D.①③
解析:选B 水分子高温下很稳定是因为分子中O—H键的键能大。
[课堂真题集训——明考向]
1.(2017·江苏高考)短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的是( )
A.原子半径:r(X)r(N)>r(O)>r(H),A项错误;NaOH为强碱,B项错误;非金属性:O>N,则氧化性O2(或O3)强于N2,C项错误;H、N和O可以组成共价化合物如HNO3,也可以组成离子化合物如NH4NO3,D项正确。
2.(2015·全国卷Ⅱ)原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是( )
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a、b、c各自最高和最低化合价的代数和分别为 0、4、6
解析:选B 由a的最外层电子数为1,a-的电子层结构与氦相同可知,a为H;b和c的次外层有8个电子,则b、c处于第三周期,又知b、c的最外层电子数分别为6、7,从而推知,b、c分别为S、Cl;由c-和d+的电子层结构相同可知,d为K。A项,S、Cl处于第三周期,Cl的原子序数大于S,则Cl的非金属性强于S;由H2S中S元素显-2价、H元素显+1价可知,S的非金属性强于H,因此三种元素的非金属性次序为Cl>S>H,正确;B项,H和S、Cl可形成共价化合物H2
S和HCl,而H与K则形成离子化合物KH,错误;C项,K和H、S、Cl均可形成离子化合物,分别为KH、K2S和KCl,正确;D项,H、S、Cl的最高化合价分别为+1、+6和+7,最低化合价分别为-1、-2和-1,因此三种元素各自最高和最低化合价的代数和分别为0、4、6,正确。
3.判断正误(正确的打“√”,错误的打“×”)。
答案:(1)× (2)× (3)√ (4)×
4.书写下列物质的电子式:
(1)(2017·海南高考)P与H组成的最简单化合物的电子式为________________。
(2)(2017·天津高考)NaOH的电子式为________________。
(3)(2016·全国卷 Ⅱ)联氨(N2H4)的电子式为_____________________________________。
(4)(2016·浙江高考)硫化氢的电子式为__________________________________________。
(5)(2015·全国卷Ⅰ)硼氢化钠(NaBH4)的电子式为________________。
(6)(2015·浙江高考)H2O2的电子式为________________________ _________________。
(7)(2015·海南高考)甲硅烷(SiH4)的电子式为____________________。
5.(2017·海南高考)X、Y、L、M为核电荷数依次增大的前20号主族元素。X2是最轻的气体,Y、L与M三种元素的质子数均为5的倍数。回答下列问题:
(1)X与L组成的最简单化合物的电子式为________。
(2)X与M组成的物质为__________(填“共价”或“离子”
)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为___________________________。
(3)Y在周期表中的位置是______________________,其含氧酸的化学式为____________。
(4)L与M形成的化合物中L的化合价是________。
解析:X2为最轻的气体,即X为H,Y、L、M三种元素的质子数为5的倍数,质子数等于原子序数,质子数可能为5、10、15、20中的三个,因四种元素为主族元素,故质子数为10舍去,即三种元素分别为B、P、Ca。(1)形成的简单化合物是PH3,其电子式为。(2)形成的化合物是CaH2,属于离子化合物,与水发生的反应是CaH2+2H2O===Ca(OH)2+2H2↑。(3)Y为B,属于第二周期ⅢA族元素,其含氧酸为H3BO3。(4)形成的化合物是Ca3P2,其中P显-3价。
答案:(1)
(2)离子 CaH2+2H2O===Ca(OH)2+2H2↑
(3)第二周期ⅢA族 H3BO3 (4)-3
[课下能力测评——查缺漏]
1.下列化学用语的表述正确的是( )
解析:选A B项,NaClO的电子式应为;C项,碳原子半径应大于氧原子半径;D项,HClO的结构式应为H—O—Cl。
2.下列说法中正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.NH4NO3中含共价键,是共价化合物
C.H2O2、N2H4分子中只含有极性共价键
D.某化合物熔融状态能导电,可以证明该化合物内一定存在离子键
解析:选D A项,离子键是阴、阳离子的静电作用,包括引力和斥力,错误;B项,NH4NO3是离子化合物,含有离子键和共价键,错误;C项,H2O2、N2H4分子中均含有极性共价键和非极性共价键,错误;D项,离子化合物在熔融状态下导电,共价化合物在熔融状态下不导电,正确。
3.下列关于化学键的说法正确的是( )
①含有金属元素的化合物一定是离子化合物
②ⅠA族和ⅦA族元素原子化合时, 一定形成离子键
③由非金属元素形成的化合物一定不是离子化合物
④活泼金属与活泼非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物
⑥离子化合物中可能同时含有离子键和共价键
A.①②⑤ B.④⑤⑥
C.①③④ D.②③⑤
解析:选B AlCl3属于共价化合物,①错;ⅠA族的H元素和ⅦA族卤素化合时形成共价键,②错;非金属元素形成的铵盐都是离子化合物,③错。
4.(2018·日照模拟)2017年1月,南京理工大学胡炳成教授团队成功合成世界首个全氮阴离子盐,全氮阴离子化学式为N。下列关于全氮阴离子盐的说法正确的是( )
A.每个N含有26个电子
B.N的摩尔质量为71 g·mol-1
C.全氮阴离子盐既含离子键又含共价键
D.全氮阴离子盐可能属于电解质,也可能属于非电解质
解析:选C A项,每个N含有36个电子,错误;B项,N的摩尔质量为70 g·mol-1,错误;C项,全氮阴离子盐既含离子键(存在于离子之间)又含共价键(存在于N内部N原子之间),正确;D项,全氮阴离子盐属于离子化合物,不可能属于非电解质,错误。
5.在下列变化过程中,属于“破坏极性键和非极性键,形成极性键和非极性键”过程的是( )
A.冰→水→水蒸气→H2和O2
B.2Na+Cl2===2NaCl
C.2H2+O22H2O
D.2H2O2===2H2O+O2↑
解析:选D A项,冰转化为水是物理变化,水蒸气转化为H2和O2,破坏极性键,形成非极性键,错误;B项,钠是金属,与氯气反应生成氯化钠形成离子键,错误;C项, 氢气与氧气反应生成水,破坏非极性键,形成极性键,错误;D项,双氧水分解形成水和氧气,破坏极性键和非极性键,形成极性键和非极性键,正确。
6.元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期。下列有关推测正确的是( )
A.XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY
B.XYZ3是一种微溶于水的盐,且X与Z可形成离子化合物XZ
C.XYZ3是一种易溶于水的盐,且Y与Z可形成离子化合物YZ
D.XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ2
解析:选B 由题目可知,XYZ3可能为NaNO3、MgCO3,溶于水不能形成酸,A项错;若XYZ3为MgCO3,微溶于水,则XZ形成离子化合物MgO,B项正确;若XYZ3为NaNO3,易溶于水,YZ(NO)不是离子化合物,C项错;若XYZ3是离子化合物,YZ2为NO2或CO2,均不是离子化合物,D项错。
7.短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是( )
A.元素W、X的氯化物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1∶1的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成共价化合物XZ2
解析:选A 根据题意,推断出W是Li,X是C,Y是Al,Z是S。A项,LiCl中的Li不满足8电子稳定结构,错误;B项,C元素和H元素可形成C2H2、C6H6、C8H8等多种化合物;C项,Al与强酸、强碱溶液都能反应放出H2;D项,C元素和S元素能形成CS2。
8.X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见气体甲。X、Y、Z 3种元素形成化合物乙。下列说法错误的是( )
A.气体甲可与Z的某种氢化物反应生成强酸
B.化合物乙中一定只含共价键
C.W和Z元素形成的化合物中只含极性键
D.X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM
解析:选B X的质子总数与电子层数相同,X为H,Z和与其同主族的短周期元素可形成常见气体甲,则甲为SO2,Z只能是O,Y、Z、M同周期且相邻,则它们分别为N、O、F。W原子核外电子数是M原子最外层电子数的2倍,W的核外电子数为14,W为Si,X、Y、Z、M、W分别为H、N、O、F、Si。SO2与H2O2反应生成H2SO4,故A正确;H、N、O三种元素形成的化合物乙可能为HNO3、HNO2、NH3·H2O、NH4NO3等,NH4NO3中有离子键,故B错误;SiO2中只含极性键,故C正确;X分别与Y、Z、M、W形成的常见化合物分别为NH3、H2O、HF、SiH4,非金属性越强其氢化物越稳定,最稳定的为HF,故D正确。
9.(2018·陕西宝鸡检测)X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法不正确的是( )
A.R的氧化物都含有离子键
B.M的氢化物常温常压下为气体
C.最高价含氧酸的酸性:Z<Y
D.Y形成的化合物种类最多
解析:选C 根据题图可推知,X为H,Y为C,Z为N,M为S,R为Na。Na的氧化物为Na2O、Na2O2,二者均为离子化合物,A项正确;S的氢化物为H2S,常温常压下为气体,B项正确;非金属性:N>C,故最高价含氧酸的酸性:HNO3>H2CO3,C项错误;含碳化合物种类最多,D项正确。
10.(2018·福建龙海模拟)二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2遇水易与水发生反应,并产生能使品红退色的气体。下列说法错误的是( )
A.S2Cl2的结构中各原子均达到8电子的稳定结构
B.S2Cl2为含有极性键和非极性键的共价化合物
C.若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2> S2Br2
D.S2Cl2与H2O反应的化学方程式可能为2S2Cl2+2H2O===SO2↑+3S↓+4HCl
解析:选C A项,由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为,各原子均达到8电子的稳定结构,正确;B项,S2Cl2分子中S—S为非极性键,S—Cl键为极性键,正确;C项,S2Br2与S2Cl2的组成与结构相似,相对分子质量越大,范德华力越大,其熔沸点越高,所以熔沸点:S2Br2>S2Cl2,错误;D项,S2Cl2遇水易水解,并产生能使品红溶液退色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),正确。
11.(1)请用下列10种物质的序号填空:
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2
⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
其中既含离子键又含非极性键的是________;既含离子键又含极性键的是________。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为______________________;若XY2为共价化合物时,其结构式为____________。
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为 190 ℃,但在180 ℃就开始升华。据此判断,氯化铝是______________(填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是_______________________________________________________。
(4)现有a~g 7种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
①元素的原子间最容易形成离子键的是________(填序号,下同),容易形成共价键的是________。
A.c和f B.b和g
C.d和g D.b和e
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式________。
解析:(2)1∶2型离子化合物,通常X为+2价,Y为-1价,故X可能是Mg2+或Ca2+,Y可能是F-或Cl-,结合XY2中含有38个电子可推出XY2为CaF2。1∶2型共价化合物一般是碳族元素与氧族元素化合形成的,如CO2、CS2等,再由XY2中共有38个电子,可推出XY2为CS2。
答案:(1)④ ③⑤
(2) S===C===S
(3)共价化合物 氯化铝在熔融状态下不能导电
(4)①B C ②CCl4(或PCl3)
12.原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:_____________________________________________________,
其中含有的化学键是________________。
(2)用电子式表示Y2O的形成过程:__________________________________________
________________________________________________________________________。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是________(填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是____________(填化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式:_________________
________________________________________________________________________。
解析:根据短周期元素Y可形成Y2O和Y2O2两种离子化合物可判断,Y为Na,由分子式XH3、H2Z和HW可知,X、Z、W分别属于ⅤA、ⅥA、ⅦA三个主族,再由原子序数的关系不难判断:X、Z、W分别为N、S、Cl。
答案:(1) 离子键、非极性共价键
(2) (3)HNO3
(4)NH3 (5)NCl3+3H2O===3HClO+NH3
13.A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。请回答以下问题:
(1)F位于第________周期________族。
(2)G的离子结构示意图为________________。
(3)用电子式表示D2的形成过程:______________________________________。
(4)由A、E、F三种元素形成的化合物的化学式为______,含有的化学键有____________________(填写完整化学键类型),属于________化合物。
(5)B的最高价是__________,由A、B组成的化合物中,含A量最高的物质的化学式是__________;与D2相对分子质量相等的物质的化学式是__________,含有的化学键有________________________________(填写完整化学键类型),有________对共用电子对。
解析:A、F同主族,且A与其他非金属元素化合时易形成共价键,但F与其他非金属元素化合时易形成离子键,则为ⅠA族元素,且A为氢元素。F+与E2-核外电子排布相同,则F为Na,E为O,B为C,D为N,E、G同主族,且为短周期元素,则G为S。(1)Na位于第三周期ⅠA族。(2)S2-结构示意图为。(3)N2的形成过程为。(4)NaOH中既有离子键又有极性共价键,属于离子化合物。(5)C的最高化合价为+4;C2H4中既有极性共价键(C—H)又有非极性共价键(C===C)。
答案:(1)三 ⅠA (2)
(3)
(4)NaOH 离子键和极性共价键 离子
(5)+4 CH4 C2H4 极性共价键和非极性共价键 6
一、辨清易错易混不失分
1.原子结构
(1)不同的核素,一定具有相同的中子数( )
(2)不同的核素,一定具有不同的质子数( )
(3)通过化学变化可以实现16O和18O的相互转化( )
(4)质子数相同的微粒一定属于同一种元素( )
(5)H、D、T之间互称为同位素,H2、D2、T2之间互称为同素异形体( )
(6)质子数和中子数决定原子的种类( )
(7)质子数和中子数之和等于该元素的相对原子质量( )
(8)原子最外层只有一个电子的元素一定都是金属元素( )
(9)原子核都是由质子和中子构成的( )
答案:(1)× (2)× (3)× (4)× (5)× (6)√
(7)× (8)× (9)×
2.元素周期律和元素周期表
(1)最外层电子数是次外层电子数3倍的短周期元素一定是O元素( )
(2)内层电子总数是最外层电子数2倍的短周期元素一定是P元素( )
(3)最外层电子数是电子层数2倍的短周期元素共有3种( )
(4)最外层电子数是2的元素一定是ⅡA族( )
(5)同周期ⅡA族和ⅢA族的原子序数一定相差1( )
(6)同主族从上到下,非金属性:F>Cl>Br;酸性:HF>HCl>HBr( )
(7)主族元素的最外层电子数等于族序数,也等于其最高正化合价数( )
(8)元素的一个原子失去的电子数越多,其金属性越强( )
(9)碱金属元素是指ⅠA族的所有元素( )
(10)第三周期元素的简单离子中半径最小的是Al3+( )
(11)金属元素的最外层电子数不一定小于4( )
(12)同主族的两种元素原子序数之差可能为16( )
(13)短周期元素形成离子后,最外层都达到8电子稳定结构( )
答案:(1)√ (2)× (3)√ (4)× (5)× (6)× (7)×(8)× (9)× (10)√ (11)√ (12)√ (13)×
3.化学键
(1)所有物质中都存在化学键( )
(2)金属与非金属化合形成的一定是离子键( )
(3)非金属元素之间只能形成共价键( )
(4)存在离子键的化合物一定是离子化合物,但存在共价键的化合物不一定是共价化合物( )
(5)共价化合物中只含极性共价键,离子化合物中一定含有离子键,可能含有共价键( )
(6)化学键被破坏的变化,一定是化学变化( )
(7)熔融状态下能导电的化合物一定是离子化合物( )
(8)由非金属元素组成的化合物一定是共价化合物( )
答案:(1)× (2)× (3)× (4)√ (5)× (6)×
(7)√ (8)×
二、掌握内在规律快得分
1.元素性质递变规律
(1)同主族元素
①碱金属元素(按Li、Na、K的顺序)性质的递变规律
a.金属性逐渐________,表现在:单质与O2反应的产物越来越________(4Li+O22Li2O、2Na+O2Na2O2),反应程度越来越________;单质与水(或酸)反应的剧烈程度逐渐________;最高价氧化物对应水化物的碱性逐渐______。
b.单质的密度逐渐增大(______特殊),熔、沸点逐渐________。
②卤族元素(按F、Cl、Br、I的顺序)性质的递变规律
a.非金属性逐渐减弱,表现在:单质与氢气化合由易到难的顺序:____________;气态氢化物的稳定性:____________;最高价氧化物对应水化物的酸性:____________________;卤素单质的氧化性:________________;简单阴离子的还原性:________________。
b.单质的颜色逐渐________,密度逐渐________,熔、沸点逐渐________。
(2)同周期元素(按Na、Mg、Al、Si、P、S、Cl)性质的递变规律
①原子半径大小顺序为___________________________________________________。
②金属性逐渐减弱,表现在:单质置换水或酸中的氢,由易到难的顺序为_____S_______;最高价氧化物对应水化物的碱性由强到弱的顺序为_______________________。
③
非金属性逐渐增强,表现在:单质与氢气化合由难到易的顺序为______________;气态氢化物的稳定性由弱到强的顺序为________________;最高价氧化物对应水化物的酸性由弱到强的顺序为________________________。
答案:(1)①a.增强 复杂 剧烈 增强 增强
b.K 降低
②a.F2>Cl2>Br2>I2
HF>HCl>HBr>HI HClO4>HBrO4>HIO4
F2>Cl2>Br2>I2 Cl-<Br-<I-
b.加深 增大 升高
(2)①Na>Mg>Al>Si>P>S>Cl
②Na>Mg>Al NaOH>Mg(OH)2>Al(OH)3
③Si<P<S<Cl SiH4<PH3<H2S<HCl
H2SiO3<H3PO4(中强酸)<H2SO4<HClO4
2.微粒半径比较规律
(1)同周期元素(电子层数相同)的原子半径随核电荷数的增大,自左至右逐渐_________。如r(Na)________r(Mg)________r(Al)。
(2)稀有气体元素的原子半径比与它相邻的卤素原子的原子半径大。如r(Ar)________r(Cl)。
(3)同主族元素的原子半径随电子层数的增多而增大。如r(F)________r(Cl)________r(Br)________r(I)。
(4)核外电子排布相同的粒子的半径,随核电荷数的增多而减小。如离子的半径大小是r(Ca2+)____________r(K+)________r(Cl-)________r(S2-)。
(5)对同一元素来讲,价态越高半径越小。如r(Fe3+)________r(Fe2+)________r(Fe)。
(6)不同周期、不同主族元素原子半径大小的比较。先找参照元素,使其建立起同周期、同主族的关系,然后进行比较。比较S与F的原子半径大小,先找O做参照,因为O与F同周期,r(F)______r(O);而O与S同主族,r(O)________r(S),所以 r(F)________r(S)。
答案:(1)减小 > > (2)> (3)< < < (4)<
< < (5)< < (6)< < <
3.化学键与物质类别关系规律
(1)只含非极性共价键的物质:___________________,如N2、I2、P4、金刚石、晶体硅。
(2)只含有极性共价键的物质:______________________,如HCl、NH3、CS2等。
(3)既含有非极性键又含有极性键的物质:如________________________________
____________等。
(4)只含有离子键的物质:______________和活泼非金属元素形成的化合物,如Na2S、NaCl等。
(5)既含有离子键又含有非极性键的物质,如_________________________________等。
(6)由强极性键构成但又不是强电解质的物质是 ________。
(7)只含有共价键而无范德华力的化合物,如原子晶体 ____________等。
(8)无化学键的物质:稀有气体,如 ________等。
答案:(1)同种非金属元素构成的单质 (2)一般是由不同种非金属元素构成的化合物 (3)H2O2、CH3CH3、C6H6 (4)活泼金属元素 (5)Na2O2、CaC2 (6)HF
(7)SiO2、SiC (8)He、Ne、Ar
[综合评估验收]
一、选择题(每个小题只有一个选项符合题意,每题5分,共50分)
1.(2018·枣庄模拟)在二氯化铂的HCl溶液中,通入乙烯气体,再加入KCl,可得K[Pt(C2H4)Cl3]·H2O(蔡氏盐)。下列相关表示正确的是( )
A.中子数为117,质子数为78的铂原子:Pt
B.KCl的电子式:
C.乙烯的结构简式:CH2CH2
D.氯离子的结构示意图:
解析:选B A项,质量数=质子数+中子数,故铂原子的质量数为195,表示为78Pt,错误; B项,KCl由K+和Cl-构成,故电子式为K+[C]-,正确; C项,乙烯的结构简式中碳碳双键不能省略,即CH2===CH2,错误;D项,氯离子的核内有17个质子,带17个正电荷,核外有18个电子,故结构示意图为,错误。
2.下列有关元素周期表结构的说法中正确的是( )
A.原子最外层电子数为2的元素一定处于周期表ⅡA族
B.在元素周期表中金属和非金属分界线附近可以寻找合金材料
C.某元素原子核外的电子数为51,则它是第五周期ⅤA族元素
D.除短周期外,其他周期均为18种元素,副族元素没有非金属元素
解析:选C 最外层电子数为2的元素可能是He,位于0族,A错误;金属与非金属分界线附近可以寻找半导体材料,B错误;8-(54-51)=5,所以该元素为第五周期ⅤA族元素,C正确;第六周期有32种元素,D错误。
3.下列事实不能用元素周期律解释的是( )
A.气态氢化物的稳定性:HBr>HI
B.0.1 mol·L-1溶液的pH:NaOH > LiOH
C.向Na2SO3溶液中加盐酸,有气泡产生
D.Mg、Al与同浓度盐酸反应,Mg更剧烈
解析:选C A.同一主族从上到下,气态氢化物的稳定性依次减弱,则稳定性:HBr>HI,能用元素周期律解释,A项不选;B.同一主族从上到下,金属性逐渐增强,氢氧化物的碱性逐渐增强,碱性:NaOH>LiOH,则同浓度的两种溶液,NaOH溶液的pH较大,能用元素周期律解释,B项不选;C.Na2SO3与盐酸反应生成SO2,能够证明酸性:HCl>H2SO3,不能体现元素周期律,C项选;D.同周期从左到右,金属性逐渐减弱,金属单质的还原性逐渐减弱,因此Mg比Al与等浓度的盐酸反应更剧烈,能用元素周期律解释,D项不选。
4.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述不正确的是( )
A.X与Y元素能形成两种常见的气态化合物
B.原子半径的大小顺序:r(Z)>r(R)>r(X)>r(Y)
C.X、Z分别与R形成的化合物中化学键类型不同
D.含有Y、Z、R三种元素的化合物最多只有2种
解析:选D X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,最外层电子数不超过8个,则X是C(碳);Y元素在地壳中的含量最多,则Y是O;Z元素的化合物的焰色反应呈黄色,则Z是Na;R原子的核外电子数是X原子与Z原子的核外电子数之和,则R的核外电子数是17,R是Cl。X与Y元素形成的两种常见的气态化合物有CO和CO2,A项叙述正确;同主族元素原子的电子层数越多,原子半径越大,同周期主族元素的原子半径随着原子序数的增大而减小,C、O位于第二周期,Na、Cl位于第三周期,且O的原子序数大于C的,Cl的原子序数大于Na的,所以原子半径大小顺序是r(Z)>r(R)>r(X)>r(Y),B项叙述正确;X、Z与R形成的化合物分别是CCl4、NaCl,CCl4中只含有共价键,NaCl中只含有离子键,C项叙述正确;Y、Z、R分别是O、Na、Cl,含有三种元素的化合物有NaClO、NaClO2、NaClO3、NaClO4等,D项叙述错误。
5.四种相邻的主族短周期元素的相对位置如表所示,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。下列说法中正确的是( )
A.x最高价氧化物对应水化物的碱性比y弱
B.m可形成多种氢化物,而n只形成一种氢化物
C.x的单质在m的最高价氧化物中燃烧,生成两种固体物质
D.m、n两元素所形成的化合物分子中,既含有离子键,也含有共价键
解析:选C 4元素都是短周期元素,且为相邻主族,根据元素在周期表中的位置知,m和n位于第二周期、x和y位于第三周期,x原子核外电子数是m的2倍,y的氧化物具有两性,则y是Al元素,根据元素位置知,x是Mg元素、m是C元素、n是N元素;A.Mg(OH)2
的碱性比Al(OH)3强,故A错误;B.碳元素可形成多种氢化物,N也能形成多种氢化物,如NH3、N2H4等,故B错误;C.Mg在CO2中燃烧,生成MgO和C两种固体物质,故C正确;D.C、N两元素所形成的化合物分子中,只含有共价键,D错误。
6.部分短周期元素的有关信息:
元素代号
元素性质或原子结构
T
第二层上的电子数是第一层的3倍
R
与T 同一族
L
L2+与T2-的核外电子数相等
Q
与L同族
Z
元素最高正价是+3价,与L同周期
根据上表中信息,判断以下叙述正确的是( )
A.氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.Z与T形成的化合物具有两性
D.L与R通过离子键形成的化合物阴阳离子的核外电子数相等
解析:选C 短周期元素中,T元素原子第二层上的电子数是第一层的3倍,则L层电子数为6,故T为O元素;R与T 同一族,则R为S元素;L2+与T2-的核外电子数相等,则L为Mg;Q与L同族,则Q为Be;Z元素最高正价是+3价,与L同周期,则Z为Al;A.非金属性:O>S,故氢化物的稳定性为H2O>H2S,故A错误;B.金属性:L(Mg)>Q(Be),故Mg与盐酸反应更剧烈,故B错误;C.Z与T形成的化合物为Al2O3,属于两性氧化物,故C正确;D.L与R通过离子键形成的化合物为MgS,Mg2+离子核外电子数为10、S2-离子核外电子数为18,故D错误。
7.现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列推断不正确的是( )
A.Y、Z组成的化合物只含离子键
B.简单氢化物的沸点和稳定性排序:RR
D.由X、Y、Z、T四种元素组成的化合物水溶液一定显酸性
解析:选A 根据题意判断X、Y、Z、R、T分别为H、O、Na、C、S元素。Na2O2中含有非极性共价键,A项错误;氢化物的沸点和稳定性排序为CH4H2CO3,C项正确;NaHSO3和NaHSO4的水溶液均呈酸性,D项正确。
8.被誉为“矿石熊猫”
的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是( )
A.原子半径:Y>Z>R>T
B.气态氢化物的稳定性:WZ
D.XR2、WR2两种化合物中R的化合价相同
解析:选D 根据题给信息知T无正价,则T为氟元素;Y、Z、R、T位于同周期,则在第二周期,由R最外层电子数为次外层的3倍,则R为氧元素;Z的最外层电子数与次外层相等,则Z为铍元素;Y、Z为金属元素,Y在第二周期,则Y为锂元素;X、Z位于同主族,则X为镁元素或钙元素;若X为镁元素,则由X与R原子序数之和是W的2倍,则=10,推出W为氖元素不符合题意,若X为钙元素,则由X与R原子序数之和是W的2倍,=14,推出W为硅元素,即X为钙元素、Y为锂元素、Z为铍元素、R为氧元素、W为硅元素、T为氟元素。A.位于同周期的元素的原子半径从左向右半径在减小,正确;B.非金属性:F>O>Si,则气态氢化物的稳定性:SiH4Al3+、S2->Cl-,因为S2-、Cl-比Na+、Al3+多一个电子层,所以离子半径的大小顺序:S2->Cl->Na+>Al3+,错误;B项,x的位置若是第2周期Ⅰ
A族,则原子半径大小顺序应该是x>y>z>d,错误;C项,H、N、O三种元素形成的化合物NH4NO3中含有离子键,正确;D项,NaOH、Al(OH)3、H2SO4、HClO4中,H2SO4与HClO4不能发生反应,错误。
10.X、Y、Z、W、R属于短周期主族元素,X的原子半径在短周期主族元素中最大,Y元素原子的最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为(m+n),M层电子数为(m-n),W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2∶1。下列叙述错误的是( )
A.X与Y形成的两种化合物中阴、阳离子的个数比均为1∶2
B.Y的氢化物比R的氢化物稳定,熔、沸点高
C.Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z
D.RY2、WY2通入BaCl2溶液中均有白色沉淀生成
解析:选D X的原子半径在短周期主族元素中最大,应为Na元素;Y元素原子的最外层电子数为m,次外层电子数为n,Z元素原子的L层电子数为(m+n),M层电子数为(m-n),因为L层电子最多为8,则n=2,m=6,所以Y为O元素,Z为Si元素,W元素与Z元素同主族,应为C元素,R元素原子与Y元素原子的核外电子数之比为2∶1,Y的核外电子数为8,则R的核外电子数为16,应为S元素。A项,X与Y形成的两种化合物分别为Na2O、Na2O2,两种化合物中阴、阳离子的个数比均为1∶2,正确;B项,H2O的稳定性强于H2S,沸点高于H2S,正确;C项,非金属性:S>C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,正确;D项,SO2、CO2对应的酸的酸性比盐酸弱,与氯化钡都不反应,错误。
二、非选择题(3个小题,共50分)
11.(15分)现有A、B、C、D、E、F六种原子序数依次增大的短周期主族元素。已知A与D同主族且能形成离子化合物DA,B元素氢化物的水溶液呈碱性,C与E同主族且EC2是一种具有刺激性气味的气体。用化学用语回答下列问题:
(1)元素F在周期表中的位置为________________。
(2)C、D、E三种元素原子半径由大到小的顺序为________________。A、C、D三种元素组成的化合物和单质F反应的离子方程式为_________________________________。
(3)B与F形成的化合物分子中,各原子最外层均达8电子结构,则该分子的电子式为____________。
(4)已知0.50 mol EC2被C2氧化成气态EC3,放出49.15 kJ热量,其热化学方程式为________________________________________________________________________。
(5)A、B、C以原子个数比4∶2∶3所形成的化合物,所含的化学键类型为___________;0.1 mol·L-1的该化合物水溶液中的离子浓度由大到小的顺序为______________。
解析:
A、B、C、D、E、F是六种原子序数依次增大的短周期主族元素,A与D同主族且能形成离子化合物DA,则A、D是第一主族元素,A是氢元素,D是钠元素,B元素氢化物的水溶液呈碱性,B是氮元素,C与E同主族且EC2是一种具有刺激性气味的气体,C是氧元素,E是硫元素,则F是氯元素。(1)Cl元素在周期表中的位置是第三周期ⅦA族。(2)C(O)、D(Na)、E(S)三种元素原子半径由大到小的顺序为r(Na)>r(S)>r(O);A、C、D三种元素组成的化合物是NaOH,和Cl2反应的离子方程式为Cl2+2OH-===Cl-+ClO-+H2O。(3)B与F形成的化合物分子中,各原子最外层均达8电子结构,应为NCl3,该分子的电子式为。(4)0.50 mol SO2被O2氧化成气态SO3,放出49.15 kJ热量,其热化学方程式为2SO2(g)+O2(g)===2SO3(g) ΔH=-196.6 kJ·mol-1。(5)A、B、C以原子个数比4∶2∶3所形成的化合物为NH4NO3,所含的化学键类型为离子键、共价键;NH4NO3是强酸弱碱盐,水解显酸性,则0.1 mol·L-1 NH4NO3水溶液中的离子浓度由大到小的顺序为c(NO)>c(NH)>c(H+)>c(OH-)。
答案:(1)第三周期ⅦA族
(2)r(Na)>r(S)>r(O) Cl2+2OH-===Cl-+ClO-+H2O
(3)
(4)2SO2(g)+O2(g)===2SO3(g)ΔH=-196.6 kJ·mol-1
(5)离子键、共价键 c(NO)>c(NH)>c(H+)>c(OH-)
12.(18分)(2018·日照模拟)TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:
资料:TiCl4及所含杂质氯化物的性质
化合物
SiCl4
TiCl4
AlCl3
FeCl3
MgCl2
沸点/℃
58
136
181(升华)
316
1412
熔点/℃
-69
-25
193
304
714
在TiCl4中的溶解性
互溶
—
微溶
难溶
(1)Ti是一种活泼金属,原子核内有22个质子,它在周期表中的位置是__________________。
(2)根据上表信息推测TiCl4中含有的化学键类型是________。
(3)MgCl2的电子式为____________。
(4)氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有____________。
(5)精制过程:粗TiCl4经两步蒸馏得纯TiCl4如图
①物质a是__________________(填化学式)。
②T1应控制在______________________。
解析:(1)Ti在周期表中的位置是第4周期ⅣB族。(2)根据表中信息可知,TiCl4的沸点较低,则TiCl4中应含有共价键。(3)MgCl2的电子式为。(4)若将氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含熔点相对较高且在TiCl4中溶解度较低的MgCl2、AlCl3、FeCl3。(5)由图示可知,蒸馏塔一塔顶是沸点相对较低的SiCl4,塔釜为沸点相对较高的TiCl4,所以蒸馏塔一温度T1应控制在二者沸点之间,即58 ℃~136 ℃之间。
答案:(1)第4周期ⅣB族 (2)共价键
(3)
(4)MgCl2、AlCl3、FeCl3 (5)①SiCl4 ②58 ℃~136 ℃
13.(17分)已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D,C和F为同一主族元素,A与B、A与G形成共价化合物,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中离子半径最小的元素,F形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是__________________。
(2)由A、C、D三种元素形成的化合物的电子式为_______。画出G离子的结构示意图______________。
(3)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为________________________________________________________________________。
(4)将两份足量的E单质分别加入到等体积等浓度的硫酸和NaOH溶液中,充分反应生成的气体的体积比为________________________________________________________。
(5)由 A、B、C所形成的常见离子化合物是____________ (写化学式),该化合物与D的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为________________________________________________________________________。
(6)已知一包白色晶体为某种正盐,经元素分析仪分析,包含以上七种元素中的若干种,为测定其组成,进行如下实验:
①称取固体2.37
g溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到的白色沉淀经过滤、洗涤、干燥后,称得质量为4.66 g。
②再取等质量的该固体溶于水,逐滴滴加1 mol·L-1的氢氧化钠溶液,得到的沉淀和滴加的氢氧化钠溶液体积的关系如图,则该正盐的化学式为_______________;该物质可以用作净水剂,其原理为____________________________(用离子方程式表示)。
解析:A、B、C、D、E、F、G是原子序数依次递增的短周期元素,B原子的最外层电子数比次外层多3,B原子只能有2个电子层,最外层电子数为5,为N元素;F形成的化合物是造成酸雨的主要原因,F为S元素;C和F为同一主族元素,C为O元素; A、 D同主族,D的原子序数大于氧,则D为Na元素;E、G处于第三周期,E是同周期中离子半径最小的元素,E为Al元素,G元素的最高正化合价与最低负化合价的代数和为6,最外层电子数为7,G为Cl元素;A与 B、A与G形成共价化合物,A为H元素。(1)七种元素中,非金属性最强的元素为O,处于周期表中第二周期ⅥA族。(2)由A、 C、 D形成的化合物为NaOH,其电子式为,G离子为Cl-,离子结构示意图为。(3)G元素的单质为氯气,其与NaOH溶液反应的离子方程式为Cl2+2OH—===Cl—+ClO—+H2O 。(4)等体积等浓度的硫酸和NaOH溶液,H2SO4、NaOH的物质的量相等,金属Al足量,H2SO4、NaOH完全反应,设H2SO4、NaOH均为3 mol,由2Al+3H2SO4===Al2(SO4)3+3H2↑、2Al+2NaOH+2H2O===NaAlO2+3H2↑,可知生成氢气体积之比为3 mol∶=2∶3。(5)由H、N、O所形成的常见离子化合物是NH4NO3,该化合物与NaOH的浓溶液加热时反应的离子方程式为NH+OH-NH3↑+H2O 。(6)①称取固体 2.37 g 溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到白色沉淀,则说明含有SO,白色沉淀为BaSO4,其物质的量为=0.02 mol,则溶液中n(SO)=n(BaSO4)=0.02 mol;
②再取等质量的该固体溶于水,逐滴滴加1 mol·L-1的NaOH溶液,开始生成沉淀,最终沉淀完全溶解,说明含有Al3+,30 mL~40 mL时Al(OH)3质量不变,则溶液中还含有NH,由Al3++3OH-===Al(OH)3↓可知,溶液中n(Al3+)=0.03 L×1 mol·L-1×=0.01 mol,由NH+OH-===NH3·H2O可知,溶液中n(NH)=0.01 L×1 mol·L-1=0.01 mol,符合2n(SO)=3n(Al3+)+n(NH)。由于m(SO)+m(Al3+)+m(NH)=0.02 mol×96 g·mol-1+0.01 mol×27 g·mol-1+0.01 mol×18 g·mol-1=2.37 g,等于样品的质量,故该晶体不含结晶水,应为NH4Al(SO4)2。Al3+水解生成Al(OH)3胶体,所以NH4Al(SO4)2可用作净水剂。
答案:(1)第二周期ⅥA族
(2)
(3)Cl2+2OH—===Cl—+ClO—+H2O (4)2∶3
(5)NH4NO3 NH+OH-NH3↑+H2O
(6)NH4Al(SO4)2 Al3++3H2OAl(OH)3(胶体)+H+