- 2021-05-13 发布 |
- 37.5 KB |
- 9页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
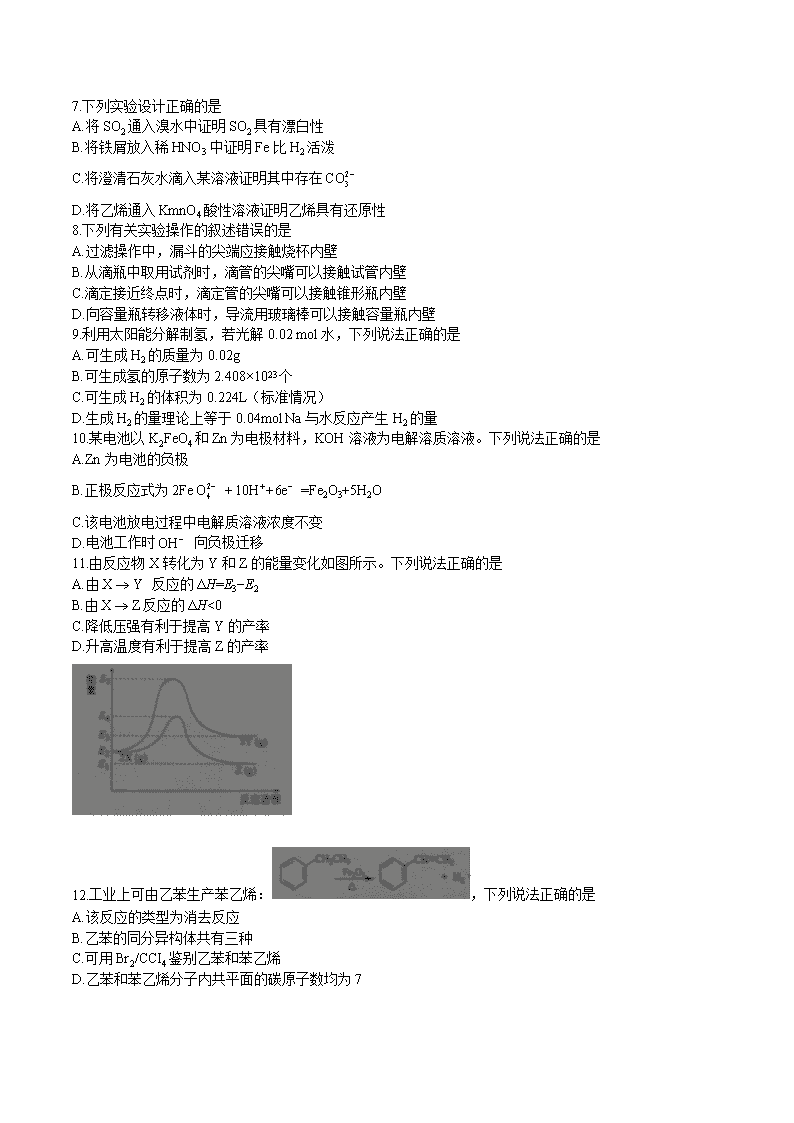
海南省高考化学试题及答案
2016年普通高等学校招生全国统一考试(海南卷) 化学 可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 35.5 Fe 56 Cu 64 Zn 65 第Ⅰ卷 一、选择题:本题共6小题,每小题2分,共12分。在每小题给出的四个选项中,只有一项是符合题目要求的。 1.下列物质中,其主要成分不属于烃的是 A.汽油 B.甘油 C.煤油 D.柴油 2.下列物质不可用作食品添加剂的是 A.谷氨酸单钠 B.柠檬酸 C.山梨酸钾 D.三聚氰胺 3.下列反应可用离子方程式“H++OH−=H2O” 表示的是 A. NaHSO4溶液与Ba(OH)2溶液混合 B.NH4Cl溶液与Ca(OH) 2溶液混合 C. HNO3溶液与KOH溶液混合 D. Na2HPO4溶液与NaOH溶液混合 4.下列叙述错误的是 A.氦气可用于填充飞艇 B.氯化铁可用于硬水的软化 C.石英砂可用于生产单晶硅 D.聚四乙烯可用于厨具表面涂层 5.向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是 A.c() B. c() C. c(H+) D.Ksp(Mg) 6.油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应: C37H104O6(s)+80O2(g)=57CO2(g)+52H2O(l) 已知燃烧1kg该化合物释放出热量3.8104kJ,油酸甘油酯的燃烧热 为 A. B. C. D. 二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,选两个且都正确得4分,但只要选错一个就得0分。 7.下列实验设计正确的是 A.将SO2通入溴水中证明SO2具有漂白性 B.将铁屑放入稀HNO3中证明Fe比H2活泼 C.将澄清石灰水滴入某溶液证明其中存在 D.将乙烯通入KmnO4酸性溶液证明乙烯具有还原性 8.下列有关实验操作的叙述错误的是 A.过滤操作中,漏斗的尖端应接触烧杯内壁 B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 D.向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁 9.利用太阳能分解制氢,若光解0.02 mol水,下列说法正确的是 A.可生成H2的质量为0.02g B.可生成氢的原子数为2.408×1023个 C.可生成H2的体积为0.224L(标准情况) D.生成H2的量理论上等于0.04mol Na与水反应产生H2的量 10.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液。下列说法正确的是 A.Zn为电池的负极 B.正极反应式为2Fe + =Fe2O3+5H2O C.该电池放电过程中电解质溶液浓度不变 D.电池工作时 向负极迁移 11.由反应物X转化为Y和Z的能量变化如图所示。下列说法正确的是 A.由 反应的ΔH=E3−E2 B.由反应的ΔH<0 C.降低压强有利于提高Y的产率 D.升高温度有利于提高Z的产率 12.工业上可由乙苯生产苯乙烯:,下列说法正确的是 A.该反应的类型为消去反应 B.乙苯的同分异构体共有三种 C.可用Br2/CCI4鉴别乙苯和苯乙烯 D.乙苯和苯乙烯分子内共平面的碳原子数均为7 第Ⅱ卷 本卷包括必考题和选考题两部分。第13~17题为必考题,每个试题考生都必须作答,第18~20题为选考题,考生根据要求作答。 13.(8分) 短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+电子层结构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体,回答下列问题: (1)M元素位于周期表中的第______周期、_______族。 (2)Z元素是____,其在自然界中常见的二元化合物是____。 (3)X与M的单质在高温下反应的化学方程式为______,产物分子为直线形,其化学键属__________共价键(填“极性”或“非极性”)。 (4)四种元素中的____可用于航空航天合金材料的制备,其单质与稀盐酸反应的化学方程式为_________。 14.(8分) KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题: (1)为尽量少引入杂质,试剂①应选用___(填标号)。 a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液 (2)易拉罐溶解过程中主要反应的化学方程式为________。 (3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。 (4)已知:Kw=1.0×10-14,Al(OH)3 AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。 15.(8分) 乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成。回答下列问题: (1)B和A为同系物,B的结构简式为_______。 (2)反应①的化学方程式为___________,其反应类型为__________。 (3)反应③的反应类型为____________。 (4)C的结构简式为___________。 (5)反应②的化学方程式为______。 16.(9分) 顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化: 该反应的速率方程可表示为:v(正)=k(正)c(顺)和v(逆)=k(逆)c(反),k(正)和k(逆)在一定温度时为常数,分别称作正,逆反应速率常数。回答下列问题: (1) 已知:t1温度下,,,该温度下反应的平衡常数值K1=_____;该反应的活化能Ea(正)小于Ea(逆),则________0(填“小于”“等于”或“大于”)。 (2) t2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_______(填曲线编号),平衡常数值K2=_____;温度t1___t2(填“小于”“等于”或“大于”),判断理由是______。 17.(11分) 某废催化剂含58.2%的SiO2、21.0%的ZnO、4.5%的ZnS和12.8%的CuS。某同学用15.0 g该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下: 回答下列问题: (1)在下列装置中,第一次浸出必须用____________,第二次浸出应选用____________。(填标号) (2),第二次浸出时,向盛有滤液1的反应器中加入稀硫酸,后滴入过氧化氢溶液。若顺序相反,会造成___________。滤渣2的主要成分是____________________。 (3)浓缩硫酸锌、硫酸铜溶液使用的器皿名称是________________。 (4)某同学在实验完成之后,得到1.5gCuSO4﹒5H2O,则铜的回收率为__________________。 请考生从第18~20题中任选一题作答。如果多做,则按所做的第一题计分。第18~20题的第Ⅰ题为选择题,在给出的四个选项中,有两个选项是符合题目要求的,请将符合题目要求的选项标号填在答题卡相应位置;第Ⅱ 题为非选择题,请在答题卡相应位置作答并写明小题号。 18.[选修5——有机化学基础] 18-Ⅰ(6分) 下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为2︓1的有 A. 乙酸甲酯 B.对苯二酚 C. 2-甲基丙烷 D.对苯二甲酸 18-Ⅱ 富马酸(反式丁烯二酸)与Fe2+形成的配合物——富马酸铁又称“富血铁”,可用于治疗缺铁性贫血。以下是合成富马酸铁的一种工艺路线: 回答下列问题: (1)A的化学名称为_____由A生成B的反应类型为_____。 (2)C的结构简式为_____。 (3)富马酸的结构简式为_____。 (4)检验富血铁中是否含有Fe3+的实验操作步骤是_____。 (5)富马酸为二元羧酸,1mol富马酸与足量饱和NaHCO3溶液反应可放出____L CO2(标况);富马酸的同分异构体中,同为二元羧酸的还有____________(写出结构简式)。 19.[选修3——物质结构与性质] 19–Ⅰ(6分) 下列叙述正确的有 A.第四周期元素中,锰原子价电子层中未成对电子数最多 B.第二周期主族元素的原子半径随核电荷数增大依次减小 C.卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小 D. 价层电子对相斥理论中,Π键电子队数不计入中心原子的价层电子对数 19–Ⅱ(14分) M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题: (1)单质M的晶体类型为______,晶体中原子间通过_____作用形成面心立方密堆积,其中M原子的配位数为______。 (2)元素Y基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。 (3)M与Y形成的一种化合物的立方晶胞如图所示。 ①该化合物的化学式为_______,已知晶胞参数a=0.542 nm,此晶体的密度为_______g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA) ②该化合物难溶于水但易溶于氨水,其原因是________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______。 20.[选修2——化学与技术] 20-I(6分) 下列单元操作中采用了热交换设计的有 A.电解食盐水制烧碱 B.合成氨中的催化合成 C.硫酸生产中的催化氧化 D.氨碱法中的氨盐水碳酸化 20-II 海水晒盐的卤水中还有氧化镁,以卤水为原料生产镁的一中工艺流程如下图所示。 回答下列问题: (1)脱硫槽、搅拌槽均用于脱除卤水中的 (填离子符号),M的主要成分是 (填化学式)。 (2)除溴塔中主要的离子方程式为 。 (3)沸腾炉①和②的主要作用是 。沸腾炉③通入热氯化氢的主要目的是 。 (4)电解槽中阴极的电极反应方程式为 。 (5)电解槽中阳极产物为 ,该产物可直接用于本工艺流程中的 。 2016年普通高等学校招生全国统一考试 化学试题答案及评分参考答案 评分说明: 第Ⅱ卷中,考生如给出其他符合题目要求的答案,同样给分。 第Ⅰ卷 1.B 2.D 3.C 4.B 5.A 6.D 7.D 8.B 9.D 10.AD 11.BC 12.AC 第Ⅱ卷 13.(8分) (1)三 ⅥA (每空1分,共2分) (2)Si SiO2 (每空1分,共2分) (3)C+2SCS2 极性 (每空1分,共2分) (4)Mg Mg+2HCl==MgCl2+H2↑ (每空1分,共2分) 14.(8分) (1)d (2分) (2)2Al+2NaOH+2H2O==2NaAlO2+3H2↑ (2分) (3)Al(OH)3 Al3+水解,使溶液中H+浓度增大 (每空1分,共2分) (4)20 (2分) 15.(8分) (1)CH2CHCH3 (1分) (2) 加成反应 (2分,1分,共3分) (3)取代反应 (1分) (4)HOOC—COOH (1分) (5) (2分) 16.(9分) (1)3 小于 (每空2分,共4分) (2)B (1分,2分,共3分) 大于 放热反应升高温度时平衡向逆反应方向移动 (每空1分,共2分) 17.(11分) (1)D A (每空1分,共2分) (2)H2O2与固体颗粒接触分解 (每空2分,共4分) (3)蒸发皿 (2分) (4)30% (3分) 18.(20分) 18-Ⅰ BD (6分) 18-Ⅱ(14分) (1)环己烷 取代反应 (每空2分,共4分) (2) (2分) (3) (2分) (4)取少量富血铁,加入稀硫酸溶解,再滴加KSCN溶液,若溶液显血红色,则产品中含有Fe3+;反之,则无。 (2分) (5)44.8 (每空2分,共4分) 19.(20分) 19-Ⅰ BD (6分) 19-Ⅱ (14分) (1)金属晶体 金属键 12 (每空1分,共3分) (2)1s22s22p63s23p5 Ar HClO4 正四面体 (每空1分,共4分) (3)①CuCl (每空2分,共4分) ②Cu+可与氨形成易溶于水的配位化合物(或配离子) [Cu(NH3)4]2+ (2分,1分,共3分) 20.(20分) 20-Ⅰ BC (6分) 20-Ⅱ (14分) (1)SO42- BaSO4 (每空1分,共2分) (2)Cl2+2Br-==2Cl-+Br2 (2分) (3)脱除氯化镁晶体中的部分水 防止氯化镁晶体进一步脱水过程中发生水解 (每空2分,共4分) (4)Mg2++2e-==Mg (2分) (5)氯气 除溴塔(除溴工段) (每空2分,共4分)查看更多