- 2021-05-10 发布 |
- 37.5 KB |
- 6页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
中考化学 第三篇 第6-7单元测试题 新人教版1
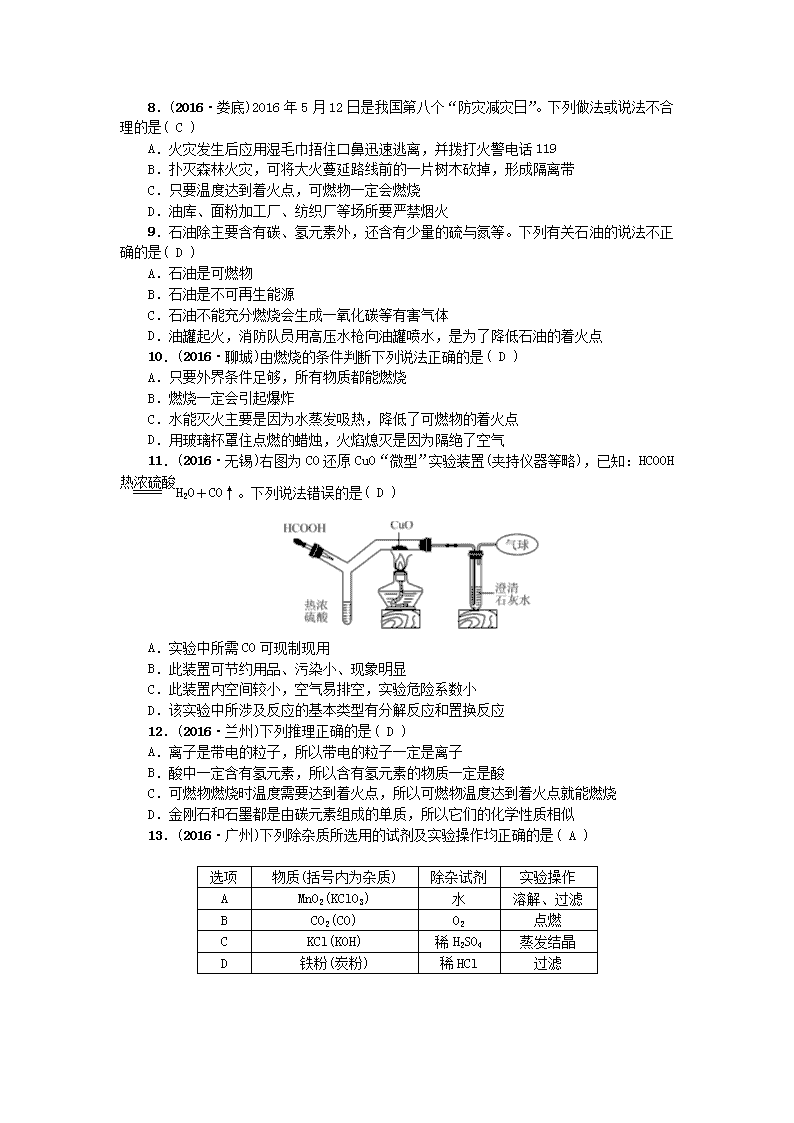
第六、七单元测试题 (满分:100分 时间:45分钟) 相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40 Cu—64 一、选择题(每小题3分,共45分) 1.(2016·盐城)以下燃料中对环境最友好的是( C ) A.煤 B.石油 C.氢气 D.天然气 2.做铁丝在氧气中燃烧的实验时,要先点燃铁丝上系着的火柴,再伸入集满氧气的集气瓶中。火柴燃烧所起的作用是( B ) A.升高铁丝的着火点 B.升高铁丝的温度 C.增加可燃物 D.增大与氧气的接触面积 3.通过实验探究可获得较多的化学知识,对右图所示的实验分析错误的是( D ) A.两支蜡烛自下而上依次熄灭 B.二氧化碳不能燃烧 C.二氧化碳的密度比空气大 D.二氧化碳支持燃烧 4.(2015·自贡)“碳海绵”是已知最轻的固体材料,由碳元素组成,具有疏松多孔的结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是( D ) A.具有吸附性 B.可重复使用 C.可处理海上石油泄漏 D.以上答案都对 5.化学反应在生成新物质的同时,还伴随着能量的变化,下列反应发生时吸收热量的是( D ) A.C+O2CO2 B.Mg+2HCl===MgCl2+H2↑ C.CaO+H2O===Ca(OH)2 D.CO2+C2CO 6.(2016·盐城)右图是探究燃烧条件的实验装置,有关该探究的说法不正确的是( A ) A.只有左侧试管中的红磷能燃烧 B.只有右侧试管中的白磷能燃烧 C.磷燃烧的反应属于氧化反应 D.烧碱溶液的作用是吸收燃烧产物,减轻污染 7.(2016·郴州)下列有关燃烧、灭火的分析正确的是( B ) A.火上浇油:增大可燃物与氧气的接触面积 B.钻木取火:提高可燃物的温度达到着火点 C.吹灭烛火:降低着火点 D.电器着火:用水浇灭 8.(2016·娄底)2016年5月12日是我国第八个“防灾减灾日”。下列做法或说法不合理的是( C ) A.火灾发生后应用湿毛巾捂住口鼻迅速逃离,并拨打火警电话119 B.扑灭森林火灾,可将大火蔓延路线前的一片树木砍掉,形成隔离带 C.只要温度达到着火点,可燃物一定会燃烧 D.油库、面粉加工厂、纺织厂等场所要严禁烟火 9.石油除主要含有碳、氢元素外,还含有少量的硫与氮等。下列有关石油的说法不正确的是( D ) A.石油是可燃物 B.石油是不可再生能源 C.石油不能充分燃烧会生成一氧化碳等有害气体 D.油罐起火,消防队员用高压水枪向油罐喷水,是为了降低石油的着火点 10.(2016·聊城)由燃烧的条件判断下列说法正确的是( D ) A.只要外界条件足够,所有物质都能燃烧 B.燃烧一定会引起爆炸 C.水能灭火主要是因为水蒸发吸热,降低了可燃物的着火点 D.用玻璃杯罩住点燃的蜡烛,火焰熄灭是因为隔绝了空气 11.(2016·无锡)右图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOHH2O+CO↑。下列说法错误的是( D ) A.实验中所需CO可现制现用 B.此装置可节约用品、污染小、现象明显 C.此装置内空间较小,空气易排空,实验危险系数小 D.该实验中所涉及反应的基本类型有分解反应和置换反应 12.(2016·兰州)下列推理正确的是( D ) A.离子是带电的粒子,所以带电的粒子一定是离子 B.酸中一定含有氢元素,所以含有氢元素的物质一定是酸 C.可燃物燃烧时温度需要达到着火点,所以可燃物温度达到着火点就能燃烧 D.金刚石和石墨都是由碳元素组成的单质,所以它们的化学性质相似 13.(2016·广州)下列除杂质所选用的试剂及实验操作均正确的是( A ) 选项 物质(括号内为杂质) 除杂试剂 实验操作 A MnO2(KClO3) 水 溶解、过滤 B CO2(CO) O2 点燃 C KCl(KOH) 稀H2SO4 蒸发结晶 D 铁粉(炭粉) 稀HCl 过滤 14.(2016·资阳)为检验某混合气体成分做了如下实验:将一定体积的该混合气体通过过量的澄清石灰水,石灰水无明显现象,气体总体积减小;把剩余气体导出后,可在氧气中燃烧,燃烧产物能使白色CuSO4粉末变蓝色。则原混合气体的成分可能是( B ) A.HCl和CO B.HCl和H2 C.CH4和CO2 D.CO2和CO 15.在一定条件下,让置于密闭容器中的下列各组物质充分反应后,再冷却至常温,密闭容器中的气态物质属于纯净物的是( A ) A.质量比为1∶9的H2和O2 B.质量比为3∶6的C和O2 C.质量比为1∶6的CH4和O2 D.质量比为7∶2的CO和O2 解析:2H2+O22H2O,反应后生成水在常温下是液体,密闭容器中气体只有O2,A正确;当<<时,产物既有CO2,又有CO,密闭容器中气体有CO2和CO,B错误;,反应后O2有剩余,生成物CO2是气体,C错误;2CO+O22CO2,7∶4 ),反应后CO有剩余,生成物CO2是气体,D错误。 二、填空题(共29分) 16.(4分)(2015·长春)回答下列与含碳物质有关的问题: (1)在金刚石和石墨中,能用于制作干电池电极的是__石墨__; (2)制糖工业中利用活性炭的__吸附__性脱色制白糖; (3)CO2与H2O反应,生成一种能使石蕊溶液变红的物质,这种物质是__碳酸__; (4)炼铁时高炉内发生如下反应:CO2+C2CO,其中__C__发生氧化反应。 17.(6分)(2015·北京)依据如图进行实验(夹持仪器略去)。实验过程:①通入N2,点燃酒精灯,一段时间后,a、b中均无明显现象;②熄灭酒精灯,立即改通O2,a中无明显现象,b中红磷燃烧。 (1)实验过程②中,红磷燃烧的化学方程式为__4P+5O22P2O5__。 (2)实验过程②中,对比a、b中的实验现象,可知可燃物燃烧的条件之一是__燃烧需要温度达到可燃物的着火点__。 (3)实验过程中,能说明可燃物燃烧需要氧气的实验是__步骤①中b通N2,不燃烧;步骤②中b通O2,燃烧__。 18.(4分)对比、分析、归纳是学习化学的重要方法。 (1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应: H2+CuOCu+H2O 3CO+Fe2O32Fe+3CO2 C+O2CO2 得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后__升高__(填“升高”“降低”或“不变”)。 (2)依据上述结论,则在反应SO2+2H2S===3S↓+2H2O中作为还原剂的物质是__H2S__;该还原剂中所含元素化合价的变化是:由__-2__价变为__0__价。 19.(7分)(2015·资阳)碳及碳的化合物间的转化关系可表示为:,由此可写出各步反应的化学方程式。硫及硫的化合物间的转化关系可表示为: (1)模仿碳及碳的化合物间转化反应方程式的书写,写出硫及硫的化合物转化反应中指定反应的化学方程式:反应①:__S+O2SO2__;反应③:__SO3+H2O===H2SO4__。 (2)反应②中,V2O5在反应前后的质量均为m,则V2O5在该反应中起__催化__作用。 (3)上述反应中,属于化合反应的有:__①②③__(填反应序号)。 (4)实验室因操作不当,将浓硫酸滴在书页上,一会书页出现了黑色,且由糊状至烂洞状。这是因为浓硫酸具有__脱水性__。 20.(8分)(2016·孝感)A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“—”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。请回答下列问题: (1)若A、B为组成元素相同的气体,E为大理石的主要成分,则B的化学式为__CO2__,物质D的类别为__酸__(填“酸”“碱”“盐”或“氧化物”)。 (2)若A是能供给人类呼吸的气体,B是一种最常用的溶剂,D的水溶液显蓝色。 则C—D反应的基本类型是__置换反应__, D—E反应的化学方程式是__CuSO4+Ca(OH)2===Cu(OH)2↓+CaSO4(其他合理答案也可)。 三、实验探究题(共17分) 21.(8分)(2016·淄博)我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来。小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是__增大反应物的接触面积,加快反应速率__。 (1)同学们按右图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时,__不能 __(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。 (2)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例。你建议选择__A__(填写字母),简要说明你的理由__部分炭粉没与CuO反应等__。 A.36∶3 B.40∶3 C.48∶3 解析:用超细炭粉与氧化铜粉末混合进行实验,可以增大反应物的接触面积,加快反应速率;(1)将混合固体加热,炭粉与O2反应所需温度较低,部分炭粉先燃烧生成CO2,使澄清石灰水变浑浊;(2)2CuO+C2Cu+CO2↑,40∶3 ),CuO与C恰好完全反应时,CuO与炭粉的质量比为40∶3,但在实验中,有些炭粉先燃烧,有些炭粉变成CO,实际消耗炭粉的质量比理论值大。 22.(9分)(2016·宜宾)下图是初中化学中常见仪器装置,回答下列问题: (1)D中仪器a的名称是__集气瓶__。实验室用氯酸钾和二氧化锰制取氧气,可选用的发生装置为__B__(选填装置编号,下同)。 (2)用大理石和稀盐酸制取并收集二氧化碳,可选用的发生装置是__A__,收集装置为__D__,为防止气体从发生装置泄漏的必要措施是__长颈漏斗的末端管口要插入液面下__。 (3)F装置有多种用途。用于气体干燥、除杂时,气体应从__c__(选填导管口编号)处进入。干燥二氧化碳时,瓶中液体可以是__①__(选填下列试剂编号,下同);除去一氧化碳中的二氧化碳时,瓶中液体可以是__②__。 ①浓硫酸 ②烧碱溶液 ③稀硫酸 ④饱和碳酸氢钠溶液 四、计算题(共9分) 23.(9分)(2016·遂宁)某校学习小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石灰石样品10 g加入烧杯中,再把80 g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应): 实验次数 第1次 第2次 第3次 第4次 加入稀盐酸的质量/g 20 20 20 20 剩余固体的质量/g 7 4 2.6 m 分析表中数据,完成下列问题: (1)表中m的数值为__2.6__。 (2)该石灰石样品中碳酸钙的质量分数为__74%__。 (3)计算第一次实验反应结束后所得溶液中溶质质量分数(计算结果精确到0.1%)。 解:(3)设生成氯化钙的质量为x,生成二氧化碳的质量为y, CaCO3+2HCl===CaCl2+H2O+CO2↑ 100 111 44 3 g x y == x=3.33 g y=1.32 g 所以第一次实验反应结束后所得溶液中溶质质量分数为:×100%≈15.4% 答:第一次实验反应结束后所得溶液中溶质质量分数为15.4%。查看更多