- 2021-11-10 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
浙江省温州市2012年中考科学试题化学部分
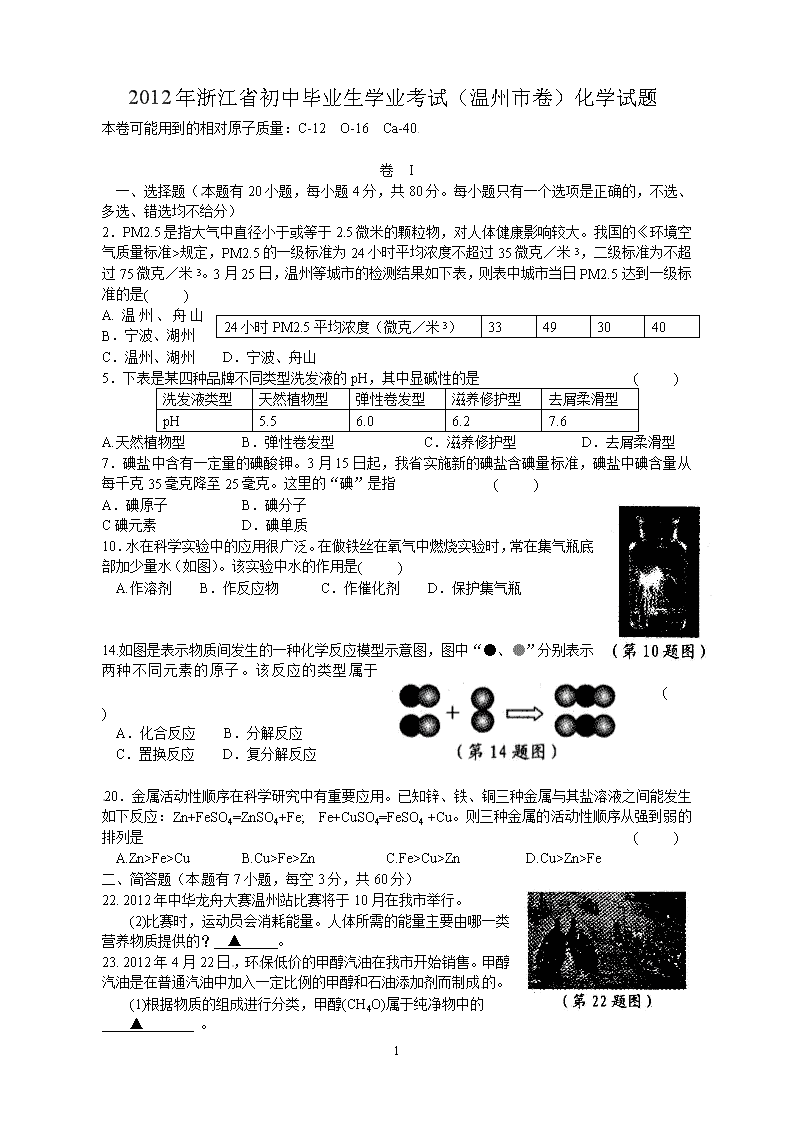
2012年浙江省初中毕业生学业考试(温州市卷)化学试题 本卷可能用到的相对原子质量:C-12 O-16 Ca-40 卷 I 一、选择题(本题有20小题,每小题4分,共80分。每小题只有一个选项是正确的,不选、多选、错选均不给分) 24小时PM2.5平均浓度(微克/米3) 33 49 30 40 2.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响较大。我国的《环境空气质量标准>规定,PM2.5的一级标准为24小时平均浓度不超过35微克/米3,二级标准为不超过75微克/米3。3月25日,温州等城市的检测结果如下表,则表中城市当日PM2.5达到一级标准的是( ) A.温州、舟山 B.宁波、湖州 C.温州、湖州 D.宁波、舟山 5.下表是某四种品牌不同类型洗发液的pH,其中显碱性的是 ( ) 洗发液类型 天然植物型 弹性卷发型 滋养修护型 去屑柔滑型 pH 5.5 6.0 6.2 7.6 A.天然植物型 B.弹性卷发型 C.滋养修护型 D.去屑柔滑型 7.碘盐中含有一定量的碘酸钾。3月15日起,我省实施新的碘盐含碘量标准,碘盐中碘含量从每千克35毫克降至25毫克。这里的“碘”是指 ( ) A.碘原子 B.碘分子 C碘元素 D.碘单质 10.水在科学实验中的应用很广泛。在做铁丝在氧气中燃烧实验时,常在集气瓶底部加少量水(如图)。该实验中水的作用是( ) A.作溶剂 B.作反应物 C.作催化剂 D.保护集气瓶 14.如图是表示物质间发生的一种化学反应模型示意图,图中“●、●”分别表示两种不同元素的原子。该反应的类型属于 ( ) A.化合反应 B.分解反应 C.置换反应 D.复分解反应 20.金属活动性顺序在科学研究中有重要应用。已知锌、铁、铜三种金属与其盐溶液之间能发生如下反应:Zn+FeSO4=ZnSO4+Fe; Fe+CuSO4=FeSO4 +Cu。则三种金属的活动性顺序从强到弱的排列是 ( ) A.Zn>Fe>Cu B.Cu>Fe>Zn C.Fe>Cu>Zn D.Cu>Zn>Fe 二、简答题(本题有7小题,每空3分,共60分) 22. 2012年中华龙舟大赛温州站比赛将于10月在我市举行。 (2)比赛时,运动员会消耗能量。人体所需的能量主要由哪一类营养物质提供的? ▲ 。 23. 2012年4月22日,环保低价的甲醇汽油在我市开始销售。甲醇汽油是在普通汽油中加入一定比例的甲醇和石油添加剂而制成的。 (1)根据物质的组成进行分类,甲醇(CH4O)属于纯净物中的 ▲ 。 5 (2)工业制取甲醇的方法之一:利用二氧化碳与氢气在一定条件下反应制取甲醇,同时生成 另一种常见物质。请完成该反应的化学方程式:CO2+3H2CH4O+ ▲ 。 24.铬是人体必需的微量元素之一,最近由于毒胶囊事件,引发人们对铬的关注。 (1)金属铬呈银白色,难溶于水,在空气中不易被氧化、耐腐蚀,在金属防锈上应用广泛。根据上述信息,写出金属铬的一种物理性质: ▲ 。 (2)含铬物质的毒性与铬元素(Cr)的化合价有关。已知CrCl3中氯元素的化合价为-1,则CrCl3中铬元素的化合价为 ▲ 。 (3)如图表示人体生理机能与必需元素含量的关系。若长期摄入铬超标的食品和饮用水,会导致人体生理机能从最佳区向 ▲ 区移动,从而影响健康。 25.近年来,许多地区的冬季出现了极端严寒天气,给当地人们生活带来一定危害。 (3)极寒天气加剧了部分地区煤、石油等能源的消耗,会在一定程度上导致空气中的 ▲ 增加,从而易引发酸雨。 27.为提高学生安全自救和使用灭火器的能力,学校开展消防安全演习。 (2)打开阀门后,灭火器内的物质喷射到可燃物上,这不但可以降低可燃物的温度,而且在可燃物表面形成一层泡沫,起到 ▲ 作用,从而达到灭火目的。 三、实验探究题(本题有5小题,每空2分,共30分) 29.科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验。 (一)选择装置并检查气密性。 (二)称取0.1克的二氧化锰粉末加入容器中。 (三)量取50毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积。 (四)改变二氧化锰的质量,重复上述实验,记录数据如下。 时间/秒 生成氧气的体积/毫升 0.1克MnO2 0.2克MnO2 0.3克MnO2 0.4克MnO2 40 49 61 75 86 80 77 87 90 92 120 89 92 92 92 160 92 92 92 92 (1)本实验探究的问题是 ▲ 。 (2)实验中除了量筒外,还需要用到的测量仪器有 ▲ 。 (3)为完成本实验,应选择下图气体发生和收集装置中的组合是 ▲ 。(选填序号) 5 四、分析计算题(本题有4小题,第33题7分,第34题6分,第35题9分,第36题8分,共30分) 33.海洋与人类密切相关,如何更好地利用和保护海洋成为科学家研究的课题。 (2)在海底热液中溶有一些矿物质,冷却热液,这些矿物质就会不断结晶析出。由此可知,这些矿物质的溶解度随着温度的降低而 ▲ 。 34.“雷贝拉唑钠肠溶片”是治疗胃病的一种药。下面为该药说明书上的部分信息: 【主要成分】雷贝拉唑钠,化学式:C18H20N3O3SNa 【用法用量】成人每日口服1次10毫克,根据病情也可每日口服1次20毫克。 【药物实验】健康成年男子分别在空腹情况下或饭后口服本药20毫克,血浆中药物浓度随 时间的变化情况如图所示。 结合上述信息,回答下列问题: (1) C18H20N3O3SNa中C、H原子的个数比为 ▲ 。 (3)有人根据图中信息,认为空腹服用该药比饭后服用效果更好。他的依据是: ▲ 。 35.为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图。每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前18分钟数据如下表。(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑) 时间/分 0 2 4 6 8 10 12 14 16 18 大理石碎屑生成的CO2质量/克 0 1.45 1.75 1.98 2.18 2.30 2.36 2.40 2.40 2.40 块状大理石生成的CO2质量/克 0 0.45 0.80 1.10 1.36 1.60 1.81 1.98 2.11 2.20 5 (1)实验过程中,通过观察如图装置中的哪一现象可判断反应结束? ▲ 。 (2)结合表格分析,块状大理石与稀盐酸反应最多能生成多少克二氧化碳?简要说明判断 的理由: ▲ 。 (3)当反应进行到18分钟时,块状大理石中有多少克碳酸钙与稀盐酸发生了反应?(写出计算过程) 5 2012年浙江省初中毕业生学业考试(温州市卷) 参考答案和评分细则 一、选择题(本题有20小题,每小题4分,共80分。每小题只有一个选项是正确的,不选、多 选、错选均不给分) 2.A 5. D 7.C 10.D 14.A 20.A 二、简答题(本题有7小题,每空3分,共60分) 22. (2)糖类(或葡萄糖) (4)反射 23.(1)化合物(或有机物) (2) H2O 24.(1)银白色(或难溶于水) (2)+3 (3)毒性(或致死) 25. (3)二氧化硫(或氮氧化物) 27. (2)隔绝助燃剂(氧气或空气) 三、实验探究题(本题有5小题,每空2分,共30分) 29.(1)二氧化锰的质量对过氧化氢分解快慢的影响(其它合理答案也给分) (2)天平、停表(或秒表) (3)②⑤ 四、分析计算题(本题有4小题,第33题7分,第34题6分,第35题9分,第36题8分,共30分) 33. (2)减小 (2分) 34. (1)9:10(2分) (3)空腹服用该药时血浆中药物浓度最大值比饭后服用大;达到最大值所需时间比饭后 服用短(其它合理答案也给分)(2分) 35.(1)容器内不再产生气泡(或电子天平的示数不再变化) (2分) (2)2. 40克;查表可知,大理石碎屑完全反应生成的二氧化碳质量是2.40克,而块状大理石与其质量、成分都相同,所以完全反应生成的二氧化碳质量也是2. 40克(3分) (3)解:18分钟时块状大理石生成CO2的质量为2.2克。 (1分) 设:此时块状大理石中发生反应的CaCO3质量为x。 CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 x 2.2克 l00/x=44/2.2克(2分) 解得x=5克(1分) 答:块状大理石中有5克碳酸钙与稀盐酸发生了反应。 5查看更多