- 2021-11-10 发布 |
- 37.5 KB |
- 12页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019九年级化学全册 第三单元 海水中的化学 到实验室去 粗盐中难溶性杂质的去除同步测试
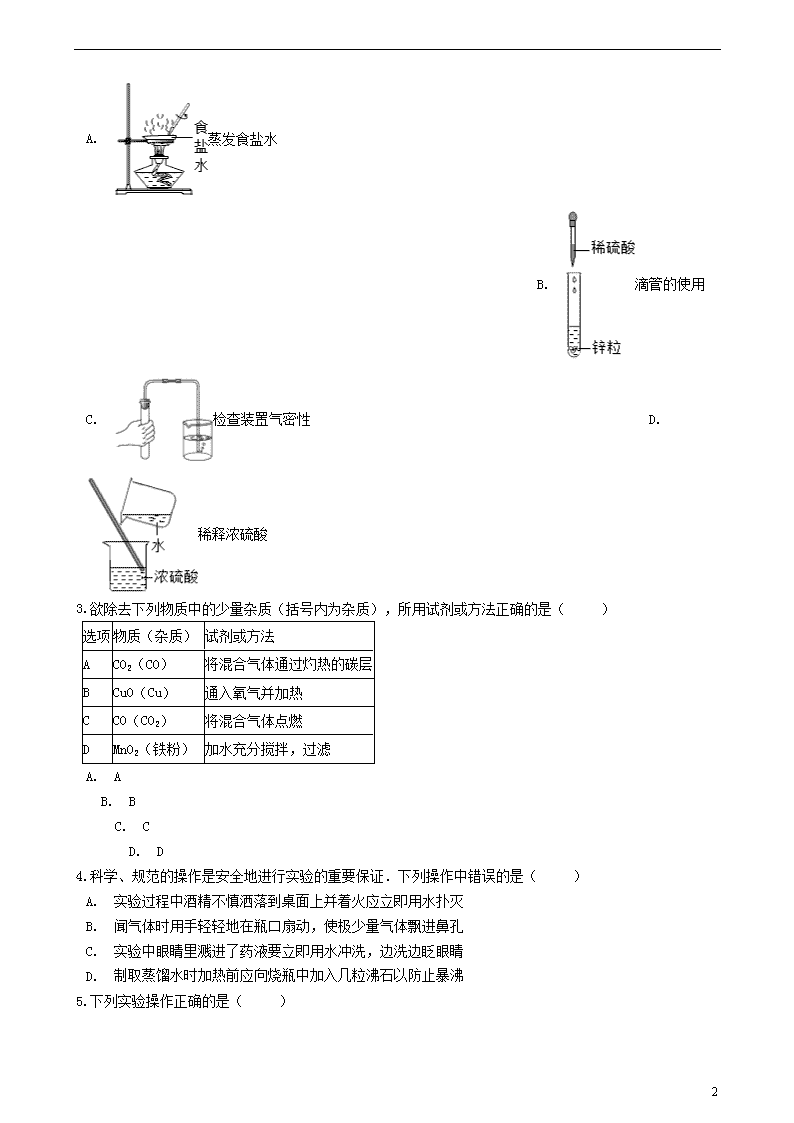
到实验室去:粗盐中难溶性杂质的去除 同步测试 一、单选题 1.下列实验的基本操作正确的是( ) A. 浓硫酸的稀释 B. 称量一定质量的食盐 C. 过滤 D. 检查装置的气密性 2.规范实验操作是获得实验成功的重要保证.下列实验操作错误的是( ) 12 A. 蒸发食盐水 B. 滴管的使用 C. 检查装置气密性 D. 稀释浓硫酸 3.欲除去下列物质中的少量杂质(括号内为杂质),所用试剂或方法正确的是( ) 选项 物质(杂质) 试剂或方法 A CO2(CO) 将混合气体通过灼热的碳层 B CuO(Cu) 通入氧气并加热 C CO(CO2) 将混合气体点燃 D MnO2(铁粉) 加水充分搅拌,过滤 A. A B. B C. C D. D 4.科学、规范的操作是安全地进行实验的重要保证.下列操作中错误的是( ) A. 实验过程中酒精不慎洒落到桌面上并着火应立即用水扑灭 B. 闻气体时用手轻轻地在瓶口扇动,使极少量气体飘进鼻孔 C. 实验中眼睛里溅进了药液要立即用水冲洗,边洗边眨眼睛 D. 制取蒸馏水时加热前应向烧瓶中加入几粒沸石以防止暴沸 12 5.下列实验操作正确的是( ) A. 稀释浓硫酸 B. 蒸发食盐水 C. 套橡胶 D. 测溶液pH 6.除去下列各物质中混有的少量杂质,所选试剂和操作均正确的是( ) 选项 物质 杂质 除杂质方法 A CO2 CO 点燃 B NaCl固体 泥沙 加水溶解、过滤 C H2 HCl 通入过量的NaOH溶液,浓硫酸 D CuO 木炭粉 加入足量稀硫酸 A. A B. B C. C D. D 7.除去下列物质中的少量杂质,所选试剂及操作都正确的是( ) 序号 物质 杂质 试剂 操作 A CO CO2 足量NaOH溶液 洗气 B O2 水蒸气 足量稀硫酸 洗气 C NaOH溶液 Na2CO3 适量CaCl2溶液 过滤 12 D Fe粉 CuO 过量盐酸 过滤 A. A B. B C. C D. D 8.下列除去杂质的方法中,正确的是( ) 选项 物质 杂质 除杂质的方法 A ZnCl2溶液 CuCl2 过量锌粉,过滤 B CaCl2溶液 盐酸 加适量 NaOH C CuO Cu 加水,过滤 D O2 H2 点燃 A. A B. B C. C D. D 9.过滤时不需要用到的仪器是( ) A. B. C. D. 10.有关实验方案设计正确的是( ) 选项 实验目的 实验方案 A 检验某物质中是否含有碳酸根 加稀盐酸,观察是否有气泡冒出 B 除去KCl固体中混有的少量MnO2 加水溶解,过滤,洗涤,干燥 C 鉴别H2、CH4、CO三种气体 分别点燃,观察火焰颜色 12 D 鉴别稀盐酸、NaOH、NaCl三种溶液 分别滴入酚酞溶液,再相互混合,观察溶液颜色变化 A. A B. B C. C D. D 11.下列方法中,不能达到目的是( ) 选项 物质(括号内为杂质) 除去杂质的方法 A NaOH溶液(Na2SO4) 加入适量的Ba(OH)2溶液、过滤 B CaO(CaCO3) 加水溶解、过滤 C CO(CO2) 通过足量氢氧化钠溶液,并干燥 D CuSO4溶液(H2SO4) 加足量氧化铜粉末,过滤 A. A B. B C. C D. D 12.规范的实验操作是实验成功的保证.下列实验操作不正确的是( ) A. 加热液体 B. 滴加液体 12 C. 加热蒸发 D. 测定溶液pH 13.下列除杂设计(括号内为杂质)正确的是( ) 序号 物 质 选用试剂 操 作 A CO2(HCl) NaOH溶液 洗气 B CaO(CaCO3) H2O 加入足量的水,充分溶解,过滤 C KNO3溶液(K2CO3) 稀盐酸 加入适量的盐酸至不再产生气泡为止 D NaCl溶液(CaCl2) ①Na2CO3溶液②稀盐酸 先加入过量试剂①,过滤;再向滤液中加入适量试剂② A. A B. B C. C D. D 二、填空题 14.水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质. (1)写出实验室电解水反应的化学方程式:________ . (2)城镇自来水厂生产流程可用如图表示: 除去水中固态杂质的设备是:________ ;投药(多为ClO2)的作用是________ . (3)自然界的水多含有杂质.含有较多可溶性钙、镁化合物的水通常称为硬水,一种软化硬水的简易办法是:________ . 15.从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl2、NaCl、KCl的混合液)转化为氯化镁晶体.实验室中模拟该转化的过程如下,回答有关问题. (1)制备氢氧化镁:向卤水中加入适量生石灰,充分反应后过滤. 12 ①生石灰的主要成分为(填化学式)________ .该过程中发生了多个反应,其中会大量放热的反应是(填化学方程式)________ . ②过滤操作需用到的玻璃仪器除烧杯外,还有________ . (2)制备氯化镁溶液:用盐酸溶解Mg(OH)2 . 为了便于后续操作,盐酸不宜过量. ①反应的化学方程式是________ . ②通过计算,可准确知道所需盐酸的量.理论上溶解5.8g Mg(OH)2需要36.5% HCl溶液________ g. ③由于准确称量Mg(OH)2的步骤繁琐,实验中并不常用,而是通过一定操作方法来达到控制盐酸用量的目的.操作方法是:将Mg(OH)2加入烧杯中,________ ,直到Mg(OH)2完全溶解为止. (3)制备氯化镁晶体:蒸发浓缩MgCl2溶液,冷却结晶. 16.初中化学教材中的一些实验如图,请回答下列问题: ①甲的实验现象________ ; ②实验乙中可以观察到烧杯底部的硝酸钾晶体溶解了,该实验说明________ ; ③实验丙中玻璃棒的作用是________ . 17.小伟同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末,搅拌溶解,静置一会后,采用如图所示装置进行过滤.请问: (1)加入明矾的作用是________ ,图中还缺少的一种仪器是________ ,其作用是________ ,漏斗下端紧靠烧杯内壁是为了________ ; (2)过滤后观察发现滤液仍然浑浊,可能的原因________ ; (3)经改进后过滤,得到了澄清透明的水,他兴奋的宣布:我终于制得纯水.他的说法是否正确?________ , 理由是________ ,要制得纯水需要采用的净化方法是________ . 18.粗盐中常含有氯化钙,氯化镁,硫酸钠等杂质.粗盐提纯得到氯化钠晶体的流程如下. 12 ①为了使杂质能够完全被除去,对所加入试剂的量的要求是________. ②操作X是________. ③加入试剂N可以除去的杂质是________ ④后续操作是________. 三、实验探究题 19.我国化学家侯德榜发明了联合制碱法,其生产纯碱和副产品氯化铵的工艺流程如图所示: 请回答下列问题: (1)操作a的名称是________; (2)上述工艺流程中可循环利用的物质是________(填名称). (3)铵盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,原因是________. (4)某制碱厂制出的Na2CO3中含有NaCl,取12g该样品放入烧杯中,逐渐滴加溶质质量分数为10%的稀盐酸,烧杯中物质的总质量与所滴入稀盐酸的质量关系曲线如图所示,当恰好完全反应时,烧杯中为不饱和溶液,试通过计算求出此时溶液中所含溶质的质量. 20.如图1为粗盐提纯的操作流程: (1)图1中操作Ⅱ是________,可以除去________;操作Ⅲ是________,可以除去滤液中________;所得精盐的主要成分俗称________. (2)在这过程中玻璃棒总共用到________次,其中操作Ⅱ中使用玻璃棒的作用是________,操作Ⅲ中使用玻璃棒的作用是________. 12 (3)小张同学用托盘天平称得了以下实验数据: ①粗盐的质量:5克; ②蒸发皿的质量:50.4克;③蒸发皿和食盐晶体的质量:53.4克.请你根据以上数据帮助小张计算他所得到的食盐晶体占粗盐的百分含量是________(只要求写最终答案).全班同学实验结束后,老师进行了数据汇总,大家发现小张同学的百分含量偏小.请你帮助他分析可能的原因________.(写出一条即可) (4)实验室现有10mL、50mL、100mL的量筒,现要量取80mL的蒸馏水,应该选择________规格的量筒,量液时,量筒必须放平稳,视线要与量筒内液体________保持水平.图2是10mL量筒的片断,根据图示,此时所取的水的体积是________ mL. (5)①进行过滤操作时,小李同学发现他的过滤后的液体还是有点浑浊,你认为还可能的原因是________;________. ②蒸发结束前,为了防止________,要用玻璃棒不断搅拌或用酒精灯间歇加热.实验中,小红不小心把燃着的酒精灯打翻了,此时最适宜的方法是迅速用________ 熄灭酒精灯,从而隔绝空气达到灭火效果. 四、综合题 21.化学实验是科学探究的重要途径.请回答下列问题: (1)胶头滴管用过后,应________,再去吸取其他药品. (2)如图所示的化学实验基本操作中,正确的是________. 22.(2017•黄石)随着环境问题的日益严重,垃圾的处理问题正日益被人们所重视.某垃圾处理厂对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)处理及综合利用的部分工艺如图所示.请回答下列问题: (1)I、II均为________操作,此操作中玻璃棒的作用是搅拌、________; (2)步骤③所发生的反应属于基本反应类型中的________; (3)请写出步骤②、④所发生反应的化学方程式: ②________;④________. 23.分析如图微观模拟图,你能总结出的一条结论:水是生命之源,人类的日常生活与工农业生产都离不开水,某化学兴趣小组为了探究“水的净化”过程,从江中取了水样,观察到:水样呈黄色,有异味,浑浊,有固体小颗粒.现对水样进行如下处理. 12 (1)向水样中加入明矾溶液,搅拌、静置,一段时间后,进行________(填操作名称),该操作需要用到的玻璃仪器有________(填字母); A.带铁圈的铁架台 B.酒精灯 C.漏斗 D.玻璃棒 E.量筒 F.烧杯 (2)经过以上处理过的水发现还有异味和盐水,则利用如图简易装置继续进行净化处理,其原理是利用了活性炭的________,装置中水样从下端入水口进入的目的是________. (3)硬水会给生产、生活带来许多不便,硬水中主要含有较多的可溶性钙和镁的化合物,可以通过煮沸的方法来降低水的硬度,硬水在煮沸过程中发生的化学反应之一是:“碳酸氢钙 碳酸钙+二氧化碳+水”,根据以上信息推测:碳酸氢钙可能具有的物理性质有________(写出一点即可).长期烧水的水壶内会有水垢,水垢中一定含有的物质是________(写出一种物质的化学式即可); (4)据最新报道,18名韩国人因使用了小小的空气加湿器杀菌剂而患了肺病死亡.电热式加湿器原理是将水在加热体中加热到100℃,产生蒸汽,用电机将蒸汽送出.此过程属于________(选填“物理变化”或“化学变化”). 12 答案解析部分 一、单选题 1.【答案】D 2.【答案】D 3.【答案】B 4.【答案】A 5.【答案】C 6.【答案】C 7.【答案】A 8.【答案】A 9.【答案】D 10.【答案】D 11.【答案】B 12.【答案】D 13.【答案】D 二、填空题 14.【答案】2H2O2H2↑+O2↑;过滤池;杀菌消毒;煮沸 15.【答案】CaO;CaO+H2O═Ca(OH)2;漏斗,玻璃棒;2HCl+Mg(OH)2═MgCl2+2H2O;20;滴加稀盐酸 16.【答案】瓶子变瘪了;硝酸钾的溶解度随着温度的升高而增大;使液体受热均匀,防止局部受热过高造成液体飞溅 17.【答案】吸附小颗粒泥尘,使其沉淀;玻璃棒;引流;防止液体溅出;滤纸破损或液面高于滤纸边缘;不正确;水中仍然含有一些可溶于水的物质;蒸馏 18.【答案】稍过量;过滤;BaCl2和 CaCl2;加入过量稀盐酸,蒸发 三、实验探究题 19.【答案】(1)过滤 (2)二氧化碳 (3)相同条件下碳酸氢钠的溶解度较小 (4)解:设Na2CO3的质量为x,反应后生成NaCl的质量为y, Na2CO3+ 2HCl=H2O+CO2↑+ 2NaCl 1016 73 117 x 73g×10% y = = , x10.6g,y=11.7g, 12 此时溶液中所含溶质的质量为:12g﹣10.6g+11.7g=13.1g, 答:溶液中所含溶质的质量为13.1g. 20.【答案】(1)过滤;不溶于水的固体杂质;蒸发结晶;水分;食盐 (2)4;引流;搅拌,使溶液均匀受热 (3)60%;量取的水偏少,导致粗盐没有完全溶解(答案合理即可) (4)100mL;凹液面最低处;9.5 (5)滤纸破损;液面高于滤纸边缘或仪器不干净;液体暴沸;湿抹布 四、综合题 21.【答案】(1)用清水洗涤后 (2)③⑤ 22.【答案】(1)过滤;引流 (2)复分解反应 (3)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;2Fe(OH)3 Fe2O3+3H2O 23.【答案】(1)过滤;CDF (2)吸附;减缓水的流速,使活性炭充分吸附水中的杂质 (3)可以溶于水;CaCO3 (4)分解反应 12 查看更多