- 2021-11-06 发布 |
- 37.5 KB |
- 9页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
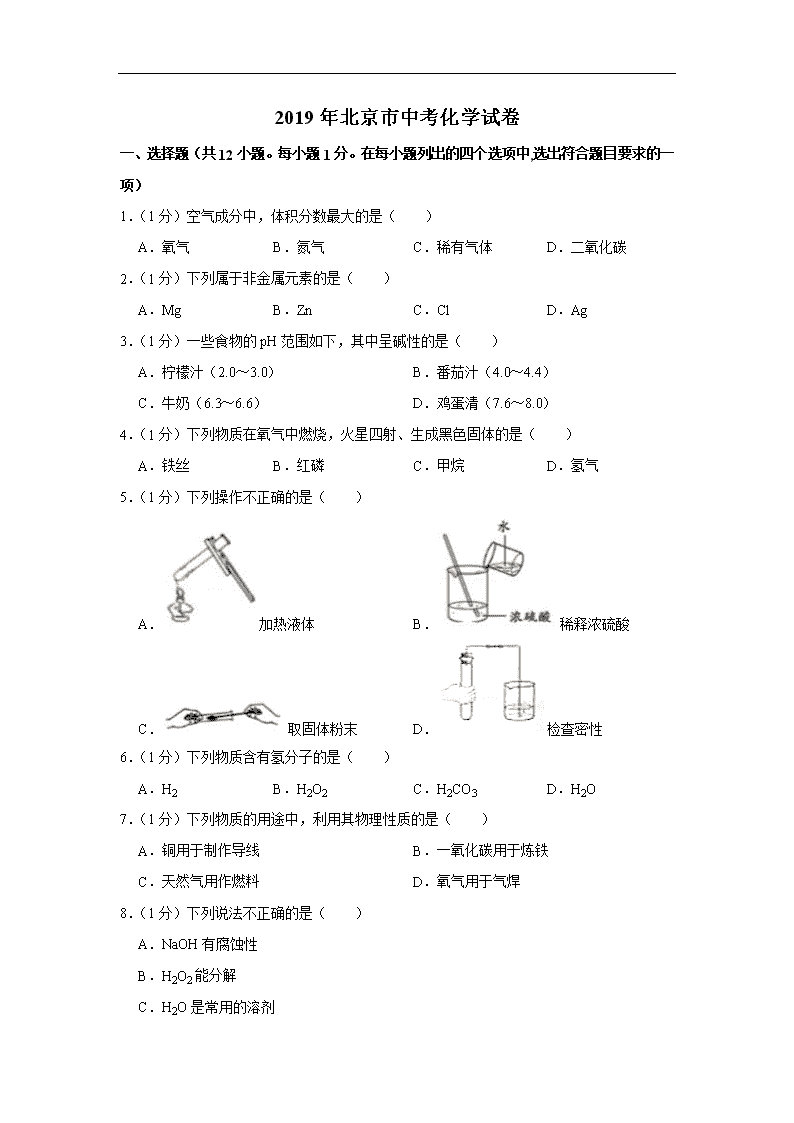
2019年北京市中考化学试卷
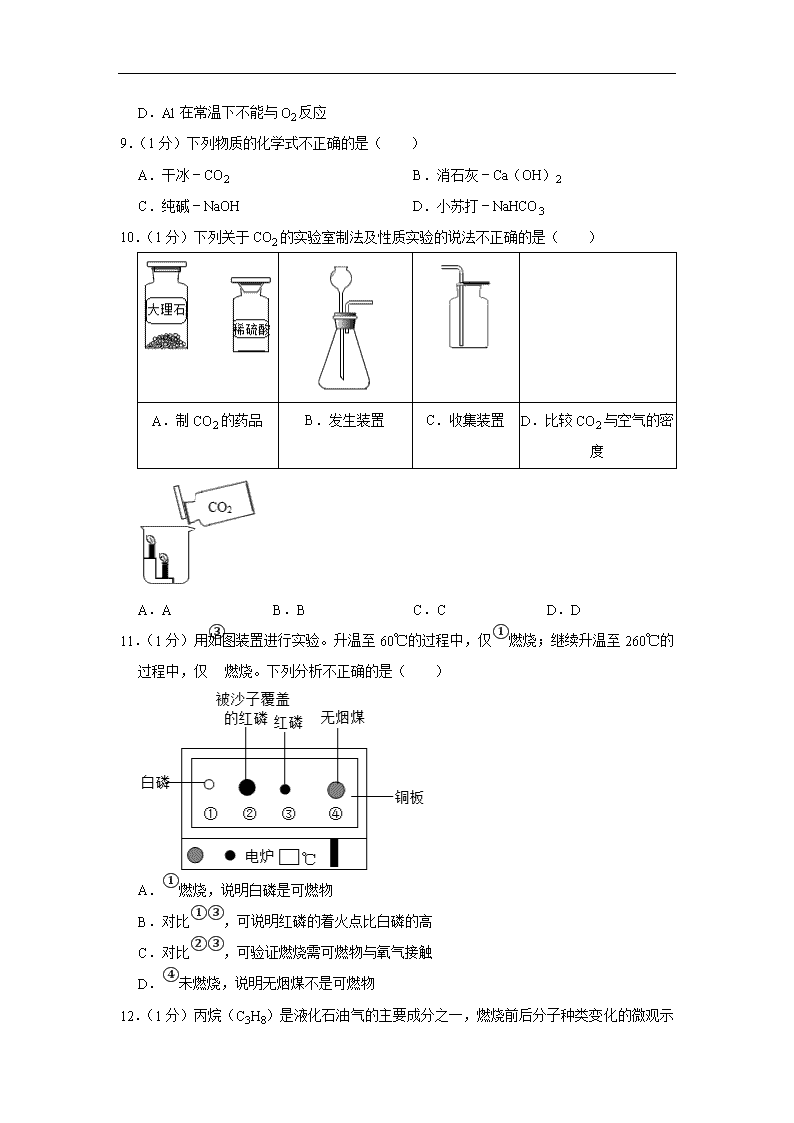
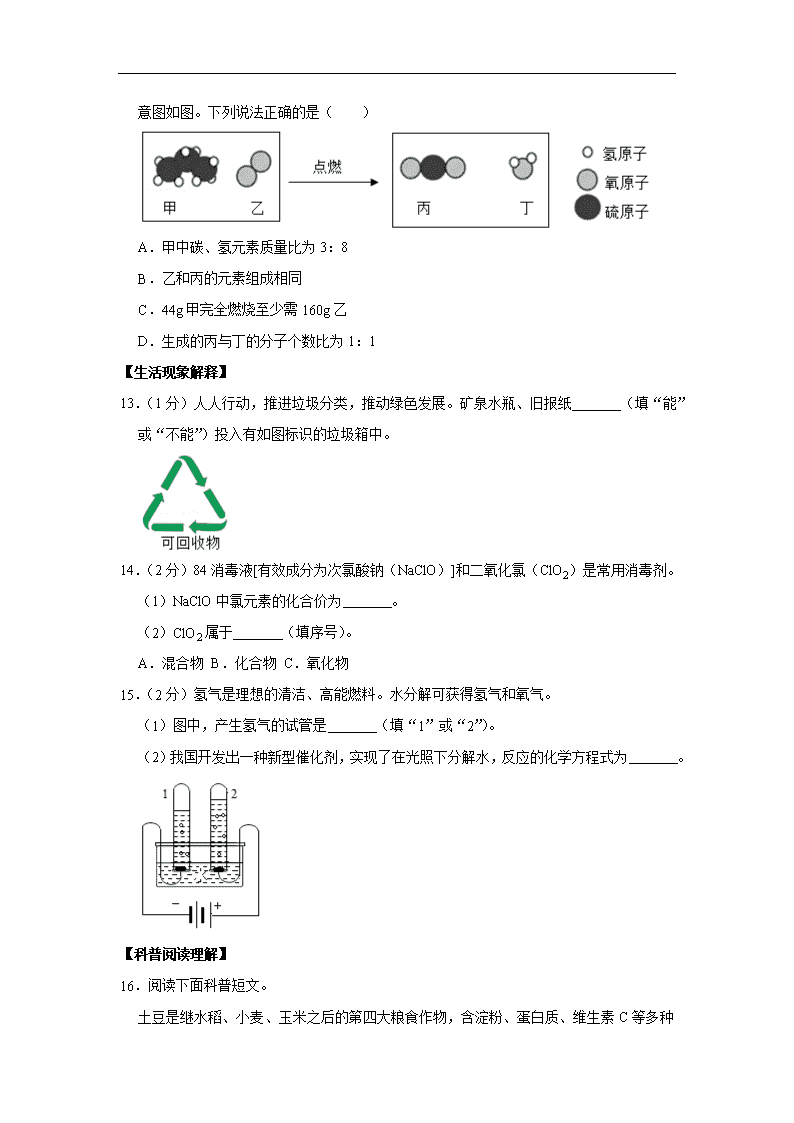
2019年北京市中考化学试卷 一、选择题(共12小题。每小题1分。在每小题列出的四个选项中,选出符合题目要求的一项) 1.(1分)空气成分中,体积分数最大的是( ) A.氧气 B.氮气 C.稀有气体 D.二氧化碳 2.(1分)下列属于非金属元素的是( ) A.Mg B.Zn C.Cl D.Ag 3.(1分)一些食物的pH范围如下,其中呈碱性的是( ) A.柠檬汁(2.0~3.0) B.番茄汁(4.0~4.4) C.牛奶(6.3~6.6) D.鸡蛋清(7.6~8.0) 4.(1分)下列物质在氧气中燃烧,火星四射、生成黑色固体的是( ) A.铁丝 B.红磷 C.甲烷 D.氢气 5.(1分)下列操作不正确的是( ) A.加热液体 B.稀释浓硫酸 C.取固体粉末 D.检查密性 6.(1分)下列物质含有氢分子的是( ) A.H2 B.H2O2 C.H2CO3 D.H2O 7.(1分)下列物质的用途中,利用其物理性质的是( ) A.铜用于制作导线 B.一氧化碳用于炼铁 C.天然气用作燃料 D.氧气用于气焊 8.(1分)下列说法不正确的是( ) A.NaOH有腐蚀性 B.H2O2能分解 C.H2O是常用的溶剂 D.Al在常温下不能与O2反应 9.(1分)下列物质的化学式不正确的是( ) A.干冰﹣CO2 B.消石灰﹣Ca(OH)2 C.纯碱﹣NaOH D.小苏打﹣NaHCO3 10.(1分)下列关于CO2的实验室制法及性质实验的说法不正确的是( ) A.制CO2的药品 B.发生装置 C.收集装置 D.比较CO2与空气的密度 A.A B.B C.C D.D 11.(1分)用如图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( ) A.①燃烧,说明白磷是可燃物 B.对比①③,可说明红磷的着火点比白磷的高 C.对比②③,可验证燃烧需可燃物与氧气接触 D.④未燃烧,说明无烟煤不是可燃物 12.(1分)丙烷(C3H8 )是液化石油气的主要成分之一,燃烧前后分子种类变化的微观示意图如图。下列说法正确的是( ) A.甲中碳、氢元素质量比为3:8 B.乙和丙的元素组成相同 C.44g甲完全燃烧至少需160g乙 D.生成的丙与丁的分子个数比为1:1 【生活现象解释】 13.(1分)人人行动,推进垃圾分类,推动绿色发展。矿泉水瓶、旧报纸 (填“能”或“不能”)投入有如图标识的垃圾箱中。 14.(2分)84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。 (1)NaClO中氯元素的化合价为 。 (2)ClO2属于 (填序号)。 A.混合物 B.化合物 C.氧化物 15.(2分)氢气是理想的清洁、高能燃料。水分解可获得氢气和氧气。 (1)图中,产生氢气的试管是 (填“1”或“2”)。 (2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为 。 【科普阅读理解】 16.阅读下面科普短文。 土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C等多种营养物质,是餐桌上的美味食材。 表1鲜土豆中主要营养物质的含量(每100g) 蛋白质/g 脂肪/g 淀粉/g 钙/mg 磷/mg 维生素C/mg 1.5﹣2.3 0.4﹣0.94 17.5﹣28.0 11﹣60 15﹣68 20﹣40 土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验,测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如图: 土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。 ﹣﹣(原文作者宋国安、杨铭铎等,有删改) 依据文章内容回答下列问题。 (1)表1中的“钙”指的是 (填“元素”或“原子”)。 (2)由图1可知:60min内, (填序号,下同) A.浸泡30min比10min脆性分值高 B.浸泡10min,硬度、咬碎感均无明显变化 C.随着浸泡时间的增加,粘结性、弹性分值均降低 (3)由图2可知:土豆片的淀粉含量与浸泡时间的关系是 。 (4)变绿、发芽的土豆不宜食用,其原因是 。 (5)下列说法正确的是 。 A.土豆是四大粮食作物之一 B.土豆中维生素C含量最高 C.用水泡可防止土豆片褐变 D.土豆开发应用的前景广阔 【生产实际分析】 17.(3分)利用生锈废铁屑和钛白废酸(含硫酸、硫酸亚铁)制备硫酸亚铁的主要转化过程如图: (1)Ⅰ中除铁锈的化学方程式为 。 (2)Ⅱ中反应属于基本反应类型中的 。 18.(4分)利用电石渣[主要成分为Ca(OH)2、MgO]制备硫酸钙的主要工艺流程如图: 已知:MgO难溶于水;MgSO4易溶于水; CaSO4微溶于水。 (1)反应器中搅拌的目的是 。 (2)反应器中发生的反应主要有MgO+H2SO4=MgSO4+H2O和 。 (3)上述流程中,用于分离提纯的设备有 。 【基本实验及其原理分析】 19.(2分)用如图装置进行实验,挤出浓盐酸。 (1)实验现象是 。 (2)该实验说明分子具有的性质是 。 20.(3分)用如图装置进行实验。 (1)高锰酸钾分解的化学方程式为 。 (2)能说明木炭在氧气中燃烧的产物为二氧化碳的现象是 。 21.(3分)用粗木棍在涂有蜡的锌板上写“明”“和”两个字,露出下面的锌板。向“明”字上滴加CuSO4溶液,向“和”字上滴加盐酸。 (1)“明”字上的现象是 。 (2)“和”字上产生气泡,用化学方程式解释: 。 22.(4分)用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。 (1)先推入的溶液是 。 (2)bc段压强不变,原因是 。 (3)cd段压强变大,用化学方程式解释: 。 23.(4分)请从A~D中任选三个作答,若均作答,按前三个计分。如图,在一只烧杯中进行实验。补全实验方案。 序号 目的 步骤 A 探究 ①加入NaOH溶液; ②滴加酚酞溶液;③加入适量盐酸 B 检验NaCl中混有Na2CO3 ①加入少量样品;②加入适量水至全部溶解; ③加入 C 验证KCl不能无限溶解 20℃时,①加入100g水; ②加入18g KCl; ③加入 (已知:20℃时,KCl的溶解度为34g) D 配制 。 ①加入2.5gNaCl; ②加入47.5g水; ③搅拌至全部溶解 【科学探究】 24.(5分)如图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。 【提出问题】改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢? 【进行实验】分别取5g糖粉进行实验,根据前2min的现象对实验效果进行评分, 记录如下:表1实验记录。 实验 糖 浓硫酸体积/mL 水的滴数 温度/℃ 效果得分 1 蔗糖 4 5 22 65 2 蔗糖 5 10 30 81 3 蔗糖 6 15 50 93 4 冰糖 4 10 50 91 5 冰糖 5 15 22 88 6 冰糖 a 5 30 75 7 葡萄糖 4 15 30 0 8 葡萄糖 5 5 50 0 9 葡萄糖 6 10 22 0 【处理数据】分析表1,计算效果得分均值,结果如下: 表2效果得分均值 因素 糖 浓硫酸体积/mL 水的滴数 温度/℃ 蔗糖 冰糖 葡萄糖 4 5 6 5 10 15 22 30 50 均值 79.7 84.7 0 52.0 56.3 56.0 46.7 57.3 60.3 51.0 52.0 61.3 依据均值推断最佳实验方案,均值越高,效果越好。 【解释与结论】 (1)蔗糖变成黑色的炭,发生了 (填“物理”或“化学”)变化。 (2)推测放出的气体含SO2,从元素守恒角度说明理由: 。 (3)实验6中,a为 mL。 (4)根据表2推断,“黑面包”实验最好选择5g冰糖、5mL浓硫酸、 滴水和50℃。 【反思与评价】 (5)表2中,22℃对应的均值为51.0,计算该值所依据的3个数据分别是 。 (6)综合分析,使实验3的效果得分高于实验4的因素有 。 2019年北京市中考化学试卷 参考答案 一、选择题(共12小题。每小题1分。在每小题列出的四个选项中,选出符合题目要求的一项) 1.B; 2.C; 3.D; 4.A; 5.B; 6.A; 7.A; 8.D; 9.C; 10.A; 11.D; 12.C; 【生活现象解释】 13.能; 14.+1;BC; 15.1;2H2O2H2↑+O2↑; 【科普阅读理解】 16.元素;ABC;在其他条件相同时,在研究范围内,土豆片的淀粉含量随着浸泡时间的延长而降低;土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒;ACD; 【生产实际分析】 17.Fe2O3+6HCl=2FeCl3+3H2O;置换反应; 18.使反应物充分接触,加快反应速率;Ca(OH)2+H2SO4=CaSO4+2H2O;过滤器、洗涤槽; 【基本实验及其原理分析】 19.湿润的紫色石蕊试纸变红;分子是在不断的运动的; 20.2KMnO4K2MnO4+MnO2+O2↑;澄清的石灰水变浑浊; 21.“明”字位置上逐渐出现红色固体,溶液由蓝色变为无色;Zn+2HCl═ZnCl2+H2↑; 22.氢氧化钠溶液;氢氧化钠溶液与二氧化碳充分反应,反应停止;Na2CO3+2HCl═2NaCl+H2O+CO2↑; 23.盐酸能否与氢氧化钠发生反应;稀盐酸;超过16g的氯化钾;50g质量分数为5%的氯化钠溶液; 【科学探究】 24.化学;浓硫酸中含有硫、氧元素,蔗糖中也含有氧元素,所以生成物中也会含有硫、氧元素;6;15;65、88、0;浓硫酸的体积和水的滴数; 声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布 日期:2019/7/3 14:19:04;用户:初中校园号;邮箱:wjwl@xyh.com;学号:24424282查看更多