- 2021-08-24 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018-2019学年湖北省宜昌市协作体高一上学期期末考试化学试卷
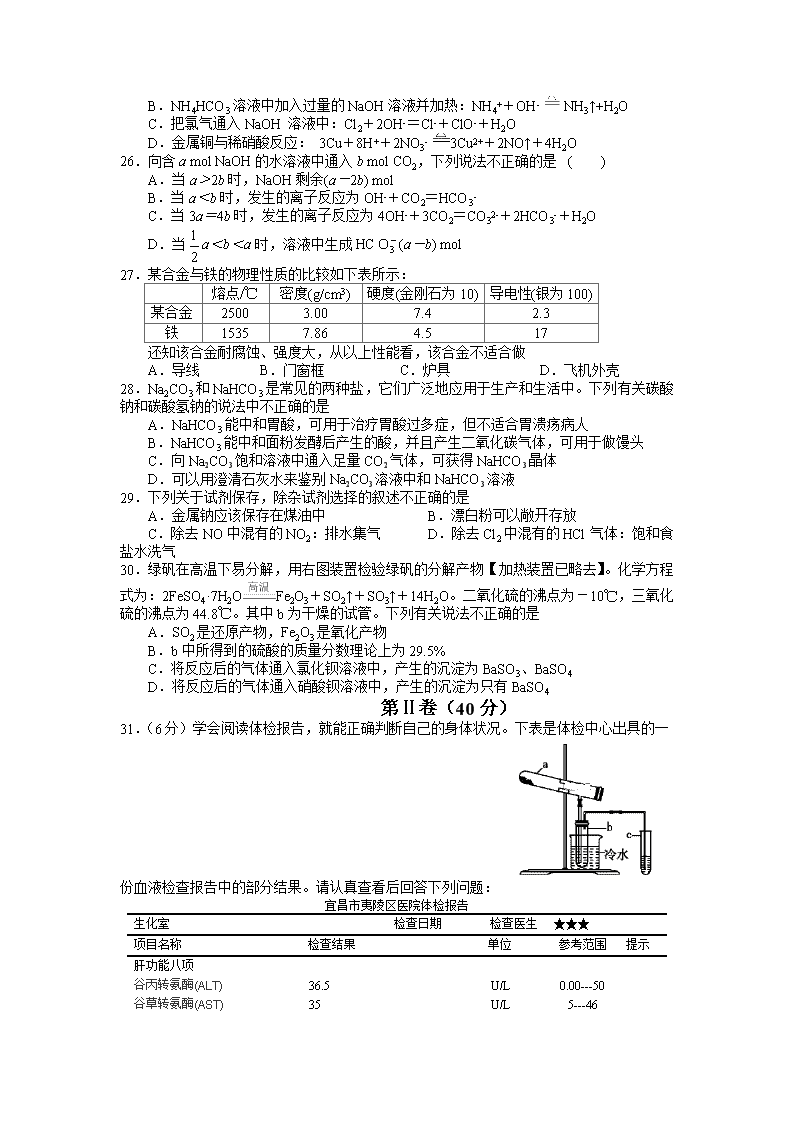
2018-2019学年湖北省宜昌市协作体高一上学期期末考试化学试卷 (全卷满分:100分 考试用时:90分钟) 可能用到的相对原子质量:H-1;C-12;N-14;O-16;Na-23;S-32;Cl-35.5;Fe-56。 第Ⅰ卷(40分) 选择题(本卷包括30个小题,每个小题只有一个选项符合题意,每小题2分,共计60分。) 1.下列物理量不属于国际单位制中的基本物理量的是 A.质量 B.浓度 C.时间 D.物质的量 2.下列物质不属于空气质量日报监测报道的是 A.悬浮颗粒 B.CO2 C.NO2 D.SO2 3.进入冬季后,宜昌经常被雾霾笼罩。其中雾属于下列分散系中的 A.胶体 B.悬浊液 C.溶液 D.乳浊液 4.判断下列有关化学基本概念的依据正确的是 A.溶液与胶体:本质区别是能否发生丁达尔效应 B.纯净物与混合物:是否仅含有一种元素 C.物理变化与化学变化:是否有新物质生成 D.电解质与非电解质:物质本身的导电性 5.下列物质用于漂白脱色,其过程不属于化学变化的是 A.氯水 B.过氧化钠 C.活性炭 D.SO2 6.下列属于电解质的是 A.SO3 B.熔融的K2SO4 C.乙醇 D.NaOH溶液 7.下列物质的水溶液不能使酚酞变红的是 A.NaOH B.Na2CO3 C.NaCl D.NH3 8.下列仪器的名称错误的是 A.表面皿 B.分液漏斗 C.直形冷凝管 D.坩埚 9.生活中离不开化学。从化学的角度分析,下列做法不当的是 A.餐桌上酒精失火,立即用湿抹布盖灭 B.烤炭火时在火炉旁放一杯水防止CO中毒 C.自来水厂用氯水对原水进行杀菌消毒 D.用“84”消毒液对茶具、餐具和洁具进行清洗消毒 10.实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是 11.下列说法正确的是 A.12gC所含的原子数就是阿伏伽德罗常数 B.4.9 g H2SO4是0.05 mol H2SO4 C.氢原子的摩尔质量是1.008 g D.1 mol氧的质量是32 g 12.下列各物质所含原子个数按由大到小的顺序排列的是 ①11.2L标准状况下的NH3; ②1 mol He; ③9g H2O;④0.2 mol H3PO4 A.①④③② B.④③②① C.②③④① D.①④②③ 13.如右图两集气瓶体积相等,在同温同压时瓶内气体的关系一定正确的是 A.所含原子数相等 B.气体密度相等 C.气体质量相等 D.摩尔质量相等 14.实验室有一瓶溶液,标签上标有“BaCl2 0.2 mol·L-1”的字样,下面对该溶液的叙述正确的是 A.配制500mL该溶液,可将0.1 mol BaCl2溶于500mL水中 B.Ba2+和Cl-的物质的量浓度都是0.1 mol·L-1 C.将该瓶溶液稀释一倍,则所得溶液的c(Cl-)为0.2 mol·L-1 D.从试剂瓶中取该溶液的一半,则所取溶液的物质的量浓度为0.1 mol·L-1 15.分类与归类是识别化学物质的基本方法,也是理解化学语言的基本途径。下列各项中的物质,能满足如图中阴影部分关系的是 ① ② ③ ④ A NaCl K2SO4 KCl (NH4)2SO4 B NaCl K2SO4 KCl NH4Cl C Na2SO4 K2SO4 KHCO3 NH4Cl D Na2SO4 K2SO4 KHCO3 NH4HSO4 16.设NA为阿伏伽德罗常数的值,下列说法正确的是 A.56g铁粉在氯气中充分燃烧时转移电子数等于2NA B.1 mol Na与足量O2反应生成Na2O和Na2O2的混合物,钠失去2NA个电子 C.标准状况下,2.24 LCl2被NaOH溶液吸收,转移电子数为0.2NA D.16g氧气与臭氧【分子式为O3】的混合气体中,含有NA个氧原子 17.下列物质露置在空气中,不能吸收CO2的是 A.Na2O B.Na2O2 C. NaOH D.NaHCO3 18.下列物质不能通过化合反应得到的是 A.Fe(OH)2 B.Fe(OH)3 C.FeCl2 D.FeCl3 19.下列物质溶于稀盐酸后,滴加KSCN溶液没有颜色变化,再加氯水呈红色的是 A.Fe3O4 B.Fe2O3 C.FeCl3 D.FeO 20.在下列反应中,水既未被氧化,也未被还原的是 A.2H2O2H2↑+O2↑ B.2F2+2H2O=4HF+O2↑ C.3Fe+4H2OFe3O4+4H2↑ D.3NO2+H2O=2HNO3+NO2↑ 21.不用其他试剂,用最简单的方法鉴别下列物质,正确的鉴别顺序是 ①NaOH溶液; ②Mg(NO3)2溶液; ③CuSO4溶液; ④KCl溶液。 A.①②③④ B.③④②① C.④①②③ D.③①②④ 22.下列关于NO2和SO2的说法中错误的是 A.它们都是易溶于水的有色气体 B.它们都是具有刺激性气味的有毒气体 C.大气中的NO2和SO2可以形成酸雨 D.提高机动车尾气排放标准有利于提高空气质量 23.在无色透明的溶液中,可以大量共存的离子组是 A.MnO4-、Fe2+、K+、Cl- B.Cu2+、Na+、Cl-、SO42- C.Ca2+、Cl-、NO3-、K+ D.Ca2+、Na+、OH-、HCO3- 24.下列试剂或方法不能用来区分CO2与SO2的是 A.品红溶液 B.酸性高锰酸钾溶液 C.澄清石灰水 D.闻气味 25.下列反应的离子方程式的书写不正确的是 A.金属钠和水反应:2Na+2H2O=2Na++2OH-+H2↑ B.NH4HCO3溶液中加入过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O C.把氯气通入NaOH 溶液中:Cl2+2OH-=Cl-+ClO-+H2O D.金属铜与稀硝酸反应: 3Cu+8H++2NO3- 3Cu2++2NO↑+4H2O 26.向含a mol NaOH的水溶液中通入b mol CO2,下列说法不正确的是 ( ) A.当a>2b时,NaOH剩余(a-2b) mol B.当a<b时,发生的离子反应为OH-+CO2=HCO3- C.当3a=4b时,发生的离子反应为4OH-+3CO2=CO32-+2HCO3-+H2O D.当a<b<a时,溶液中生成HC(a-b) mol 27.某合金与铁的物理性质的比较如下表所示: 熔点/℃ 密度(g/cm3) 硬度(金刚石为10) 导电性(银为100) 某合金 2500 3.00 7.4 2.3 铁 1535 7.86 4.5 17 还知该合金耐腐蚀、强度大,从以上性能看,该合金不适合做 A.导线 B.门窗框 C.炉具 D.飞机外壳 28.Na2CO3和NaHCO3是常见的两种盐,它们广泛地应用于生产和生活中。下列有关碳酸钠和碳酸氢钠的说法中不正确的是 A.NaHCO3能中和胃酸,可用于治疗胃酸过多症,但不适合胃溃疡病人 B.NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头 C.向Na2CO3饱和溶液中通入足量CO2气体,可获得NaHCO3晶体 D.可以用澄清石灰水来鉴别Na2CO3溶液中和NaHCO3溶液 29.下列关于试剂保存,除杂试剂选择的叙述不正确的是 A.金属钠应该保存在煤油中 B.漂白粉可以敞开存放 C.除去NO中混有的NO2:排水集气 D.除去Cl2中混有的HCl气体:饱和食盐水洗气 30.绿矾在高温下易分解,用右图装置检验绿矾的分解产物【加热装置已略去】。化学方程式为:2FeSO4·7H2OFe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是 A.SO2是还原产物,Fe2O3是氧化产物 B.b中所得到的硫酸的质量分数理论上为29.5% C.将反应后的气体通入氯化钡溶液中,产生的沉淀为BaSO3、BaSO4 D.将反应后的气体通入硝酸钡溶液中,产生的沉淀为只有BaSO4 第Ⅱ卷(40分) 31.(6分)学会阅读体检报告,就能正确判断自己的身体状况。下表是体检中心出具的一份血液检查报告中的部分结果。请认真查看后回答下列问题: 宜昌市夷陵区医院体检报告 生化室 检查日期 检查医生 ★★★ 项目名称 检查结果 单位 参考范围 提示 肝功能八项 谷丙转氨酶(ALT) 36.5 U/L 0.00---50 谷草转氨酶(AST) 35 U/L 5---46 血清总蛋白(T PROT) 69.7 g/L 60---82 血清白蛋白(ALB) 44.7 g/L 35---56 球蛋白(GLB) 25.0 G/L 20---35 白球比(A/G) 1.8 1.2---2.3 总胆红素(TB-K) 12.3 umol/L 3.0---25 直接胆红素(DB-K) 1.5 umol/L 0---6.0 血糖 葡萄糖(GLU) 4.9 mmol/L 3.38---6.2 (1)该老师上述各项检查指标 (填“有”或“无”)不正常之处。 (2)上述单位中的“g/L”的意义是 ; (3)上述单位中的mmol/L就是10-3mol/L,则1L人体血液中所含葡萄糖(相对分子质量为180)的正常质量范围为 g。 32.(12分)已知A为正盐。根据下列变化进行推断,回答有关问题: (1)推断A、B、C、D的化学式:A________、B________、C________、D________。 (2)写出下列反应的离子方程式: 反应①生成气体B: ; 反应②白色沉淀溶解: 。 33.(8分)自然界中存在很多物质循环过程。下图是自然界中氮循环示意图,请回答下列问题: (1)自然界中的固氮和人工固氮的共同点是 。 (2)硝化细菌可以将氨氧化成亚硝酸,请配平该反应: NH3+ O2→ HNO2+ H2O 其中还原产物为 。 (3)根据循环图判断下列说法不正确的是______。 a.氮元素均被氧化 b.含氮无机物和含氮有机物可相互转化 c.工业合成氨属于人工固氮 d.模拟生物固氮是人工固氮发展的方向 34.(14分)实验室常下图装置进行铜跟浓硫酸反应等一系列实验。请回答下列问题 (1)装置B就是右上图的集气瓶,则装置A的导管应连接集气瓶的 (填“a”或“b”) 进口; (2)用装置A制备SO2的优点主要是 。【任答一条即可】; (3)装置A中的反应方程式为 ; (4)装置C中的现象是 ;反应结束后加热D中溶液,现象是 ; (5)装置E中出现的现象可以说明SO2具有 性; (6)装置F中的反应的离子方程式为 ; 宜昌市部分示范高中教学协作体2018年秋期末联考 高一化学参考答案与评分标准 选择题: 题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 答案 B B A C C B C A B B B A A C D 题号 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 答案 D D A D D D A C C B D A D B C 31(6分)每空2分 ⑴ 无; ⑵ 每升血液中含有的该物质的质量; ⑶ 0.608~1.116; 32.(12分) 每空2分 ⑴ A:(NH4)2CO3;B:NH3;C:BaCO3;D:CO2。 ⑵ NH4++OH- NH3↑+H2O;BaCO3+2H+=Ba2++CO2↑+H2O 33.(8分) 每空2分 ⑴ 将游离态的氮转化为化合态的氮或将氮气转化为氮的化合物 ⑵ 2、3、2、2;HNO2和H2O【对一个给1分】 ⑶ a 34.(14分) 每空2分 ⑴ a ⑵ 可以控制反应的发生与停止、可以防止倒吸【只要合理就给分】; ⑶ Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O ⑷ 溶液变红;溶液恢复红色; ⑸ 还原性 ⑹ SO2+2OH-=SO32-+H2O 宜昌市部分示范高中教学协作体2018年秋期末联考 高一化学命题双向细目表 题号 题型 分值 考查知识点 能力要求 试题难度 试题来源 1 选择题 2 基本计量单位 了解 容易 2 选择题 2 空气质量日报 了解 容易 3 选择题 2 胶体 了解 容易 4 选择题 2 基本概念 了解 容易 5 选择题 2 漂白原理 了解 容易 6 选择题 2 电解质判断 了解 容易 7 选择题 2 溶液酸碱性 了解 容易 8 选择题 2 常见仪器 了解 容易 9 选择题 2 化学与生活 理解 适中 10 选择题 2 化学实验仪器、原理与操作 应用 较难 11 选择题 2 基本概念与计量 理解 适中 12 选择题 2 微粒数计算与排序 理解 适中 13 选择题 2 气体性质与微粒组成 理解 适中 14 选择题 2 物质的量浓度解读 理解 容易 15 选择题 2 物质分类 理解 适中 16 填空题 2 阿伏伽德罗常数与电子转移、微粒组成 理解 较难 17 选择题 2 物质化学性质 理解 容易 18 选择题 2 物质化学性质 理解 较难 19 选择题 2 物质检验与元素价态 理解 容易 20 选择题 2 氧化还原判断 理解 容易 21 选择题 2 物质鉴别 理解 适中 22 选择题 2 物质性质 理解 容易 23 填空题 2 离子共存 理解 适中 24 选择题 2 物质区分与鉴别 理解 适中 25 选择题 2 离子方程式正误判断 理解 适中 26 选择题 2 反应原理与用量 理解 难 27 选择题 2 金属材料的选用 理解 适中 28 选择题 2 物质化学性质 掌握 适中 29 选择题 2 物质保存、除杂 理解 适中 30 选择题 2 实验、性质、计算 理解 较难 31⑴ 填空题 2 指标判断 理解 容易 31⑵ 填空题 2 单位含义 理解 适中 31⑶ 填空题 2 物质的量与质量的计算 理解 适中 32⑴ 填空题 8 物质推断 理解 适中 32⑵ 填空题 4 离子方程式书写 理解 适中 33⑴ 填空题 2 基本概念 理解 适中 33⑵ 填空题 4 氧化还原方程式配平及产物判断 理解 容易 33⑶ 选择题 2 化学变化过程判断 理解 适中 34⑴ 填空题 2 气体收集方法 理解 容易 34⑵ 填空题 2 装置优化作用说明 理解 较难 34⑶ 填空题 2 化学方程式书写 理解 适中 34⑷ 填空题 4 化学实验现象描述 理解 适中 34⑸ 填空题 2 依据现象判断性质 理解 适中 34⑹ 填空题 2 离子方程式书写 理解 适中查看更多