- 2021-08-24 发布 |
- 37.5 KB |
- 10页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
辽宁省大连市2020届高三下学期第一次模拟考试 化学
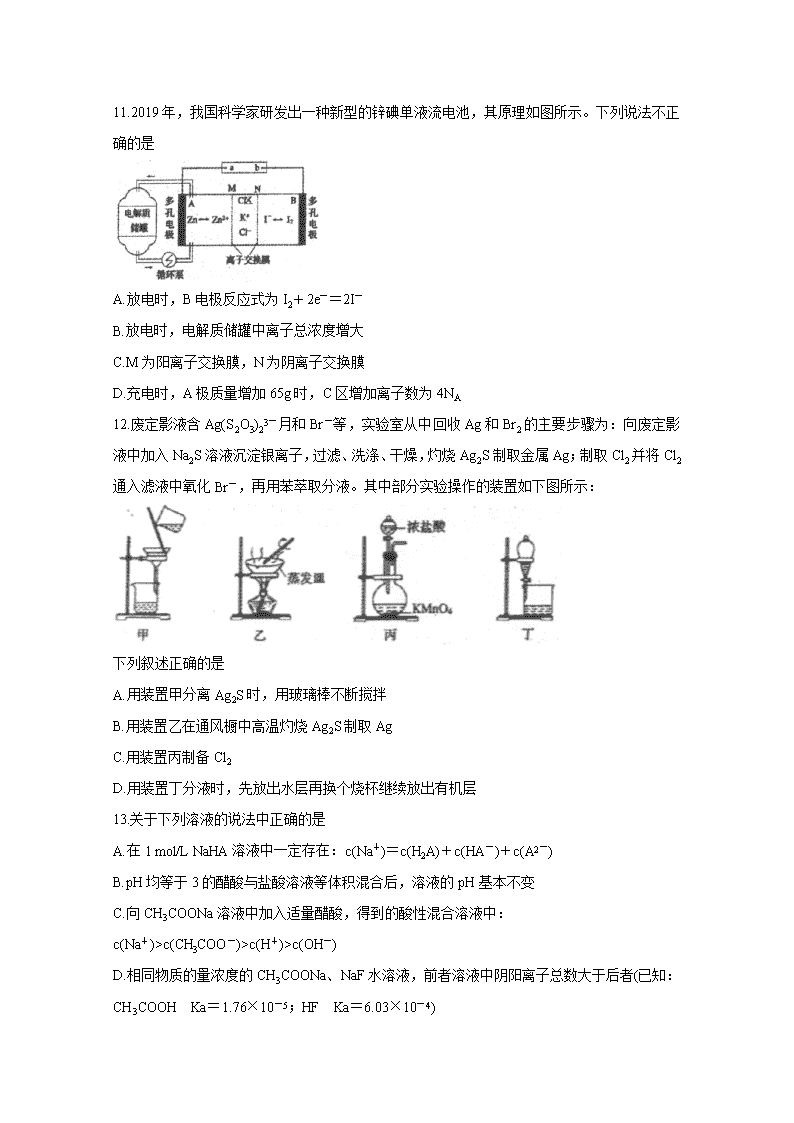
2020年大连市高三第一次模拟考试 理科综合 化学部分 考生注意: 说明: 1.本试卷分为第I卷(选择题)和第II卷(非选择题)两部分。共300分,考试用时150分钟。 2.试题全部答在“答题纸上”,答在试卷上无效。 可能用到的相对原子质量:H1 B11 C12 N14 O16 Na23 S32 Mn55 Fe56 Zn65 Ba137 第I卷 选择题(共126分) 一、选择题:本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项是符合题目要求的。 7.下列诗词的描述与物质变化不对应的是 A.爆竹声中一岁除-黑火药受热爆炸 B.日照香炉生紫烟-碘升华 C.烈火焚烧若等闲-石灰石分解 D.炉火照天地,红星乱紫烟-金属的冶炼 8.对二乙烯苯()可用作树脂、油漆及特种橡胶的原料。下列说法正确的是 A.分子中所有原子可能共平面 B.易溶于甲苯,沸点比甲苯低 C.不能使酸性高锰酸钾溶液褪色 D.1 mol该物质最多可与2 mol H2加成 9.已知NA为阿伏加德罗常数的值。下列说法正确的是 A.1 L 0.1 mol/L的Na2CO3溶液中含阴离子总数为0.1NA B.7.8 g Na2O2与过量CO2反应时,转移的电子数为0.2NA C.2 g H218O与D216O的混合物中所含的中子数和电子数均为NA D.足量乙烷与22.4 L(标准状况)Cl2发生取代反应,形成C-Cl键的数目为2NA 10.下图是部分短周期主族元素原子半径与原子序数的关系图,下列说法正确的是 A.M、N的氧化物都能与Z、R的最高价氧化物对应水化物反应 B.Y的单质能从含R简单离子的水溶液中置换出R单质 C.某物质焰色反应呈黄色,该物质一定是含Z元素的盐 D.X、M两种元素组成的化合物熔点很高 11.2019年,我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法不正确的是 A.放电时,B电极反应式为I2+2e-=2I- B.放电时,电解质储罐中离子总浓度增大 C.M为阳离子交换膜,N为阴离子交换膜 D.充电时,A极质量增加65g时,C区增加离子数为4NA 12.废定影液含Ag(S2O3)23-月和Br-等,实验室从中回收Ag和Br2的主要步骤为:向废定影液中加入Na2S溶液沉淀银离子,过滤、洗涤、干燥,灼烧Ag2S制取金属Ag;制取Cl2并将Cl2通入滤液中氧化Br-,再用苯萃取分液。其中部分实验操作的装置如下图所示: 下列叙述正确的是 A.用装置甲分离Ag2S时,用玻璃棒不断搅拌 B.用装置乙在通风橱中高温灼烧Ag2S制取Ag C.用装置丙制备Cl2 D.用装置丁分液时,先放出水层再换个烧杯继续放出有机层 13.关于下列溶液的说法中正确的是 A.在1 mol/L NaHA溶液中一定存在:c(Na+)=c(H2A)+c(HA-)+c(A2-) B.pH均等于3的醋酸与盐酸溶液等体积混合后,溶液的pH基本不变 C.向CH3COONa溶液中加入适量醋酸,得到的酸性混合溶液中: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) D.相同物质的量浓度的CH3COONa、NaF水溶液,前者溶液中阴阳离子总数大于后者(已知:CH3COOH Ka=1.76×10-5;HF Ka=6.03×10-4) 第II卷 非选择题(共174分) 三、非选择题:包括必考题和选考题两部分。第22题~第32题为必考题,每个试题考生都必须做答。第33题~第38题为选考题,考生根据要求做答。 (一)必考题(共129分) 26.(15分)碱式碳酸铜在烟火、农药、颜料、杀菌剂等方面应用广泛。一种以辉铜矿(Cu2S,含有SiO2和少量Fe2O3等杂质)为原料制备碱式碳酸铜的流程如图所示: 己知:①有关金属离子形成氢氧化物沉淀的pH范围如下: ②[Cu(NH3)4]SO4常温稳定,在热的水溶液中会分解生成NH3; ③Ksp[Fe(OH)3]=4.0×10-38。 ④硫在二硫化碳中的溶解度随温度升高而增大。 回答下列问题: (1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有 (任写一种)。 (2)滤渣I经CS2提取后可获得一种淡黄色副产品,则滤渣I中的主要成分是 (填化学式)。回收淡黄色副产品过程中温度控制在50~60℃之间,不宜过低或过高的原因是 。 (3)常温下“除铁”时加入的试剂A可用CuO等,调节pH的范围 ,若加A后溶液的pH调为5,则溶液中Fe3+的浓度为 mol/L。 (4)写出“沉锰”(除Mn2+)过程中反应的离子方程式: 。 (5)“赶氨”时,最适宜的操作方法是 。 (6)测定副产品MnSO4·H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100 mL 溶液,取出25.00 mL用标准浓度的BaCl2溶液测定,完全反应后得到了4.66 g沉淀,则此样品的纯度为 (保留到小数点后两位)。 27.(14分)甘氨酸亚铁络合物[(H2NCH2COO)2Fe]是一种新型的铁营养强化剂, 广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下: 已知: 请回答: (1)合成装置中仪器b的名称是 。 (2)请指出合成过程中,为了防止Fe2+被氧化,采取的措施是 。 (3)写出水浴加热过程中生成甘氨酸亚铁络合物的离子方程式: 。 (4)下列说法正确的是 。 A.滴入液体前,应先打开合成装置中滴液漏斗a的上口玻璃塞 B.根据题中所给信息,步骤I中亚铁盐应选用FeSO4·7H2O C.步骤III中分离方法可以是过滤 D.步骤IV,提纯操作中的干燥过程最好选用真空干燥 (5)合成过程需控制pH=5.5,试说明理由 。 (6)步骤III加入无水乙醇的目的是 。 (7)若甘氨酸的投料量为300kg,得到纯品344.8kg,则产品的产率为 %(保留一位小数)。 28.(14分)“绿水青山就是金山银山”,近年来我国着力推进绿色发展、循环发展等,形成了节约资源和环境保护的空间格局。 I.为了寻求对环境无污染的燃料燃烧法,有人曾研究了在一 定条件下氮的氧化物与碳的氧化物相互作用的机理, (1)确定该反应的反应过程如下: 第一步:NO2(g)+CO(g)→O-N…O…C-O △H=+134kJ/mol 第二步:O-N…O…C-O→NO(g)+CO2(g) △H=-368kJ/mol 总反应式:NO2(g)+CO(g)→NO(g)+CO2(g) △H= kJ/mol (2)对于任意一个化学反应,通过实验可以确定其反应速率与反应物浓度的定量关系:v=kcm(NO2)·cn(CO),该方程称为速率方程,其中k称为速率常数。分析表中数据,写出该反应的速率方程表达式: 。 II.活性炭也可处理大气污染物NO,其原理:2NO(g)+C(s)CO2(g)+N2(g) △H>0。 在T℃时,在容积一定的刚性容器中加入NO气体和活性炭粉,使之发生反应测得各物质的物质的量如下: (3)计算T℃时,该反应的平衡常数K= 。 (4)为了提高NO的转化率和反应速率,可采取的措施有 (填字母)。 A.增加NO的用量 B.增加活性炭的用量 C.升高温度 D.增大体系压强 II.用间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图所示。 (5)电极I电极反应式为 。 (6)电解时H+的移动方向 (填“从左向右”、“从右向左”或“不移动”)。 (7)标况下,每处理1 mol NO的同时,可产生O2的体积 L。 (二)选考题:共45分。请考生从2道物理题、2道化学题、2道生物题中任选一题作答。如果多做,则每科按所做的第一题计分。 35.[化学——选修3:物质结构与性质](15分) 室温离子液体是在室温和室温附近温度下呈液态的盐类物质,由于其具有良好的化学稳定性,较低的熔点和良好的溶解性,应用越来越广泛。如图为某离子液体的结构简式,回答下列问题: (1)B原子核外有 种运动状态不同的电子。BF4-中,B原子价层电子对数为 ,与BF4-互为等电子体的分子为 (填分子式,写出一种即可)。在周期表中,与B的化学性质最相近的邻族元素是 ,它们性质相近的原因是 。 (2)NH3极易溶于水的原因与氢键有关,结合NH3的水合物的电离推测NH3的水合物的合理结构式为 (填字母)。 (3)该离子液体常温下为液体,而NaBF4常温下为固体,原因是 。 (4)分子中的大π键可用符号表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为),上述阳离子中存在一个大π键,可表示为 。 (5)某硼的含氧酸根离子为无限链状结构,节选部分结构如图所示,其离子的化学式可用通式表示为 (用n代表B原子数)。 (6)某种含B和N两种元素的功能陶瓷,其晶胞结构如图所示,已知该晶胞底面为菱形,其边长为a cm,高为b cm,晶体密度为ρ g/cm3,,则阿伏加德罗常数NA的计算表达式为 mol-1(列出计算式)。 36.[化学——选修5:有机化学基础](15分) 格氏试剂(RMgX,X=Cl、Br、I)是一种重要的有机合成中间体,酯类化合物与格氏试剂的反应是合成叔醇类化合物的重要方法。由只含一种官能团的有机物A制备E的合成路线如下。回答下列问题: 已知信息如下: (1)A→B的反应类型为 ,E的分子式为 。 (2)B中所含官能团的名称 。 (3)C→D的化学方程式为 。 (4)M是比C多一个碳的C的同系物,符合下列条件的M的同分异构体(不考虑立体异构)有 种。①含六元碳环结构,不含甲基;②能与NaHCO3溶液反应放出CO2;③能发生银镜反应。 写出其中核磁共振氢谱有7组峰,且峰面积之比是4:4:2:1:1:1:1的所有同分异构体的结构简式 (5)将下列D→E的流程图补充完整:查看更多