- 2021-08-23 发布 |
- 37.5 KB |
- 11页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
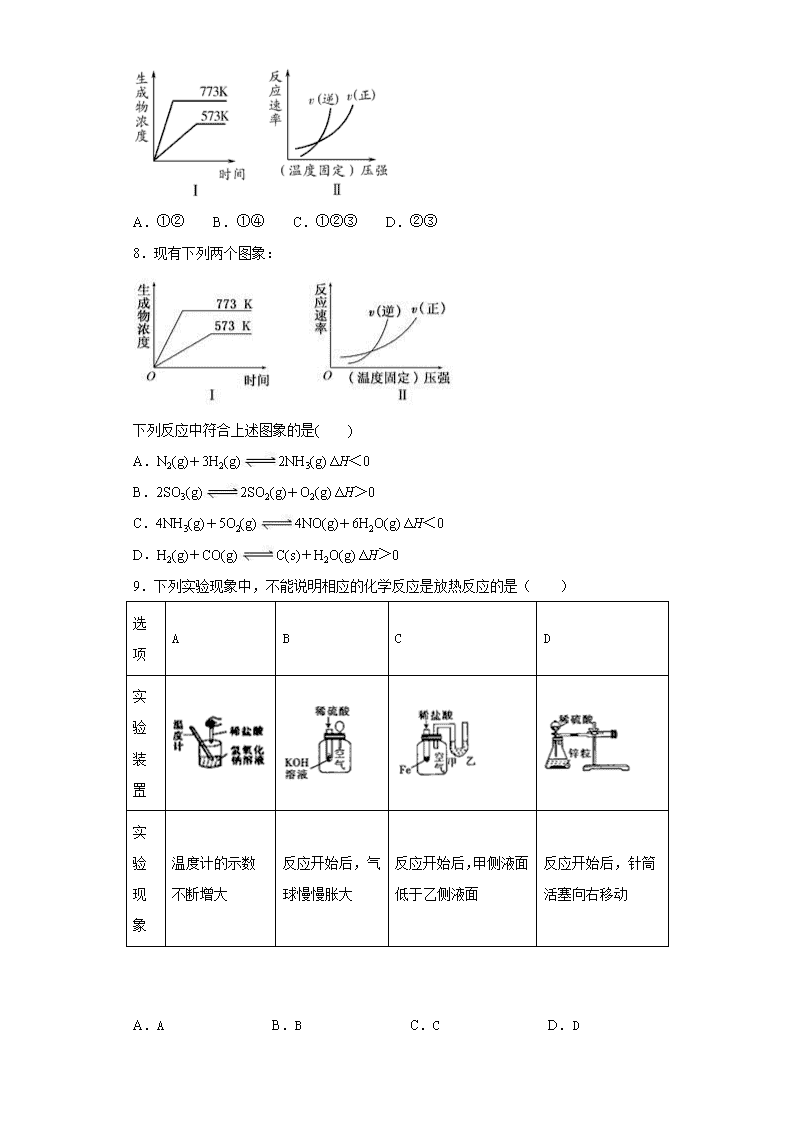
湖北省宜昌市协作体2018-2019学年高二上学期期末考试化学试题
绝密★启用前 湖北省宜昌市协作体2018-2019学年高二上学期期末考试化学试题 试卷副标题 考试范围:xxx;考试时间:100分钟;命题人:xxx 题号 一 二 三 总分 得分 注意事项: 1.答题前填写好自己的姓名、班级、考号等信息 2.请将答案正确填写在答题卡上 第I卷(选择题) 请点击修改第I卷的文字说明 评卷人 得分 一、单选题 1.对中国古代著作涉及化学的叙述,下列解读错误的是( ) A.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 B.《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 C.《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐 D.《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油 2.通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提髙生活质量。下列各图所示的措施中,是为了加快化学反应速率的是 A.铁门表面喷漆 B.橡胶里价炭黑 C.扇子扇煤炉子 D. 3.某反应由两步反应ABC构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)。下列有关叙述正确的是 A.三种化合物的稳定性顺序:B﹤A﹤C B.两步反应均为放热反应 C.加入催化剂不改变反应的焓变,但能提高产率 D.整个反应的ΔH=E1-E2 4.下列方程式书写正确的是( ) A.NaHSO4在水溶液中的电离方程式:NaHSO4===Na++HSO4- B.HF与NaOH溶液反应:H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ/mol C.1g H2燃烧生成液态水放出142.9 kJ的热量,其热化学方程式:2H2(g)+ O 2(g) = 2H2O (l) ΔH = —142.9 kJ·mol-1 D.CaCO3沉淀溶解平衡方程式:CaCO3(s) Ca2+(aq)+CO32-(aq) 5.下列指定溶液中,各组离子可能大量共存的是 A.使石蕊变红的溶液中:Na+、Cl-、SO42-、AlO2- B.在中性溶液中:Na+、Al3+、Cl-、HCO3- C.常温下pH=13的溶液中:NH4+、Ca2+、NO3-、SO42- D.由水电离出的c(H+)=10-13 mol·L-1的溶液中:Mg2+、Cl-、K+、SO42- 6.如图所示是某离子X的水解过程示意图,则离子X可能是( ) A.NH4+ B.HCO3- C.Na+ D.CO32- 7.对于一定条件下进行的化学反应:2SO2(g)+O2(g)2SO3(g),改变下列条件,可以提高反应物中活化分子百分数的是( ) ①增大压强 ②升高温度 ③加入催化剂 ④减小反应物浓度 A.①② B.①④ C.①②③ D.②③ 8.现有下列两个图象: 下列反应中符合上述图象的是( ) A.N2(g)+3H2(g)2NH3(g) ΔH<0 B.2SO3(g)2SO2(g)+O2(g) ΔH>0 C.4NH3(g)+5O2(g)4NO(g)+6H2O(g) ΔH<0 D.H2(g)+CO(g)C(s)+H2O(g) ΔH>0 9.下列实验现象中,不能说明相应的化学反应是放热反应的是( ) 选项 A B C D 实验 装置 实验现象 温度计的示数不断增大 反应开始后,气球慢慢胀大 反应开始后,甲侧液面低于乙侧液面 反应开始后,针筒活塞向右移动 A.A B.B C.C D.D 10.在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。下列判断不正确的是( ) A.原上层液体可能是KI的水溶液,原下层液体可能是CCl4 B.搅拌后两层液体颜色发生变化的原因是I2在CCl4中的溶解度大于在水中溶解度,所以绝大部分I2都转移到CCl4中 C.阴极区域pH增大的原因是水分子得电子生成了OH— D.阳极上的电极反应式2H++2e - =H2↑ 11.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12,下列说法正确的是( ) A.向含有浓度均为0.010 mol·L-1的Cl-和Br-溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,先产生沉淀的离子为Cl- B.向饱和AgCl水溶液中加入浓盐酸,Ksp值变大 C.向AgCl悬浊液中加入足量KBr溶液,沉淀将由白色转化为淡黄色 D.由方程式:Ag2CrO4(s)2Ag+(aq)+CrO42-(aq),可推知Ag2CrO4的饱和溶液一定有2c(Ag+)=c(CrO42-) 12.已知:HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是( ) A.常温下,用pH计测等浓度的两种酸的pH值 B.在相同条件下,对比相同浓度的两种酸,与相同大小镁条反应的初始速率 C.常温下,用pH试纸测量等浓度、等体积的两种钠盐的酸碱性 D.同温同压下,对比等浓度、等体积的两种酸,与足量Zn反应,生成H2的体积 13.已知4NH3(g)+5O2(g) =4NO(g)+6H2O(g),若化学反应速率分别用v(NH3)、v(O2)、 v(NO)、v(H2O)(单位:mol·L-1·s-1)表示,则正确关系是( ) A.4/5v(O2)=v(NO) B.5/6v(O2)=v(H2O) C.2/3v(NH3)=v(H2O) D.4/5v(NH3)=v(O2) 14.下图是用0.1000 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞做指示剂)的滴定曲线。下列说法正确的是 A.水电离出的氢离子浓度:a>b B.盐酸的物质的量浓度为0.0100 mol·L-1 C.指示剂变色时,说明盐酸与NaOH恰好完全反应 D.当滴加NaOH溶液10.00 mL时,该混合液的pH= 1+lg3 15.如图所示装置中,在U形管底部盛有CCl4,分别在U形管两端小心倒入饱和食盐水和稀硫酸,并使a、b两端液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述中错误的是( ) A.铁丝在两处的腐蚀速率:a<b B.a、b两端相同的电极反应式为Fe-2e-===Fe2+ C.一段时间后,a端液面高于b端液面 D.生铁丝中的碳在a、b两处分别作原电池的负极和正极 16.25℃时,几种弱酸的电离常数如下: 酸 CH3COOH HCN H2S 电离常数 (25℃) 1.8×10-3 4.9×10-10 K1=1.3×10-7 K2=7.1×10-13 下列说法正确的是( ) A.等物质的量浓度的各溶液pH关系为pH(CH3COONa)>pH(Na2S)>pH(NaCN) B.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定大于b C.NaHS和Na2S混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) D.某浓度HCN的水溶液的pH=d,则其中c(OH-)=10-dmol/L 第II卷(非选择题) 请点击修改第II卷的文字说明 评卷人 得分 二、综合题 17.完成并分析下列化学原理 (1)在配制三氯化铁溶液时,为了防止发生水解,可以加入少量的________。 (2)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是____________; (3)除去CuCl2溶液中少量的FeCl3,加入的试剂可以是_____________。 (4)在常温下,稀释等PH值的HCl、HF两种酸的稀溶液时,溶液pH随加水量的变化如图所示,能表示HF的稀释过程的曲线是:_____________ (5)amol·L-1(NH4 )2SO4溶液pH=5,其原因是_______(用相应的方程式说明)。 (6)有4种混合溶液,分别由等体积0.1 mol·L-1的两种溶液混合而成:①NH4Cl与 CH3COONa ②NH4Cl与HCl ③NH4Cl与NaCl ④NH4Cl与NH3·H2O(混合液呈碱性)。溶液中c(H+)由小到大的顺序为:(填混合溶液的编号)____________ (7)在做Zn与稀H2SO4反应制取H2的实验中,向溶液中滴加几滴CuSO4溶液,反应放出H2速度加快的原因是:__________________________ 18.温室效应是由于大气里温室气体(二氧化碳、甲烷等)含量增大而形成的。回答下列问题: (1)利用CO2可以制取甲醇,有关化学反应如下: ①CO2(g)+3H2(g)CH3OH(g)+H2O(g ) ΔH1=-178 kJ·mol-1 ②2CO(g)+O2(g)2CO2(g) ΔH2=-566 kJ·mol-1 ③2H2(g)+O2(g)2H2O(g) ΔH3=-483.6 kJ·mol-1 已知反应①中相关的化学键键能数据如下: 化学键 C—C C—H H—H C—O H—O 键能/kJ·mol-1 348 413 436 358 463 由此计算断开1 mol CO需要吸收____________kJ的能量。 (2)甲烷燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:通入a气体的电极是原电池的______极(填“正”或“负”),其电极反应式为______ 。 (3)如图是用甲烷燃料电池(电解质溶液为KOH溶液)实现铁上镀铜,则b处通入的是____(填“CH4”或“O2”),电解前,U形管的铜电极、铁电极的质量相等,电解2min后,取出铜电极、铁电极,洗净、烘干、称量,质量差为12.8g,在通电过程中,电路中通过的电子为_____mol,消耗标准状况下CH4______mL. 19.氮及其化合物是重要的化工原料 (1)在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示。其中温度为T1时平衡混合气体中氨气的体积分数为25.0%。当温度由T1变化到T2时,平衡常数关系K1 ______K2(填“>”、“<”或“=”),焓变△H______0(填“>”或“<”)。 (2)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是_____(填字母代号)。 a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂 (3)已知:2NO2(g)N2O4(g),N2O4为无色气体。 ① 在上述条件下反应能够自发进行,则反应的ΔH________0(填写“>”、“<”或“=”) ② 一定温度下,在密闭容器中反应2NO2(g)N2O4(g)达到平衡,达到平衡状态的标志 _______。 A.单位时间内生成n mol N2O4的同时生成2 nmolNO2 B.用NO2、N2O4的物质的量浓度变化表示的反应速率之比为2:1的状态 C.混合气体的颜色不再改变的状态 D.混合气体的密度不再改变的状态 E.混合气体的平均相对分子质量不再改变的状态 (4)17℃、1.01×105Pa,往10L密闭容器中充入NO2,达到平衡时,c(NO2)=0.2 mol·L-1,c(N2O4)=0.16 mol·L-1。则反应达到平衡时, NO2的转化率为__________;此温度下该反应的平衡常数K=________. 评卷人 得分 三、实验题 20.为测定某H2C2O4溶液的浓度,取25.00mL该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。 (1)滴定实验反应的离子方程式为:__MnO4-+___H2C2O4+___H+=___Mn2++ 8H2O+___(_____) (2)滴定时,KMnO4溶液应装在 _______________ (填“酸式滴定管”或“碱式滴定管”)中,达到滴定终点的现象为 _________________________________。 (3)若滴定时,没用标准液洗涤滴定管,会使得草酸溶液的物质的量浓度_______(填“偏高”、“偏低”、“无影响”) (4)取0.50 mol·L-1 H2SO4溶液30 mL与同浓度的NaOH溶液50 mL做中和热的实验,发现|△H|<57.3 kJ·mol-1,产生此偏差的原因可能是______(填字母)。 a.实验装置保温、隔热效果差 b.用量身量取NaOH溶液的体积时仰视读数 c.一次性把NaOH溶液倒入盛有H2SO4溶液的小烧杯中 d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 参考答案 1.B 2.C 3.A 4.D 5.D 6.A 7.D 8.B 9.D 10.D 11.C 12.D 13.D 14.D 15.D 16.C 17.稀盐酸或稀HCl Al2O3 或氧化铝 氧化铜、氢氧化铜、碳酸铜、碱式碳酸铜 HB NH4+ + H2ONH3·H2O+H+ ④< ①< ③< ② 形成锌—铜—稀硫酸原电池,加快反应速率 18.750 负 CH4 + 2H2O - 8e- CO2 + 8H+ O2 0.2 560 19.> < c < A C E 62% 或61.5% 4 20.2 5 6 2 10 CO2 酸式滴定管 滴入最后一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色 偏高 a d 查看更多