化学卷·2019届河南省商丘市第一高级中学高二10月月考(2017
2017-2018学年第一学期10月份考试
高二化学试卷
命题人:贾晓 审题:赵永芳
可能用到的相对原子质量:H:1 C:12 O:16 Na:23
第I卷 选择题
每小题3分,共54分,每小题只有一个正确选项
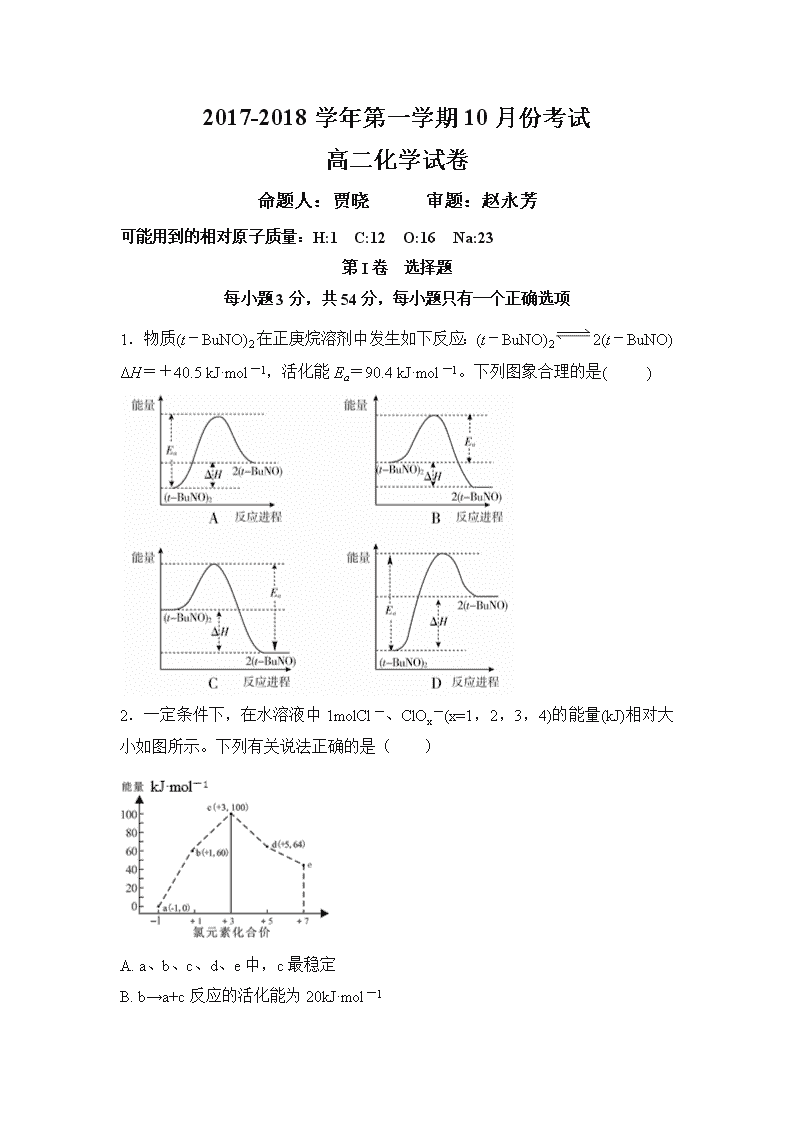
1. 物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)22(t-BuNO)
ΔH=+40.5 kJ·mol-1,活化能Ea=90.4 kJ·mol-1。下列图象合理的是( )
2.一定条件下,在水溶液中1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是( )
A. a、b、c、d、e中,c最稳定
B. b→a+c反应的活化能为20kJ·mol-1
C. b→a+d反应的热化学方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq) △H=+116kJ·mol-1
D. 一定温度下,Cl2与NaOH溶液反应生成的产物有a、b、d,溶液中a、b、d的浓度之比可能为11:1:2
3.下列说法正确的是( )
A. KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
B. 向Cr2O72- + H2O 2CrO42-+ 2H+ 的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)2NH3(g) △H=-38.6kJ·mol-1
D. 已知:
共价键
C-C
C=C
C-H
H-H
键能/ kJ·mol-1
348
610
413
436
则可以计算出反应的ΔH为-384 kJ·mol-1
4. 下列热化学方程式书写正确的是(ΔH的绝对值均正确) ( )
A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=—1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HI(aq)=NaI(aq)+H2O(l) ΔH=—57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)=SO3(g) ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2=O2+2NO ΔH=+116.2 kJ·mol-1(反应热)
5.研究小组发现一种化合物在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4 min~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是
( )
A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
6.下列说法中不正确的有( )个
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g)B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
A. 2 个 B. 3 个 C. 4 个 D. 5个
7.700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g) 反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min
n(CO)/mol
n(H2O)/mol
0
1.20
0.60
t1
0.80
t2
0.20
下列说法正确的是 ( )
A. 反应在t1 min内的平均速率为v(H2)=mol·L-1·min-1
B. 保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.30 mol
C. 保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D. 温度升高至800 ℃,上述反应平衡常数为0.64,则正反应为吸热反应
8.在某温度T℃时,将N2O4、NO2分别充入两个各为1L
的密闭容器中,反应过程中浓度变化如下[2NO2(g)N2O4(g) △H<0]:
容器
物质
起始浓度/(molL-1)
平衡浓度/(molL-1)
Ⅰ
N2O4[
0.100
0.040
NO2
0
0.120
Ⅱ
N2O4
0
0.0142
NO2
0.100
0.0716
下列说法不正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应的转化率a(N2O4)>a(NO2)
B. 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)
0
D. 4NH3+5O24NO+6H2O △H<0
10. 在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)2C(g) ΔH<0
某时刻达到平衡后,在时刻改变某一条件,其反应过程如图所示。下列说法正确的是
( )
A.
B.I、Ⅱ两过程达到平衡时,A的体积分数I>II
C.时刻改变的条件是向密闭容器中加C
D.I、II两过程达到平衡时,平衡常数IC>A=D=E
B. 若从A点到D点,可采用:温度不变在水中加入少量的酸
C. 若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D. 若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
15.25℃时,将浓度均为0.1mol/L,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是( )
A. Ka(HA)=1×10-6mol/L
B. b点c (B+)=c(A-)=c(OH-)=c(H+)
C. c点时,随温度升高而减小
D. a→c过程中水的电离程度始终增大
16.某化学研究性学习小组对电解质溶液作如下的归纳总结(均在常温下),其中正确的是 ( )
① pH=1的强酸溶液,加水稀释后,溶液中各离子浓度都会降低
② 1 L 0.50 mol·L-1NH4Cl 溶液与2 L 0.25 mol·L-1NH4Cl 溶液含NH4+ 物质的量完全相等
③ pH相等的四种溶液:a.CH3COONa b.NaClO c.NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d < b < c < a
④ pH=8.3的NaHCO3溶液:c(Na+) > c(HCO3-) > c(CO32-)> c(H2CO3)
⑤ pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-) ≤ c(H+)
⑥ pH=4浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液中:
c(CH3COO-)+c(OH-) > c(CH3COOH)+c(H+)
A.③⑤⑥ B.①③⑤ C.①②④ D.②④⑥
17.若用AG来表示溶液的酸度,其表达式为:AG=lg[]。298 K时,用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L 的MOH溶液,滴定曲线如图所示:
下列说法正确的是( )
A. 该滴定实验最好选择酚酞作为指示剂
B. C点时加入盐酸溶液的体积等于10 mL
C. 滴定过程中从A点到D点,溶液中水的电离程度
先逐渐减小,后逐渐增大
D. 若B点加入的盐酸溶液体积为5mL,则所得溶液中:c(M+)+2c(H+)=c(MOH)+2c(OH−)
18. 改变0.1二元弱酸溶液的pH,溶液中的、、的物质的量分
数随pH的变化如图所示[已知]。
下列叙述错误的是( )
A.pH=1.2时,
B.
C.pH=2.7时,
D.pH=4.2时,
第II卷 非选择题(共46分)
19.(10分,每空2分)
(1)1L 0.05mol/LNaHCO3溶液与足量的盐酸完全反应,放出10kJ的热量,写出此反应的热化学方程式
(2)写出明矾溶液与碳酸氢钠溶液反应的离子方程式
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象
(4) 在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好沉淀完全(浓度等于1.0×10−5mol·L−1)时,溶液中c(Ag+)为_______mol·L−1,此时溶液中c(CrO42−)等于__________mol·L−1。(已知Ag2 CrO4、AgCl的Ksp分别为2.0×10−12和2.0×10−10)。
20.(12分)
I.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
装置如图
(1) 图中A的名称是:
(1) 若实验过程中酸碱添加过慢,所得△H将 (填:偏大、偏小或者无影响)
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
实验次数
起始温度t1/℃
终止温度
t2/℃
H2SO4
NaOH
平均值
1
26.2
26.0
26.1
30.1
2
27.0
27.4
27.2
33.3
3
25.9
25.9
25.9
29.8
4
26.4
26.2
26.3
30.4
近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H= (取小数点后一位).
II.为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
(4) 请完成此实验设计,其中:V6= ,V8=
(5)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,请分析主要原因 。
III.利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取xmL一定物质的量浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V0mL。
步骤Ⅱ:移取ymL BaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
(6)BaCl2溶液的浓度为 mol·L-1,若步骤Ⅱ中滴加盐酸时有少量盐酸滴至锥形瓶外,Ba2+浓度测量值将 (填“偏大”或“偏小”)。
21.(12分,每空2分)
氧和氮是大气的主要成分,氮的化合物在工业上均有重要的应用。
(1)根据下列反应写出由热化学循环在较低温度下由水分解制备氢气的热化学方程式:
(2)在恒容密闭容器中,发生反应N2(g)+3H2(g) 2NH3(g),下列说法可以证明反应已达到平衡状态的是 。(填序号)
①单位时间内生成n molN2的同时生成2n molNH3
②1个N≡N键断裂的同时,有6个N—H键形成
③1个N≡N键断裂的同时,有3个H—H键形成
④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态。
为提高H2的转化率,实际生产中宜采取的措施有________(填字母)。
A.及时移出氨 B.最适合催化剂活性的适当高温
C.适当增大压强 D.循环利用和不断补充氮气
E.减小压强 F.降低温度
(3)电厂烟气脱氮的主反应①: 4NH3(g)+6NO(g)5N2(g)+6H2O(g),副反应②: 2NH3(g)+8NO(g)5N2O(g)+3H2O(g)。平衡混合气中N2与N2O
含量与温度的关系如图,请解释在400K~600K时,平衡混合气中这两种气体的含量随温度的变化而改变的原因是
(4)肼(N2H4)是一种重要的化工原料,既可用于制药,又可用作火箭燃料。向2 L的恒容密闭容器中充入2mol N2H4,发生反应N2H4(g)N2(g)+2H2(g),(用x表示)与时间的关系如图1所示,则该温度下,此反应的平衡常数K= 。
肼在另一条件下也可达到分解平衡,同时生成两种气体,且其中一种气体能使湿润的红色石蕊试纸变蓝。图2为平衡体系中肼的体积分数与温度、压强的关系,则p2_______ (填“大于”或“小于”) p1。
22.(12分)
已知醋酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOHCH3COO-+H+ K=1.75×10-5。
(1)计算0.01mol/L的CH3COOH溶液的pH= 。(已知lg1.75=0.24)
(2)25℃,将0.1mol/L的CH3COOH溶液和0.1mol/L的NaOH溶液等体积混合后溶液的pH=10,则该混合溶液中由水电离出的c(OH-)= mol/L
,写出该混合溶液中下列算式的精确结果(不能做近似计算),c(Na+)-c(CH3COO-)= mol/L。
(3)下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是 。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量镁粉 f.加入少量0.10 mol·L-1的NaOH溶液
(4) SOCl2是一种液态化合物,向盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有雾形成,产生可以使品红溶液褪色的气体,往溶液中滴加AgNO3溶液,有白色沉淀析出,请写出SOCl2与水反应的化学方程式 ,蒸干AlCl3溶液不能得到无水AlCl3,用SOCl2和AlCl3·6H2O混合加热可以得到无水AlCl3,试解释原因
(5) 常温下,反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数
K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
第二次月考答案
1-5 ADBBB 6-10 CCBDC 11-15 BADCC 16-18 ADD
19.
(1)NaHCO3(aq)+HCl(aq)=NaCl(aq)+CO2(g)+H2O(l) △H= -200kJ/mol
(2)Al3++3HCO3-=Al(OH)3↓+3CO2↑
(3)当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变.
(4)2×10-5 5 ×10-3
20.
(1)环形玻璃搅拌棒 (2)偏大 (3)-53.5kJ/mol (4)7 9.5
(5)Zn与CuSO4反应生成了Cu,Zn 和Cu形成了原电池加快反应速率
(6) 偏小
21.
(1)H2O(l)=H2(g)+O2(g) ΔH=+286 kJ/mol
(2)①③⑤⑥ ABCD
(3)反应①为放热反应,温度升高平衡左移,N2含量降低;反应②为吸热反应,温度升高平衡右移,N2O含量升高
(4)1 大于
22.
(1)3.38 (2)10-10 10-4-10-10 (3)bcef
(4)SOCl2+H2O=SO2↑+2HCl↑ SOCl2与AlCl3·6H2O中的结晶水作用生成无水AlCl3及SO2和HCl ,SO2和HCl抑制AlCl3水解
(5)1.25×10-3 或者 0.125×10-2 或者 0.00125