江苏省南通市如皋县2021届高三化学上学期期中试卷(Word版附答案)
江苏省南通市如皋县 2021 届高三期中调研考试
化 学
注意事项:
1. 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分 100 分,考试时间 90 分钟。
2. 答题前,请考生务必将自己的学校、班级、姓名写在密封线内,并认真核对。
可能用到的相对原子质量:H—1 C—12 N—14 O—16 K—39 Fe—56
第Ⅰ卷 选择题(共 40 分)
单项选择题:本题包括 15 小题,每小题 2 分,共计 30 分。每小题只有一个选项符合题意。
1. 正确回收和利用物质能节约资源、保护环境。下列处理垃圾的方法正确的是
( )
A. 回收废油脂制取食用油 B. 从阳极泥中回收金、银等金属
C. 回收医用塑料制取玩具 D. 工业废水直接灌溉农田
2. 下列有关化学用语表示正确的是 ( )
A. 中子数为 1 的氦原子:
2
3
He
B. Na2O 的电子式: N
a
·
·
O
··
··
·
·Na
C. S2-的结构示意图:
D. 基态 O 原子的轨道表示式:
3. 下列有关物质的性质与用途具有对应关系的是 ( )
A. MgCO3 分解吸热,可用于治疗胃酸过多
B. 浓硫酸难挥发,可用于催化酯化反应
C. FeCl3 具有氧化性,可用作净水剂
D. 碳酸钠溶液呈碱性,可用于去除油污
4. 常温下,下列各组离子在指定溶液中能大量共存的是 ( )
A. 无色透明的溶液中: K+、Mg2+、Mn
O4
- 、S
O4
2
-
B. c(Fe3+ )=1 mol·L-1 的溶液中: Ca2+、Cu2+、SCN-、Cl-
C. -
�w
�
(
OH
-)=1×10-13 mol·L-1 的溶液中: Ba2+、K+、Cl-、N
O3
-
D. 能使甲基橙变红的溶液中: Na+、N
H4
+
、I-、ClO-
5. 实验室制取、收集 NH3,并组装 NH3 的喷泉实验装置。下列图示装置和原理能达到实验
目的的是 ( )
A. 制 NH3 B. 干燥 NH3 C. 收集 NH3
D. 喷泉实验装置
6. 下列指定反应的离子方程式正确的是 ( )
A. 用惰性电极电解 CuCl2 溶液: 2Cl-+2H2O Cl2↑+H2↑+2OH-
B. 用 SO2 水溶液吸收少量 Br2: SO2+2H2O+Br2 H2SO4+2H++2Br-
C. AgCl 溶于过量氨水: AgCl+2NH3·H2O [Ag(NH3)2 ]++Cl-+2H2O
D. 少量 NO2 通入水中: NO2+H2O 2H++N
O3
-
7. 下列有关说法正确的是 ( )
A. 新制氯水光照时会释放出氧气
B. 室温下,铝和浓硫酸不发生反应
C. 过量铁粉在氯气中加热生成 FeCl2
D. 右图装置可以验证铁发生了析氢腐蚀
8. 在给定条件下,下列所示的转化关系均能实现的是 ( )
A. NH3(g) NO(g) NaNO3(aq)
B. Na NaOH(aq) NaHCO3(aq)
C. MgCl2·6H2O 无水 MgCl2 Mg
D. SiO2 H2SiO3 Na2SiO3(aq)
9. X、Y、Z 和 W 为原子序数依次增大的四种短周期主族元素。X 的基态原子中 s 轨道电
子总数是 p 轨道电子总数的两倍,Y 的基态原子中未成对电子数是同周期最多的,Z 是地壳中
含量最多的金属元素,W 和 X 位于同一主族。下列说法正确的是 ( )
A. 原子半径: r(X)
Y
C. Y 的简单气态氢化物的分子构型为平面正三角形
D. X 的简单气态氢化物是含极性共价键的非极性分子
10. 下列有关说法正确的是 ( )
A. 常温下,向 NH4Cl 溶液中加入少量盐酸,溶液中
�
(
H+
)
�
(
NH4
+
)的值增大
B. 一定温度下向恒容密闭容器中充入 SO2 和 O2,当反应到达平衡时,容器中 SO2、O2 、SO3
的物质的量之比为 2∶1∶2
C. 电解法精炼铜时,以粗铜作阴极,纯铜作阳极
D. 反应 N2(g)+3H2(g) 2NH3(g)的ΔH 可通过下式估算:
ΔH=反应中形成新共价键的键能之和-反应中断裂旧共价键的键能之和
不定项选择题:本题包括 5 小题,每小题 4 分,共计 20 分。每小题只有一个或两个选项符合题
意。若正确答案只包括一个选项,多选时,该小题得 0 分;若正确答案包括两个选项时,只选一
个且正确的得 2 分,选两个且都正确的得满分,但只要选错一个,该小题就得 0 分。
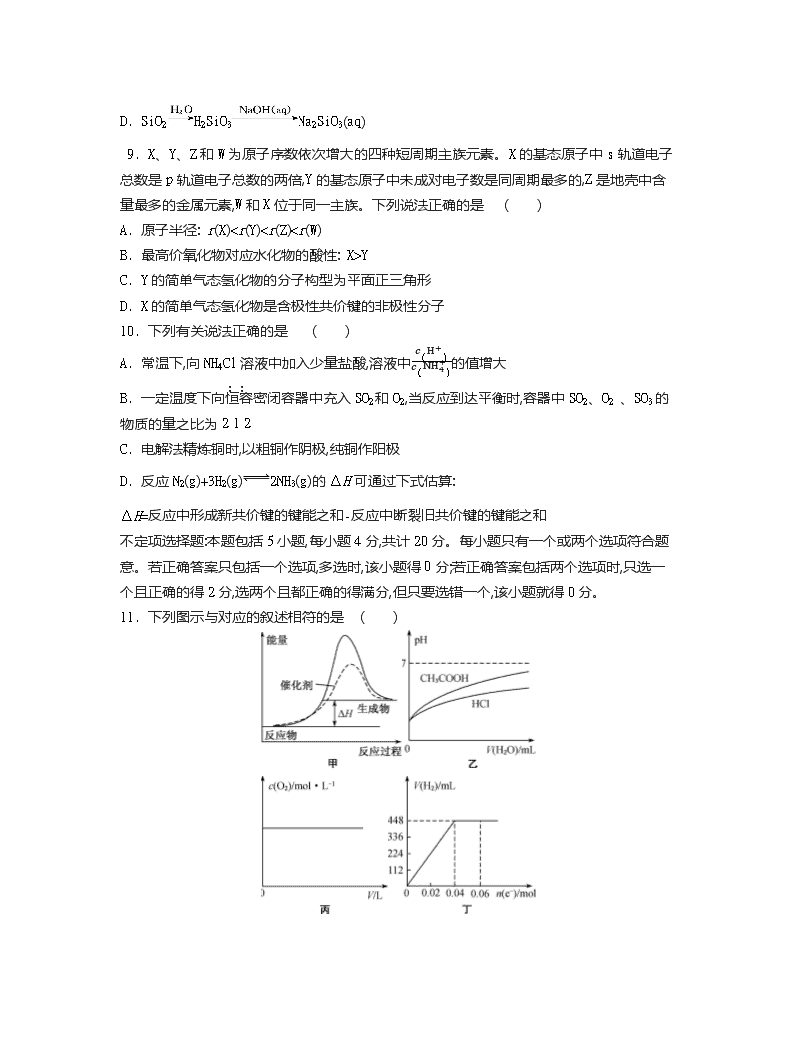
11. 下列图示与对应的叙述相符的是 ( )
A. 图甲表示反应“2SO2(g)+O2(g) 2SO3(g) ΔH<0”在有、无催化剂存在下反应过程中能
量的变化
B. 图乙表示稀释等 pH、等体积的盐酸和醋酸时,溶液的 pH 随所加入水的体积变化
C. 图丙表示一定温度下向不同体积的恒容密闭容器中投入 2 mol BaO2(s),发生反应
2BaO2(s) 2BaO(s)+O2(g),平衡时各容器中 c(O2)随容器体积的变化
D. 图丁表示常温下电解 400 mL 0.1 mol·L-1 NaCl 溶液过程中,产生氢气体积与转移电子物
质的量的关系
12. 合成药物异搏定路线中某一步骤如下。下列说法正确的是 ( )
A. 一定条件下,化合物 X 可与 HCHO 发生缩聚反应
B. 分子 X 的同分异构体中含有苯环且属于酯类的只有 2 种
C. 1 mol Y 与足量 NaOH 溶液共热时,最多消耗 1 mol NaOH
D. 化合物 Z 存在顺反异构现象
13. 根据下列实验操作和现象所得到的结论正确的是 ( )
选项 实验操作和现象 结论
A 向淀粉溶液中加入稀硫酸并加热,冷却后加 NaOH 溶液中和,再加入
银氨溶液,水浴加热,有银镜产生 淀粉已完全水解
B
相同条件下,在两支试管中各加入 4 mL 0.01 mol·L-1 KMnO4 和 2 mL
0.1 mol·L-1 H2C2O4,再向其中一支试管中迅速加入少量 MnSO4 固体,
加有 MnSO4 的试管中溶液褪色较快
MnSO4 对该反应有催化作
用
C 用 pH 计测得 0.100 mol·L-1 CH3COONa 的 pH 比
0.100 mol·L-1 NaNO2 溶液的大
CH3COOH 电离出 H+的能
力比 HNO2 的强
D
室温下,向 10 mL 0.2 mol·L-1 NaOH 溶液中滴入 2 滴 0.1 mol·L-1
MgCl2 溶液,产生白色沉淀,再滴加 2 滴 0.1 mol·L-1 FeCl3 溶液,有红褐
色沉淀生成
Ksp[Mg(OH)2]>
Ksp[Fe(OH)3]
14. 室温下,将两种溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微
粒物质的量浓度关系正确的是 ( )
A. 0.1 mol·L-1 HF(Ka =6.8×10-4)溶液和 0.1 mol·L-1 NaOH 溶液混合:
c(Na+)>c(OH-)>c(F-)>c(H+)
B. 0.1 mol·L-1 NaHCO3 溶液和 0.1 mol·L-1 Na2CO3 溶液混合:
2c(Na+)=3c(C
O3
2
-)+3c(HC
O3
- )+3c(H2CO3)
C. 0.1 mol·L-1 NaOH 溶液和 0.1 mol·L-1 H2C2O4(Ka1=5.4×10-2,Ka2=5.4×10-5)溶液混合:
c(Na+)>c(HC2
O4
- )>c(C2
O4
2
-)>c(H2C2O4)
D. 0.1 mol·L-1 CH3COONa 和 0.1 mol·L-1 HCl 溶液混合:
c(Na+)+c(CH3COO-)=c(Cl-)+c(H+)
15. 向体积为 1 L 的恒容密闭容器中充入 0.5 mol SO2 和 0.6 mol NO,发生反
应:SO2(g)+2NO(g) 2NO2(g)+S(s) ΔH
平衡时 c(NO)与温度的关系如图所示。下列说法正确的是 ( )
A. 该反应的ΔH>0
B. 压强 p(a)∶p(b)=20∶21
C. 维持容器温度 T1 K 不变,起始向容器中投入 0.2 mol SO2、0.2 mol NO 和 0.1 mol NO2,此
时 v(正)”或“<”),T1 K 后,反应主要以 (填“反应Ⅰ”、“反应Ⅱ”或
“反应Ⅲ”)为主。T2 K 后,曲线重合的原因是 。
(2) 以甲醇为原料,通过电化学法可以合成碳酸二甲酯[(CH3O)2CO],工作原理如图乙所示。
①阳极的电极反应式为 。
②若以铅蓄电池为电源,B 应与铅蓄电池的 (填“Pb”或“PbO2” )相连。
20. (10 分)酸碱混合时可以得到滴定图像、物种分布图像等。
(1) 室温下,用未知浓度 NaOH 溶液分别滴定 20.00 mL 物质的量浓度相同的盐酸和醋酸,所
得溶液的 pH 随 NaOH 溶液体积的变化如下图甲所示。
①在滴定的某时刻,滴定管中液面如图乙所示,此时滴定管读数为 mL。
②A 点时溶液中 c(Na+)、c(CH3COOH)、c(CH3COO-)由大到小的顺序为 。
③B 点时溶液中由水电离出的 c(H+)= mol·L-1。若忽略混合时溶液体积的变化,B 点
时所滴加 NaOH 溶液的体积为 mL。(结果保留 1 位小数)
(2) 已知 25 ℃时,向 0.100 mol·L-1 的 H3PO4 溶液中滴加 NaOH 溶液,各含磷微粒的分布系数
δ随 pH 变化的关系如图丙所示。
①若以酚酞为指示剂,当溶液由无色变为浅红色时主要反应的离子方程式
为 。
②25 ℃,pH=3 时溶液中
�
(
H3�O4
)
�
(
H2�O4
- )= 。
21. (10 分)以 FeCl3、NH4H2PO4、LiCl 和苯胺( )为原料可制备磷酸亚铁锂
(LiFePO4),LiFePO4 可用作锂电池的正极材料。
(1) 基态 Fe2+的电子排布式为 。
(2) N、P、O 三种元素的电负性由大到小的顺序是 。
(3) NH4H2PO4 中原子的轨道杂化方式为 sp3 杂化的原子有 。
(4) 1 mol 苯胺分子中含有σ键的数目为 。
(5) LiCl、苯胺和甲苯的熔点由高到低的顺序是 ,理由
是 。
(6) LiFePO4 的晶胞结构示意图如图甲所示(“●”为 Li+,位置分别在顶角、棱中心和面心,正八
面体和正四面体由 O 围绕 Fe 和 P 形成,它们通过共顶点、共棱形成空间链结构)。每个晶胞
中含有 LiFePO4 的单元数为 。电池充电时,LiFePO4 脱出 Li+,形成 Li1-xFePO4,
结构示意图如图乙所示,x= 。
2020~2021 学年度高三年级第一学期教学质量调研(二)
参考答案与评分标准
选择题(共 40 分)
单项选择题:本题包括 10 小题。每小题 2 分,共计 20 分。每小题只有一个....选项符合题意
1.B 2.A 3.D 4.C 5.D 6.C 7.A 8.B 9.D 10.A
不定项选择题:本题包括 5 小题,每小题 4 分,共计 20 分。每小题只有一个或两个选项
符合题意。若正确答案只包括一个选项,多选时,该小题得 0 分;若正确答案包括两个选
项,只选一个且正确的得 2 分,选两个且都正确的得满分,但只要选错一个,该小题就得
0 分。
11.C 12.AD 13.B 14.BC 15.CD
非选择题(共 60 分)
16.⑴①2FeSO4+2H3PO4+4NH3·H2O+H2O2=======70~75℃ 2FePO4·3H2O↓+2(NH4)2SO4 (3 分)
②温度过高会导致 H2O2 分解、氨水挥发(两者任答一点)
③3.25×10-15
⑵①6Fe2++6H2O+O2=2Fe3O4+12H+
②Fe2O3[或 Fe(OH)3] (1 分)
(除指定分值外,每空 2 分,共 10 分)
17.⑴加成反应(1 分)
⑵ (2 分) ⑶ (2 分)
⑷
(5 分)
(共 10 分)
18.⑴有(黄血盐)沉淀生成(2 分)
⑵①b (1 分)
②溶液恰好变为浅红色(1 分)
③AB(2 分)
④m(Fe2O3) =0.4 g
在 25.00 mL 溶液 A 中:n(Fe2+) =
0.4g
160g· mol −1
×2 = 5.00×10−3mol (1 分)
n(MnO-
4 )=2.000 mol·L-1×30.50×10−3L=6.10×10−2 mol
根据电子得失守恒可得 n(Fe2+)+10n(CN-)= 5n(MnO-
4 )
n(CN-)=3.00×10−2 mol (2 分)
根据电荷守恒:n(K+) =2.00×10−2 mol
x∶y = n(K+)∶n(CN-) =2∶3 (1 分)
(共 10 分)
19.⑴①ΔS>0
②> (1 分) 反应Ⅲ
反应Ⅲ前后气体分子数相等,改变压强对平衡没有影响
⑵①2CH3OH+CO-2e-===(CH3O)2CO+2H+
②Pb (1 分)
(除指定分值外,其余每空 2 分,共 10 分)
20.⑴①19.80 (1 分)
②c(CH3COO-)>c(Na+)>c(CH3COOH) (1 分)
③1.0×10-12 16.4
⑵①H2PO-4 +OH-=HPO2-4 +H2O
②0.1
(除指定分值外,其余每空 2 分,共 10 分)
21.⑴[Ar]3d6 (1 分)
⑵O>N>P (1 分)
⑶N、P
⑷14 mol (1 分)
⑸LiCl>苯胺>甲苯 (1 分)
LiCl 是离子晶体,苯胺和甲苯是分子晶体,离子晶体内的离子键强于分子晶体内的分
子间作用力;苯胺可形成分子间氢键,氢键强于甲苯内的范德华力
⑹4 (1 分) 0.5 (1 分)
(除指定分值外,其余每空 2 分,共 10 分)