- 2021-07-08 发布 |
- 37.5 KB |
- 10页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020-2021学年高三上学期月考化学试题(湖北省安陆市第一中学)
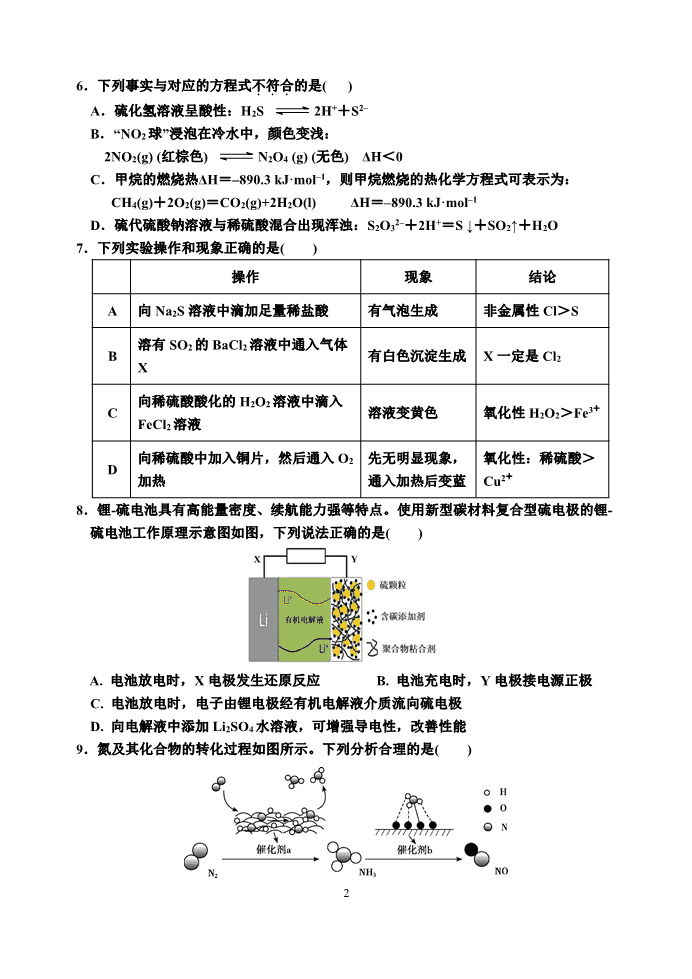
1 安陆一中 2021 届高三年级 8 月诊断性考试 化 学 试 题 可能用到的相对原子质量:H:1 C:12 N:14 O:16 Mn:55 Sn:119 一、选择题:本题共 10 小题,每小题 2 分,共 20 分。每小题只有一个选项符合题意。 1.以下是中华民族为人类文明进步做出巨大贡献的几个事例,运用化学知识对其进行的 分析不合理的是( ) A.四千余年前用谷物酿造出酒和醋,酿造过程中只发生水解反应 B.商代后期铸造出工艺精湛的司母戊鼎,该鼎属于铜合金制品 C.汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏士 D.屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作 2.下列物质的名称正确的是( ) A.C6H10O5:纤维素 B.[Ag(NH3)2]+:二氨合银离子 C.Na2SiO3:水玻璃 D. :2-甲基-1-丙醇 3.油条的做法是将矾、碱、盐按比例加入温水中,再加入面粉搅拌成面团;放置,使面 团产生气体,形成孔洞。放置过程发生反应: 2KAl(SO4)2·12H2O+3Na2CO3 = 2Al(OH)3↓+3Na2SO4+K2SO4+3CO2↑+21H2O 下列有关判断正确的是( ) A.放置过程发生的反应中,反应物和生成物均为电解质 B.放置过程发生的反应为氧化还原反应 C.反应的离子方程式为 2Al3++3CO32﹣==2Al(OH)3↓+3CO2↑ D.从物质的分类角度来看,油条配方中的“矾、碱、盐”均为盐 4.硒(Se)元素是人体必需的微量元素之一。下列说法正确的是( ) A. 硒的摄入量越多对人体健康越好 B. SeO32-空间构型为正四面体 C. H2Se 的熔沸点比 H2S 高 D. H2SeO4 的酸性比 H2SO4 强 5.设 NA 为阿伏加德罗常数的数值,下列说法正确的是( ) A.2.8g14N2 与 14C16O 的混合物中,中子数目为 l.4NA B.含 0. l molFeCl3 的溶液与 0. l mol 锌充分反应,转移电子数为 0.l NA C.标准状况下,5.6gC4H8 中 C-C 的数目可能为 0.4NA D.某温度下,1LpH=9 的 Na2CO3 溶液中,水电离产生的 OH-数目为 10-5 NA 2 6.下列事实与对应的方程式不符合...的是( ) A.硫化氢溶液呈酸性:H2S 2H++S2– B.“NO2 球”浸泡在冷水中,颜色变浅: 2NO2(g) (红棕色) N2O4 (g) (无色) ΔH<0 C.甲烷的燃烧热ΔH=–890.3 kJ·mol–1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=–890.3 kJ·mol–1 D.硫代硫酸钠溶液与稀硫酸混合出现浑浊:S2O32–+2H+=S ↓+SO2↑+H2O 7.下列实验操作和现象正确的是( ) 操作 现象 结论 A 向 Na2S 溶液中滴加足量稀盐酸 有气泡生成 非金属性 Cl>S B 溶有 SO2 的 BaCl2 溶液中通入气体 X 有白色沉淀生成 X 一定是 Cl2 C 向稀硫酸酸化的 H2O2 溶液中滴入 FeCl2 溶液 溶液变黄色 氧化性 H2O2>Fe3+ D 向稀硫酸中加入铜片,然后通入 O2 加热 先无明显现象, 通入加热后变蓝 氧化性:稀硫酸> Cu2+ 8.锂-硫电池具有高能量密度、续航能力强等特点。使用新型碳材料复合型硫电极的锂- 硫电池工作原理示意图如图,下列说法正确的是( ) A. 电池放电时,X 电极发生还原反应 B. 电池充电时,Y 电极接电源正极 C. 电池放电时,电子由锂电极经有机电解液介质流向硫电极 D. 向电解液中添加 Li2SO4 水溶液,可增强导电性,改善性能 9.氮及其化合物的转化过程如图所示。下列分析合理的是( ) 3 A. 催化剂 a 表面发生了极性共价键的断裂和形成 B. 催化剂 a、b 能提高反应的平衡转化率 C. 在催化剂 b 表面形成氮氧键时,不涉及电子转移 D. N2 与 H2 反应生成 NH3 的原子利用率为 100% 10.习主席在 2020 年新年贺词中强调“5G 商用加速推出,凝结着新时代奋斗者的心血和 汗水,彰显了不同凡响的中国风采、中国力量”,制造芯片用到高纯硅,用 SiHCl3 与过 量 H2 在 1100~1200℃反应制备高纯硅的装置如下图所示(热源及夹持装置略去)。 已知: SiHCl3 遇水 H2O 强烈水解,在空气中易自燃。下列说法错误的是( ) A.装置 B 中的试剂是浓硫酸 B.实验时先打开装置 C 中分液漏斗的旋塞 C.装置 C 中的烧瓶需要加热,其目的是使滴入烧瓶中的 SiHCl3 气化 D.装置 D 不能采用普通玻璃管的原因是在反应温度下,普通玻璃管会软化 二、选择题:本题共 5 小题,每小题 4 分,共 20 分。每小题有一个或两个选项符合题意, 全部选对得 4 分,选对但不全的得 2 分,有选错的得 0 分。 11.向盛有 KMnO4 溶液的试管中加入过量的 MnSO4 溶液,产生黑色沉淀,溶液由紫红色 变为无色;过滤,向滤液中加入少量的铋酸钠(NaBiO3)粉末,溶液又变为紫红色。下列 推断错误的是( ) A. 氧化性:NaBiO3>KMnO4>MnO2 B. 生成 8.7g 黑色沉淀,转移 0.2mol 电子 C. 利用 NaBiO3 可以检验溶液中的 Mn2+ D. NaBiO3 不能与浓盐酸发生反应生成氯气 12. 甲、乙均为 1L 的恒容密闭容器,向甲中充入 1molCH4 和 1molCO2,乙中充入 1molCH4 和 nmolCO2,在催化剂存在下发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g),测得 CH4 的平衡转化率随温度的变化如图所示。下列说法正确的是( ) A. 该反应的正反应是吸热反应 B. 773K 时,该反应的平衡常数小于 12.96 C. H2 的体积分数: φ(b)=φ(c) D. 873K 时,向甲的平衡体系中再充入 CO2、CH4 各 0.4mol,CO、H2 各 1.2mol,平衡不发生移动 13.科学家研制出了一种漂白效率极高的新型漂白剂(结构如图所示),其中 W、X、Y、Z 均为短周期元素且原子序数依次增大。常温下,0.1 mol/L Z 的氢化物的水溶液中 4 c(H+ )=0.1 mol/L,且 Z 与 Y 位于不同周期。下列叙述正确的是( ) A.原子半径:W> X> Y B.氢化物的沸点: X>Y> Z> W C.X 的氧化物的水化物是强酸 D.Y 的单质均具有杀菌消毒作用 14.某实验小组探究 SO2 与 AgNO3 溶液的反应,实验记录如下表,下列说法正确的是( ) A. 通过测Ⅰ中无色溶液 a 的 pH 可以判断 SO2 是否被氧化 B. 实验Ⅱ说明白色沉淀 b 具有还原性 C. 实验Ⅲ说明溶液 a 中一定有 2- 4SO 生成 D. 实验Ⅰ、Ⅱ、Ⅲ说明 SO2 与 AgNO3 溶液反应既有 Ag2SO4 生成,又有 Ag2SO3 生成 15. 室温时,向 100mL 0.1mol·L-1 NH4HSO4 溶液中滴加 0.1mol·L-1NaOH 溶液,溶液 pH 随 NaOH 溶液体积的变化如图所示。下列说法正确的是( ) A. 图中 a、b、c、d 四个点,水的电离程度最大的是 d 点 B. a 点处存在 c(NH4+)+c(NH3·H2O)=0.1mol·L-1 C. b 点处存在 c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) D. 由 b 到 c 发生反应的离子方程式为 NH4++OH-=NH3·H2O 序号 Ⅰ Ⅱ Ⅲ 实验 步骤 实 验 现象 得到无色溶液 a 和白 色沉淀 b 产生无色气体,遇空气变为 红棕色 产生白色沉淀 5 三、非选择题:本题共 5 小题,共 60 分。 16.(12 分)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵 ((NH4)3Fe(C6H5O7)2)。 (1)Fe 基态原子核外电子排布式为_________________________; 2 2 6Fe H O 中与 Fe2+配位的原子是_________。 (2)NH3 分子中氮原子的轨道杂化类型是____________;与 NH + 4 互为等电子体的一种分 子为_________(填化学式)。 (3)柠檬酸的结构简式见右图。1 mol 柠檬酸分子中 碳原子与氧原子形成的σ键的数目为_______mol。 (4) 2CaCN 是离子化合物,各原子均满足 8 电子稳定结构, 2CaCN 的电子式是_______。 17.(12 分)某小组探究 2 3Na SO 溶液和 3KIO 溶液的反应原理。 (实验一)将含淀粉的 -1 2 30.01mol L Na SO 溶液加入 -1 30.01mol L KIO 酸性溶液(过量) 中,混合后约 5 秒内无明显变化,随后有少量蓝色出现并迅速变蓝。 (1)溶液变蓝,说明 3KIO 具有__________性。 (2)查阅文献: 反应Ⅰ: - 2- - 2- 3 3 4IO +3SO =I +3SO 慢 反应Ⅱ: - - 3IO +I + _____=_____+_____ 较快 反应Ⅲ: 2- - 2- + 2 3 2 4I +SO +H O=2I +SO +2H 快 写出酸性条件下,反应Ⅱ的离子方程式______________________________________。 (3)向实验一所得蓝色溶液中加入少量 2 3Na SO 溶液,蓝色迅速褪去,后又变蓝色。据此 得出 2I 氧化性比 - 3IO 强,该结论______(填“合理”或“不合理”),理由是____ 。 (4)为了进一步研究 2 3Na SO 溶液和 3KIO 溶液的反应原理,设计如下实验。 (实验二)装置如图所示, K 闭合后,电流表的指针偏转情况记录如表: 表盘 时间 /min 10~t 2 3t ~t 4t 偏转 位置 右偏至 “Y”处 指针回到“0”处,又返至“X” 处;如此周期性往复多次 指针归 零 6 ① K 闭合后,检验 b 极附近溶液存在放电产物 2- 4SO 的实验操作是______________。 ② 1t 时,直接向 a 极区滴加淀粉溶液,溶液未变蓝。取 a 极附近溶液于试管中,滴 加淀粉溶液,溶液变蓝。判断 - 3IO 在 a 极放电的产物是__________。 (5)下列关于上述实验解释合理的是__________(填字母序号)。 A.实验一中:5 秒内无明显变化,可能是因为反应Ⅰ的活化能太小,反应速率太慢 B.实验二中:指针回到“0”处,可能是因为反应Ⅱ比反应Ⅰ快,导致 - 3IO 难与 2- 3SO 发 生反应 C.实验二中:又返至“X”处,可能是因为发生了反应Ⅲ,重新形成了原电池 18(11 分)苯胺( )是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。 已知:① 和 NH3 相似,与盐酸反应生成易溶于水的盐 ②用硝基苯制取苯胺的反应原理:2 +3Sn+12HCl→2 +3SnCl4+4H2O ③有关物质的部分物理性质见表: 物质 熔点/℃ 沸点/℃ 溶解性 密度/g∙cm-3 苯胺 -6.3 184 微溶于水,易溶于乙醚 1.02 硝基苯 5.7 210.9 难溶于水,易溶于乙醚 1.23 乙醚 -116.2 34.6 微溶于水 0.7134 Ⅰ.比较苯胺与氨气的性质 (1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为_________; 用苯胺代替浓氨水重复上述实验,却观察不到白烟,原因是_________________________。 Ⅱ.制备苯胺。往图所示装置(夹持装置略,下同)的冷凝管口 分批加入 20mL 浓盐酸(过量),置于热水浴中回流 20min, 使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量 50% NaOH 溶液,至溶液呈碱性。 7 (2)冷凝管的进水口是____(填“a”或“b”); (3)滴加 NaOH 溶液的主要目的是析出苯胺,反应的离子方程式为__________________。 Ⅲ.提取苯胺。 i.取出上图所示装置中的三颈烧瓶, 改装为如右图所示装置: ii.加热装置 A 产生水蒸气,烧瓶 C 中收集到苯胺与水的混合物;分离混合物得到粗 苯胺和水溶液。 iii.往所得水溶液加入氯化钠固体,使溶液达到饱和状态,再用乙醚萃取,得到乙醚萃 取液。 iv.合并粗苯胺和乙醚萃取液,用 NaOH 固体干燥,蒸馏后得到苯胺 2.79g。 (4)操作 ii 中,为了分离混合物,取出烧瓶 C 前,应先打开止水夹 d,再停止加热,理 由是_____________________________________。 (5)该实验中苯胺的产率为 _____________。 19.(12 分)氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精 矿为原料生产 CuCl 的工艺如下: 已知 CuCl 难溶于醇和水,溶于 c(Cl-)较大的体系[CuCl(s)+Cl- CuCl2-],潮湿空气 中易水解氧化。 (1)步骤 1 开始前需要对硫化铜精矿进行粉碎,目的是__________________________; (2)步骤 1 是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是 ______________________________; (3)步骤 2 是溶解过程,溶解时反应的离子方程式____ ; (4)步骤 3 为主反应,Cu+的沉淀率与加入的 NH4Cl 的量关系如图所示。 ①比较 c(Cu+)相对大小:A 点______C 点(填“>”、“<”或“=”); ②提高 C 点状态混合物中 Cu+沉淀率的措施是______________ ______________________________________________________ 8 (5)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是 。 20.(13 分)1,3 - 环己二酮( )常用作医药中间体,用于有机合成。下列是 一种合成 1,3-环己二酮的路线。 回答下列问题: (1)甲的分子式为 ___________________。 (2)丙中含有官能团的名称是______________________ 。 (3)反应①的反应类型是 _____________;反应②的反应类型是 ______________。 (4)反应③的化学方程式为_______________________________________________。 (5)符合下列条件的乙的同分异构体共有_____________种。 ①能发生银镜反应 ②能与 NaHCO3 溶液反应,且 1 mol 乙与足量 NaHCO3 溶液反应时产生气体 22. 4 L( 标准状况)写出其中在核磁共振氢谱中峰面积之比为 1 : 6 : 2 : 1 的一种同分异构 体的结构简式 __________________。(任意一种) (6)设计以乙醇、 (丙酮)为原料制备 (2,4 -戊二酮)的合成 路线___________________________________________________________(无机试任 选)。 1 2021 届高三年级 8 月诊断性考试化学答案 1-5:ABDCC 6-10:ACBDB 11-15:BD AB A B CD 16(12 分,每空 2 分) (1)1s22s22p63s23p63d64s2 或[Ar]3d64s2 O 或氧 (2)sp3 CH4 或 SiH4 (3) 7 (4) 2-.. .. 2+ .. .. Ca N::C::N 17(12 分,除标注外,每空 2 分) (1)氧化 ----------------- 1 分 (2) 3 2 2IO 5I 6H 3I 3H O + (3)不合理 ------------------- 1 分 由于反应Ⅲ比反应Ⅰ快,故现象显示 2I 与 2 3SO 的反应,但速率快不能说明氧化性就强 (4)取样于试管中,先加入过量稀 HCl 除去 2 3SO ,再滴加少量 2BaCl 溶液,有白色沉 淀生成 I (5)BC 18(11 分,除标注外,每空两分) (1)NH3+HCl=NH4Cl 苯胺沸点较高,不易挥发 (2) b ------------------1 分 (3)C6H5NH3++OH-→ C6H5NH2+H2O (4) 防止 B 中液体倒吸 (5) 60.0% 19(12 分,每空 2 分) (1) 增大接触面积、加快反应速率、提高铜的浸出速率等合理性答案 (2)CuS+H2SO4+H2O2=CuSO4+S+2H2O (3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 或 Cu+4H++2NO3-=Cu2++2NO2↑+2H2O 2 (4) ① > ②加水稀释 (5) HNO3 具有强氧化性会把 CuCl 氧化 20(13 分,除标注外,每空 2 分) (1)C6H11Br --------------- 1 分 (2)醛基、羰基(酮基) (3)消去反应 ---------1 分 氧化反应 ----------1 分 (4) +CH3CH2OH +H2O (5)12 或 (6)CH3CH2OH CH3COOH CH3COOCH2CH3查看更多