- 2021-07-06 发布 |
- 37.5 KB |
- 11页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
安徽省滁州市定远县育才学校2019-2020学年高一(实验班)上学期期末考试化学试题
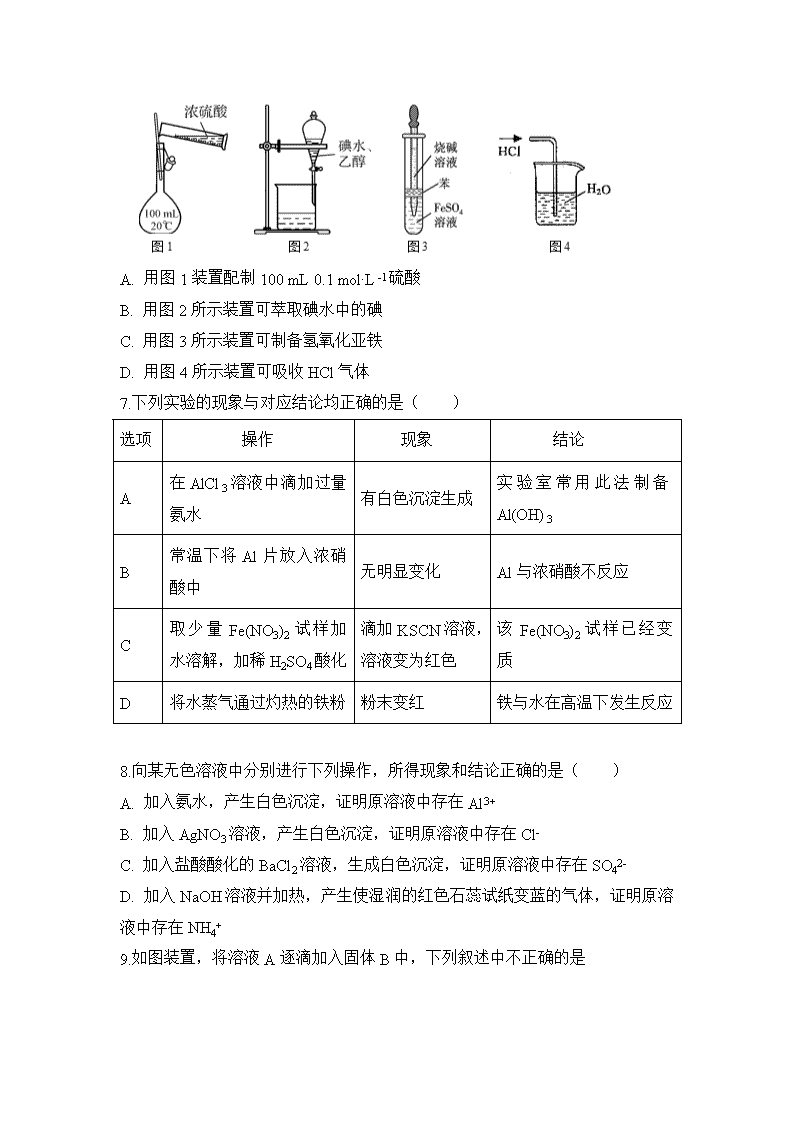
育才学校2019-2020学年度第一学期期末考试 高一实验班化学 一、选择题(共20小题,每小题2分,共40分) 1.下列化学物质在生活、生产的运用描述不正确的是 A. 氢氧化钠能与二氧化硅反应,故常用氢氧化钠在玻璃上进行刻画 B. 工业上常用氨气来检查氯气管道是否泄漏 C. 氧化铝俗名刚玉,耐磨,常用于做轴承材料 D. 钠和鉀的合金呈液态,常做核反应堆的导热剂 2.下列有关物质的分离和提纯的方法中正确的是 A. 除去Cl2的HCl气体可以通过浓硫酸 B. 碳酸钠固体中的碳酸氢钠杂质可以通过加热除去 C. SO2可以通过碱石灰干燥 D. FeCl3溶液中含有CuCl2可以加入足量NaOH溶液除去 3.下列离子方程式中,错误的是( ) A. 在浓NaOH溶液中滴入几滴NH4Cl溶液:NH4+ + OH- = NH3↑ + H2O B. 铁与盐酸反应:2Fe + 6H+ = 2Fe3+ + 3H2↑ C. 将少量铜屑放入浓硝酸中:Cu + 4H+ + 2NO3- = Cu2+ + 2NO2↑+ 2H2O D. 氯气与烧碱溶液反应:Cl2 + 2OH- = Cl- + ClO- + H2O 4.下列关于氢氧化铁胶体的说法不正确的是: A. 往NaOH饱和溶液中滴加FeCl3饱和溶液,加热煮沸制备氢氧化铁胶体 B. 氢氧化铁胶体的胶粒大小在1-100nm之间 C. 氢氧化铁胶体可发生丁达尔效应 D. 往氢氧化铁胶体中滴加电解质溶液可发生聚沉现象 5.证明某溶液只含有Fe2+而不含有Fe3+的实验方法是( ) A.先滴加氯水,再滴加KSCN溶液后显红色 B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色 C.滴加NaOH溶液,产生红褐色沉淀 D.只需滴加KSCN溶液 6.下图所示的实验操作,能达到相应目的的是 A. 用图1装置配制100 mL 0.1 mol·L-1硫酸 B. 用图2所示装置可萃取碘水中的碘 C. 用图3所示装置可制备氢氧化亚铁 D. 用图4所示装置可吸收HCl气体 7.下列实验的现象与对应结论均正确的是( ) 选项 操作 现象 结论 A 在AlCl3溶液中滴加过量氨水 有白色沉淀生成 实验室常用此法制备Al(OH)3 B 常温下将Al片放入浓硝酸中 无明显变化 Al与浓硝酸不反应 C 取少量Fe(NO3)2试样加水溶解,加稀H2SO4酸化 滴加KSCN溶液,溶液变为红色 该Fe(NO3)2试样已经变质 D 将水蒸气通过灼热的铁粉 粉末变红 铁与水在高温下发生反应 8.向某无色溶液中分别进行下列操作,所得现象和结论正确的是( ) A. 加入氨水,产生白色沉淀,证明原溶液中存在Al3+ B. 加入AgNO3溶液,产生白色沉淀,证明原溶液中存在Cl- C. 加入盐酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中存在SO42- D. 加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH4+ 9.如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是 A. 若a为浓硫酸,b为Na2SO3固体,c中盛石蕊溶液,则c中溶液先变红后褪色 B. 若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液不褪色 C. 若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊 D. 若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀 10.已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示。则甲和X 不可能是 A. 甲为C,X为O2 B. 甲为SO2,X为NaOH溶液 C. 甲为Fe,X为Cl2 D. 甲为AlCl3,X为NaOH溶液 11.下列反应的离子方程式书写正确的是( ) A. 4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合4AlO2-+7H++H2O=3Al(OH)3↓+Al3+ B. 硫酸氢钠溶液与氢氧化钡溶液混合显中性:H++SO42ˉ+Ba2++OH-===H2O+BaSO4↓ C. 稀硝酸中加入过量的铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O D. 向AlCl3溶液中加入过量氨水: Al3++4NH3·H2O= AlO2-+4NH4++2H2O 12.向只含有Fe3+、Cu2+、H+各0.1mol及a mol SO42-的某溶液中加入足量锌粉,搅拌使其充分反应,下列说法中正确的是( ) A. 当消耗13克Zn时, 得到的还原产物为0.25mol B. 当溶液中不再产生气泡时,溶液中大量存在的阳离子只有Zn2+ C. 反应中最多有两种单质生成 D. 反应结束时,可得到0.25molZnSO4 13.将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是 A.与NaOH反应的氯气一定为0.3 mol B.若反应中转移的电子为n mol,则0.15<n<0.25 C.n(Na+):n(Cl-)可能为7:3 D.n(NaCl):n(NaClO):n(NaClO3)可能为8:2:1 14.有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于某一反应中的反应物和生成物。下列叙述不正确的是( ) A. 该反应一定为氧化还原反应 B. 若NH4+为产物,则Fe3+也是产物 C. 该反应过程中,溶液的pH不断增大 D. 该反应的离子方程式中,Fe2+、NH4+两者计量数之比为1:8 15.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是 ( ) 选项 现象 解释 A 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色 该溶液中一定含有Na+,一定无K+ B SO2能使酸性高锰酸钾溶液褪色 SO2具有漂白性 C 某溶液中先加入稀盐酸无现象,再加入氯化钡溶液,有白色沉淀生成 该溶液中一定含有SO42﹣ D 铁加入稀硝酸中有气泡产生 铁与稀硝酸发生了置换反应 16.24mL浓度为0.05mol·L-1 Na2SO3溶液恰好与20mL 浓度为0.02mol·L-1 的 K2X2O7 溶液完全反应,已知Na2SO3 可被K2X2O7 氧化为Na2SO4 ,则元素X 在还原产物中的化合价为( ) A. +2 价 B. +3 价 C. +4价 D. +5价 17.NA表示阿伏加德罗常数,下列说法正确的是( ) A.2 mol·L-1 的Na2SO4溶液中含有4 NA个Na+ B.将含有0.1 mol FeCl3的饱和溶液逐滴滴入足量沸水中,得到Fe(OH)3胶体数目为0.1 NA C.在标准状况下,11.2 L氖气中含有NA个氖原子 D.7.8 g Na2O2中阴离子数目为0.1NA 18.下列对有关实验描述和解释正确的是( ) A. SO2气体通入酸性高锰酸钾溶液中,使高锰酸钾褪色说明SO2有漂白性 B. 浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸 C. 常温下,将铝、铁片放入浓硫酸、浓硝酸中,无明显现象,说明铝、铁不与冷的浓硫酸、浓硝酸反应 D. 向CuSO4溶液中加入一小块金属钠,则钠与Cu2+反应可置换出铜 19.对于某盐溶液的检验,其结论一定正确的是( ) A. 加入稀盐酸产生无色气体,该气体可使澄清石灰水变浑浊,则一定含有CO32- B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定含有SO42- C. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则一定含有NH4+ D. 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,则一定含有Ba2+ 20.把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液加热,恰好使NH4+完全转化为NH3逸出,另取一份加入含bmolHCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( ) A. (2b-a)mol/L B. (10b-5a)mol/L C. ()mol/L D. ( ) mol/L 二、非选择题((共3小题,60分) 21.(20分) 作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一.成外某化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究. I.甲同学老家在阆中,对儿时在家乡品尝到的阆中老陈醋的滋味记忆犹新,跟随父母来到成都后,总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知如图1信息: ①醋分两种,酿造醋和配制醋.正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋. ②酿造醋国家标准为醋酸含量必须大于3.50g/100mL,而配制醋国家标准仅为1.50g~3.50g/100mL. ③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L. (1)请帮助甲同学计算从超市购买的食醋中醋酸含量为_____g/100mL,属于_____醋(填“酿造”或“配制”).(提示:醋酸摩尔质量为60g/mol) (2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_____。 II.如图1是成外化学实验室浓盐酸试剂标签上的部分内容.乙同学现用该浓盐酸配制100mL 1mol•L﹣1的稀盐酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒.请回答下列问题: (1)配制稀盐酸时,还缺少的仪器有_____; (2)经计算,配制100mL1mol•L﹣1的稀盐酸需要用量筒量取上述浓盐酸的体积为_____mL(保留小数点后一位); (3)对所配制的稀盐酸进行测定,发现其浓度小于1mol•L﹣1,引起误差的原因可能是_____。 A.定容时俯视容量瓶刻度线 B.容量瓶在使用前未干燥,里面有少量蒸馏水 C.转移溶液后,未洗涤烧杯和玻璃棒 D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 III.丙同学对课堂上学到的胶体的相关知识产生了浓厚兴趣. (1)他利用买来的鸡蛋的蛋清配制成溶液,用激光笔照射溶液,发现一条光束穿过鸡蛋清溶液,此现象称为_____。 (2)他将乙同学配制好的盐酸溶液加入到鸡蛋清溶液中,发现出现絮状沉淀,此现象称为_____。 IV.丁同学试图测定CO2的相对分子质量. ①利用丙同学用完后剩下的鸡蛋壳和乙同学配制好的稀盐酸溶液制备CO2; ②查询相关书籍后,设计了如图2所示装置: (1)其他同学认为B装置在此处没必要,请简述原因_____。 (2)A装置中的饱和NaHCO3溶液可以吸收_____。 (3)实验前测得C装置(含水)重量为50.00g,实验完毕后C装置(含水)重量为40.02g,D中量筒读数为10.0mL,已知H2密度为0.09g/L(以上数据均已折合为标况下数值),请根据以上数据,计算CO2的相对分子质量为_____(保留小数点后一位). 22. (20分)某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸 ②Na+水 请回答下列问题: (1)写出①、②反应的离子方程式 ①__________________________________________; ②________________________________________________________ (2)在点燃H2之前必须先进行_______________________________________。 (3)实验小组在点燃用上述装置制得的H2时,①实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因_____________________ (4)实验小组查阅钠、苯、水的密度分别为0.97g/mL、0.88g/mL、1.00g/mL,并据此对实验进行了改进。在改进后的实验中H2的生成速率会_______________。改进后的实验现象为___________________。 (5)2.3 g钠投入20 mL水中完全反应放出的气体在标准状况下的体积是____________,所得溶液的物质的量浓度是______________________。(不计溶液体积的变化) 23. (20分)氯及其化合物有广泛用途。 (1)二氧化氯是一种新型的消毒剂。 ①NaClO2中Cl的化合价为____________。 ②实验室用氯酸钾与浓盐酸反应制备ClO2,产物除ClO2外,还有Cl2,KCl等,写出该反应的化学方程式 __________。若生成11.2L氯气(标准状况),转移电子数为 _________。 ③ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的_________倍。 ④自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1﹣0.8 mg•L-1之间。碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下: Ⅰ.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。 Ⅱ.加入一定量的Na2S2O3溶液。(己知:2S2O32-+I2═S4O62-+2I-) Ⅲ.加硫酸调节水样pH至1﹣3。 请问答: 若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol•L-1的Na2S2O3溶液10mL.则水样中ClO2的浓度是_____ mg•L-1。 (2)ICl,ICl3的化学性质与卤素相似,被称为卤素互化物。三氯化碘(ICl3,其中Cl为-1价)常以二聚体的I2Cl6形式存在,经电导仪测定知,它能发生部分电离,生成的两种离子的摩尔质量分别为198 g/mol和269 g/mol,则其电离方程式为 ________________ 。 (3)向盛有一定量的溴化亚铁溶液和四氯化碳溶液的试管中持续通入氯气,反应完毕后,振荡、静置、分层,发现有机层呈红棕色,经检验生成了BrCl(其中Cl为-1价)。可能发生如下反应: ①2Br-+Cl2=2Cl-+Br2 ②Br2+Cl2=2BrCl ③2Fe2++Cl2=2Fe3++2Cl- 按通入氯气,发生先后反应的顺序为 ____________(填序号)。 参考答案 1.A 2.B 3.B 4.A 5.B 6.C 7.A 8.D 9.A 10.C 11.A 12.A 13.B 14.D 15.C 16.B 17.D 18.B 19.C 20.B 21. 4.50 酿造 CaCO3+2CH3COOH═Ca2++2CH3COO﹣+CO2↑+H2O 100mL容量瓶 8.5 CD 丁达尔效应 胶体的聚沉 排水法收集气体,不需要对气体进行干燥 HCl 44.4 22. (1)Zn+2H+=Zn2++ H2↑ 2Na+2H2O = 2Na++2OH-+H2↑ (2)检验H2的纯度 (3)大块的钠与水反应剧烈,放出大量的热,可能使试管内H2和O2的混合气点燃而爆炸 (4)减缓 钠处于苯和水的交界处,钠与水反应产生的H2使钠浮起,脱离水面,反应停止,当钠表面的H2逸出,钠又回落水层,如此反复,钠间歇与水反应 (5) 1.12L 5mol/L 23. (一) ①+3 ②2KClO3+4HCl=2KCl+2ClO2↑+Cl2↑+2H2O NA或6.02×1023 ③2.5 (二) (1)0.675 mg•L-1 (2)I2Cl6ICl2++ICl4- (3) ③①②查看更多