- 2021-07-02 发布 |
- 37.5 KB |
- 14页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
【化学】广东省深圳外国语学校2019-2020学年高一上学期期中考试试题(解析版)
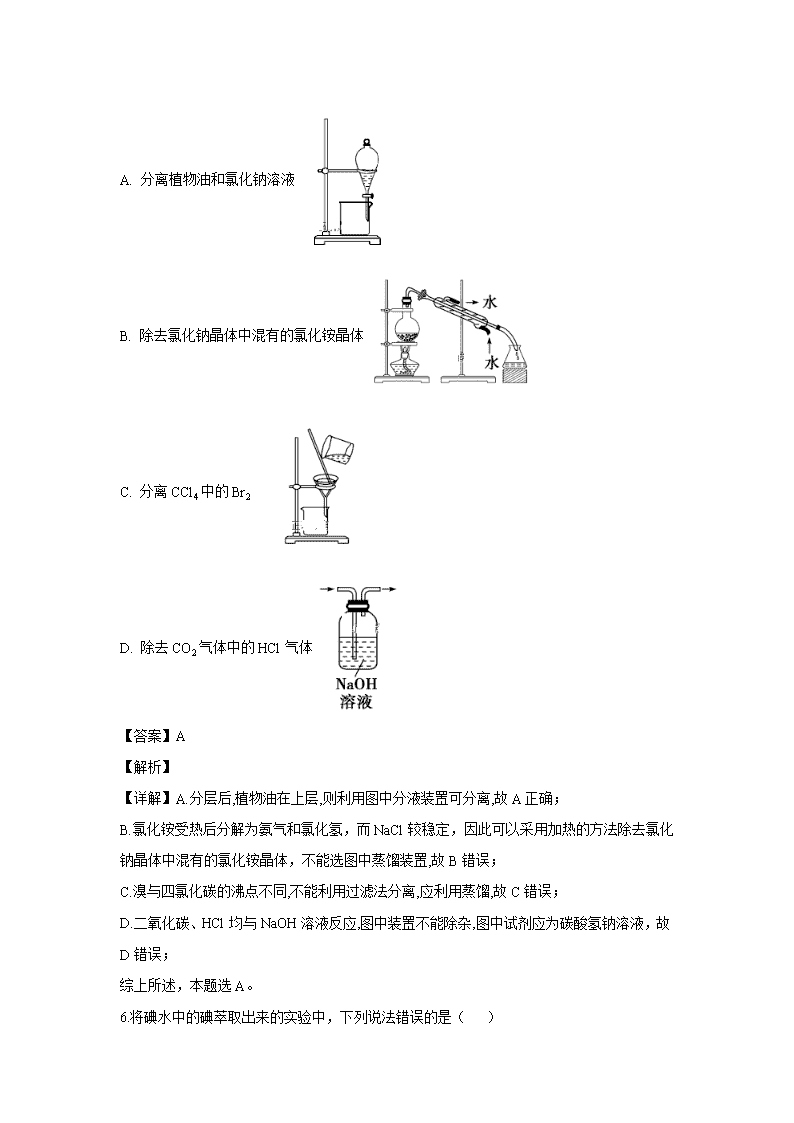
广东省深圳外国语学校2019-2020学年高一上学期期中考试试题 一、单选题(共16题,每题3分,共48分) 1.下列关于古籍中的记载说法不正确的是( ) A. 《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应 B. 《吕氏春秋•别类编》中“金(即铜)柔锡柔,合两柔则刚”体现了合金硬度方面的特性 C. 《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应 D. 《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油 【答案】C 【解析】A. 《天工开物》中“凡石灰,经火焚炼为用”涉及的是碳酸钙的受热分解,故A正确;B. 合金的硬度一般大于成分金属,“金(即铜)柔锡柔,合两柔则刚”体现了合金硬度方面的特性,故B正确;C. 《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应的条件不同,不属于可逆反应,故C错误;D. “高奴县有洧水可燃”,这里的“洧水”指的是石油,石油能够燃烧,故D正确;故选C。 2. 下列说法都正确的是( ) ①江河入海口三角洲的形成通常与胶体的性质有关 ②蔗糖、硫酸钡和纯碱分别属于非电解质、弱电解质和强电解质 ③用玻璃棒搅拌漏斗中的液体以加快过滤速度 ④在容量瓶中加入一体积的水,再加入浓硫酸配制准确浓度的稀硫酸 ⑤常用的自来水消毒剂有氯气和二氧化氯,氯气的消毒效率低于二氧化氯。 A. ②③⑤ B. ②④ C. ①⑤ D. ①④ 【答案】C 【解析】 【详解】①江河中的泥沙属于胶体分散系,海水中含有电解质氯化钠,胶体遇电解质发生聚沉,①正确; ②蔗糖属于非电解质,硫酸钡和纯碱都是盐,属于强电解质,②错误; ③用玻璃棒搅拌漏斗中的液体,会导致滤纸坏掉,不能起到过滤作用,③错误; ④稀释浓硫酸应该在烧杯中进行,不能在容量瓶中进行,④错误; ⑤ 常用的自来水消毒剂有氯气和二氧化氯,1mol氯气反应获得2mol电子,而1mol二氧化氯反应获得5mol电子,因此氯气的消毒效率低于二氧化氯,⑤正确; 则说法正确的序号为①⑤; 故合理选项是C。 3. 进行化学实验时必须要有安全意识,下列做法错误的是( ) A. 加热试管或烧杯时,应首先擦干外壁上的水 B. 不慎将浓碱溶液溅到皮肤上,要立即用大量水冲洗,然后再涂硼酸溶液 C 温度计摔坏导致水银散落到地面上,应立即用水冲洗水银 D. 酒精及其它易燃有机物小面积失火,应迅速用湿抹布扑灭,烫伤(灼伤)要就医 【答案】C 【解析】A正确,防止试管炸裂;B正确,不慎将浓碱溶液溅到皮肤上,要立即用大量水冲洗,然后再涂硼酸溶液;C错,温度计摔坏导致水银散落到地面上,应立即用硫粉处理;D正确,小面积失火,应迅速用湿抹布扑灭,烫伤(灼伤)要就医; 4.对于易燃、易爆、有毒的化学物质,往往会在其包装上贴上危险警告标签。下面所列的物质中,标签贴错了的是( ) 【答案】C 【解析】 【详解】A.浓硫酸具有强烈的腐蚀性,应贴腐蚀品标志,符合题意,故A正确; B.汽油属于易燃物,应贴易燃液体标志,符合题意,故B正确; C.乙醇属于易燃物,不属于剧毒品,应贴易燃液体的标志,故C错误; D.硝酸铵属于易爆物,应贴爆炸品的标志,符合题意,故D正确; 答案选C。 5.完成下列实验所需选择的装置或仪器都正确的是( ) A. 分离植物油和氯化钠溶液 B. 除去氯化钠晶体中混有的氯化铵晶体 C. 分离CCl4中的Br2 D. 除去CO2气体中的HCl气体 【答案】A 【解析】 【详解】A.分层后,植物油在上层,则利用图中分液装置可分离,故A正确; B.氯化铵受热后分解为氨气和氯化氢,而NaCl较稳定,因此可以采用加热的方法除去氯化钠晶体中混有的氯化铵晶体,不能选图中蒸馏装置,故B错误; C.溴与四氯化碳的沸点不同,不能利用过滤法分离,应利用蒸馏,故C错误; D.二氧化碳、HCl均与NaOH溶液反应,图中装置不能除杂,图中试剂应为碳酸氢钠溶液,故D错误; 综上所述,本题选A。 6.将碘水中的碘萃取出来的实验中,下列说法错误的是( ) A. 分液漏斗使用前要检验它是否漏水 B. 萃取剂要求不溶于水,且比水更容易使碘溶解 C. 注入碘水和萃取剂,倒转分液漏斗反复用力震荡后立即分液 D. 分液时,打开旋塞,使下层液体从下口流出,上层液体从上口倒出 【答案】C 【解析】 【详解】A.为防止漏液,使用前要检查分液漏斗是否漏液,故A正确; B.碘在CCl4中的溶解度比在水中的溶解度大,可用四氯化碳萃取,故B正确; C.震荡后需静置分层后分液,故C错误; D.下层液体下口流出,上层液体从上口倒出,以免污染液体,故D正确; 故选C。 7.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( ) 选项 物质 选用试剂 操作方法 A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干 B CO(CO2) KOH溶液、浓硫酸 洗气、干燥 C CaO(CaCO3) 水 过滤、烘干 D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶 【答案】B 【解析】 【详解】A. Fe2O3和Fe均能与稀盐酸反应,不符合除杂原则,A项错误; B. CO2能与氢氧化钾溶液反应生成碳酸钾和水,CO不与氢氧化钾溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,B项正确; C. CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,C项错误; D. Na2CO3能与Ca(NO3)2溶液反应生成碳酸钙沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,D项错误; 答案选B。 8.现有Ag某结晶水合物(R·xH2O)受热后失去全部结晶水,质量变为ag,则R相对原子质量( ) A. B. C. D. 【答案】A 【解析】 【详解】设结晶水合物R•xH2O的相对分子质量为M,结晶水合物的质量为A克,受热失去全部结晶水后,质量为a克,则水的质量为(A-a)克,则:=,解得M=,故R相对原子质量是M-18x=-18x=,故答案为A。 9.设NA为阿伏加德罗常数值,下列说法不正确的是( ) A. 常温常压下,32gO2和32gO3所含氧原子数都是2NA B. 同温、同压下,相同体积的氟气和氩气所含的原子数相等 C. 18g D2O含有的电子数为9NA D. 2.4g金属镁变成镁离子时失去的电子数目为0.2NA 【答案】B 【解析】试题分析:32gO2和32gO3中氧元素质量均为32g,O物质的量为2mol,A正确;同温同压下,同体积的气体分子数相同,但氟气是双原子分子、氩气是单原子分子,B错误;D2O摩尔质量为20g/mol,D2O电子数为10,C正确;1个镁原子在反应中失去2个电子,D正确。 10. 在150℃时碳酸铵可以受热完全分解,则其完全分解后所产生的气态混合物的密度是相同条件下氢气密度的几倍 ( ) A. 96倍 B. 48倍 C. 12倍 D. 32倍 【答案】C 【解析】 【分析】(NH4)2CO3发生反应: NH4)2CO3=2NH3↑+H2O↑+CO2↑;由方程式可以知道, 1mol(NH4)2CO3分解生成4mol混合气体,4mol混合气体的质量等于1mol(NH4)2CO3的质量,先根据M=m/n计算混合气体的平均摩尔质量,然后利用密度之比等于摩尔质量之比计算。 【详解】碳酸铵受热发生分解,方程式为:(NH4)2CO3=2NH3↑+H2O↑+CO2↑;据反应可以知道,1mol(NH4)2CO3分解生成4mol混合气体,4mol混合气体的质量等于1mol(NH4)2CO3 的质量,则混合气平均摩尔质量为=1×96/4=24g/mol;因气体密度之比等于摩尔质量之比,所以混合气的密度是相同条件下的氢气密度的24/2=12倍; 故答案选C。 11.下列有关混合物、纯净物、电解质、非电解质的正确组合为( ) 纯净物 混合物 电解质 非电解质 A. 氯化氢 水煤气 稀硫酸 干冰 B. 蒸馏水 蔗糖溶液 氧化铝 二氧化硫 C. 胆矾 氢氧化铁胶体 铁 碳酸钙 D. 水银 澄清石灰水 氯化铜 碳酸钠 【答案】B 【解析】 【分析】依据概念结合物质组成结构进行分析判断;由同种物质组成的为纯净物,包括单质和化合物;由不同物质组成的为混合物;在水溶液或熔融状态下能导电的化合物为电解质;在水溶液和熔融状态下都不能导电的化合物为非电解质。 【详解】A. 稀硫酸是H2SO4的水溶液,属于混合物,不是电解质;A项错误; B. 蒸馏水、蔗糖溶液、氧化铝、二氧化硫分别属于纯净物、混合物、电解质、非电解质,B项正确; C. 铁是单质,既不属于电解质又不属于非电解质,碳酸钙在熔融状态下可电离,属于电解质,不属于非电解质,C项错误; D. 碳酸钠在水溶液里或熔融状态下能电离出自由移动的阴阳离子,属于电解质,不属于非电解质,D项错误; 答案选B。 12.下列离子方程式正确的是( ) A. 氢氧化钠溶液中通入足量二氧化硫:SO2+2OH ═SO32-+2H2O B. 石灰石与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ C. 向Ba(OH)2溶液加入足量的NaHSO4溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O D. 向少量碳酸氢钠溶液中滴加足量澄清石灰水:Ca2++2OH-+2HCO3- =CaCO3↓+2H2O+CO32- 【答案】C 【解析】 【详解】A. 氢氧化钠溶液中通入足量二氧化硫会生成亚硫酸氢根离子,其离子反应方程式为SO2+OH−═HSO3−,A项错误; B. 醋酸为弱电解质,在离子方程式中需保留化学式,石灰石与醋酸反应离子反应为CaCO3+2CH3COOH═2CH3COO−+Ca2++H2O+CO2↑,B项错误; C. 向Ba(OH)2溶液加入足量的NaHSO4溶液,溶液呈中性,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,C项正确; D. 向少量碳酸氢钠溶液中滴加足量澄清石灰水的离子反应为Ca2++OH−+HCO3−=CaCO3↓+H2O,D项错误; 答案选C。 13.在溶液中能大量共存,加入OH-有沉淀产生,加入H+有气体放出的是( ) A. Na+、Cu2+、Cl-、SO42- B. Fe3+、K+、SO42-、NO3- C. Na+、CO32-、OH-、NO3- D. Na+、Ca2+、Cl-、HCO3- 【答案】D 【解析】A.该组离子之间不反应,可大量共存,但加H+无气体生成,故A错误;B.该组离子之间不反应,可大量共存,但加H+无气体生成,故B错误;C.该组离子之间不反应,可大量共存,但加入OH-无沉淀生成,故C错误;D.该组离子之间不反应,可大量共存,加入OH-有碳酸钙沉淀产生,加入H+有二氧化碳气体生成,故D正确;答案为D。 点睛:考查离子共存的正误判断,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等。 14.下列说法中不正确的是( ) A. 向某未知溶液中滴加NaOH溶液,并加热,在试管口放湿润的红色石蕊试纸,可检验原溶液中是否含有NH4+ B. 向某未知溶液中滴加硝酸银溶液,若产生白色沉淀,则证明原溶液中有Cl- C. 除去FeCl2溶液中混有的FeCl3可加入过量铁粉,再过滤 D. 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制氯水,溶液变红色,则该溶液中一定含有Fe2+ 【答案】B 【解析】A. 铵盐能与氢氧化钠反应生成氨气,因此向某未知溶液中滴加NaOH溶液,并加热,在试管口放湿润的红色石蕊试纸,可检验原溶液中是否含有NH4+,A正确;B. 向某未知溶液中滴加硝酸银溶液,若产生白色沉淀,白色沉淀也可能是硫酸银,因此不能证明原溶液中有Cl-,B错误;C. 除去FeCl2溶液中混有的FeCl3可加入过量铁粉,氯化铁和铁反应生成氯化亚铁,然后再过滤即可,C正确;D. 向某溶液中加入2滴KSCN溶液,溶液不显红色,说明不存在铁离子。再向溶液中加入几滴新制氯水,溶液变红色,说明有铁离子产生,这说明该溶液中一定含有Fe2+,D正确,答案选B。 15.在标准状况下有①6.72L CH4,②3.01×1023个HCl分子,③13.6g硫化氢,④0.2mol氨气(NH3)。下列对这四种气体的关系从大到小描述不正确的是( ) A. 体积②>③>①>④ B. 密度②>③>④>① C. 质量②>③>①>④ D. 氢原子数①>④>③>② 【答案】D 【解析】 【详解】①6.72LCH4的物质的量为0.3mol,②3.01×1023个HCl分子的物质的量为0.5mol, ③13.6g硫化氢的物质的量为=0.4mol,④0.2mol氨气(NH3),则 A. 同温同压下,体积之比等于物质的量之比,所以体积②>③>①>④,A项正确; B. ①CH4相对分子质量为16,②HCl相对分子质量为36.5③硫化氢相对分子质量为34,④氨气相对分子质量为17,同温同压下,密度之比等于相对分子质量之比,所以密度②>③>④>①,B项正确; C. ①6.72L CH4的质量为0.3mol×16g/mol=4.8g,②3.01×1023个HCl分子的质量为0.5mol×36.5g/mol=18.25g,③13.6g硫化氢,④0.2mol氨气(NH3)的质量为0.2mol×17g/mol=3.4g,所以质量②>③>①>④,C项正确; D. 氢原子物质的量分别为:①0.3mol×4=1.2mol,②0.5mol,③0.4mol×2=0.8mol,④0.2mol×3=0.6mol,所以氢原子数①>③>④>②,D项错误; 答案选D。 16.标准状况下,n L 气体溶于m mL 中,得密度为 的R L的氨水,则此氨水的物质的量浓度为( ) A. B. C. D. 【答案】B 【解析】 【详解】标准状况下nL氨气的物质的量为:,该氨气的质量为:,mmL水的质量约为mg,则所得溶液质量为:,所得溶液的体积为:,所以该氨水的物质的量浓度为:;故B正确; 故答案选B。 二、非选择题(共5题,共52分) 17. 某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为: (1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于 上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在 上冷却,不能直接放在桌面上。 所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹 (2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是 。 a.灼烧过程中部分氧化铜被还原 b.灼烧不充分铜未被完全氧化 c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化 (3)通过途径II实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、_____、冷却结晶、 、自然干燥。 (4)由粗制氧化铜通过两种途径制取胆矾,与途径I相比,途径II有明显的两个优点是: 、 。 (5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验中,若测定结果x值偏高,可能的原因是 。 a.加热温度过高 b.胆矾晶体的颗粒较大 c.加热后放在空气中冷却 d.胆矾晶体部分风化 【答案】(10分,每空1分) (1)c; e; b。 (2)a; b。 (3)蒸发; 过滤。 (4)产生等量胆矾途径II消耗硫酸少; 途径II不会产生污染大气的气体。(5)a 【解析】 18.有一包白色固体粉末,其中可能含有KCl、BaCl2、Cu(NO3)2、K2CO3中的一种或几种,现做以下实验: ①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色: ②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生; ③取少量②的溶液,滴入稀硫酸,有白色沉淀产生; ④另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀。 试根据上述实验事实,回答下列问题: (1)写出原白色粉末中一定含有的物质的化学式 (2)写出原白色粉末中一定不含有的物质的电离方程式 (3)写出下列各步变化的离子方程式: ② ④ 【答案】(1) BaCl2、K2CO3(2) Cu(NO3)2=Cu2++2NO3-(3)② BaCO3+2H+=Ba2++CO2↑+H2O ④ Ag++Cl-=AgCl↓ 【解析】试题分析:将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色,说明固体中没有Cu(NO3)2。向① 的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生,说明固体中有K2CO3和BaCl2。取少量②的溶液,滴入稀硫酸,有白色沉淀产生,说明固体中有BaCl2,另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀,说明溶液中含有Cl-,KCl、BaCl2至少含有一种。所以固体中一定含有的是K2CO3和BaCl2,一定不含的是Cu(NO3)2,可能含有的是KCl。 19.海洋是人类巨大的资源宝库,如图为从海水中提取金属镁的简易流程图。 (1)海洋中含量最多的物质是______。 (2)实验室中进行操作1时,玻璃棒的作用是________。 (3)生石灰转化为石灰乳的过程是________反应(选填“吸热”或“放热”)。 (4)上述流程中未涉及到的基本反应类型是________反应。 【答案】(1). 水 (2). 引流 (3). 放热 (4). 置换 【解析】 【分析】(1)根据海洋中的物质分析回答; (2)根据玻璃棒的应用分析回答; (3)根据能量的变化分析回答; (4)根据反应的特点分析。 【详解】(1)海洋中最主要是溶剂水,则含量最多的物质是水,故答案为:水; (2)由实验的过程可知,操作I能将固液分开,操作是过滤,实验室中进行过滤时,玻璃棒 的作用是引流,故答案为:引流; (3)生石灰转化为石灰乳的过程是放热反应,故答案为:放热; (4)由题意可知,上述流程中煅烧石灰石、通电氯化镁得到了镁均发生了分解反应;生石灰转 化为石灰乳是化合反应;氢氧化钙与氯化镁反应、氢氧化镁与稀盐酸反应是复分解反应,则未涉及的反应类型为置换反应,故答案为:置换。 20.教材中有两个关于混合物分离的实验,请回答下列有关问题 实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示 (1)写出下列仪器的名称:①___________ ②_____________ (2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是______________,将仪器补充完整后进行的实验操作的名称是______________;①的进水口是__________ (填“f”或“g”) (3)仪器②中常加入碎瓷片,这样做的目的是___________________ 实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液. 其实验操作中有如下两步: ①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔. ②静置分层后,旋开活塞,用烧杯接收下层液体 (4)下层流出的是__________溶液,上层液体从_________ 得到(填“上口”或“下口”) (5)萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是( ) A.不与碘反应 B.碘在其中的溶解度大于在水中的溶解度 C.该萃取剂与水不互溶且密度不同 D.可以选用CCl4、 酒精做萃取剂. 【答案】(1). 冷凝器 (2). 蒸馏烧瓶 (3). 酒精灯 (4). 蒸馏 (5). g (6). 防止液体暴沸 (7). 含有碘单质的CCl4溶液 (8). 上口 (9). ABC 【解析】 【详解】本题主要考查物质的分离或提纯方法。 (1)下列仪器的名称:①冷凝器, ②蒸馏烧瓶。 (2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是酒精灯。将仪器补充完整后进行的实验操作的名称是蒸馏;冷凝水的流向是“下进上出”,①的进水口是g。 (3)仪器②中常加入碎瓷片,这样做的目的是防止液体暴沸。 (4)下层流出的是碘单质的CCl4溶液,上层液体从上口得到。 (5)A.不与碘反应,故A正确;B.碘在其中的溶解度大于在水中的溶解度,保证萃取效果,故B正确;C.该萃取剂与水不互溶且密度不同,保证液体显著分层,故C正确;D.酒精溶于水,不能用作萃取剂,故D错误。故选ABC。 21.下图为某市售盐酸试剂瓶标签上的部分数据。问: (1)该盐酸的物质的量浓度为_________ (2)下列实验操作会导致实验结果偏低的是( ) ①配制100g 10%的CuSO4溶液,称取10g 硫酸铜晶体溶于90g水中 ②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮 ③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为0.2g,所得溶液的浓度 ④用酸式滴定管量取用98%,密度为1.84g/cm3的浓H2SO4配制200mL 2mol•L-1的稀H2SO4时,先平视后仰视。 A.只有① B.只有② C.②③④ D.①③④ (3)已知CO和CO2的混合气体14.4g,在标准状况下所占的体积为8.96L。则该混合气体中,CO的质量为____________________g,CO2的物质的量为____________________mol。 (4)1mol氧气在放电条件下,有30%转化为臭氧(O3),则放电后所得混合气体对氢气的相对密度是( ) A.16 B.178 C.18.4 D.35.6 【答案】(1). 11.8mol/L (2). ①③④ (3). 5.6 (4). 0.2 (5). B 【解析】 【分析】(1)根据物质的量浓度c=计算出该盐酸的物质的量浓度; (2)根据操作不当对溶质的质量或溶液的体积的影响效果分析作答; (3)混合气体的体积为8.96L,则物质的量为=0.4mol,根据气体的总质量和总物质的量列方程式计算; (4)根据公式ρ= 可知,相同条件下,气体摩尔体积相同,所以不同气体的密度之比等于其摩尔质量之比,先根据转化关系计算混合气体的摩尔质量,再计算混合气体摩尔质量与氢气的摩尔质量之比。 【详解】(1)该盐酸的物质的量浓度为:c== =11.8mol/L, 故答案为:11.8mol/L; (2)① 硫酸铜晶体为CuSO4H2O,则称取10g 硫酸铜晶体溶于90g水中形成硫酸铜溶液,硫酸铜的实际质量小于10g,所配硫酸铜溶液的质量分数小于10%的,实验结果偏低,①项正确; ②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮,称取的碳酸钠晶体中水的质量增大,实验测量结果偏高,②项错误; ③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为0.2g,实际称取的药品质量减小,所配溶液的浓度偏低,③项正确; ④酸式滴定管的“0”刻度在上部,由上而下数值增大,先平视后仰视,实际量取浓硫酸的体积偏小,所配溶液浓度偏低,④项正确;故答案为:①③④; (3)混合气体的体积为8.96 L,则物质的量为=0.4mol,设混合气体中CO的物质的量为x mol,CO2的物质的量为y mol,则28x+44y=14.4①,x+y=0.4②,联立方程组解之得:x=0.2,y=0.2,所以m(CO)=0.2mol×28g/mol=5.6g,故答案为:5.6;0.2; (4)1 mol O2有30%转化为臭氧(O3),发生反应的O2为1 mol×30%=0.3 mol. 由反应3O22O3知,生成的O3为0.2 mol,故反应后所得气体为0.2 mol O3和O2为(1-0.3)mol=0.7 mol,故M==35.6 g/mol,氢气的摩尔质量是2g/mol,混合气体的摩尔质量和氢气的摩尔质量之比等于其密度之比=35.6g/mol:2g/mol=17.8,B项正确; 故答案为:B。查看更多