- 2021-07-02 发布 |
- 37.5 KB |
- 25页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
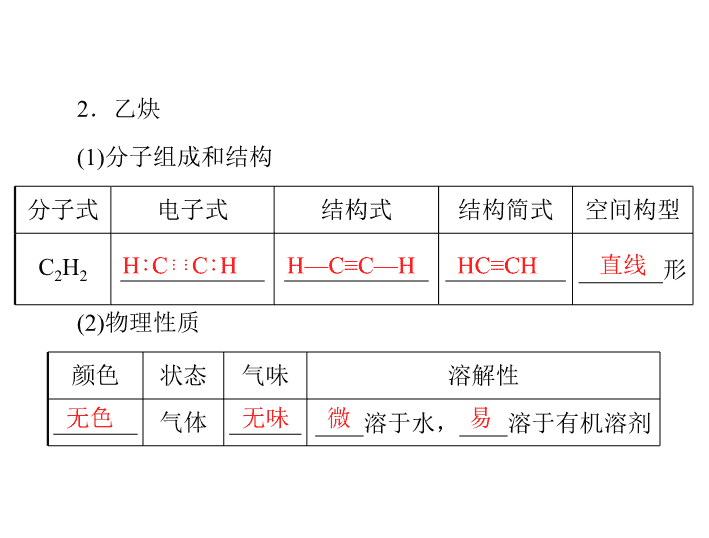
人教版选修5课件 第二章 第一节 脂肪烃 第2课时 炔烃 脂肪烃的来源及其应用
第 2 课时 炔烃 脂肪烃的来源及其应用 一、炔烃 碳碳三键 C n H 2 n - 2 1 .炔烃的概念及通式 分子里含有 _____________ 的一类脂肪烃称为炔烃。通式为 ____________ 。 分子式 电子式 结构式 结构简式 空间构型 C 2 H 2 ____________ ____________ __________ _______ 形 颜色 状态 气味 溶解性 _______ 气体 ______ ____ 溶于水, ____ 溶于有机溶剂 2 .乙炔 H∶C⋮⋮C∶H H—C≡C—H (1) 分子组成和结构 HC≡CH 直线 (2) 物理性质 无色 无味 微 易 (3) 实验室制法 CaC 2 饱和食盐水 ①药品: _______ 、 __________________ 。 ②反应原理: _______________________________ 。 图 2 - 1 - 1 ③ 发生装置:使用“固+液→气”的装置 ( 见图 2 - 1 - 1) 。 CaC 2 + 2H 2 O→Ca(OH) 2 + C 2 H 2 ↑ ④收集方法: _______________ 。 排水集气法 (4) 化学性质 明亮 浓烟 含碳量高 ①氧化反应 a .燃烧:乙炔燃烧时,火焰 ________ 并伴有 _________ , 这是由于乙炔 ___________________ 的缘故。燃烧的化学方 程式 为 ______________________________ 。 b .乙炔易被氧化剂氧化,如使酸性 KMnO 4 溶液褪色。 ②加成反应 a .使溴的 CCl 4 溶液褪色 CH≡CH + Br 2 →_______________ ; CHBr CHBr CHBr 2 CHBr 2 CH≡CH + 2Br 2 →______________ 。 b .与 H 2 加成 CH≡CH + H 2 CH 2 CH 2 CH≡CH + 2H 2 CH 3 — CH 3 c .与 HCl 加成 CH≡CH + HCl CH 2 CHCl _________________ ; _________________ 。 __________________ 。 二、脂肪烃的来源及其应用 1 .来源 石油 天然气 (1) 脂肪烃的来源有 ________ 、 __________ 、 _____ 等。 (2) 石油通过常压分馏可以得到石油气、汽油、 ________ 、 ________ 等;而减压分馏可以得到滑润油、 ________ 等相对分 子质量较大的烷烃;通过石油的催化裂化及裂 解可以得到较多 的轻质油和 ______________ ;催化重整是获得 __________ 的主 要途径。 气态烯烃 芳香烃 2 .应用:燃料、化工原料。 煤 煤油 柴油 石蜡 乙烷 乙烯 乙炔 结构简式 CH 3 — CH 3 HC≡CH 结构特点 全部单键; 饱和链烃; 四面体结构 含碳碳双键;不饱 和链烃;平面形分 子,键角 120° 含碳碳三键;不饱 和链烃;直线形分 子,键角 180° 物理性质 无色气体,难溶于水而易溶于有机溶剂 乙烷、乙烯、乙炔的比较 乙烷 乙烯 乙炔 化 学 性 质 化学活 动性 稳定 活泼 活泼 取代 反应 光照发生卤代 加成 反应 能与 H 2 、 X 2 、 HX 、 H 2 O 、 HCN 等发 生加成反应 续表 乙烷 乙烯 乙炔 化 学 性 质 氧化 反应 燃烧火焰较明 亮 燃烧火焰明亮,带 黑烟 燃烧火焰很明 亮,带浓黑烟 不与酸性 KMnO 4 溶液 反应 使酸性 KMnO 4 溶 液褪色 使酸性 KMnO 4 溶 液褪色 加聚 反应 不能发生 能发生 能发生 鉴别 溴水不褪色; 酸性 KMnO 4 溶液不褪色 溴水褪色;酸性 KMnO 4 溶液褪色 续表 实验室制取乙炔的注意事项 1 .因电石与水反应很剧烈,应选用分液漏斗,以便控制水 的流速。 2 .为获得平稳的乙炔气流,常用饱和食盐水代替水。 3 .不能用启普发生器制取乙炔。因该反应剧烈,放出大量 的热,会损坏启普发生器,且生成的 Ca(OH) 2 是糊状物,会堵 塞反应容器,使水面难以升降。 4 .由于电石制得的乙炔中往往含有 H 2 S 、 NH 3 等杂质,使 混合气体通过盛有 CuSO 4 溶液的洗气瓶可使杂质除去。 炔烃的性质 【 例 1 】 下列有关乙炔性质的叙 述中,既不同于乙烯又不 同于乙烷的是 ( ) 。 A .能燃烧生成二氧化碳和水 B .能发生加成反应 C .能与酸性高锰酸钾溶液 发生氧化反应 D .能与氯化氢反应生成氯乙烯 【 解析 】 乙炔、乙烯、乙烷都能燃烧生成二氧化碳和水; 乙炔、乙烯都能与溴水发生加成反应;乙炔、乙烯都能与酸性 KMnO 4 溶液发生氧化反应;只有乙炔可与 HCl 发生加成反应生 成氯乙烯。 【 答案 】 D 1 .既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔 的方法是 ( ) 。 A .通入足量的溴的四氯化碳溶液 B .与足量的氢氧化钠溶液反应 C .点燃 D .在一定条件下与氢 气加成 解析: A 项,乙 烷不能与溴反应,乙炔能与溴反应生成 CHBr 2 CHBr 2 而被吸收, A 正确;乙烷、乙炔都不能与 NaOH 溶液反应,二者点燃时都能燃烧, B 、 C 项均错误; D 项,乙炔 与氢气反应条件要求高,且会引入新的杂质氢气, D 项错误。 答案: A 2 .用乙炔为原料制取 CH 2 Br— CHBrCl ,可行的反应途径 是 ( ) 。 D A .先加 Cl 2 ,再加 Br 2 B .先加 Cl 2 ,再加 HBr C .先加 HCl ,再加 HBr D .先加 HCl ,再加 Br 2 乙炔的实验室制备 【 例 2 】 用电石制备 的乙炔气体中常混有少量 H 2 S 气体。 请用图 2 - 1 - 2 中的仪器和药品组成一套制备、 净化、验证乙 炔性质的装置,并通过测定乙炔的量,从而计算电石的纯度。 图 2 - 1 - 2 (1) 进行实验时,所制气体从左向右的流向,仪器的正确连 接顺序是 _________________________________( 填接口字母 ) 。 (2) 为了使实验中气流平稳,甲中分液漏斗里的液体 X 通常 用 __________________ 。 (3) 若在标准状况下溴水与乙炔完全反应生成 C 2 H 2 Br 4 ,已 知称取电石 m g ,测得量筒内液体体积为 V mL ,则电石纯度可 表示为 ______________________ 。 (4) 若没有除 H 2 S 的装置,测定结果将会 ______( 填“偏 高”、“偏低”或“不变” ) ,理由是 ______________________ _____________________________________________________ 。 【 解析 】 电石与足量水反应生成乙炔,其中混有的 H 2 S 可 用 NaOH 溶液吸收,乙炔气体被溴水吸收后剩 余部分通过排水 法测量体积。若无除 H 2 S 装置,则排出水的体积偏大,计算出 的结果偏高。设电石中 CaC 2 的物质的量为 x 。 【 答案 】 (1)A→G→H→E→F→D→C→B (2) 饱和 NaCl 溶液 (3) (4) 偏高 若没有除 H 2 S 的装置,其中的 H 2 S 会与 Br 2 发生 反应,消耗部分 Br 2 ,使得排水法测得的乙炔体积增大,而在计 算中将与 H 2 S 反应掉的 Br 2 忽略,使得计算结果偏高 A .为了加快反应速率可用饱和食盐水代替水反应 B .此反应是放热反应 C .为了除去杂质气体,除了用硫酸铜溶液外还可用氢氧 化钠溶液 D .反应中不需要加碎瓷片或沸石 解析: 由于 CaC 2 与 H 2 O 反应太剧烈,为减缓反应速率, 主要措施有:以饱和食盐水代替水; 通过分液漏斗向反应器中 滴加饱和食盐水。 A 4 .在室温和大气压强下,用图 2 - 1 - 3 所示的装置进行实 验,测得 a g 含 CaC 2 90% 的样品与水完全反应产生的气体体积 为 b L 。现欲在相同条件下,测定某电石试样中 CaC 2 的质量分 数,请回答下列问题: 图 2 - 1 - 3 (1)CaC 2 与水反应的化学方程式是 ____________________ 。 (2) 若反应刚结束时,观察到的实验现象如图 2 - 1 - 3 所示, 这时不能立即取出导气管,理由是 ________________________ _______________________________________________ 。 (3) 本实验中测量气体体积时应注意到的事项有 ________ _______________________________________________ 。 (4) 如果电石试样质量为 c g 。测得气体体积为 d L ,则电石 试样中 CaC 2 的质量分数计算式 w (CaC 2 ) = _______________ 。 ( 杂质所生成的气体体积忽略不计 ) b × c 答案: (1)CaC 2 + 2H 2 O→Ca(OH) 2 + C 2 H 2 ↑ (2) 因为装置内气体的温度没有恢复到室温,气体压强还不 等于大气压强 (3) 待装置内气体的温度恢复到室温后,调节量筒使其内外 液面持平 a × d (4) ×90%查看更多