- 2021-05-13 发布 |
- 37.5 KB |
- 2页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
中考化学复习热点题型饱和溶液与不饱和溶液的转化
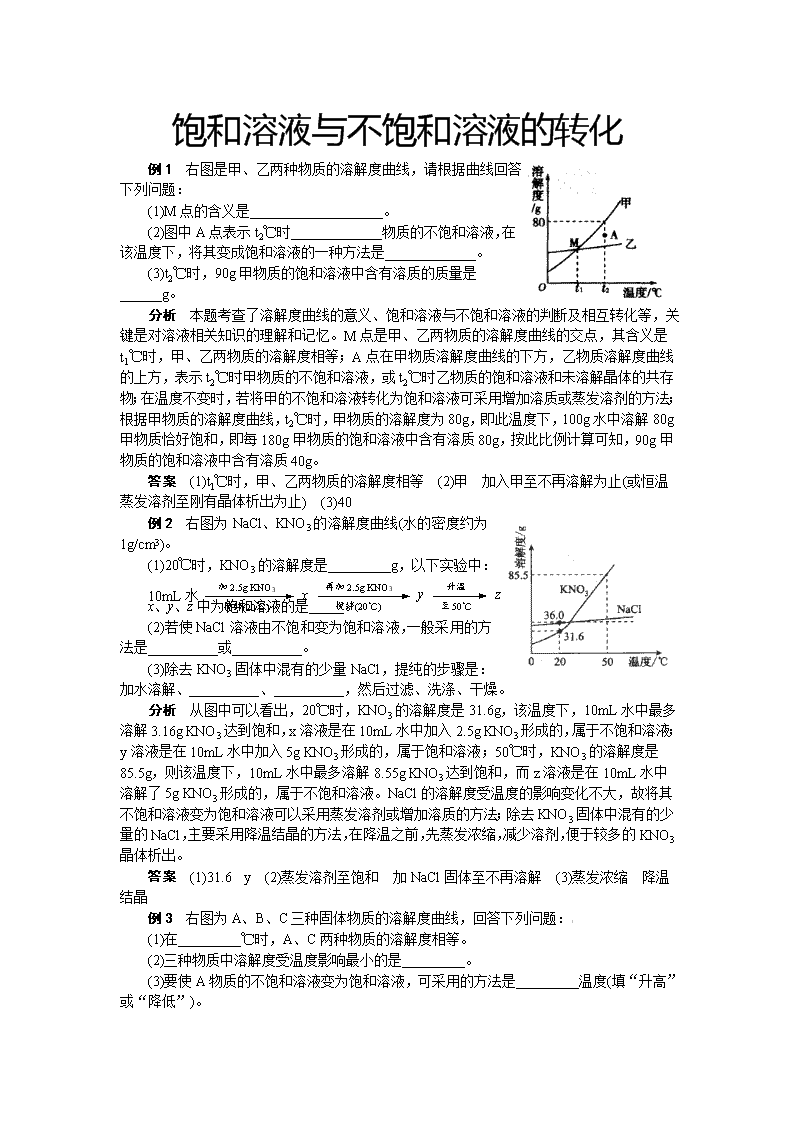
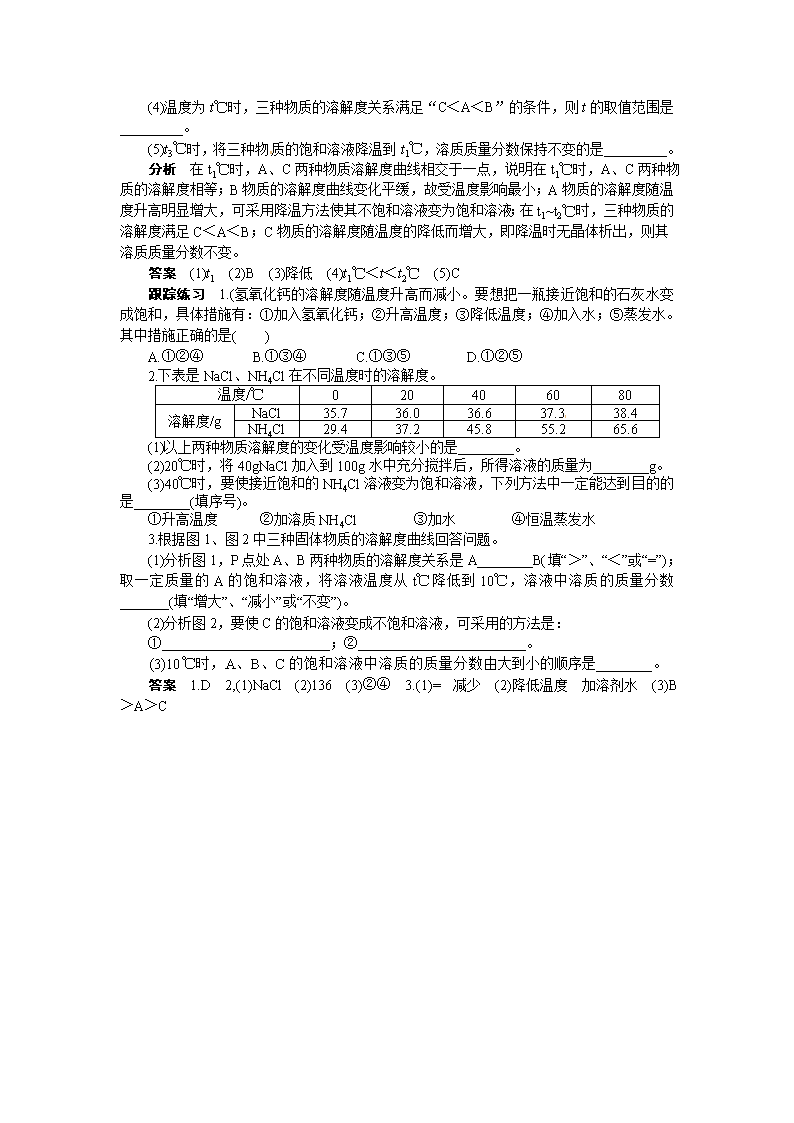
饱和溶液与不饱和溶液的转化 例1 右图是甲、乙两种物质的溶解度曲线,请根据曲线回答下列问题: (1)M点的含义是___________________。 (2)图中A点表示t2℃时_____________物质的不饱和溶液,在该温度下,将其变成饱和溶液的一种方法是_____________。 (3)t2℃时,90g甲物质的饱和溶液中含有溶质的质量是______g。 分析 本题考查了溶解度曲线的意义、饱和溶液与不饱和溶液的判断及相互转化等,关键是对溶液相关知识的理解和记忆。M点是甲、乙两物质的溶解度曲线的交点,其含义是t1℃时,甲、乙两物质的溶解度相等;A点在甲物质溶解度曲线的下方,乙物质溶解度曲线的上方,表示t2℃时甲物质的不饱和溶液,或t2℃时乙物质的饱和溶液和未溶解晶体的共存物;在温度不变时,若将甲的不饱和溶液转化为饱和溶液可采用增加溶质或蒸发溶剂的方法;根据甲物质的溶解度曲线,t2℃时,甲物质的溶解度为80g,即此温度下,100g水中溶解80g甲物质恰好饱和,即每180g甲物质的饱和溶液中含有溶质80g,按此比例计算可知,90g甲物质的饱和溶液中含有溶质40g。 答案 (1)t1℃时,甲、乙两物质的溶解度相等 (2)甲 加入甲至不再溶解为止(或恒温蒸发溶剂至刚有晶体析出为止) (3)40 例2 右图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3)。 (1)20℃时,KNO3的溶解度是_________g,以下实验中: 加2.5g KNO3 搅拌(20℃) 10mL水 x 再加2.5g KNO3 搅拌(20℃) y 升温 至50℃ z x、y、z中为饱和溶液的是_____。 (2)若使NaCl溶液由不饱和变为饱和溶液,一般采用的方法是__________或__________。 (3)除去KNO3固体中混有的少量NaCl,提纯的步骤是:加水溶解、__________、__________,然后过滤、洗涤、干燥。 分析 从图中可以看出,20℃时,KNO3的溶解度是31.6g,该温度下,10mL水中最多溶解3.16g KNO3达到饱和,x溶液是在10mL水中加入2.5g KNO3形成的,属于不饱和溶液;y溶液是在10mL水中加入5g KNO3形成的,属于饱和溶液;50℃时,KNO3的溶解度是85.5g,则该温度下,10mL水中最多溶解8.55g KNO3达到饱和,而z溶液是在10mL水中溶解了5g KNO3形成的,属于不饱和溶液。NaCl的溶解度受温度的影响变化不大,故将其不饱和溶液变为饱和溶液可以采用蒸发溶剂或增加溶质的方法;除去KNO3固体中混有的少量的NaCl,主要采用降温结晶的方法,在降温之前,先蒸发浓缩,减少溶剂,便于较多的KNO3晶体析出。 答案 (1)31.6 y (2)蒸发溶剂至饱和 加NaCl固体至不再溶解 (3)蒸发浓缩 降温结晶 例3 右图为A、B、C三种固体物质的溶解度曲线,回答下列问题:[ (1)在_________℃时,A、C两种物质的溶解度相等。 (2)三种物质中溶解度受温度影响最小的是_________。 (3)要使A物质的不饱和溶液变为饱和溶液,可采用的方法是_________温度(填“升高”或“降低”)。 (4)温度为t℃时,三种物质的溶解度关系满足“C<A<B”的条件,则t的取值范围是_________。 (5)t3℃时,将三种物质的饱和溶液降温到t1℃,溶质质量分数保持不变的是_________。 分析 在t1℃时,A、C两种物质溶解度曲线相交于一点,说明在t1℃时,A、C两种物质的溶解度相等;B物质的溶解度曲线变化平缓,故受温度影响最小;A物质的溶解度随温度升高明显增大,可采用降温方法使其不饱和溶液变为饱和溶液;在t1~t2℃时,三种物质的溶解度满足C<A<B;C物质的溶解度随温度的降低而增大,即降温时无晶体析出,则其溶质质量分数不变。 答案 (1)t1 (2)B (3)降低 (4)t1℃<t<t2℃ (5)C 跟踪练习 1.(氢氧化钙的溶解度随温度升高而减小。要想把一瓶接近饱和的石灰水变成饱和,具体措施有:①加入氢氧化钙;②升高温度;③降低温度;④加入水;⑤蒸发水。其中措施正确的是( ) A.①②④ B.①③④ C.①③⑤ D.①②⑤ 2.下表是NaCl、NH4Cl在不同温度时的溶解度。 温度/℃ 0 20 40 60 80 溶解度/g NaCl 35.7 36.0 36.6 37.3[ 38.4 NH4Cl 29.4 37.2 45.8 55.2 65.6 (1)以上两种物质溶解度的变化受温度影响较小的是________。 (2)20℃时,将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为________g。 (3)40℃时,要使接近饱和的NH4Cl溶液变为饱和溶液,下列方法中一定能达到目的的是________(填序号)。 ①升高温度 ②加溶质NH4Cl ③加水 ④恒温蒸发水 3.根据图1、图2中三种固体物质的溶解度曲线回答问题。 (1)分析图1,P点处A、B两种物质的溶解度关系是A________B(填“>”、“<”或“=”);取一定质量的A的饱和溶液,将溶液温度从t℃降低到10℃,溶液中溶质的质量分数_______(填“增大”、“减小”或“不变”)。 (2)分析图2,要使C的饱和溶液变成不饱和溶液,可采用的方法是: ①________________________;②________________________。 (3)10℃时,A、B、C的饱和溶液中溶质的质量分数由大到小的顺序是________。 答案 1.D 2,(1)NaCl (2)136 (3)②④ 3.(1)= 减少 (2)降低温度 加溶剂水 (3)B>A>C查看更多