北京市中考化学试卷含答案
2018 年北京市高级中等学校招生考试
化学试卷
学校姓名准考证号
1.本试卷共8页,共四道大题,35道小题,满分80 分.考试时间100分钟.
2.在试卷和答题卡上准确填写学校名称、姓名和准考证号.
考3.试卷答案一律填涂或书写在答题卡上,在试卷上作答无效.
生4.在答题卡上,选择题用2B铅笔作答,其他试卷用黑色字迹笔作答.
须5.考试结束,将本试卷、答题和草稿纸一并交回.
知6.本试卷化学方程式中的“”和“¾¾®”含义相同.
可能用到的相对原子质量
H1 C12 N14 O16 Na23 S32 Ca 40 Cu 64 Zn 65
一、选择题<每小题只有1个选项符合题意.共25个小题,每小题1分,共25 分)
1.空气成分中,体积分数最大的是
A.氧气B.氮气C.二氧化碳D.稀有气体
2.下列金属活动性最强的是
A.Mg B.Ag C.Cu D.Zn
3.下列食物富含蛋白质的是
A.M饭B.黄瓜C.牛肉D.苹果
4.下列物质在氧气中燃烧,产生大量白烟的是
A.木炭B.甲烷C.蜡烛D.红磷
5.决定元素种类的是
A.电子数B.质子数C.中子数D.最外层电子数
6.下列物品所使用的主要材料属于有机合成材料的是
A.塑料瓶B.纯棉衣服C.玻璃杯D.羊毛围巾
7.氢氧化钙可用于改良酸性土壤,其俗称是
A.小苏打B.熟石灰C.生石灰D.纯碱
8.为了防止骨质疏松,人体必须摄入的元素是
A.钙B.铁C.锌D.碘
9.下列方法能鉴别空气、氧气和二氧化碳3 瓶气体的是
A.闻气味B.将集气瓶倒扣在水中
C.观察颜色D.将燃着的木条伸入集气瓶中
10.下列数据是一些物质的pH,其中呈碱性的是
A.液体肥皂 B.西瓜汁 C.酱油 D.柠檬
11.能闻到花香的原因是
A.分子的质量变小B.分子间有间隔
C.分子在不断运动D.分子由原子构成
12.下列措施中,不.能.防止铁制品锈蚀的是
A.喷漆B.镀一层耐腐蚀的金属
C.制成不锈钢D.存放在潮湿的空气中
13.下列物质放入水中,能形成溶液的是
A.面粉B.牛奶C.食盐D.植物油
14.下列物质必须密封保存的是
A.木炭B.浓盐酸C.石灰石D.氯化钠
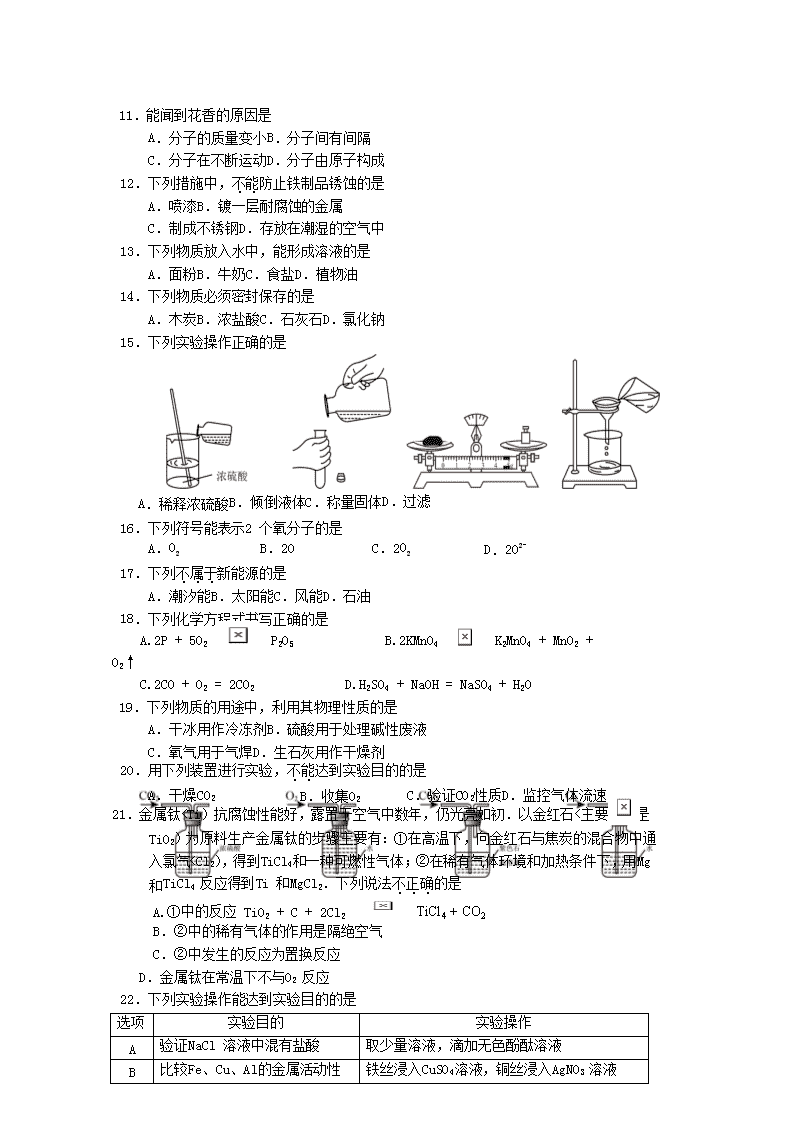
15.下列实验操作正确的是
A.稀释浓硫酸B.倾倒液体C.称量固体D.过滤
16.下列符号能表示2 个氧分子的是
A.O2
B.2O C.2O2
D.2O2-
17.下列不.属.于.新能源的是
A.潮汐能B.太阳能C.风能D.石油
18.下列化学方程式书写正确的是
A.2P + 5O2 P2O5 B.2KMnO4 K2MnO4 + MnO2 + O2↑b5E2RGbCAP
C.2CO + O2 = 2CO2 D.H2SO4 + NaOH = NaSO4 + H2Op1EanqFDPw
19.下列物质的用途中,利用其物理性质的是
A.干冰用作冷冻剂B.硫酸用于处理碱性废液
C.氧气用于气焊D.生石灰用作干燥剂
20.用下列装置进行实验,不.能.达到实验目的的是
A.干燥CO2 B.收集O2 C.验证CO2性质D.监控气体流速
21.金属钛
2
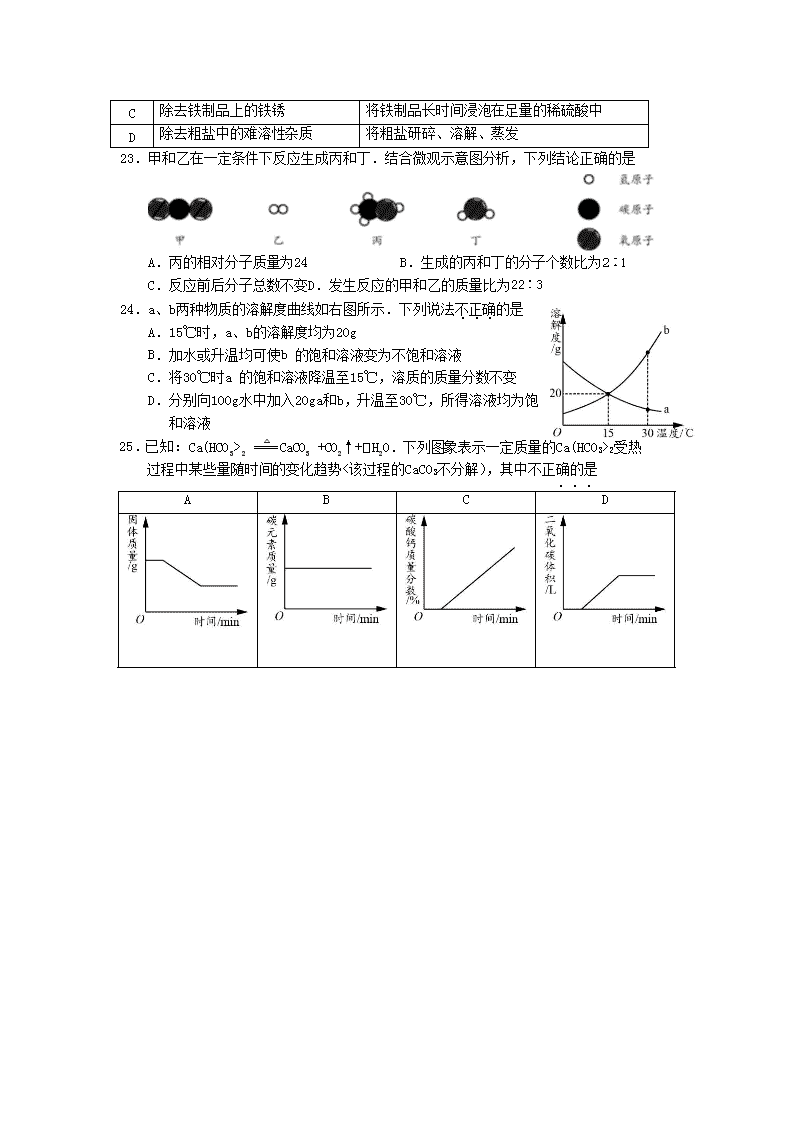
CaCO3 +CO2↑++H2O.下列图象表示一定质量的Ca(HCO3>2受热
△
过程中某些量随时间的变化趋势<该过程的CaCO3不分解),其中不正确的是
...
A
B
C
D
二、填空题<共5 个小题,共30 分)
26.<6 分)铝元素与人类关系密切.
<1)铝是地壳中含量最高的元素.
<2)元素周期表中铝元素的信息如右图所示,其原子的核外电子数为.
<3)铝元素在自然界中主要以Al2O3 存在,Al2O3 属于<填字母序号).
A.单质B.氧化物C.碱D.盐
<4)工业用电解熔融Al2O3 的方法冶炼铝,化学方程式为2Al2O3
反应属于基本反应类型中的反应.
<5)铝可制成蒸锅,主要利用铝的延展性和性.
通电冰晶石
4Al+3O2↑,该
<6)药品“氢氧化铝[Al(OH>3
]”片剂能与胃酸<主要成分为盐酸)发生中和反应,治
疗胃酸过多症,该反应的化学方程式为.
27.<6 分)水是生命之源.
<1)活性炭常用于净水,其作用是、过滤水中的杂质.
<2)生活中常用来区分硬水和软水.
<3)电解水实验如右图所示,与直流电源正极相连的玻璃管中生成的气体是,反应的化学方程式为.
<4)配制500g 溶质的质量分数为10%的葡萄糖溶液,需葡萄糖和水的质量分别为,主要步骤有称量、量取、.RTCrpUDGiT
28.<6 分)二氧化碳不仅能产生温室效应,还能作化工原料.
<1)化石燃料燃烧会产生大量的CO2 .天然气充分燃烧的化学方程式为.
<2)膜分离是一种常用的分离技术.二氧化硅2易溶于水。
④CaCl2溶液分别与NaHCO3、Na2CO3溶液等体积混合现象<表中的百分数为溶液中
溶质的质量分数):
NaHCO3
Na2CO3
0.1%
1%
5%
0.1%
CaCl2
0.1%
无明显现象
有浑浊
有浑浊
有浑浊
1%
无明显现象
有浑浊
有浑浊,有微小气泡
有沉淀
5%
无明显现象
有浑浊
有浑浊,有大量气泡
有沉淀
【进行实验】
序号
实验装置
主要实验步骤
实验现象
实验1
向2支试管中分别加入少量Na2CO3 和NaHCO3 溶液,再分别滴加盐酸
2支试管中均有气泡产生
实验2
向Ⅱ中加入试剂a,向Ⅰ中加入少量Na2CO3 或NaHCO3 固体,分别加热一段时间
Na2CO3 受热时Ⅱ中无明显现象
NaHCO3受热时Ⅱ中出现
浑浊
实验3
向Ⅱ中加入试剂a,向Ⅰ中加入少量5%的NaHCO3溶液,再滴加5%的CaCl2溶液
Ⅰ中出现浑浊,有气泡产生Ⅱ中出现浑浊
【解释与结论】
<1)实验1 中,NaHCO3与盐酸反应的化学方程式为。
<2)实验2 中,试剂a为。
<3)实验3 中,NaHCO3与CaCl2反应的化学方程式为:
2NaHCO3+ CaCl2
【反思与评价】
+++H2O。
<1)实验2 中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为<写出所有可能)。
<2)资料④中,NaHCO3 溶液与CaCl2溶液混合的现象中,有些只观察到浑浊、未观察
到气泡,原因可能是。
<3)用2种不同的方法鉴别Na2CO3 和NaHCO3固体,实验方案分别为:
①。
②。
四、计算题<共2 个小题,共6分)
△
34.<3 分)利用化学反应2Na + H2+收氢气的质量。
2NaH可实现氢气的存储,计算230g金属钠最多可吸
35.<3分)某厂烟气中SO2的平均含量为0.032g/L,用780g硫化钠3+3HCl =AlCl3 ++ 3H2O
27.<1)吸附
<2)肥皂水
通电
<3)氧气;2H2O2H2↑+ O2↑
<4)50g,450g;溶解
28.<1)CH4 +2O2 2H2O +CO2
<2)①+4;②17.7%
<3)①C,H,O;②物理;③CO2,无水乙醇
29.<1)C
<2)混合物
<3)黄铜的硬度比纯铜的硬度大
<4)①H2SO4 +Zn =ZnSO4 +H2↑
CuSO4 +Zn =ZnSO4 +Cu
②a,b,c
30.<1)火碱<烧碱,苛性钠)
<2)Fe2O3 +3CO 2Fe +3CO2
<3)Fe,O;Fe + 2HCl = FeCl2 +H2↑,Fe2O3 + 6HCl =2FeCl3 +3H2OSixE2yXPq5
<4)Ca(OH>2 +Na2CO3
31.<1)酒精灯
= CaCO3↓+ 2NaOH
<2)C;3Fe + 2O2 Fe3O4
<3)B,CaCO3 +2HClCaCl2 +H2O +CO2↑
二氧化碳的密度比空气的密度大,二氧化碳不可燃且不助燃
32.<1) 2H O 2 2H O + O ↑
MnO
2 222
<2)燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触导管口有气泡冒出,白磷燃烧6ewMyirQFL
<3)助燃性;先变大,一段时间后变小
33.<1)NaHCO3+HCl = NaCl ++H2O+CO2 ↑
<2)Ca(OH>2 溶液
<3)2NaHCO3+CaCl2【反思与评价】
= CaCO3↓++2NaCl+CO2 ↑+H2O
<1)Na2CO3;Na2CO3,NaHCO3
<2)CaCl2 溶液的溶质质量分数较小,生成的CO2 量较少,CO2溶于水,因此没有气泡
<3)①各取少量0.1%的NaHCO3 和Na2CO3加入等质量的5%的CaCl2 溶液,若无明
显现象,则为 NaHCO3,若观察到浑浊则为 Na2CO3
②各取少量Na2CO3和NaHCO3 固体于实验2装置中,若观察到澄清石灰水变浑浊,固体为NaHCO3 ,若观察到无明显现象,固体为Na2CO3kavU42VRUs
34.解:设可吸收H2质量为x
2Na+ H2
46 2
230g x
2NaH
46:2=230g:x
x=10g
答:可吸收H2质量为10g
35.解:设生成S的质量为x
2Na2S +5SO2 + 2H2O==4NaHSO3+3S↓
320 96
64gx
320:96 = 64g:x
x=19.2g
溶液质量64g +780g -19.2g =824.8g.
答:得到NaHSO3溶液的质量为824.8g
申明:
所有资料为本人收集整理,仅限个人学习使用,勿做商业用途。