- 2021-05-10 发布 |
- 37.5 KB |
- 6页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2016安庆市中考化学一模试题及答案
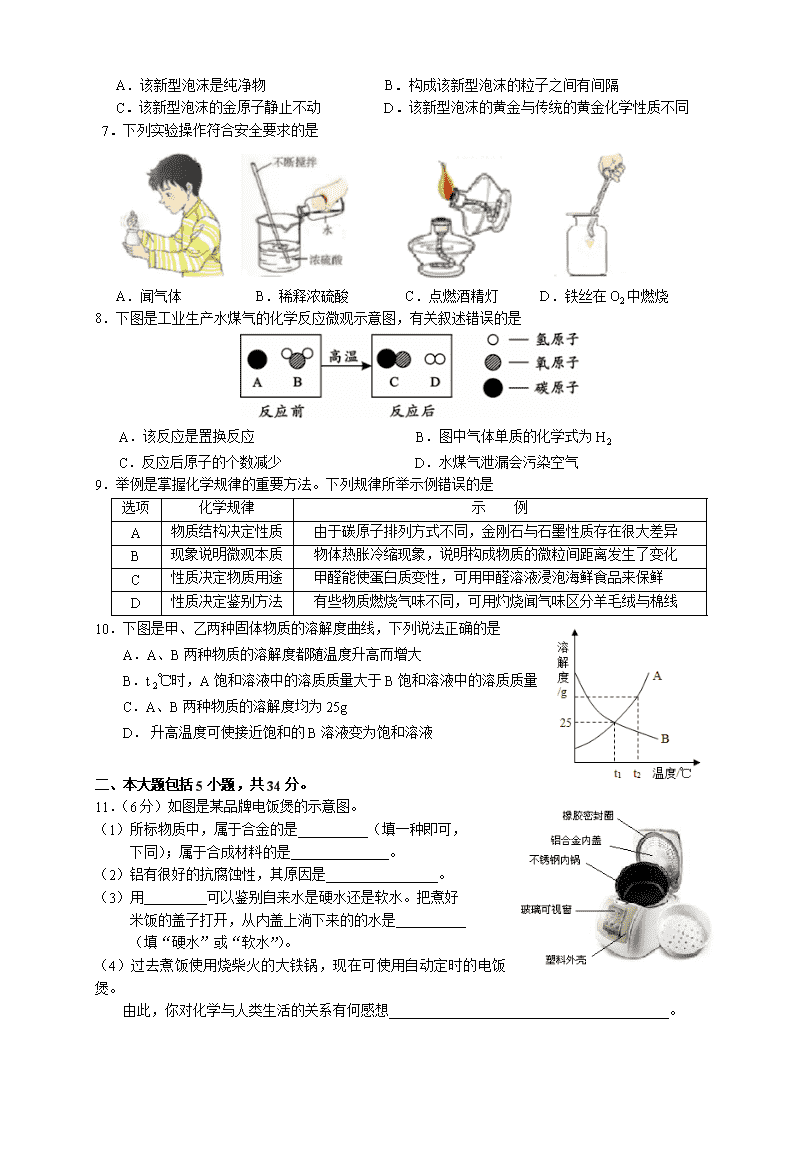
2016安庆市中考化学一模 注意事项: 1.本卷共3大题,满分60分。化学与物理的考试时间共120分钟。 2.可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 K-39 Mn-55 Cu-64 一、 本大题包括10小题,每小题2分,共20分。每小题的4个选项中只有1个答案符合题意。 1. 家庭里发生的下列变化中,属于物理变化的是 A.天燃气燃烧 B.铁钉生锈 C.豆腐切块 D.大米霉变 2.2016年4月22日是第47个世界地球日,主题是“节约集约利用资源,倡导绿色简约生活”。下列做法符合这一主题的是 A.用焚烧秸秆的灰烬给庄稼补充钾肥 B.自带布袋去农贸市场,减少使用一次性塑料袋 C.大量砍伐树木,代替煤作燃料 D. 鼓励燃煤发电,实现区域电力互惠互享 3.菜单“无鸡鸭亦可无鱼肉亦可青菜一碟足矣”是一个经典笑话。标点断句不同,吃到的食物就会不同。无论采用哪种断句方式,从均衡营养的角度分析,你认为一定还要补充的是 A.馒头 B.红烧排骨 C.胡萝卜 D.桔子 4.高锰酸钾(KMnO4)可用于检验食品中维生素C(C6H8O6)的含量。下列说法错误的是 A.高锰酸钾中锰元素的化合价为+7 B.高锰酸钾中氧元素的质量分数最大 C.维生素C属于有机化合物 D.维生素C中碳、氢、氧元素的质量比为3:4:3 5.锂常被人们誉为“金属味精”,锂元素的相关信息如图。下列有关锂的说法错误的是 A.原子的核电荷数是3 B.元素符号是Li C.相对原子质量为6.941 D.属于非金属元素 6.2015年11月26日中国科技网报道,科学家创造了一种新型泡沫,由黄金等物质组成,几乎轻如空气,仅用肉眼无法与传统黄金进行区分。下列说法正确的是 A.该新型泡沫是纯净物 B.构成该新型泡沫的粒子之间有间隔 C.该新型泡沫的金原子静止不动 D.该新型泡沫的黄金与传统的黄金化学性质不同 7.下列实验操作符合安全要求的是 A.闻气体 B.稀释浓硫酸 C.点燃酒精灯 D.铁丝在O2中燃烧 8.下图是工业生产水煤气的化学反应微观示意图,有关叙述错误的是 A.该反应是置换反应 B.图中气体单质的化学式为H2 C.反应后原子的个数减少 D.水煤气泄漏会污染空气 9.举例是掌握化学规律的重要方法。下列规律所举示例错误的是 选项 化学规律 示 例 A 物质结构决定性质 由于碳原子排列方式不同,金刚石与石墨性质存在很大差异 B 现象说明微观本质 物体热胀冷缩现象,说明构成物质的微粒间距离发生了变化 C 性质决定物质用途 甲醛能使蛋白质变性,可用甲醛溶液浸泡海鲜食品来保鲜 D 性质决定鉴别方法 有些物质燃烧气味不同,可用灼烧闻气味区分羊毛绒与棉线 10.下图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是 A.A、B两种物质的溶解度都随温度升高而增大 B.t 2℃时,A饱和溶液中的溶质质量大于B饱和溶液中的溶质质量 C.A、B两种物质的溶解度均为25g D. 升高温度可使接近饱和的B溶液变为饱和溶液 二、本大题包括5小题,共34分。 11.(6分)如图是某品牌电饭煲的示意图。 (1)所标物质中,属于合金的是__________(填一种即可, 下同);属于合成材料的是______________。 (2)铝有很好的抗腐蚀性,其原因是________________。 (3)用 可以鉴别自来水是硬水还是软水。把煮好 米饭的盖子打开,从内盖上淌下来的的水是 (填“硬水”或“软水”)。 (4)过去煮饭使用烧柴火的大铁锅,现在可使用自动定时的电饭煲。 由此,你对化学与人类生活的关系有何感想________________________________________。 12.(5分)根据右图回答问题 (1)仪器①的名称是 ,A装置的优点是 。 (2)B装置在化学实验中有广泛的用途: ① 集气:用排水法收集氧气,可在B装置装满水后, 使氧气从_________(填“a”或“b”)口进入; ② 储气:若要将储存在B中的氧气排出,水应从_______(填“a”或“b”)口进入; ③ 量气:若用B装置测量收集到的气体体积,还必须要增加的仪器是______________。 13.(7分)工业上常采用“天然碱苛化法”制取氢氧化钠。部分流程如下: (1)操作1的名称是__________,写出实验室中该操作必需的一种玻璃仪器的名称__________。 (2)写出流程中发生苛化反应的化学方程式_________________________________________。 (3)工艺中采用石灰乳而不用氢氧化钙溶液与碳酸钠反应,是因为:___________________________。 (4)生产工艺中可以回收再利用的物质是_____________。 (5)由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的是_________________________________。 14.(8分)实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式: 。某同学从课外读物中得知新鲜的肝脏中有较多的过氧化氢酶,Fe3+是一种无机催化剂,它们都可以催化过氧化氢分解。 现有实验材料如下: 新鲜的含过氧化氢酶3.5%的猪肝研磨液、3.5%的FeCl3溶液、新配制的3%的过氧化氢溶液; 量筒、滴管、试管、试管架、试管夹、小木条、火柴、酒精灯等。 某同学为比较过氧化氢酶和Fe3+催化效率,利用上述材料进行探究: 【提出问题】过氧化氢酶和Fe3+催化效率的高低 【作出猜想】 猜想1:过氧化氢酶的催化效率Fe3+高; 猜想2:Fe3+的催化效率比过氧化氢酶高。 【实验步骤】 (1)取两支洁净的试管,分别注入2mL3%的过氧化氢溶液。 (2)分别向两支试管内_____________________________________________________。 (3)将 分别放入两支试管内液面的上方,观察现象。 【实验现象与结论】 (4)观察到________________________________,证明猜想2正确。 【继续探究】 (5)该同学继续探究温度对猪肝研磨液和FeCl3溶液催化效率的影响。实验结果绘成右图,图中代表猪肝研磨液催化效果的曲线是_____,你能得到的实验结论是________________。(写一条即可) (6)你认为猪肝研磨液的催化效率还可能与________________有关。 (填一种因素即可)。 15.(8分)某研究性学习小组在探究“锌与硫酸快慢的影响因素”时,发现一个意外现象: 硫酸中混有硫酸铜溶液时,产生氢气的速率加快。 【提出问题】是什么离子导致产生氢气的速率加快? 【猜想假设】他们分别对这种意外现象作如下猜想: 甲同学:可能与铜离子有关; 乙同学:可能与硫酸根离子有关; ………… 丙同学认为乙的猜想不科学,理由是_____________________________。 【设计实验】 步骤一:检查装置气密性。检查图A所示装置气密性,你采用的方法是 ___________________________________________________。 步骤二:量取2份质量分数为20%的稀硫酸各20mL,第一份加入质量分数为10%的硫酸铜溶液1mL,第二份加入质量分数为10%的硫酸锌溶液1mL。称取2份形状相同锌粒各1g,分别与以上溶液反应。反应装置如图A所示。用此装置实验时,长颈漏斗下端要插入液面以下,目的是__________________________________________。 步骤三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125mL)所需的时间,什么时间开始收集气体? 。 【记录数据】 编号 20%的稀硫酸各20mL 锌粒 收集1瓶氢气所需的时间 ① 加入质量分数为10%的硫酸铜溶液1mL 1g 2分10秒 ② 加入质量分数为10%的硫酸锌溶液1mL 1g 3分01秒 锌与硫酸反应的化学方程式是______________________________________。 【得出结论】硫酸中混有硫酸铜溶液时,产生氢气的速率加快与____________有关。实验②中加入质量分数为10%的硫酸锌溶液1mL的作用是_____________________________________。 【注意:本题回答正确将奖励4分,但化学试卷总分不超过60分。】 【反思质疑】丁同学认为:锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与 铜单质有关,他质疑的理由是________________________________。 【继续探究】请你设计一个实验方案验证丁同学的观点是否正确。 编号 实验步骤 实验现象 实验结论 ① 取1g锌粒于锥形瓶,加入20mL 20%的稀硫酸 产生氢气的速率较快与铜单质有关 ② 三、本大题包括1小题,共6分。 16.(6分)某样品由氧化铜和铜组成,取10.0g该样品与烧杯中,向其中加入92.0g稀盐酸,恰好完全反应,最终所得溶液质量为100.0g。(化学反应方程式为:CuO+2HCl=CuCl2+H2O) (1)所取样品中铜质量为___________g (2)计算中所得溶液中溶质的质量分数。 2016安庆市中考化学一模答案 一、选择题 1 2 3 4 5 6 7 8 9 10 C B A D D B A C C D 二、填空题 11.(6分)(1)铝合金或不锈钢 塑料或橡胶(以上填构件名称也可) (2)铝在空气中与氧气反应生成致密的氧化铝薄膜 (3)肥皂水 软水 (4)化学生产出新物质,使生活更美好(合理即可) 12.(5分)(1)(长颈)漏斗 可以控制反应随时发生或停止 (2)①b ②a ③量筒或注射器 13.(7分)(1)过滤 玻璃棒、烧杯或漏斗(写一种即可) (2)Na2CO3 + Ca(OH)2 99℃~100℃ CaCO3↓+ 2NaOH (3)氢氧化钙微溶于水,溶液中的氢氧化钙含量太低,影响生成物的量 (4)碳酸钙 (5)加快溶解速率 14.(8分)2H2O2 MnO2 2H2O + O2↑; (2)分别滴入等量的猪肝研磨液和氯化铁溶液; (3)带火星的小木条; (4)滴入氯化铁溶液的试管内产生的气泡更迅速,带火星的木条易复燃(合理即可)。 (5)乙 30~40℃时,猪肝研磨液催化效果最佳(或40℃以内,温度对FeCl3溶液催化效率几乎无影响)(合理即得分) (6)猪肝研磨液中过氧化氢酶的浓度(合理即可) 15.(8分)【猜想假设】硫酸溶液中本身含有硫酸根离子 【实验验证】连接AB,用拇指堵住导管口,从长颈漏斗加水至一定高度,静置,观察液面不下降,即为气密性良好(合理即可)。 保证气体不从漏斗处逸出,等到反应开始产生气体时立刻收集 Zn + H2SO4 = ZnSO4+ H2↑ 铜离子 加入的硫酸铜溶液对硫酸浓度会产生影响,加入等量的硫酸锌溶液是为了控制硫酸浓度变化对实验数据产生干扰(答到对比实验或控制具体变量均给分) 【反思质疑】锌会与硫酸铜反应生成铜(1分) 【继续探究】 编号 实验步骤 实验现象比较 实验结论 ① ②中反应速率比①快(1分) ② 取1g锌粒于锥形瓶,加入少量铜,再加入20mL 20%的稀硫酸(2分) 三、本大题包括1小题,共6分。(1)2g (2)解:设反应所得氯化铜的质量为x CuO+2HCl=CuCl2+H2O 80 135 100g-92.0g x x=13.5g 所得溶液的溶质质量分数=13.5g/100g×100%=13.5% 答:最终所得的溶液中溶质的质量分数为13.5%。查看更多