- 2021-11-12 发布 |
- 37.5 KB |
- 10页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019九年级化学上册 第二单元 我们周围的空气 2制取氧气
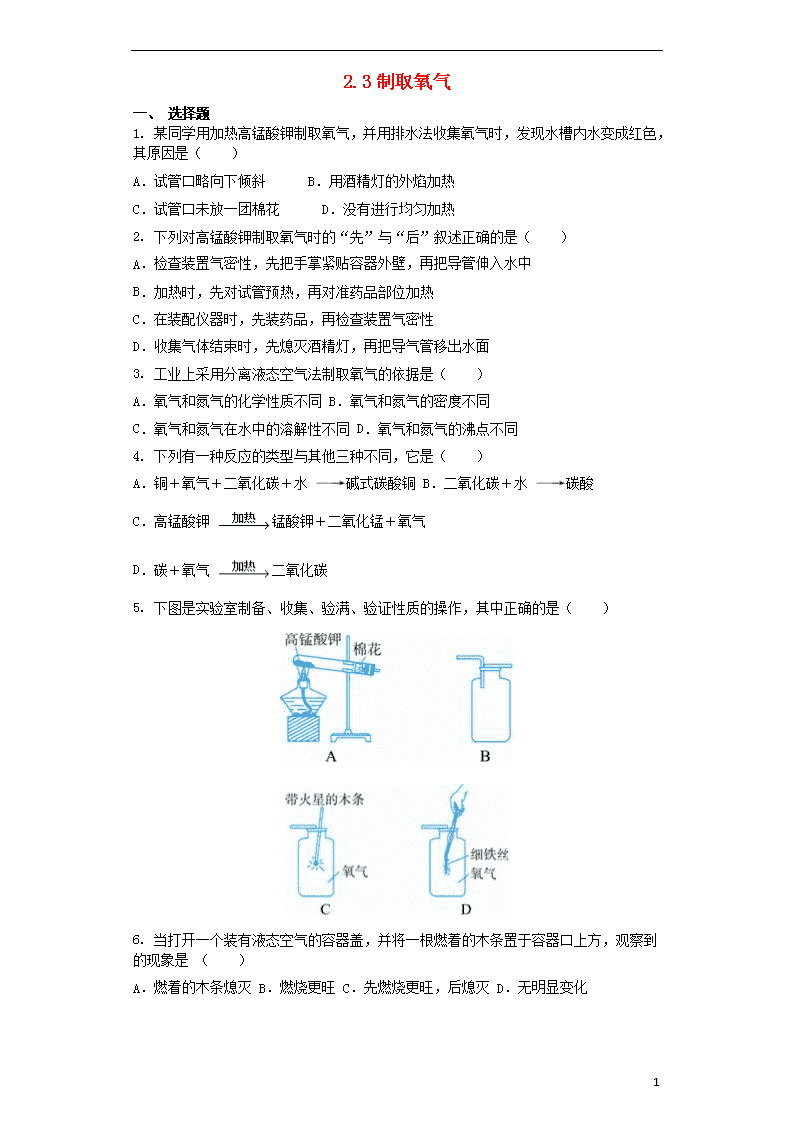
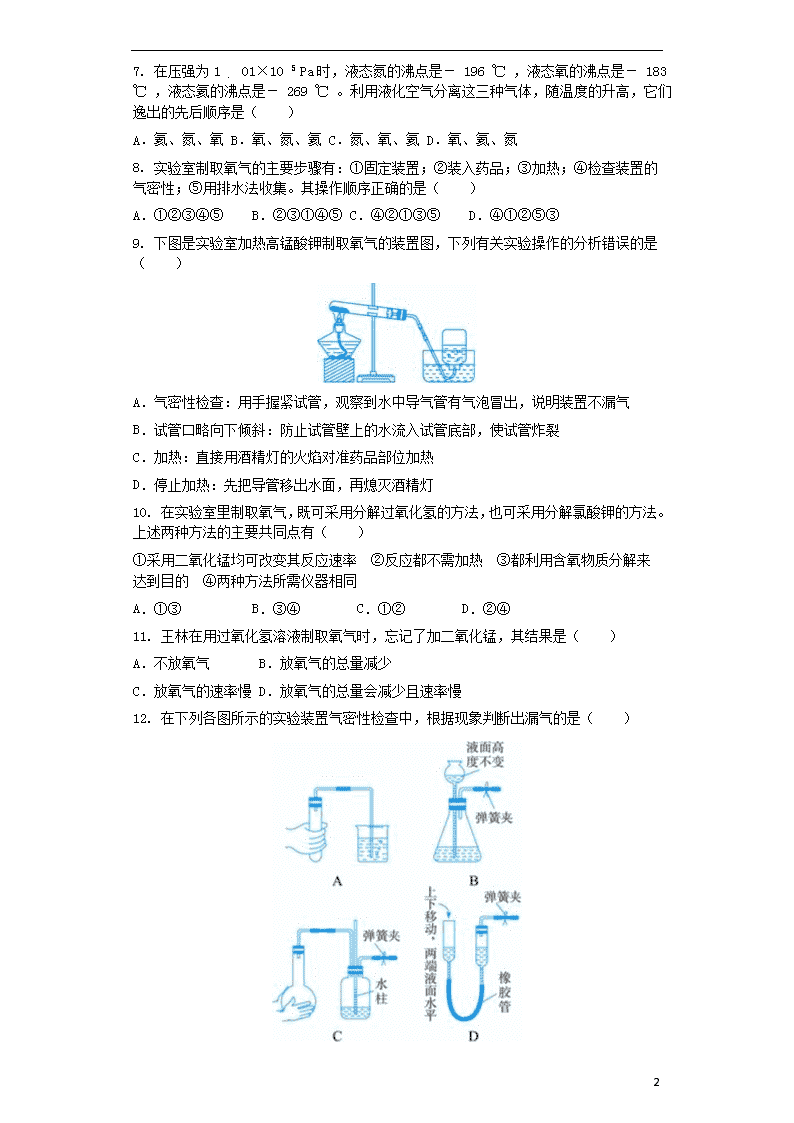
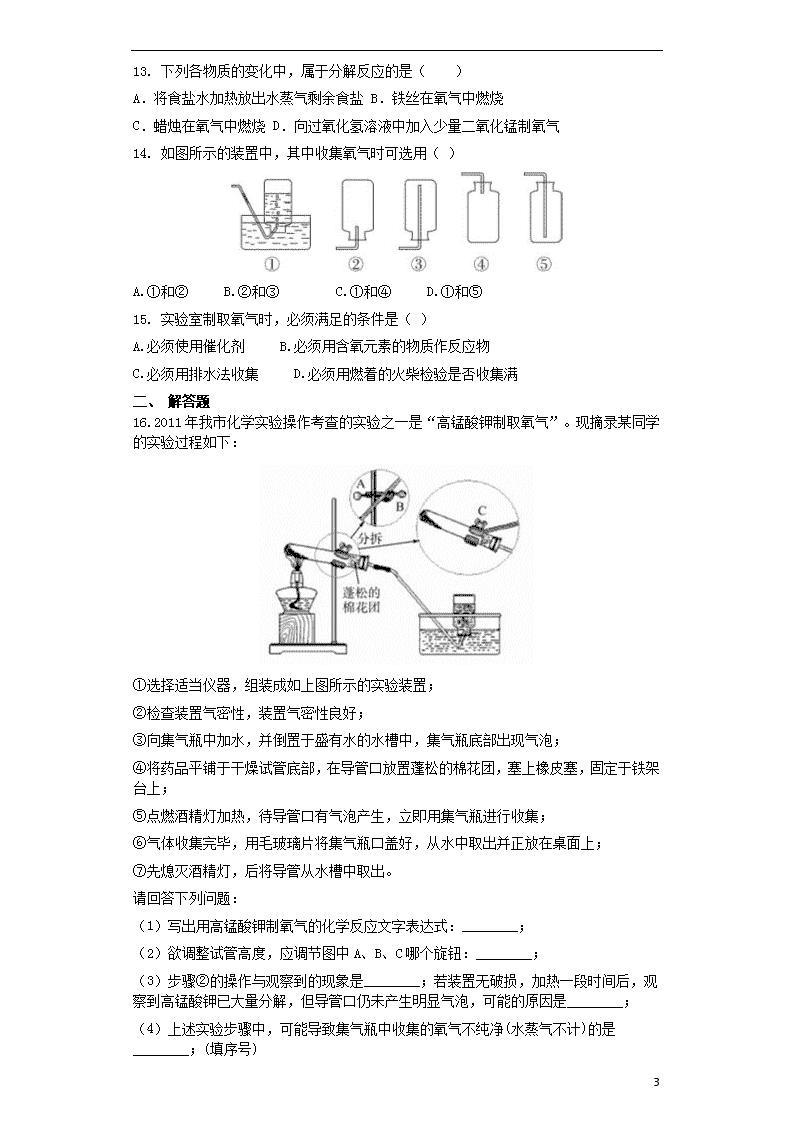
2.3制取氧气 一、 选择题 1. 某同学用加热高锰酸钾制取氧气,并用排水法收集氧气时,发现水槽内水变成红色,其原因是( ) A.试管口略向下倾斜 B.用酒精灯的外焰加热 C.试管口未放一团棉花 D.没有进行均匀加热 2. 下列对高锰酸钾制取氧气时的“先”与“后”叙述正确的是( ) A.检查装置气密性,先把手掌紧贴容器外壁,再把导管伸入水中 B.加热时,先对试管预热,再对准药品部位加热 C.在装配仪器时,先装药品,再检查装置气密性 D.收集气体结束时,先熄灭酒精灯,再把导气管移出水面 3. 工业上采用分离液态空气法制取氧气的依据是( ) A.氧气和氮气的化学性质不同 B.氧气和氮气的密度不同 C.氧气和氮气在水中的溶解性不同 D.氧气和氮气的沸点不同 4. 下列有一种反应的类型与其他三种不同,它是( ) A.铜+氧气+二氧化碳+水 碱式碳酸铜 B.二氧化碳+水 碳酸 C.高锰酸钾 锰酸钾+二氧化锰+氧气 D.碳+氧气 二氧化碳 5. 下图是实验室制备、收集、验满、验证性质的操作,其中正确的是( ) 6. 当打开一个装有液态空气的容器盖,并将一根燃着的木条置于容器口上方,观察到的现象是 ( ) A.燃着的木条熄灭 B.燃烧更旺 C.先燃烧更旺,后熄灭 D.无明显变化 7 7. 在压强为1 . 01×10 5 Pa时,液态氮的沸点是- 196 ℃ ,液态氧的沸点是- 183 ℃ ,液态氦的沸点是- 269 ℃ 。利用液化空气分离这三种气体,随温度的升高,它们逸出的先后顺序是( ) A.氦、氮、氧 B.氧、氮、氦 C.氮、氧、氦 D.氧、氦、氮 8. 实验室制取氧气的主要步骤有:①固定装置;②装入药品;③加热;④检查装置的气密性;⑤用排水法收集。其操作顺序正确的是( ) A.①②③④⑤ B.②③①④⑤ C.④②①③⑤ D.④①②⑤③ 9. 下图是实验室加热高锰酸钾制取氧气的装置图,下列有关实验操作的分析错误的是( ) A.气密性检查:用手握紧试管,观察到水中导气管有气泡冒出,说明装置不漏气 B.试管口略向下倾斜:防止试管壁上的水流入试管底部,使试管炸裂 C.加热:直接用酒精灯的火焰对准药品部位加热 D.停止加热:先把导管移出水面,再熄灭酒精灯 10. 在实验室里制取氧气,既可采用分解过氧化氢的方法,也可采用分解氯酸钾的方法。上述两种方法的主要共同点有( ) ①采用二氧化锰均可改变其反应速率 ②反应都不需加热 ③都利用含氧物质分解来达到目的 ④两种方法所需仪器相同 A.①③ B.③④ C.①② D.②④ 11. 王林在用过氧化氢溶液制取氧气时,忘记了加二氧化锰,其结果是( ) A.不放氧气 B.放氧气的总量减少 C.放氧气的速率慢 D.放氧气的总量会减少且速率慢 12. 在下列各图所示的实验装置气密性检查中,根据现象判断出漏气的是( ) 7 13. 下列各物质的变化中,属于分解反应的是( ) A.将食盐水加热放出水蒸气剩余食盐 B.铁丝在氧气中燃烧 C.蜡烛在氧气中燃烧 D.向过氧化氢溶液中加入少量二氧化锰制氧气 14. 如图所示的装置中,其中收集氧气时可选用( ) A.①和② B.②和③ C.①和④ D.①和⑤ 15. 实验室制取氧气时,必须满足的条件是( ) A.必须使用催化剂 B.必须用含氧元素的物质作反应物 C.必须用排水法收集 D.必须用燃着的火柴检验是否收集满 二、 解答题 16. 2011年我市化学实验操作考查的实验之一是“高锰酸钾制取氧气”。现摘录某同学的实验过程如下: ①选择适当仪器,组装成如上图所示的实验装置; ②检查装置气密性,装置气密性良好; ③向集气瓶中加水,并倒置于盛有水的水槽中,集气瓶底部出现气泡; ④将药品平铺于干燥试管底部,在导管口放置蓬松的棉花团,塞上橡皮塞,固定于铁架台上; ⑤点燃酒精灯加热,待导管口有气泡产生,立即用集气瓶进行收集; ⑥气体收集完毕,用毛玻璃片将集气瓶口盖好,从水中取出并正放在桌面上; ⑦先熄灭酒精灯,后将导管从水槽中取出。 请回答下列问题: (1)写出用高锰酸钾制氧气的化学反应文字表达式:________; (2)欲调整试管高度,应调节图中A、B、C哪个旋钮:________; (3)步骤②的操作与观察到的现象是________;若装置无破损,加热一段时间后,观察到高锰酸钾已大量分解,但导管口仍未产生明显气泡,可能的原因是________; (4)上述实验步骤中,可能导致集气瓶中收集的氧气不纯净(水蒸气不计)的是________;(填序号) 7 (5)步骤⑦中的操作,可能引起________。 17. 为保证长时间潜水,在潜水艇里要配备氧气再生装置。现有以下几种制取氧气的方法: ①高锰酸钾 锰酸钾+二氧化锰+氧气 ②氧化汞 汞+氧气 ③水 氢气+氧气 ④过氧化钠+二氧化碳 碳酸钠+氧气 根据文字表达式确定,其中最适合于潜水艇里制取氧气的方法是哪种(用序号回答)?与其他方法相比,这种方法的优点是什么? 18. 小明参观某养鱼池时,好奇地发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气。 〔提出问题〕过氧化钙可否用于制取氧气? 〔查阅资料〕部分内容如下:过氧化钙(CaO 2 )室温下稳定,在 300 ℃ 时分解生成氧气,可做增氧剂、杀菌剂等。 〔猜想与验证〕 (1)小明依据________提出猜想Ⅰ。 猜想Ⅰ:加热过氧化钙可制取氧气。 实验装置 实验主要过程 ①检查装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到________,松开手后,有液体进入导管②加入过氧化钙、加热,导管口有大量气泡冒出③收集满一瓶气体④停止加热。熄灭酒精灯前,应________⑤检验气体的方法是 实验结论:加热过氧化钙可制取氧气。 (2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ。 猜想Ⅱ:过氧化钙与水反应可制取氧气。 实验装置 实验主要过程 ①检查装置气密性②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢放出 7 实验结论:不能用过氧化钙与水反应制取氧气。 分析与反思: ①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是_______________。 ②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?你合理建议 。 以上建议是否可行,还需进一步通过实验验证。 19. 如下图是实验室制取气体的常用装置。请回答: (1)仪器a名称是________,A装置中的集气装置只能收集密度比空气________的气体。 (2)实验室用分解过氧化氢(H 2 O 2 )的方法来制备氧气,其化学反应文字表达式为________,反应中,MnO 2 起________作用,加快了H 2 O 2 的分解。 (3)用A或B装置制备气体的反应应该是________和液体不需要加热的反应。 三、 填空题 20. 高锰酸钾受热放出氧气反应的文字表达式是________,反应的基本类型是________。木炭在氧气中燃烧反应的文字表达式是________________,反应的基本类型是________。很多物质能在空气中燃烧,实际上是跟空气中的________反应,这些反应属于________反应。 21. 根据下图回答问题。 (1)实验仪器a的名称是________。 (2)实验室用高锰酸钾制取氧气的化学反应的文字表达式为________,所选用的发生装置是________(填字母序号)。 (3)实验室用过氧化氢溶液和二氧化锰制取氧气时,二氧化锰起________作用,所选用的收集装置是________或E。 (4)用排空气法收集一瓶氧气,验满时将带火星的木条放在瓶口,若观察到________,说明瓶中已充满氧气。 22. 小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验: 7 实验操作 实验现象 实验结论或总结 结论 总结 实验一 取5 mL 5%的过氧化氢溶液于试管中,伸入带火星木条 有气泡产生,木条不复燃 过氧化氢分解产生氧气,但是_______ 二氧化锰是 过氧化氢分 解的催化剂 实验二 向盛水的试管中加入二氧化锰,伸入带火星的木条 没有明显现象 ________ 实验三 ________ ________ ________ ________ ________ ________ 二氧化锰能加快过氧化氢的分解 (1)请你帮小丽同学填写上表中未填完的空格。 (2)在小丽的探究实验中,“实验一”和“实验二”起的作用是________________________。 (3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。 第一方面的实验操作中包含了两次称量,其目的是________; 第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。接下来的实验操作、现象和结论是________。 四、 实验题 23. 小明知道二氧化锰能作过氧化氢分解的催化剂后,再想探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白。 (1)[问题]氧化铝能不能作过氧化氢分解的催化剂呢 (2)[猜想]氧化铝能作过氧化氢分解的催化剂。 他设计并完成了下表所示的探究实验: 7 (1)请你帮助小明同学填写上表中未完的表格。 (2)在小明的探究实验中,实验一和实验二起的作用是______; (3)[讨论与反思]经过讨论,有的同学认为只有上述两个证据,不能证明 氧化铝能作过氧化氢分解的催化剂,还要补充两个方面的探究实验,最终大 家一起完成了对这个猜想的验证。 第一方面的实验操作中包含了两次称量,其目的是______ 第二方面的实验是利用实验三反应后试管内的剩余物继续实验。接下来的实 验操作是______现象和结论为______ 7 答案 一、选择题 1、C 2、B 3、D 4、C 5、A 6、 A7、 A 8、C 9、C10、A 11、C 12、D 13、D14、D15、 B 二、解答题 16、(1)高锰酸钾 锰酸钾+二氧化锰+氧气 (2)A (3)用手捂住大试管,导管口冒气泡,松手后导管口形成稳定的水柱 橡皮塞没有塞紧 (4)③⑤ (5)倒吸(或大试管破裂) 17、④ 因为此法不需要加热和消耗能源,在常温下就能进行,且能够将人呼出的二氧化碳加以利用。 18、(1)过氧化钙在 300 ℃ 时分解生成氧气 ①导管口有气泡冒出 ④先将导管移出水面 ⑤把带火星的木条伸入集气瓶中,木条复燃,证明是氧气 (2)①过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂 ②加热过氧化钙和水的混合物(或向过氧化钙和水的混合物中加入催化剂) 19、(1)长颈漏斗 大 (2)过氧化氢 水+氧气 催化 (3)固体(或液体) 三、填空题 20、高锰酸钾 锰酸钾+二氧化锰+氧气 分解反应 碳+氧气 二氧化碳 化合反应 氧气 氧化反应 21、(1)酒精灯 (2)高锰酸钾加热 锰酸钾+二氧化锰+氧气 A (3)催化 C (4)木条复燃 22、(1) 实验一 反应慢 实验二 二氧化锰加入水中不产生氧气 实验三 向盛有5 mL 5 %过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 有大量气泡产生,带火星的木条复燃 (2)对比(或对照等) (3)比较MnO 2 在过氧化氢分解前后的质量 倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明MnO 2 仍然能加快过氧化氢的分解速率(化学性质没变) 四、实验题 23、 (1)①反应慢 ②氧化铝加入水中不产生氧气③取5ml5%的过氧化氢溶液于试管中,加入氧化铝,伸入带火星的木条④有大量气泡产生,带火星的木条迅速复燃(2)对比(或对照)第一方面:比较氧化铝在过氧化氢分解前后的质量;第二方面,倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,伸入带火星的木条 有大量气泡产生,带火星的木条迅速复燃,说明氧化铝仍能加快过氧化氢的分解速率(化学性质不变) 查看更多