- 2021-11-11 发布 |
- 37.5 KB |
- 31页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
(第二辑)第9单元 溶液
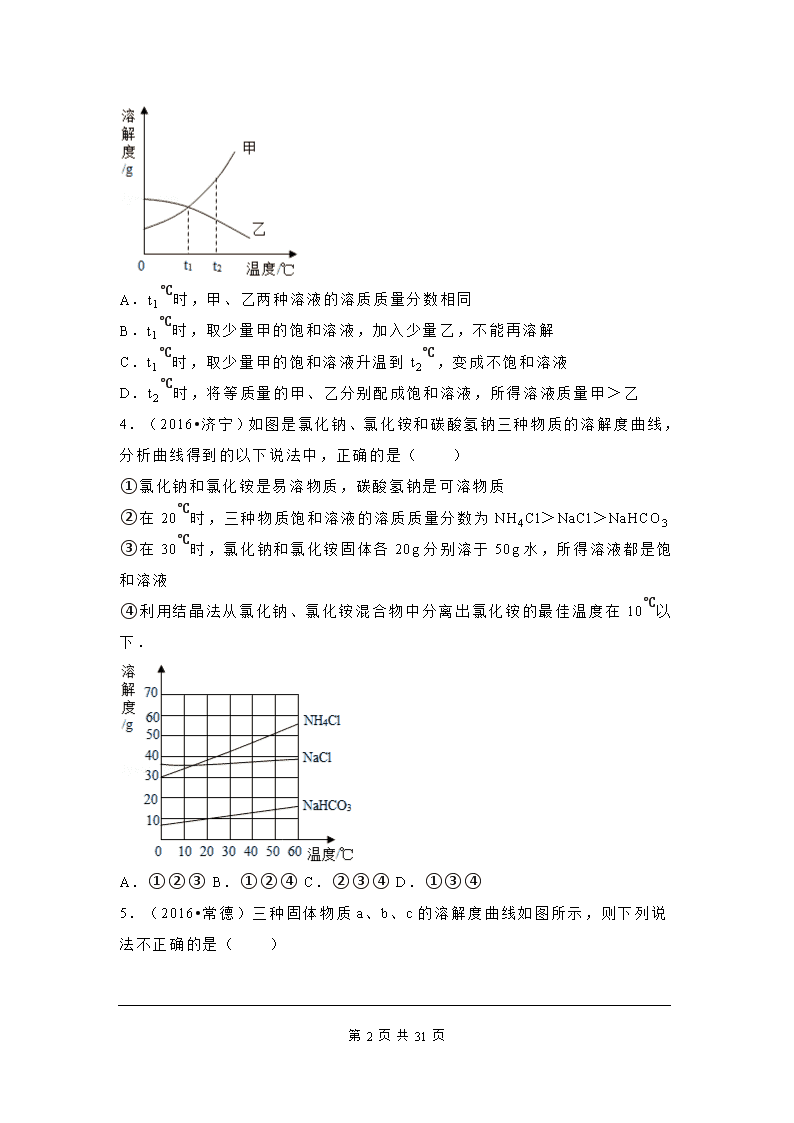
2016年全国各地中考化学试题分类解析汇编(第二辑)第9单元溶液 一.选择题(共20小题) 1.(2016•成都)甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( ) A.甲的溶解度大于乙 B.t1℃时,a点表示乙的饱和溶液 C.甲溶液从t2℃降温到t1℃,一定有晶体析出 D.t2℃时,将甲和乙各15g分别加入100g水中,均能完全溶解 2.(2016•长沙)甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( ) A.t1℃时,甲、乙两物质的溶解度相等 B.乙物质的溶解度大于甲物质的溶解度 C.t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 D.t2℃时,甲物质的饱和溶液降温至t1℃,溶液中溶质质量一定不变 3.(2016•盐城)甲、乙两种物质的溶解度曲线如图,下列说法正确的是( ) 第 31 页 共 31 页 A.t1℃时,甲、乙两种溶液的溶质质量分数相同 B.t1℃时,取少量甲的饱和溶液,加入少量乙,不能再溶解 C.t1℃时,取少量甲的饱和溶液升温到t2℃,变成不饱和溶液 D.t2℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量甲>乙 4.(2016•济宁)如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线得到的以下说法中,正确的是( ) ①氯化钠和氯化铵是易溶物质,碳酸氢钠是可溶物质 ②在20℃时,三种物质饱和溶液的溶质质量分数为NH4Cl>NaCl>NaHCO3 ③在30℃时,氯化钠和氯化铵固体各20g分别溶于50g水,所得溶液都是饱和溶液 ④利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10℃以下. A.①②③ B.①②④ C.②③④ D.①③④ 5.(2016•常德)三种固体物质a、b、c的溶解度曲线如图所示,则下列说法不正确的是( ) 第 31 页 共 31 页 A.t1℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c B.a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出 C.t2℃时,将50g a物质加入到100g水中完全溶解形成饱和溶液 D.a中混有少量b时可采取降温结晶的方法提纯得到a 6.(2016•哈尔滨)如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( ) A.通过升温可以将甲的不饱和溶液变为饱和溶液 B.20℃时分别将甲、乙溶液蒸发相等质量的水,析出甲、乙的质量相等 C.10℃时,10g水中分别溶解甲、乙达到饱和溶液,溶解较多的物质是乙 D.把100g溶质质量分数为10%的乙溶液从30℃降温到10℃,其质量分数仍为10% 7.(2016•重庆)将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( ) A.甲的溶解度随温度升高而增大 B.t1℃时,甲、乙的溶解度均为20g 第 31 页 共 31 页 C.温度由t2℃降低到t1℃时,甲溶液析出5g固体 D.a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b 8.(2016•临沂)甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( ) A.20℃时,甲物质的溶解度是40 B.升温可使乙物质的饱和溶液析出固体 C.甲物质的溶解度大于乙物质的溶解度 D.40℃时,将甲、乙两物质饱和溶液分别降温到20℃,二者都变为不饱和溶液 9.(2016•烟台)如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是( ) A.t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲 B.t2℃时,20g丙能溶解于50g水中形成70g溶液 C.若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法 D.t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲>丙 第 31 页 共 31 页 10.(2016•连云港)甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( ) A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液 B.乙的溶解度随温度的升高而增大 C.相同温度时,甲的溶解度一定大于乙的溶解度 D.分别将甲、乙的饱和溶液从a2℃降至a1℃时,所得溶液中溶质的质量分数相等 11.(2016•扬州)KNO3与NaCl的溶解度曲线如图所示.下列说法正确的是( ) A.KNO3的溶解度大于NaCl的溶解度 B.加水能使NaCl的饱和溶液变为不饱和溶液 C.t1℃时,KNO3溶液与NaCl溶液溶质的质量分数相等 D.用冷却热饱和溶液的方法,能使KNO3从溶液中结晶析出 12.(2016•乐山)甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( ) A.甲的溶解度大于乙的溶解度 B.20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数 第 31 页 共 31 页 C.40℃时,分别在100 g水中加入40g 甲、乙,所得溶液溶质的质量分数相等 D.分别将甲和乙的饱和溶液从40℃降低到20℃,甲会析出晶体,乙则不会 13.(2016•泉州)如图是硝酸钾的溶解度曲线,下列说法错误的是( ) w w w .x k b 1.c o m A.硝酸钾的溶解度随温度的升高而增大 B.降低温度可以使接近饱和的硝酸钾溶液变饱和 C.60℃时120g硝酸钾与100g水充分混合可以形成饱和溶液 D.60℃时硝酸钾溶液的溶质质量分数一定大于30℃时硝酸钾溶液的溶质质量分数 14.(2016•广安)如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( ) A.甲中混有少量杂质乙,可采用降温结晶的方法进行提纯 B.t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变 C.t2℃时,甲、丙溶液中溶质的质量分数甲>丙 D.t1℃时,60g水中溶解18g甲可得到其饱和溶液 第 31 页 共 31 页 15.(2016•无锡)NaCl、KNO3两种固体物质的溶解度曲线如图所示,下列说法正确的是( ) A.20°C时,NaCl的溶解度为31.6g B.KNO3的溶解度大于NaCl的溶解度 C.使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法 D.50℃时,在100g水中加入100gKNO3,所得溶液中KNO3的质量分数为50% 16.(2016•咸宁)列表和作图是常用的数据处理方法.结合所绘图表判断下列说法正确的是( ) 氢氧化钠、碳酸钠分别在水、酒精中的溶解度 氢氧化钠 碳酸钠 20℃ 40℃ 20℃ 40℃ 水 109g 129g 21.8g 49g 酒精 17.3g 40g 不溶 不溶 A.图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观 B.由表格数据可知,物质的溶解度只受温度影响 C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液 第 31 页 共 31 页 D.40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成 17.(2016•河南)如图是甲、乙的溶解度曲线,下列说法不正确的是( ) A.t1℃时,乙的溶解度大于甲的溶解度 B.t2℃时,甲、乙饱和溶液中溶质质量分数相等 C.降低温度能使接近饱和的甲溶液变为饱和溶液 D.t2℃时,75g甲的饱和溶液中加入50g水,可以得到质量分数为25%的溶液 18.(2016•滨州)甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( ) A.甲物质的溶解度大于乙物质的溶解度 B.甲和乙的饱和溶液从t1℃升温到t2℃时都有晶体析出 C.t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液 D.t2℃时,甲和乙的饱和溶液各100g其溶质的质量相等 19.(2016•舟山)如表是不同温度时硝酸钾的溶解度,有关说法正确的是( ) 温度/℃ 0 20 40 60 80 100 溶解度/克 13.3 31.6 63.9 110 169 246 A.20℃时,100克水中溶解的硝酸钾越多溶解度就越大 B.40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克 C.100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多 第 31 页 共 31 页 D.0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小 20.(2016•娄底)如表是NaCl和KNO3在不同温度下的溶解度,有关说法不正确的是( ) 温度/℃ 0 10 20 30 40 50 60 70 80 溶解度/g NaCl 35.7 35.8 36.0 36.3X kB1.cOM[来源:Z,xx,k.Com] 36.6 37.0 37.3w w w .x k b 1.c o m 37.8 38.4 KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 A.NaCl的溶解度比KNO3的溶解度大 B.两种物质溶解度相等的温度在20℃~30℃之间 C.20℃时,NaCl的溶解度为36.0g D.60℃时,将11gKNO3加入10g水中充分溶解,溶液刚好饱和 第 31 页 共 31 页 2016年全国各地中考化学试题分类解析汇编(第二辑)第9单元溶液 参考答案与试题解析 一.选择题(共20小题) 1.(2016•成都)甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( ) A.甲的溶解度大于乙 B.t1℃时,a点表示乙的饱和溶液 C.甲溶液从t2℃降温到t1℃,一定有晶体析出 D.t2℃时,将甲和乙各15g分别加入100g水中,均能完全溶解 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、在比较物质的溶解度时,需要指明温度,故A错误; B、t1℃时,a点表示溶质质量小于15g,所以该点是乙的不饱和溶液,故B错误; C、甲溶液的状态不能确定,所以从t2℃降温到t1℃,不一定有晶体析出,故C错误; 第 31 页 共 31 页 D、t2℃时,甲、乙物质的溶解度均大于15g,所以将甲和乙各15g分别加入100g水中,均能完全溶解,故D正确. 故选:D. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 2.(2016•长沙)甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( ) A.t1℃时,甲、乙两物质的溶解度相等 B.乙物质的溶解度大于甲物质的溶解度 C.t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液 D.t2℃时,甲物质的饱和溶液降温至t1℃,溶液中溶质质量一定不变 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、通过分析溶解度曲线可知,t1℃时,甲、乙两物质的溶解度相等,故A正确; B、在比较物质的溶解度时,需要指明温度,故B错误; C、乙物质的溶解度随温度的降低而减小,所以t2℃时,乙的饱和溶液降温至t1℃,乙溶液仍为饱和溶液,故C错误; D、t2℃时,甲物质的饱和溶液降温至t1℃,析出晶体,溶液中溶质质量一定减小,故D错误. 第 31 页 共 31 页 故选:A. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 3.(2016•盐城)甲、乙两种物质的溶解度曲线如图,下列说法正确的是( ) A.t1℃时,甲、乙两种溶液的溶质质量分数相同 B.t1℃时,取少量甲的饱和溶液,加入少量乙,不能再溶解 C.t1℃时,取少量甲的饱和溶液升温到t2℃,变成不饱和溶液 D.t2℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量甲>乙 【分析】根据题目信息和溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;t1℃时,甲、乙两种溶液的溶质质量分数相同错误,因为没有指明是饱和溶液;t1℃时,取少量甲的饱和溶液,加入少量乙,不能再溶解错误,还能溶解少量的乙;t1℃时,取少量甲的饱和溶液升温到t2℃,变成不饱和溶液正确,因为升温后,甲的溶解度变大了;t2℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量乙>甲,甲>乙是错误的. 【解答】解:A、t1℃时,甲、乙两种溶液的溶质质量分数相同错误,因为没有指明是饱和溶液;故选项错误; B、t1℃时,取少量甲的饱和溶液,加入少量乙,不能再溶解错误,还能溶解少量的乙;故选项错误; 第 31 页 共 31 页 C、t1℃时,取少量甲的饱和溶液升温到t2℃,变成不饱和溶液正确,因为升温后,甲的溶解度变大了;故选项正确; D、t2℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量乙>甲,甲>乙是错误的,故选项错误; 故选C 【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了结晶的方法等,本考点主要出现在选择题和填空题中. 4.(2016•济宁)如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线得到的以下说法中,正确的是( ) ①氯化钠和氯化铵是易溶物质,碳酸氢钠是可溶物质 ②在20℃时,三种物质饱和溶液的溶质质量分数为NH4Cl>NaCl>NaHCO3 ③在30℃时,氯化钠和氯化铵固体各20g分别溶于50g水,所得溶液都是饱和溶液 ④利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10℃以下. A.①②③ B.①②④ C.②③④ D.①③④ 【分析】①根据在20℃时,物质的溶解度与溶解性的关系解答; ②根据在20℃时,物质饱和溶液的溶质质量分数=100%解答; ③根据30℃时,氯化钠和氯化铵的溶解度解答; ④根据三种物质的溶解度变化进行分析解答. 第 31 页 共 31 页 【解答】解:①在20℃时,氯化钠和氯化铵的溶解度大于10g,是易溶物质,碳酸氢钠的溶解度大于1小于10,是可溶物质,故正确; ②在20℃时,三种物质的溶解度是为NH4Cl>NaCl>NaHCO3,由饱和溶液的溶质质量分数=100%,故三种物质饱和溶液的溶质质量分数为NH4Cl>NaCl>NaHCO3,故正确; ③30℃时,氯化铵的溶解度大于40g,20g氯化铵能完全溶于50g水,所得溶液不是饱和溶液,氯化钠的溶解度小于40g,20g氯化钠不能全部溶解,所得溶液是饱和溶液,故错误; ④由三种物质的溶解度变化规律可知:利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10℃以下,故正确. 答案:B 【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中. 5.(2016•常德)三种固体物质a、b、c的溶解度曲线如图所示,则下列说法不正确的是( ) A.t1℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c B.a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出 C.t2℃时,将50g a物质加入到100g水中完全溶解形成饱和溶液 D.a中混有少量b时可采取降温结晶的方法提纯得到a 【分析】根据题目信息和溶解度曲线可知:a、b两种固体物质的溶解度,都是随温度升高而增大,而c的溶解度随温度的升高而减少;t1 第 31 页 共 31 页 ℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c正确,因为在该温度下它们的溶解度的大小关系是b>a=c;a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出错误,因为C没有晶体析出;t2℃时,将50ga物质加入到100g水中完全溶解形成饱和溶液正确,因为该温度下a的溶解度是50g;a中混有少量b时可采取降温结晶的方法提纯得到a正确,因为a的溶解度受温度的影响比较大; 【解答】解:A、t1℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c正确,因为在该温度下它们的溶解度的大小关系是b>a=c,正确但不符合题意,故选项错误; B、a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出错误,因为C没有晶体析出,错误符合题意,故选项正确; C、t2℃时,将50ga物质加入到100g水中完全溶解形成饱和溶液正确,因为该温度下a的溶解度是50g,正确但不符合题意,故选项错误; D、a中混有少量b时可采取降温结晶的方法提纯得到a正确,因为a的溶解度受温度的影响比较大,正确但不符合题意,故选项错误; 故选B 【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液结晶的方法等,本考点主要出现在选择题和填空题中. 6.(2016•哈尔滨)如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( ) A.通过升温可以将甲的不饱和溶液变为饱和溶液 B.20℃时分别将甲、乙溶液蒸发相等质量的水,析出甲、乙的质量相等 C.10℃时,10g水中分别溶解甲、乙达到饱和溶液,溶解较多的物质是乙 第 31 页 共 31 页 D.把100g溶质质量分数为10%的乙溶液从30℃降温到10℃,其质量分数仍为10% 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、甲物质的溶解度随温度的升高而增大,所以通过升温不可以将甲的不饱和溶液变为饱和溶液,故A错误; B、20℃时,甲、乙溶液的状态不能确定,所以分别将甲、乙溶液蒸发相等质量的水,析出甲、乙的质量不一定相等,故B错误; C、10℃时,甲物质的溶解度大于乙物质的溶解度,所以10g水中分别溶解甲、乙达到饱和溶液,溶解较多的物质是甲,故C错误; D、10℃时,乙物质的溶解度对于20g,所以饱和溶液的溶质质量分数大于16.7%,所以把100g溶质质量分数为10%的乙溶液从30℃降温到10℃,其质量分数仍为10%,故D正确. 故选:D. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 7.(2016•重庆)将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( ) A.甲的溶解度随温度升高而增大 第 31 页 共 31 页 B.t1℃时,甲、乙的溶解度均为20g C.温度由t2℃降低到t1℃时,甲溶液析出5g固体 D.a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、纵坐标是剩余固体质量,温度越高,剩余固体越多,表明溶解度是随温度升高而减小的,故A错误; B、t1℃时,剩余固体都是10g,说明溶解了20g,甲、乙的溶解度均为40g,故B错误; C、温度由t2℃降低到t1℃时,固体减少5g,应该是溶解了5g,故C错误; D、c中剩余固体最少,a中次之,b中剩余固体最多,所以a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b,故D正确. 故选:D. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 8.(2016•临沂)甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( ) A.20℃时,甲物质的溶解度是40 第 31 页 共 31 页 B.升温可使乙物质的饱和溶液析出固体 C.甲物质的溶解度大于乙物质的溶解度 D.40℃时,将甲、乙两物质饱和溶液分别降温到20℃,二者都变为不饱和溶液 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、通过分析溶解度曲线可知,20℃时,甲物质的溶解度是40g,故A错误; B、乙物质的溶解度随温度的升高而减小,所以升温可使乙物质的饱和溶液析出固体,故B正确; C、在比较物质的溶解度时,需要指明温度,故C错误; D、甲物质的溶解度随温度的降低而减小,所以40℃时,将甲、乙两物质饱和溶液分别降温到20℃,甲仍是饱和溶液,故D错误. 故选:B. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 9.(2016•烟台)如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是( ) 第 31 页 共 31 页 A.t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲 B.t2℃时,20g丙能溶解于50g水中形成70g溶液 C.若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法 D.t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲>丙 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、要比较某一温度下两种溶液中溶质的质量分数,必须等质量的饱和溶液,本题没有说明是饱和溶液,无法比较,故错误; B、t2℃时,丙的溶解度为30g,20g丙溶解于50g水中,有5g丙未溶解,能形成60g溶液,故错误; C、物质的溶解度随温度的升高而增大,所以要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂或添加溶质的方法,故正确; D、甲、乙的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,所以将t3℃时甲、乙、丙的饱和溶液降温到t2℃,甲乙析出晶体,依然为饱和溶液,丙变为不饱和溶液,溶质质量分数与降温前相等,由饱和溶液中溶质质量分数的计算式×100%可知,溶解度越大质量分数也就越大,t2℃时乙的溶解度大于甲,且t2℃时甲的溶解度大于t3℃时丙的溶解度,所以此时溶液的质量分数由大到小的顺序为乙>甲>丙,故正确; 故选:CD. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 第 31 页 共 31 页 10.(2016•连云港)甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( ) A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液 B.乙的溶解度随温度的升高而增大 C.相同温度时,甲的溶解度一定大于乙的溶解度 D.分别将甲、乙的饱和溶液从a2℃降至a1℃时,所得溶液中溶质的质量分数相等 【分析】根据题目信息和溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度先随温度的升高增大,后随温度的升高而减小;a1℃时甲的饱和溶液,升温至a2℃时变成不饱和溶液,仍是饱和溶液错误;乙的溶解度随温度的升高而增大错误,因为没有指明温度;温度时,甲的溶解度一定大于乙的溶解度错误,因为没有指明温度;分别将甲、乙的饱和溶液从a2℃降至a1℃时,所得溶液中溶质的质量分数相等正确,因为降温后,甲和乙的溶解度相同. 【解答】解:A、a1℃时甲的饱和溶液,升温至a2℃时变成不饱和溶液,仍是饱和溶液错误;故选项错误; B、乙的溶解度随温度的升高而增大错误,因为没有指明温度;故选项错误; C、温度时,甲的溶解度一定大于乙的溶解度错误,因为没有指明温度;故选项错误; D、分别将甲、乙的饱和溶液从a2℃降至a1℃时,所得溶液中溶质的质量分数相等正确,因为降温后,甲和乙的溶解度相同,故选项正确; 故选D 【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了饱和溶液与不饱和溶液的转化等,本考点主要出现在选择题和填空题中. 第 31 页 共 31 页 11.(2016•扬州)KNO3与NaCl的溶解度曲线如图所示.下列说法正确的是( ) A.KNO3的溶解度大于NaCl的溶解度 B.加水能使NaCl的饱和溶液变为不饱和溶液 C.t1℃时,KNO3溶液与NaCl溶液溶质的质量分数相等 D.用冷却热饱和溶液的方法,能使KNO3从溶液中结晶析出 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、在比较物质的溶解度时,需要指明温度,故A错误; B、加水能使NaCl的饱和溶液变为不饱和溶液,故B正确; C、t1℃时,饱和的硝酸钾、饱和的氯化钠溶质的质量分数相等,故C错误; D、硝酸钾的溶解度受温度影响变化较大,所以用冷却热饱和溶液的方法,能使KNO3从饱和溶液中结晶析出,故D正确. 故选:BD. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 12.(2016•乐山)甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( ) 第 31 页 共 31 页 A.甲的溶解度大于乙的溶解度 B.20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数 C.40℃时,分别在100 g水中加入40g 甲、乙,所得溶液溶质的质量分数相等 D.分别将甲和乙的饱和溶液从40℃降低到20℃,甲会析出晶体,乙则不会 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、在比较物质的溶解度是需要指明温度,故A错误; B、20℃时,甲、乙物质的溶解度相等,所以甲、乙饱和溶液的质量分数相等,故B错误; C、40℃时,甲物质的溶解度是50g,乙物质的溶解度是40g,所以分别在100g水中加入40g甲、乙,所得溶液溶质的质量分数相等,故C正确; D、分别将甲和乙的饱和溶液从40℃降低到20℃,都会析出晶体,故D错误. 故选:C. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 13.(2016•泉州)如图是硝酸钾的溶解度曲线,下列说法错误的是( ) 第 31 页 共 31 页 A.硝酸钾的溶解度随温度的升高而增大 B.降低温度可以使接近饱和的硝酸钾溶液变饱和 C.60℃时120g硝酸钾与100g水充分混合可以形成饱和溶液 D.60℃时硝酸钾溶液的溶质质量分数一定大于30℃时硝酸钾溶液的溶质质量分数 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、通过分析溶解度曲线可知,硝酸钾的溶解度随温度的升高而增大,故A正确; B、硝酸钾的溶解度随温度的升高而增大,所以降低温度可以使接近饱和的硝酸钾溶液变饱和,故B正确; C、60℃时,硝酸钾的溶解度小于120g,所以120g硝酸钾与100g水充分混合可以形成饱和溶液,故C正确; D、60℃时的硝酸钾溶液、30℃时硝酸钾溶液状态不能确定,所以溶质质量分数不能确定,故D错误. 故选:d. 第 31 页 共 31 页 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 14.(2016•广安)如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( ) A.甲中混有少量杂质乙,可采用降温结晶的方法进行提纯 B.t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变 C.t2℃时,甲、丙溶液中溶质的质量分数甲>丙 D.t1℃时,60g水中溶解18g甲可得到其饱和溶液 【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、甲物质的溶解度受温度影响变化较大,所以甲中混有少量杂质乙,可采用降温结晶的方法进行提纯,故A正确; B、t3℃时,将甲、丙的饱和溶液降温,甲物质的溶解度减小,析出晶体,乙物质的溶解度增大,所以甲溶液溶质的质量分数减小,丙不变,故B正确; C、t2℃时,甲、丙溶液的状态不能确定,所以溶质的质量分数也不能确定,故C错误; D、t1℃时,甲物质的溶解度是30g,所以60g水中溶解18g甲可得到其饱和溶液,故D正确. 第 31 页 共 31 页 故选:C. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 15.(2016•无锡)NaCl、KNO3两种固体物质的溶解度曲线如图所示,下列说法正确的是( ) A.20°C时,NaCl的溶解度为31.6g B.KNO3的溶解度大于NaCl的溶解度 C.使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法 D.50℃时,在100g水中加入100gKNO3,所得溶液中KNO3的质量分数为50% 【分析】根据题目信息和溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大;20°C时,NaCl的溶解度为36g,不是31.6g;KNO3的溶解度大于NaCl的溶解度错误,因为没有指明温度;使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法正确,因为水分蒸发,有固体析出;50℃时,硝酸钾的溶解度是85.5g,因此在100g水中加入100gKNO3,所得溶液中KNO3的质量分数=≈46.1%,50%是错误的. 【解答】解:A、20°C时,NaCl的溶解度为36g,不是31.6g,故选项错误; B、KNO3的溶解度大于NaCl的溶解度错误,因为没有指明温度,故选项错误; C、使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法正确,因为水分蒸发,有固体析出;故选项正确; 第 31 页 共 31 页 D、50℃时,硝酸钾的溶解度是85.5g,因此在100g水中加入100gKNO3,所得溶液中KNO3的质量分数=≈46.1%,50%是错误的,故选项错误; 故选C 【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中. 16.(2016•咸宁)列表和作图是常用的数据处理方法.结合所绘图表判断下列说法正确的是( ) 氢氧化钠、碳酸钠分别在水、酒精中的溶解度 氢氧化钠 碳酸钠 20℃ 40℃ 20℃ 40℃ 水 109g 129g 21.8g 49g 酒精 17.3g 40g 不溶 不溶 A.图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观 B.由表格数据可知,物质的溶解度只受温度影响 C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液 D.40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成 【分析】 第 31 页 共 31 页 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的. 【解答】解:A、通过分析溶解度表和溶解度曲线可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点是变化规律更直观,故A错误; B、由表格数据可知,物质的溶解度受温度和溶剂影响,故B错误; C、40℃时,氢氧化钠在水中的溶解度是129g,氢氧化钠在酒精中的溶解度是40g,所以将50gNaOH分别投入到100g水和酒精中,在水中不能形成饱和溶液,故C错误; D、40℃时,碳酸钠在酒精中难溶,所以将CO2通入饱和的NaOH酒精溶液中有沉淀生成,故D正确、 故选:D. 【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力. 17.(2016•河南)如图是甲、乙的溶解度曲线,下列说法不正确的是( ) A.t1℃时,乙的溶解度大于甲的溶解度 B.t2℃时,甲、乙饱和溶液中溶质质量分数相等 C.降低温度能使接近饱和的甲溶液变为饱和溶液 D.t2℃时,75g甲的饱和溶液中加入50g水,可以得到质量分数为25%的溶液 【分析】A、据溶解度曲线可比较同一温度下不同物质的溶解度; 第 31 页 共 31 页 B、据饱和时质量分数的计算式×100%可知:溶解度相等则溶质的质量分数相等; C、甲的溶解度随温度降低而减小,所以降温可使其不饱和溶液变为饱和溶液; D、据该温度下甲的溶解度和溶质质量分数的计算方法分析解答. 【解答】解:A、由图可知:t1℃时,乙的溶解度大于甲的溶解度,正确; B、t2℃时,甲、乙的溶解度曲线交于一点,溶解度相等,则饱和溶液中溶质质量分数相等,正确; C、甲的溶解度随温度降低而减小,所以降温可使其不饱和溶液变为饱和溶液,正确; D、t2℃时甲的溶解度是50g,即100g水中最多溶解50g甲,形成饱和溶液150g,则75g甲的饱和溶液中有25g甲,加50g水得到溶液的质量分数=×100%=20%,而非25%,故错误; 故选:D. 【点评】本考点考查了溶解度曲线及其应用,溶解度概念、饱和溶液和不饱和溶液的相互转化,还考查了有关溶液和溶质质量分数的计算,据相关知识分析解答即可. 18.(2016•滨州)甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( ) A.甲物质的溶解度大于乙物质的溶解度 B.甲和乙的饱和溶液从t1℃升温到t2℃时都有晶体析出 C.t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液 D.t2℃时,甲和乙的饱和溶液各100g其溶质的质量相等 第 31 页 共 31 页 【分析】A、根据溶解度的比较方法考虑; B、对于饱和溶液升温而析出晶体,该物质的溶解度随温度升高而减小; C、t1℃时,甲和乙的溶解度分析; D、据溶解度的概念,溶液质量=溶质质量+溶剂质量解决此题. 【解答】解:A、溶解度的比较必须有温度的限制,故A错误; B、甲、乙两种物质的溶解度随温度升高而增大,故甲和乙的饱和溶液从t1℃升温到t2℃时都不会有晶体析出,故B错误; C、由甲、乙两种物质的溶解度曲线知,t1℃时,甲和乙的溶解度都是30g,故t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液,故C正确; D、由甲、乙两种物质的溶解度曲线知,t2℃时,甲和乙的饱和溶液,甲的溶解度大于乙的溶解度,据溶液质量=溶质质量+溶剂质量,当溶液质量相同时,无法比较溶质的质量,故D错误. 故选C. 【点评】主要考查了固体溶解度曲线的意义及固体溶解度和温度间的关系,并能利用所学知识来解决实际问题. 19.(2016•舟山)如表是不同温度时硝酸钾的溶解度,有关说法正确的是( ) 温度/℃ 0 20 40 60 80 100 溶解度/克 13.3 31.6 63.9 110 169 246 A.20℃时,100克水中溶解的硝酸钾越多溶解度就越大 B.40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克 C.100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多 D.0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小 【分析】利用溶解度的概念及意义,对表中的数据进行分析.根据硝酸钾在不同温度下的溶解度可知,硝酸钾的溶解度随温度升高而增大,利用这些信息结合所学的有关知识解决此题. 第 31 页 共 31 页 【解答】解:A、20℃时,硝酸钾的溶解度是一定的,是100克水中最多溶解的质量,不是溶解的硝酸钾越多溶解度就越大,故A错误; B、40℃时,163.9克硝酸钾饱和溶液中含有硝酸钾63.9克.故B错误; C、100℃的水能溶解的硝酸钾不一定比80℃的水能溶解的硝酸钾多,因为没有说明水的质量,故C错误; D、0℃的硝酸钾的溶解度比60℃的硝酸钾的溶解度小,因此0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小,故D正确. 故选D. 【点评】此题是对溶解度及影响因素的考查,解题的关键是对溶解度含义的理解及对影响溶解度大小因素的掌握. 20.(2016•娄底)如表是NaCl和KNO3在不同温度下的溶解度,有关说法不正确的是( ) 温度/℃ 0 10 20 30 40 50 60 70 80 溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 A.NaCl的溶解度比KNO3的溶解度大 B.两种物质溶解度相等的温度在20℃~30℃之间 C.20℃时,NaCl的溶解度为36.0g D.60℃时,将11gKNO3加入10g水中充分溶解,溶液刚好饱和 【分析】利用溶解度的概念及意义,对表中的数据进行分析,利用这些信息结合所学的知识解决此题. 【解答】解:A、要比较溶解度,应指明温度,故此选项错误. B、从表中数据可知,两种物质溶解度相等的温度在20℃~30℃之间,故此选项正确. C、从表中数据可知,20℃时,NaCl的溶解度为36.0g,故此选项正确. D、从表中数据可知,60℃时,硝酸钾的溶解度是110g,由溶解度的含义可知,将11gKNO3加入10g水中充分溶解,溶液刚好饱和,故此选项正确. 第 31 页 共 31 页 故选A. 【点评】此题是对溶解度及意义的考查,解题的关键是对溶解度含义的理解及应用. 第 31 页 共 31 页查看更多