- 2021-11-11 发布 |
- 37.5 KB |
- 7页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
徐州专版2020中考化学复习方案第4章认识化学变化专项06质量守恒定律应用课件
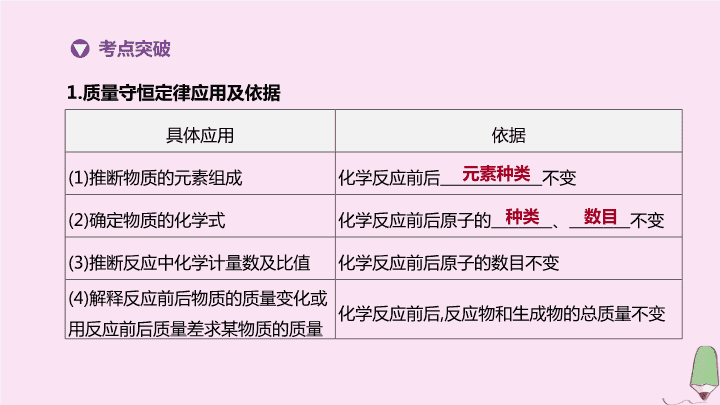
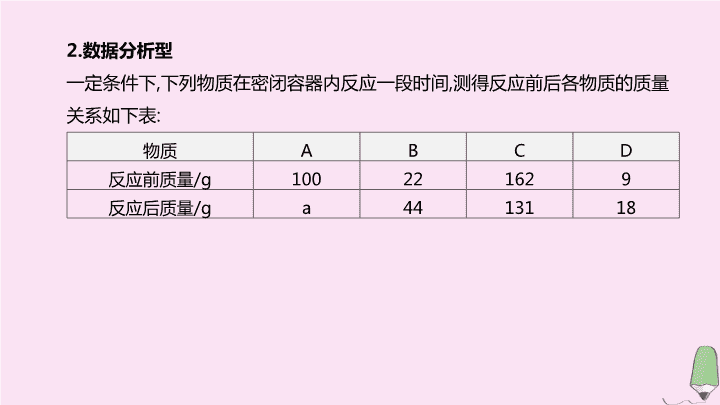
专项(六) 质量守恒定律应用 第 4 章 认识化学变化 考点突破 1. 质量守恒定律应用及依据 具体应用 依据 (1) 推断物质的元素组成 化学反应 前后 不变 (2) 确定物质的化学式 化学反应 前后原子的 、 不变 (3) 推断反应中化学计量数及比值 化学反应 前后原子的数目不变 (4) 解释反应前后物质的质量变化或用反应前后质量差求某物质的质量 化学反应 前后 , 反应物和生成物的总质量不变 元素种类 种类 数目 2. 数据分析型 一定条件下 , 下列物质在密闭容器内反应一段时间 , 测得反应前后各物质的质量关系如下表 : 物质 A B C D 反应前质量 /g 100 22 162 9 反应后质量 /g a 44 131 18 思路分析 (1) 定反应物、生成物 : 反应后质量增加的为生成物 , 减少的为反应物 ① a = ② 反应物为 , 生成物为 (2) 写反应表达式 ( 可判断出化合或分解反应 ) C → B + D (3) 定变化量 31 g 22 g 9 g (4) 分析判断 ①A ( 填“一定”或“可能” ) 是该反应的催化剂 ② 物质 C ( 填“属于”或“不属于” ) 化合物 ③ 参加反应的 B 和 D 的质量比为 100 C B 、 D 可能 属于 22∶9 3. 微观反应示意图 某反应的微观示意图如图 G6-1: 图 G6-1 思路分析 (1) 判断有无物质剩余 : 反应前后有无相同粒子 反应 前的分子个数为 3 个 , 反应后还剩余 1 个 , 即实际参加反应的分子个数为 个 (2) 写出反应物和生成物的化学式 反应物 ; 生成物 (3) 写出化学方程式 2 NO 、 CO CO 2 、 N 2 2NO+2CO 2CO 2 +N 2 (续表) (4) 分析 ① 物质种类 属于 , 属于 ② 反应物、生成物的粒子个数比 粒子个数比即为化学方程式中化学计量数之比 , 根据化学方程式 , 这四种分子个数比为 ③ 各物质质量比 物质质量比即为各物质的相对分子质量与化学计量 数 乘积 的 比 , 根据化学方程式 , 这 四种物质的质量比 为 ④ 判断反应类型 该反应 ( 填“属于”或“不属于” ) 基本反应类型 氧化物 单质 2∶2∶2∶1( 合理即可 ) 15∶14∶22∶7( 合理即可 ) 不属于查看更多