- 2021-11-11 发布 |
- 37.5 KB |
- 20页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020中考化学复习方案主题三身边的化学物质专项04常见气体的制取和净化课件
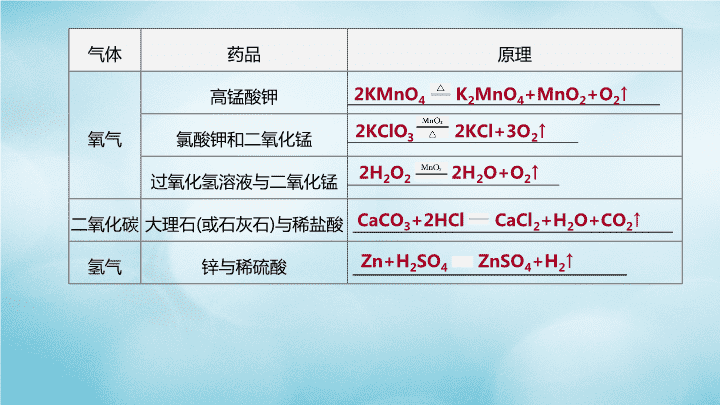
专项(四) 常见气体的制取和净化 主题三 身边的化学物质 考点突破 一、常见气体的制取 1.反应原理 选择适当的反应,即反应速率要适中,原料易获得且经济;能在一般实验室条件下 (如常温、加热、加催化剂等)进行。 气体 药品 原理 氧气 高锰酸钾 _________________________________________ 氯酸钾和二氧化锰 _________________________________________________ 过氧化氢溶液与二氧化锰 _____________________________________________ 二氧化碳 大理石(或石灰石)与稀盐酸 __________________________________________ 氢气 锌与稀硫酸 ____________________________________ 2KMnO4 K2MnO4+MnO2+O2↑ 2KClO3 2KCl+3O2↑ 2H2O2 2H2O+O2↑ CaCO3+2HCl CaCl2+H2O+CO2↑ Zn+H2SO4 ZnSO4+H2↑ 2.装置选取:包括发生装置和收集装置。 (1)发生装置 ①选择依据:药品的 和 (是否需要加热)。 状态 反应条件 ②常见发生装置 类型 固固加热型 固液常温型 装置 (续表) 类型 固固加热型 固液常温型 注意 试管口略向下倾 斜(用KMnO4制 O2时管口加棉花) 液体不宜 过多,防 止溢出 长颈漏斗 伸入液面 以下 适用于块状固体与 液体反应 优缺 点 安装简单 便于添加 液体药品 ________________ ________________ 可控制反应速率 可控制反应的 发生与停止 (续表) 类型 固固加热型 固液常温型 适用 范围 用于制取 少量气体 用于平稳 反应,并制取 较多气体 用于剧烈反 应,并制取较多 气体 用于平稳反应,且 持续时间很长的气 体制取 制取 气体 高锰酸钾制氧 气;氯酸钾和二氧 化锰制氧气 过氧化氢溶液与二氧化锰制氧气;石灰 石和稀盐酸制二氧化碳;锌粒和稀硫酸制 氢气 石灰石和稀盐酸 制二氧化碳;锌粒和 稀硫酸制氢气 (2)收集装置 ①选择依据:气体的 、 ,以及是否与空气中的成分反应、 是否与水反应、是否有毒等。 ②常见收集装置 溶解性 密度 类型 向上排空气法 向下排空气法 排空气法 排水法 装置 (续表) 类型 向上排空气法 向下排空气法 排空气法 排水法 适用 范围 密度比空气 的 气体,不与空气中成 分反应 密度比空气 的 气体,不与空气中成 分反应 与空气密度相差 较大,不与空气中成 分反应 溶于 水,不与水反应 典型 气体 CO2、O2等 H2、CH4等 H2、O2、CO2、 CH4等 H2、O2、CO、 CH4等 大 小 难 (续表) 类型 向上排空气法 向下排空气法 排空气法 排水法 注意 事项 导管伸入集气瓶底部,便于 排出集气瓶中气体 密度比空气小 从 端进; 密度比空气大从 端进 端进气 体, 端 排出水 气泡连续均匀 后开始收集,导管 不宜伸到集气瓶 内太多 优缺 点 收集气体干燥,但纯度不高 收集气体较纯,但不干燥 b a d c 3.气体的检验及验满 依据:根据气体的性质选择恰当的方法进行检验和验满。 (以向上排空气法收集O2和CO2为例) 名称 氧气 二氧化碳 检验 验满 用带火星的木条伸入集气 瓶中,木条复燃,表明是氧气 通入澄清石灰水中,石灰水 变浑浊,说明是二氧化碳 将带火星的木条放在集气 瓶口,木条复燃,表明已满 将燃着的木条放在集气瓶 口,木条熄灭,表明已满 二、气体的净化与干燥 1.装置 图G4-1 2.气体的净化 (1)将不纯气体中的杂质气体除去,从而得到较纯净气体的过程。 (2)气体净化常用的试剂 除去气体 常用试剂或方法 CO2 NaOH溶液 H2O 浓硫酸、碱石灰、生石灰等 HCl NaOH溶液、碱石灰、饱和NaHCO3溶液(可用于CO2中含HCl时除杂) CO 通过灼热的CuO将其转化为CO2,再用NaOH溶液吸收 O2 灼热的铜网 H2 通过灼热的CuO将其转化为水,再用浓硫酸或碱石灰吸收 [特别提示]除杂试剂的选择,要根据从某气体中除掉某杂质气体而定,原则是既 不能与原气体反应,又能去掉其中的杂质气体。 3.气体的干燥 (1)用干燥剂除去气体中混有的水蒸气的过程。 (2)常见的干燥剂 干燥剂 可干燥气体 不可干燥气体 干燥装置 碱 性 生石灰、碱石灰、 固体氢氧化钠 中性、碱性气体,如O2、H2、 CO、CH4、N2、NH3等 酸性气体,如CO2、HCl等 B或C 酸 性 浓硫酸 中性、酸性气体,如H2、O2、 CO2、CO、HCl、CH4等 碱性气体,如NH3 A 中 性 无水氯化钙 H2、O2、CO、CO2、HCl NH3 B或C [特别提示]选择干燥剂必须只能吸收水蒸气,而不能与被干燥的气体发生反应。 4.气体制取、检验和净化实验的先后顺序 (1)制取气体→除杂→干燥→收集→尾气处理。 (2)检验先后顺序:先检验水蒸气的存在,再检验其他气体。 (3)净化先后顺序:先除杂,后干燥。 5.多功能瓶的使用 类型 收集气体 检验、干燥、 除杂气体 检验、吸收并集气 排空气法 排水法 装置 (续表) 类型 收集气体 检验、干燥、除 杂气体 检验、吸收并集气 排空气法 排水法 注意 用A装置收集密度比 空气大的气体时,气体 应从 端通入;收 集密度比空气小的气 体时,气体应从______ 端通入;B装置气体进 出口顺序与之相反 实验时应先在瓶中 ,将气体 从 端通入。 如果将排出的水引 入量筒中,利用此 装置还可以测量产 生气体的体积 用此装置吸收或 检验气体时,应 将气体从______ 端通入,可以简 记为“长进短 出” 此装置综合性较强, 如将CO和少量CO2 混合气缓缓通入饱 和石灰水中,石灰水 检验并吸收CO2,CO 贮存在集气瓶内 a b 装满水 b a 6.尾气处理 将实验产生的有毒有害气体(或对空气造成污染的气体),用物理或化学方法进行 处理,将其消除。 序号 ① ② ③ ④ 装置 (续表) 序号 ① ② ③ ④ 常用 方法 可燃性有毒气 体采用燃烧的方 法,使其通过燃烧 转化为对空气无 污染的气体,再排 放到空气中,如CO 适用于水溶 性较大的气体, 如HCl和NH3 将尾气中有害气 体通入(酸性或碱性) 溶液,使其反应而被 吸收,如SO2 通入 NaOH溶液、NH3 通入浓硫酸 用气球收集尾 气,再集中处理或 者再利用查看更多