- 2021-11-10 发布 |
- 37.5 KB |
- 2页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
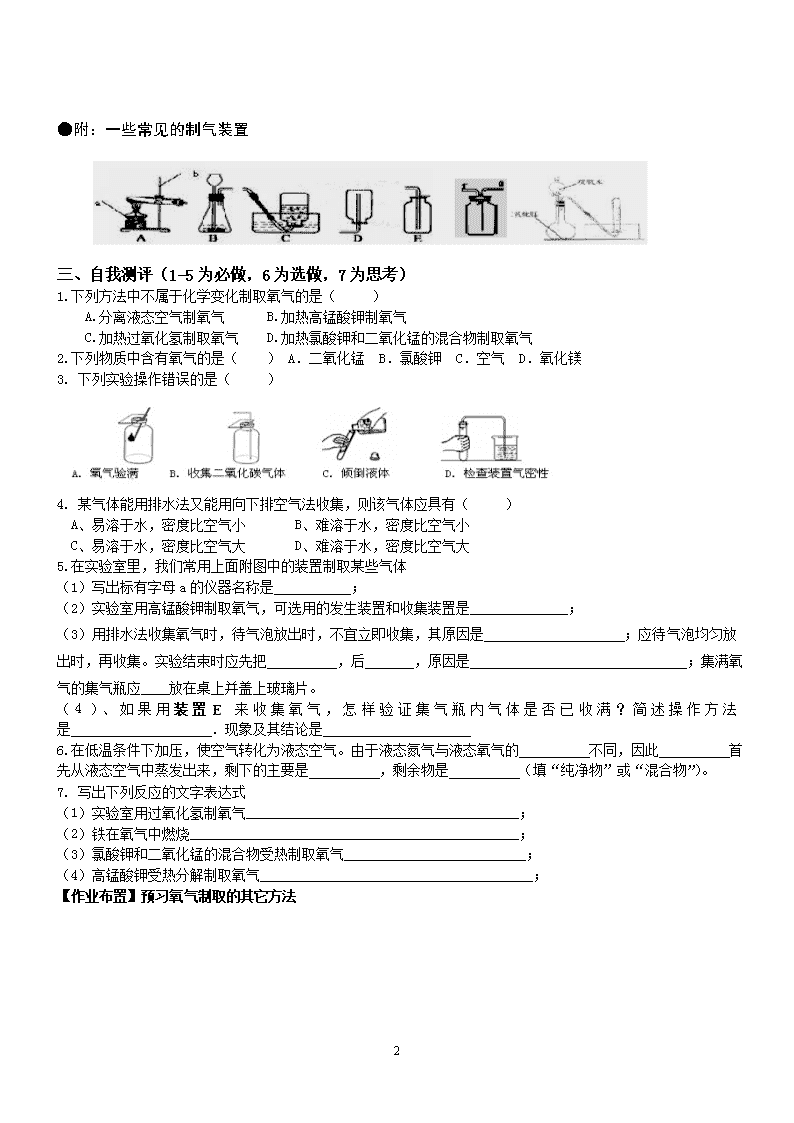
人教版九年级上册导学案2-3-制取氧气(第1课时)
1 课题:制取氧气(第一课时) 一、学习目标: 1.初步认识反应原理决定实验装置,气体的性质决定气体的收集方法。 2.能记住收集氧气及验满的方法。 3.通过练习连接仪器,熟练基本操作。 4.记住实验室制取氧气的步骤。 【课前知识积累】 1.空气中有多少体积的氧气? 2.实验室有几种制取氧气的方法? 【情境导入】上节课,我们用的氧气是怎么制取的呢? 二、自主探究: 知识点 1:如何制取气体(以高锰酸钾为例) 【观察】请用 3 分钟仔细观察课本 P37 图 2—14,回答下列问题: (1)在图中,使用了哪些仪器? (2)此装置适合于用哪种状态的物质来制取氧气? (3)哪部分是气体发生装置,哪部分是气体收集装置? 【讨论交流】阅读课本 P45-46 页,与小组成员讨论解决一下问题。 (1)加入药品之前,首先要检查装置的气密性,气密性良好,实验方可进行。如何检验装置气密性良好? (2)用高锰酸钾制氧气,为什么在试管口要塞一团棉花? (3)试管口为什么要略向下倾斜? (4)先对试管进行预热,然后对准有药品的部位集中加热。(否则会产生什么后果) (5)说出实验室可以利用什么方法收集氧气?它们是利用了氧气的什么性质? (6)导管口开始有气泡放出时,不宜立即收集,为什么?什么时候开始收集? (7)用什么方法收集氧气时需要验满?如何验满? (8)实验结束时,先把导管移出水面,然后再熄灭酒精灯。(如果先熄灭酒精灯,可能会造成什么后果?) 【归纳小结】 1.实验室装配仪器的一般顺序是什么? 2.总结一下实验室制取氧气的一般步骤有哪些?与小组成员交流一下?形成全班共识后记在下面。 【实验探究】小组合作制取 2 瓶氧气,完成实验 2-5。 知识点 2:工业上制取 O2 【阅读】用 2 分钟认真阅读课本 P40 资料。回答问题: 1.工业上大量制取氧气的原料是什么? 2.工业上大量制取氧气的原理是什么? 3.工业上制取氧气是物理变化还是化学变化? 【课堂小结】通过本节课的学习,你收获了什么? 【我的收获】 【知识总结】 1、实验室制取 O2 的实验步骤:(谐音记忆:茶庄定点收利息)⑴查:检查装置气密性;⑵装:装药品;⑶定: 固定装置;⑷点:点燃酒精灯加热;⑸收:收集气体;⑹离:从水中撤离导管;⑺熄:熄灭酒精灯。 2、工业上大量制取 O2 的流程: 空气 空气除去二氧化碳 干燥 ( ) 降温 加压 升温-196℃ 液态氧 升温-183℃ 2 ●附:一些常见的制气装置 三、自我测评(1-5 为必做,6 为选做,7 为思考) 1.下列方法中不属于化学变化制取氧气的是( ) A.分离液态空气制氧气 B.加热高锰酸钾制氧气 C.加热过氧化氢制取氧气 D.加热氯酸钾和二氧化锰的混合物制取氧气 2.下列物质中含有氧气的是( ) A.二氧化锰 B.氯酸钾 C.空气 D.氧化镁 3. 下列实验操作错误的是( ) 4. 某气体能用排水法又能用向下排空气法收集,则该气体应具有( ) A、易溶于水,密度比空气小 B、难溶于水,密度比空气小 C、易溶于水,密度比空气大 D、难溶于水,密度比空气大 5.在实验室里,我们常用上面附图中的装置制取某些气体 (1)写出标有字母 a 的仪器名称是 ; (2)实验室用高锰酸钾制取氧气,可选用的发生装置和收集装置是 ; (3)用排水法收集氧气时,待气泡放出时,不宜立即收集,其原因是 ;应待气泡均匀放 出时,再收集。实验结束时应先把 ,后 ,原因是 ;集满氧 气的集气瓶应 放在桌上并盖上玻璃片。 (4)、如果用装置 E 来收集氧气,怎样验证集气瓶内气体是否已收满?简述操作方法是 .现 象及其结论是 6.在低温条件下加压,使空气转化为液态空气。由于液态氮气与液态氧气的 不同,因此 首 先从液态空气中蒸发出来,剩下的主要是 ,剩余物是 (填“纯净物”或“混合物”)。 7. 写出下列反应的文字表达式 (1)实验室用过氧化氢制氧气_______________________________________; (2)铁在氧气中燃烧_______________________________________________; (3)氯酸钾和二氧化锰的混合物受热制取氧气__________________________; (4)高锰酸钾受热分解制取氧气_______________________________________; 【作业布置】预习氧气制取的其它方法查看更多