- 2021-11-10 发布 |
- 37.5 KB |
- 4页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
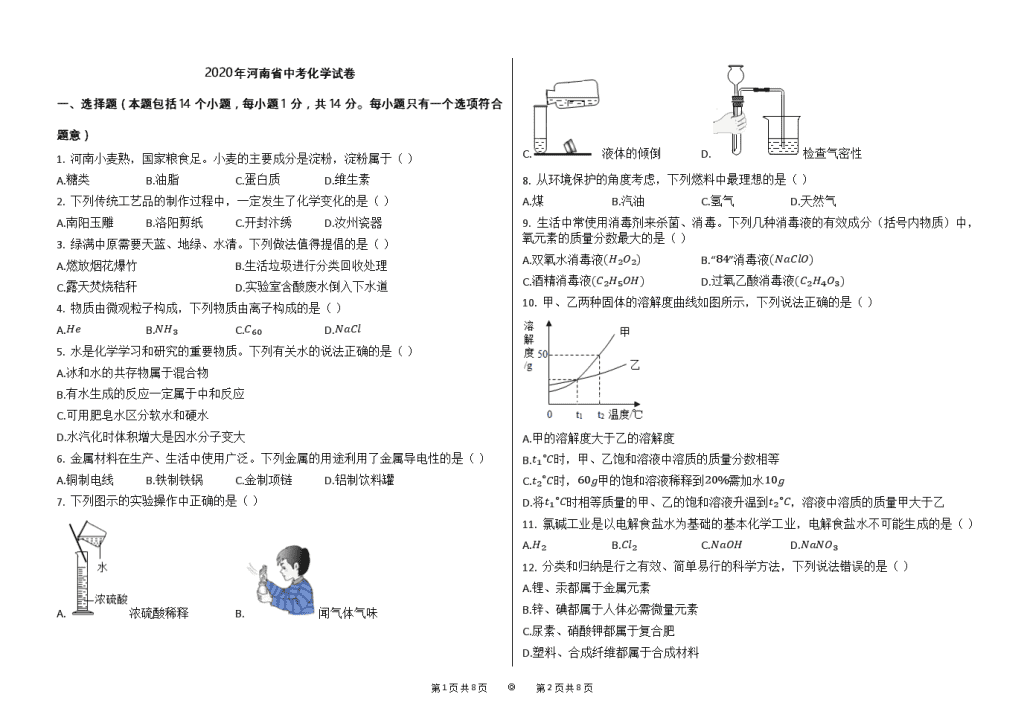
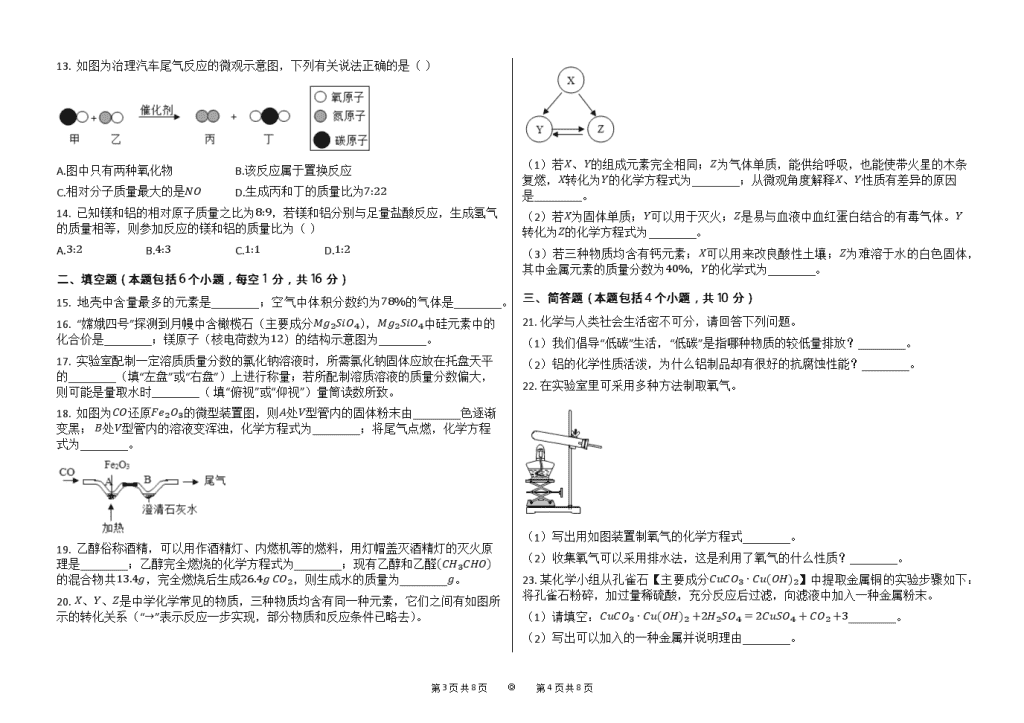
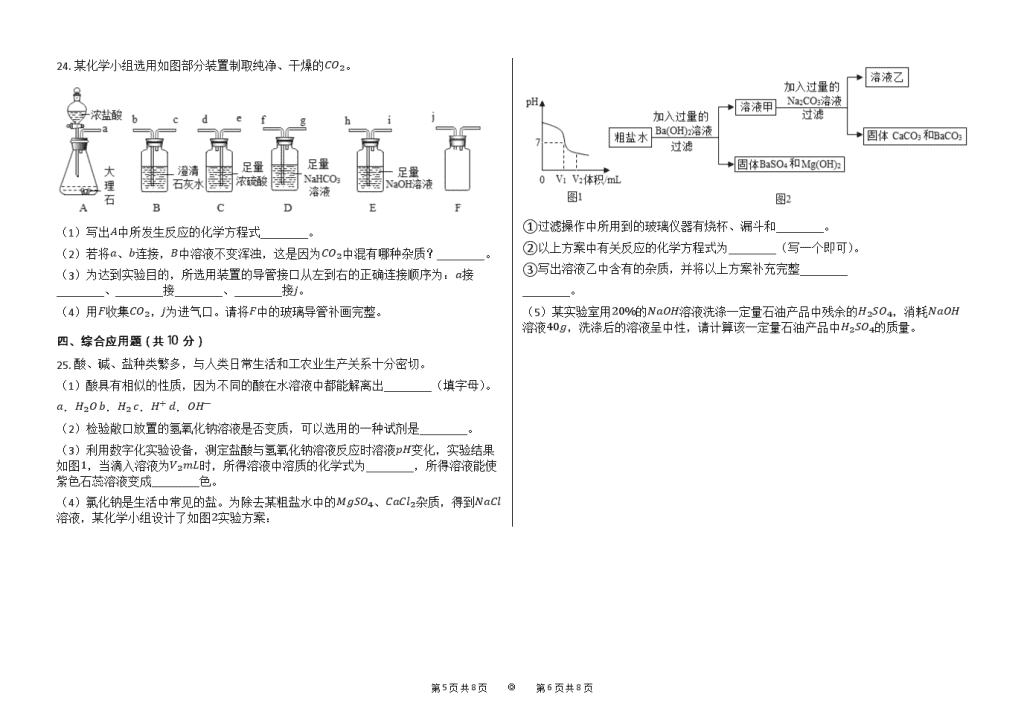
2020年河南省中考化学试卷【word版本;可编辑;含答案】
2020年河南省中考化学试卷 一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意) 1. 河南小麦熟,国家粮食足。小麦的主要成分是淀粉,淀粉属于( ) A.糖类 B.油脂 C.蛋白质 D.维生素 2. 下列传统工艺品的制作过程中,一定发生了化学变化的是( ) A.南阳玉雕 B.洛阳剪纸 C.开封汴绣 D.汝州瓷器 3. 绿满中原需要天蓝、地绿、水清。下列做法值得提倡的是( ) A.燃放烟花爆竹 B.生活垃圾进行分类回收处理 C.露天焚烧秸秆 D.实验室含酸废水倒入下水道 4. 物质由微观粒子构成,下列物质由离子构成的是( ) A.He B.NH3 C.C60 D.NaCl 5. 水是化学学习和研究的重要物质。下列有关水的说法正确的是( ) A.冰和水的共存物属于混合物 B.有水生成的反应一定属于中和反应 C.可用肥皂水区分软水和硬水 D.水汽化时体积增大是因水分子变大 6. 金属材料在生产、生活中使用广泛。下列金属的用途利用了金属导电性的是( ) A.铜制电线 B.铁制铁锅 C.金制项链 D.铝制饮料罐 7. 下列图示的实验操作中正确的是( ) A.浓硫酸稀释 B.闻气体气味 C.液体的倾倒 D.检查气密性 8. 从环境保护的角度考虑,下列燃料中最理想的是( ) A.煤 B.汽油 C.氢气 D.天然气 9. 生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是( ) A.双氧水消毒液(H2O2) B.“84”消毒液(NaClO) C.酒精消毒液(C2H5OH) D.过氧乙酸消毒液(C2H4O3) 10. 甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( ) A.甲的溶解度大于乙的溶解度 B.t1∘C时,甲、乙饱和溶液中溶质的质量分数相等 C.t2∘C时,60g甲的饱和溶液稀释到20%需加水10g D.将t1∘C时相等质量的甲、乙的饱和溶液升温到t2∘C,溶液中溶质的质量甲大于乙 11. 氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水不可能生成的是( ) A.H2 B.Cl2 C.NaOH D.NaNO3 第5页 共8页 ◎ 第6页 共8页 12. 分类和归纳是行之有效、简单易行的科学方法,下列说法错误的是( ) A.锂、汞都属于金属元素 B.锌、碘都属于人体必需微量元素 C.尿素、硝酸钾都属于复合肥 D.塑料、合成纤维都属于合成材料 13. 如图为治理汽车尾气反应的微观示意图,下列有关说法正确的是( ) A.图中只有两种氧化物 B.该反应属于置换反应 C.相对分子质量最大的是NO D.生成丙和丁的质量比为7:22 14. 已知镁和铝的相对原子质量之比为8:9,若镁和铝分别与足量盐酸反应,生成氢气的质量相等,则参加反应的镁和铝的质量比为( ) A.3:2 B.4:3 C.1:1 D.1:2 二、填空题(本题包括6个小题,每空1分,共16分) 15. 地壳中含量最多的元素是________;空气中体积分数约为78%的气体是________。 16. “嫦娥四号”探测到月幔中含橄榄石(主要成分Mg2SiO4),Mg2SiO4中硅元素中的化合价是________;镁原子(核电荷数为12)的结构示意图为________。 17. 实验室配制一定溶质质量分数的氯化钠溶液时,所需氯化钠固体应放在托盘天平的________(填“左盘”或“右盘”)上进行称量;若所配制溶质溶液的质量分数偏大,则可能是量取水时________( 填“俯视”或“仰视”)量筒读数所致。 18. 如图为CO还原Fe2O3的微型装置图,则A处V型管内的固体粉末由________色逐渐变黑; B处V型管内的溶液变浑浊,化学方程式为________;将尾气点燃,化学方程式为________。 19. 乙醇俗称酒精,可以用作酒精灯、内燃机等的燃料,用灯帽盖灭酒精灯的灭火原理是________;乙醇完全燃烧的化学方程式为________;现有乙醇和乙醛(CH3CHO)的混合物共13.4g,完全燃烧后生成26.4g CO2,则生成水的质量为________g。 20. X、Y、Z是中学化学常见的物质,三种物质均含有同一种元素,它们之间有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。 (1)若X、Y的组成元素完全相同;Z为气体单质,能供给呼吸,也能使带火星的木条复燃,X转化为Y的化学方程式为________;从微观角度解释X、Y性质有差异的原因是________。 (2)若X为固体单质;Y可以用于灭火;Z是易与血液中血红蛋白结合的有毒气体。Y转化为Z的化学方程式为________。 (3)若三种物质均含有钙元素;X可以用来改良酸性土壤;Z为难溶于水的白色固体,其中金属元素的质量分数为40%,Y的化学式为________。 三、简答题(本题包括4个小题,共10分) 21. 化学与人类社会生活密不可分,请回答下列问题。 (1)我们倡导“低碳”生活,“低碳”是指哪种物质的较低量排放?________。 (2)铝的化学性质活泼,为什么铝制品却有很好的抗腐蚀性能?________。 22. 在实验室里可采用多种方法制取氧气。 第5页 共8页 ◎ 第6页 共8页 (1)写出用如图装置制氧气的化学方程式________。 (2)收集氧气可以采用排水法,这是利用了氧气的什么性质?________。 23. 某化学小组从孔雀石【主要成分CuCO3⋅Cu(OH)2】中提取金属铜的实验步骤如下:将孔雀石粉碎,加过量稀硫酸,充分反应后过滤,向滤液中加入一种金属粉末。 (1)请填空:CuCO3⋅Cu(OH)2+2H2SO4=2CuSO4+CO2+3________。 (2)写出可以加入的一种金属并说明理由________。 24. 某化学小组选用如图部分装置制取纯净、干燥的CO2。 (1)写出A中所发生反应的化学方程式________。 (2)若将a、b连接,B中溶液不变浑浊,这是因为CO2中混有哪种杂质?________。 (3)为达到实验目的,所选用装置的导管接口从左到右的正确连接顺序为:a接________、________接________、________接j。 (4)用F收集CO2,j为进气口。请将F中的玻璃导管补画完整。 四、综合应用题(共10分) 25. 酸、碱、盐种类繁多,与人类日常生活和工农业生产关系十分密切。 (1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出________(填字母)。 a.H2O b.H2 c.H+ d.OH- (2)检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是________。 (3)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图1,当滴入溶液为V2mL时,所得溶液中溶质的化学式为________,所得溶液能使紫色石蕊溶液变成________色。 (4)氯化钠是生活中常见的盐。为除去某粗盐水中的MgSO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如图2实验方案: ①过滤操作中所用到的玻璃仪器有烧杯、漏斗和________。 ②以上方案中有关反应的化学方程式为________(写一个即可)。 ③写出溶液乙中含有的杂质,并将以上方案补充完整________ ________。 (5)某实验室用20%的NaOH溶液洗涤一定量石油产品中残余的H2SO4,消耗NaOH溶液40g,洗涤后的溶液呈中性,请计算该一定量石油产品中H2SO4的质量。 第5页 共8页 ◎ 第6页 共8页 参考答案与试题解析 2020年河南省中考化学试卷 一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意) 1.A 2.D 3.B 4.D 5.C 6.A 7.B 8.C 9.A 10.B 11.D 12.C 13.D 14.B 二、填空题(本题包括6个小题,每空1分,共16分) 15.氧(或O),氮气(或N2) 16.+4, 17.左盘,俯视 18.红棕,CO2+Ca(OH)2=CaCO3↓+H2O,2CO+O22CO2 19.隔绝氧气,C2H5OH+3022CO2+3H2O,12.6 20.2H2O2MnO22H2O+O2↑,分子的构成不同 CO2+C2CO CaCl2 三、简答题(本题包括4个小题,共10分) 21.二氧化碳 铝与氧气在常温下反应生成一层致密的氧化铝薄膜 22.2KClO3MnO2△2KCl+302↑ 不易溶于水且不与水发生化学反应 23.H2O 可以加入铁,是因为铁能和硫酸铜反应生成硫酸亚铁和铜 24.CaCO3+2HCl=CaCl2+H2O+CO2↑ 氯化氢 f,g,e,d 。 四、综合应用题(共10分) 25.c 氯化钙溶液 HCl、NaCl,红 玻璃棒,Ba(OH)2+MgSO4=BaSO4↓+Mg(OH)2↓或Ba(OH)2+Na2CO3=BaCO3↓+2NaOH或CaCl2+Na2CO3=CaCO3↓+2NaCl,溶液乙中含有的杂质:Na2CO3和NaOH;,补充方案:在溶液乙中加入适量稀盐酸 该一定量石油产品中硫酸的质量为9.8g。 第5页 共8页 ◎ 第6页 共8页查看更多