- 2021-11-10 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019年全国各地中考化学试题-广东省深圳市中考化学试题(解析)
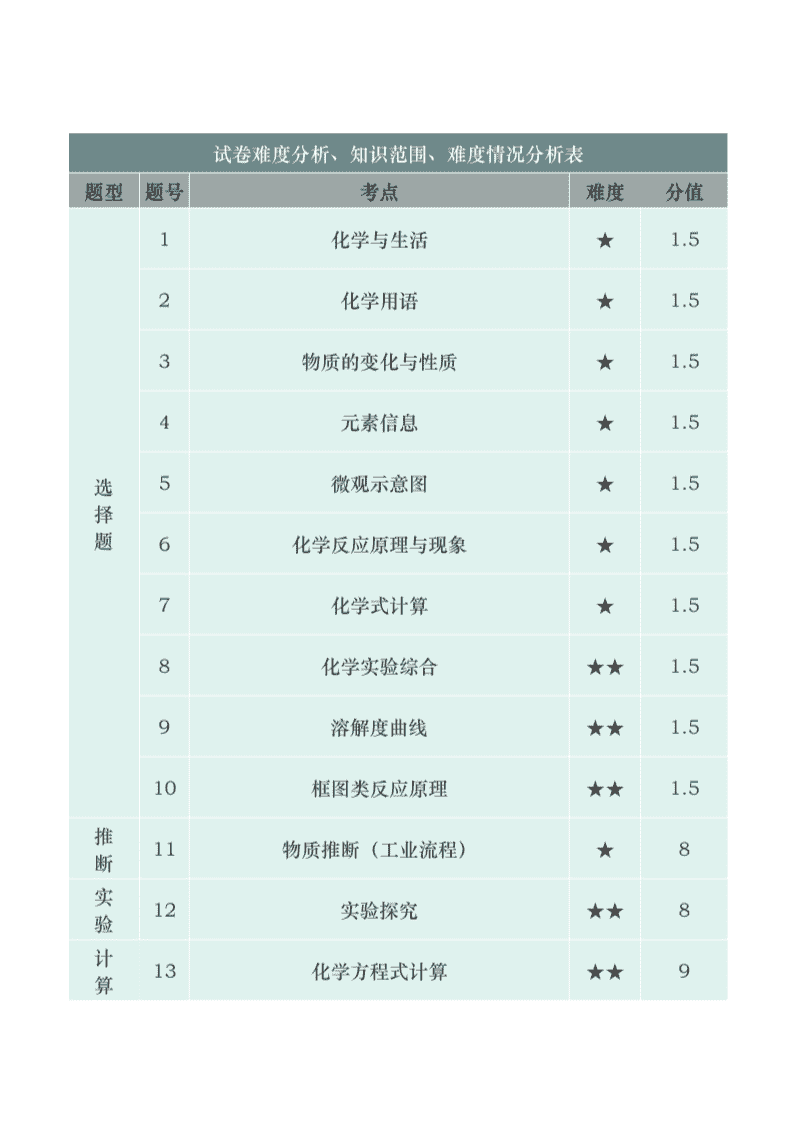
2019年深圳市中考化学试卷分析 试卷点评 今年的化学试卷与往年相比,难度有所增加,但整体难度与往年相比变化不大,在命题方面加重了综合能力的考查。 选择题方面,常规题型与往年相似,化学用语、元素信息、反应微观示意图、化学式计算、溶解度曲线与生活常识的考查基本沿用了往年固定的出题思路和考点。反应原理方面除了常规的现象和性质考查外,首次出现了框图型反应关系理解,这种题型未来有可能会演变为框图型推断。 推断题今年考查了工业流程的理解,但是流程图比较容易理解,属于课本中学过的知识,下面的问题设置与往年的框图型推断问题设置相似,并没有重点考查流程的理解,所以整体难度比较小,不易失分。 实验题今年第二次出现了探究实验,并首次出现了定量探究问题,这里可以算是今年化学中考的难点,需要学生对质量守恒定律有较深刻的认识并会灵活运动。 计算题考查形式与往年类似,依然考查了综合知识,在对数据的理解方面,采用了图象形式,但是数据不多,比较容易分析和作答。 2019 年深圳市中考化学试卷 一、选择题(共 10 小题,每小题 1.5 分,共 15 分。在每小题给出的 4 个选项中,只有一项符合题意。) 1.化学与人类的生产、生活密切相关。下列描述正确的是( ) A.引起贫血的主要原因是缺锌 B.不合理施用化肥会造成水体污染 C. 是电池回收标志 D.用水喷淋燃着的酒精以降低着火点 2.下列化学用语表述正确的是( ) A.硫酸钾的化学式:K2SO4 B.1 个氯分子:Cl ﹣ +2 C.2 个硝酸根:2NO2 D.铜离子:Cu 3.下列实验不涉及化学变化的是( ) A.测定空气中 B.验证浓 H2SO4 的腐 C.比较合金与纯金属 D.判断溶液的酸碱性 O2 的含量 蚀性 的硬度 4.钪(Kc)是一种“工业的维生素”。下图为钪在元素周期表中的相关信息及其原子的结构示意图。下列说法正确的是( ) A.钪属于非金属元素 B.钪的相对原子质量是 21 C.原子结构示意图中 X = 10 D.钪原子核外有四个电子层 5.科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),该反应过程的微观示意图如下。下列说法正确的是( ) A.物质甲为甲醛,其分子由碳原子和水分子构成 B.物质乙中氧元素的化合价为-2 价 C.该反应前后原子种类和数目均发生改变 D.该反应消耗物质甲和生成物质丁的质量比为 5﹕3 6.CuO 粉末与 H2 在加热条件下会发生反应。下列说法错误的是( ) A.反应所需 H2 可由 Cu 与稀 H2SO4 反应制得 B.反应过程可观察到固体粉末由黑色变成红色 C.发生的反应为 CuO + H2 △ Cu + H2O D.该反应说明 H2 具有还原性 7.异烟肼(化学式:C6H7N3O;相对分子质量:137)是治疗肺结核药物的有效成分。下列说法正确的是( ) A.异烟肼属于氧化物 B.异烟肼分子中 H、O 原子个数比为 7﹕1 C.异烟肼中 C、H 两种元素的质量比为 36﹕7 D.异烟肼中 N 元素质量分数的计算式为 14 ´100% 137 8.为达到以下实验目的,下列相应实验方案合理的是( ) 选项 实验目的 实验方案 A 获得廉价的新能源 电解水制 H2 B 将河水净化为纯水 经沉淀、过滤、吸附 C 验证金属活动性 Zn>Cu 利用 Zn 片与 CuSO4 溶液的反应 D 除去 NaCl 固体中少量的 MgCl2 加水溶解,再加入过量 NaOH 溶液 9.现有 t2℃时的溶液 I、II 各 100g,溶液 I 中含物质甲 50g,溶液 II 是物质乙的饱和溶液。物质甲、乙(均不含结晶水)的溶解 度曲线如图所示。下列说法正确的是() A.t2℃时,溶液 I 是甲的饱和溶液 B.t2℃时,溶液 I 中甲的质量分数为 50% C.t2℃时,溶液 II 中含乙 37g D.从 t2℃降温至 t1℃时,乙不会从溶液 II 中析出 10.关系图中“—”两端的物质能发生化学反应,“→”表示物质的转化方向。下列说法错 误的是( ) A.反应①放出热量 B.反应②所得溶液可呈中性 C.反应③可得 NaOH D.不能将图中稀盐酸换为稀 H2SO4 二、非选择题(共 3 题,共 25 分) 11.(8 分)生铁用途十分广泛。工业上利用赤铁矿(主要成分是 Fe2O3,还含少量 SiO2 等杂质)冶炼生铁的过程如下: 回答下列问题: (1)生铁属于______材料(填“合成”或“金属”)。“高炉气体”中的______(填化学 式)会导致酸雨。 (2)“煅烧”时: ①生成 CO 的反应之一为 C + CO2 高温 2CO,该反应属于_______反应(填基本反 应类型)。 ②用化学方程式表示利用 CO 炼铁的原理________________________________。 ③CaCO3 和 SiO2 固体在高温条件下发生反应,生成 CO2 气体和 CaSiO3,该反应 的化学方程式为____________________________。 (3)生活中铁制品锈蚀的过程,实际上是 Fe 与空气中________、_______等发生化学 反应的过程。下列措施能防止铁制品锈蚀的是______(填标号)。 A.涂油、喷漆 B.镀耐腐蚀的铬层 C.用盐水清洗 D.久置于酸性环境 12.(8 分)为探究某塑料的组成元素,设计了实验 I 和 II。回答下列问题: I.制取氧气 (1)若用一种暗紫色固体制取 O2,发生反应的化学方程式为_____________________, 发生装置应选择上述装置_____(填标号)。 (2)欲制取干燥的 O2,装置合理的连接顺序为:发生装置→C→_____(填标号)。连 接装置时,发生装置的出气口应与装置 C 中_____(填“a”或“b”)端相连。 II.组成探究 (3)定性检测(已知:无水 CuSO4 遇水变蓝色) 实验操作 实验现象 结论 连接装置,检查气密性,装入试 装置 K 中无水 CuSO4 变 塑料燃烧产物中有 H2O ①______色 剂并按上图进行实验。通入 O2, 装置 L 中②__________ 一段时间后,点燃 J 处酒精灯。 塑料燃烧产物中有 CO2 __________ ③由上述实验可知,该塑料一定含有的元素是________(填元素符号)。 (4)定量测定 为进一步确定组成,将 1.4g 该塑料在足量 O2 中完全燃烧,共产生了 4.4g CO2 和 1.8g H2O,依据质量守恒定律,可判断该塑料______(填“含有”或“不含”)除上述③中结论之外的元素。 13.(9 分)已知:①NaHCO3 固体受热分解 2NaHCO3 △ Na2CO3 + CO2↑+ H2O; ②Na2CO3 受热不分解。 回答下列问题: (1)关于 NaHCO3 固体的叙述错误的是______(填标号)。 A.俗称小苏打 B.难溶于水 C.可与稀盐酸发生反应 D.是发酵粉的主要成分之一 (2)欲测定某 NaHCO3 固体样品(只含 Na2CO3 杂质且分布均匀)中 NaHCO3 的质量分数,将 5.0g 该样品加热至质量不再改变,测得剩余固体的质量、生成 CO2 的质量随时间变化如图所示。 ①NaOH 溶液的 pH____7(填“>”、“=”或“<”),用该溶液将生成的 CO2 完全 吸收,发生反应的化学方程式为______________________。 ②由图中数据可知,上述 5.0g NaHCO3 样品完全分解产生 CO2 的质量为_____ g,产生 H2O 的质量是______ g。 ③计算该样品中 NaHCO3 的质量分数(根据化学方程式写出完整的计算步骤)。 2019 年深圳市中考化学试卷解析 1.【答案】B 【考点】化学与生活 【解析】B 选项中引起贫血的主要原因是缺铁;C 选项中的标志为塑料回收标志;D 选项中不可用水扑灭酒精着火且着火点为固定属性,不可降低。 2.【答案】A 【考点】化学语言 【解析】B 选项应为 Cl2;C 选项应为 2NO3﹣;D 选项应为 Cu2+。 3.【答案】C 【考点】物质的变化与性质 【解析】C 选项中没有新物质生成,属于物理变化;A、B、D 三个选项中均有新物质生成,属于化学变化。 4.【答案】D 【考点】元素信息与原子结构 【解析】A 选项中钪属于金属元素;B 选项钪的相对原子质量是 44.96;C 选项中 X = 8。 5.【答案】D 【考点】反应微观示意图 【解析】A 选项中甲醛分子由碳原子、氢原子和氧原子构成;B 选项中氧元素的化合价为 0 价;C 选项中反应前后原子的种类和数目均未发生改变。 6.【答案】A 【考点】反应原理与现象 【解析】A 选项中 Cu 与稀 H2SO4 不发生反应。 7.【答案】B 【考点】化学式及其计算 【解析】A 选项中异烟肼中有四种元素,不属于氧化物;C 选项异烟肼中 C、H 两种元素的质量比为 72﹕7;D 选项异烟肼中 N 元素质量分数的计算式为 14 ´ 3 ´100% 。 137 8.【答案】C 【考点】综合考查 【解析】A 选项中用电并不廉价;B 选项中还要进行蒸馏才能得到纯水;D 选项中需加入适量 NaOH 溶液。 9.【答案】B 【考点】溶解度曲线 【解析】A 选项中溶液 I 是甲的不饱和溶液;C 选项中溶液 II 中含乙的量大于 37g;D 选项中乙会从溶液 II 中析出。 10.【答案】D 【考点】反应原理 【解析】D 选项中稀盐酸可以换为稀 H2SO4。 11.【答案】(1)金属;SO2 (2)①化合 ②3CO + Fe2O3 高温 2Fe + 3CO2 ③CaCO3 + SiO2 高温 CaSiO3 + CO2↑ (3)水、氧气;AB 【考点】物质的性质及物质间的反应关系 【解析】本题主要考查了材料分类、空气污染问题、铁的冶炼、铁的生锈条件和防锈措施等。能够引起酸雨的是 SO2 和氮的氧化物;铁生锈需要与氧气和水同时接触,所以防锈措施包括隔绝水或氧气、保持干燥等方法。 12.【答案】(1)2KMnO4 △ K2MnO4 + MnO2 + O2↑;A (2)F;a (3)①蓝 ②澄清石灰水变浑浊 ③C、H (4)不含 【考点】实验探究 【解析】本题考查了氧气的制备和元素组成的探究。第(2)中需要制备干燥的氧气,所以应选择向上排空气法进行收集,(4)CO2 中 C 的质量是 1.2g,H2O 中 H 的质量是 0.2g,C、H 元素的质量和为 1.4g,与塑料的质量相等,所以塑料中不含 O 元素。 13.【答案】(1)B (2)①>;CO2 + 2NaOH = Na2CO3 + H2O ②1.1;0.45 ③解:设该样品中 NaHCO3 的质量为 X。 2NaHCO3 △ Na2CO3 + CO2↑+ H2O 168 44 X 1.1g 168 = X 44 1.1g X = 4.2g 该样品中 NaHCO3 的质量分数为 4.2g ´ 100% = 84% 5g 答:该样品中 NaHCO3 的质量分数为 84%。 【考点】物质的性质、应用和化学方程式的计算。 【解析】本题主要考查了信息理解和学生对图象数据的理解。查看更多