- 2021-11-06 发布 |
- 37.5 KB |
- 4页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
性质活泼的氧气 1课时
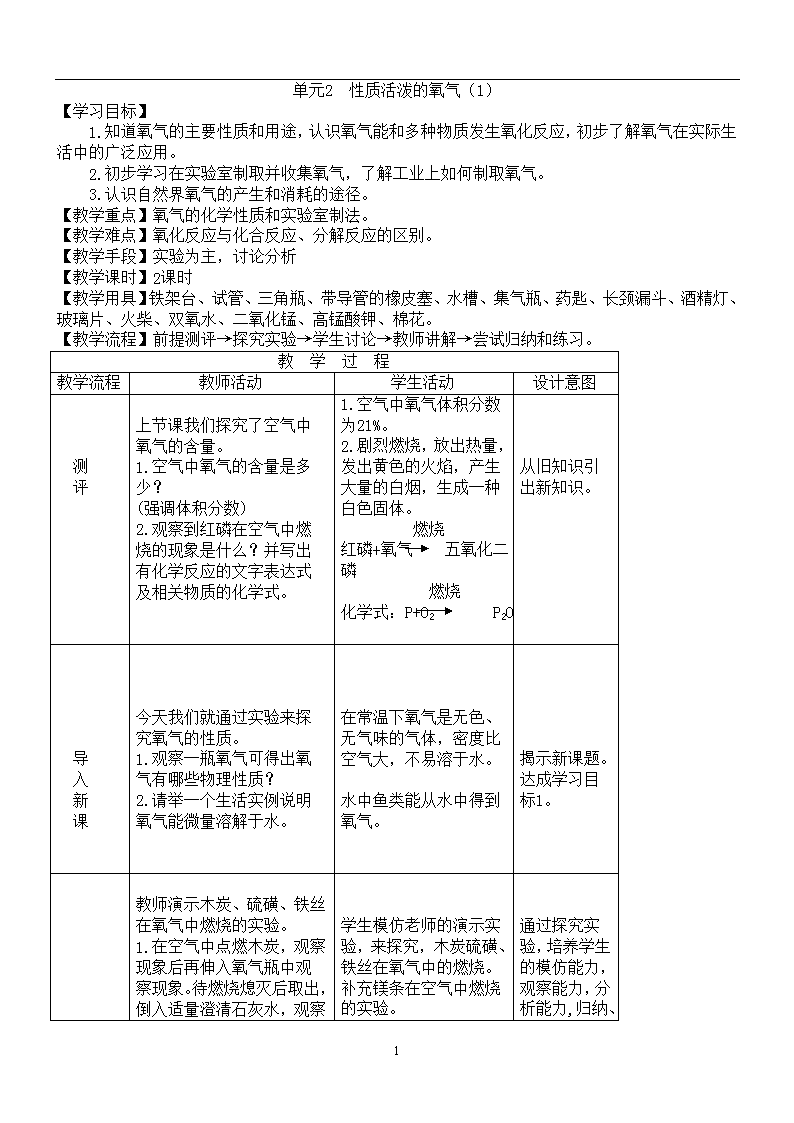
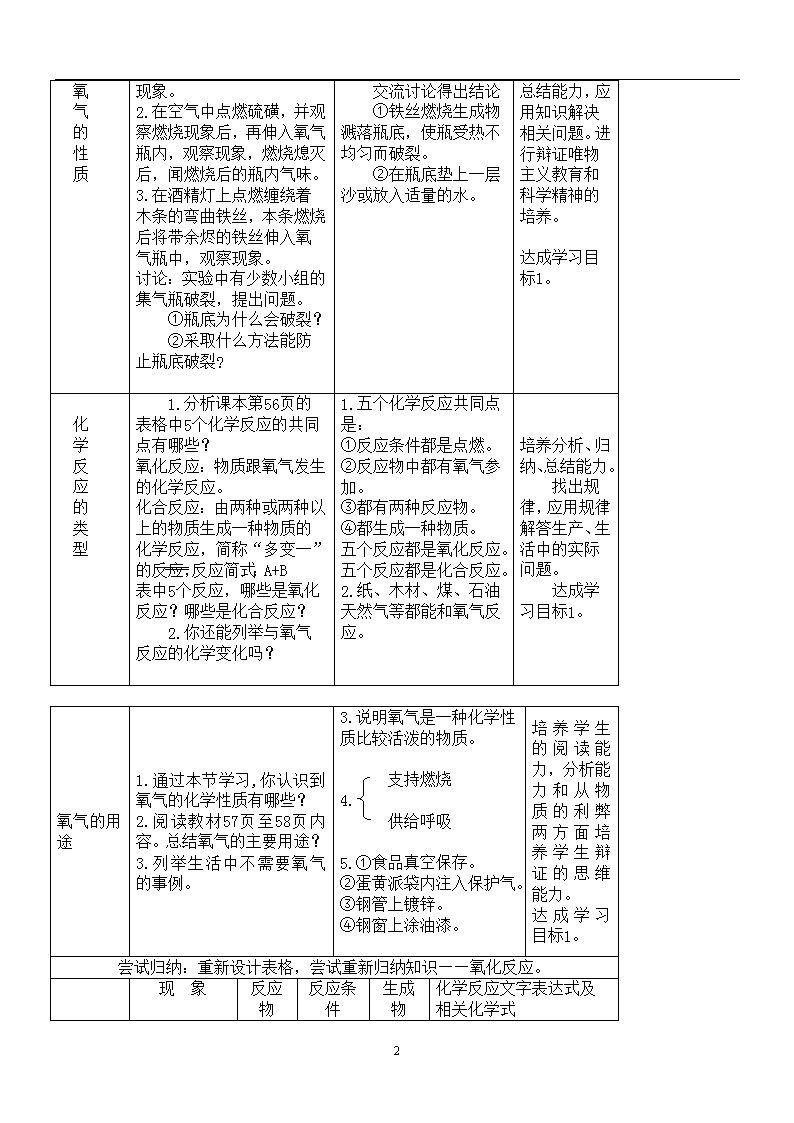
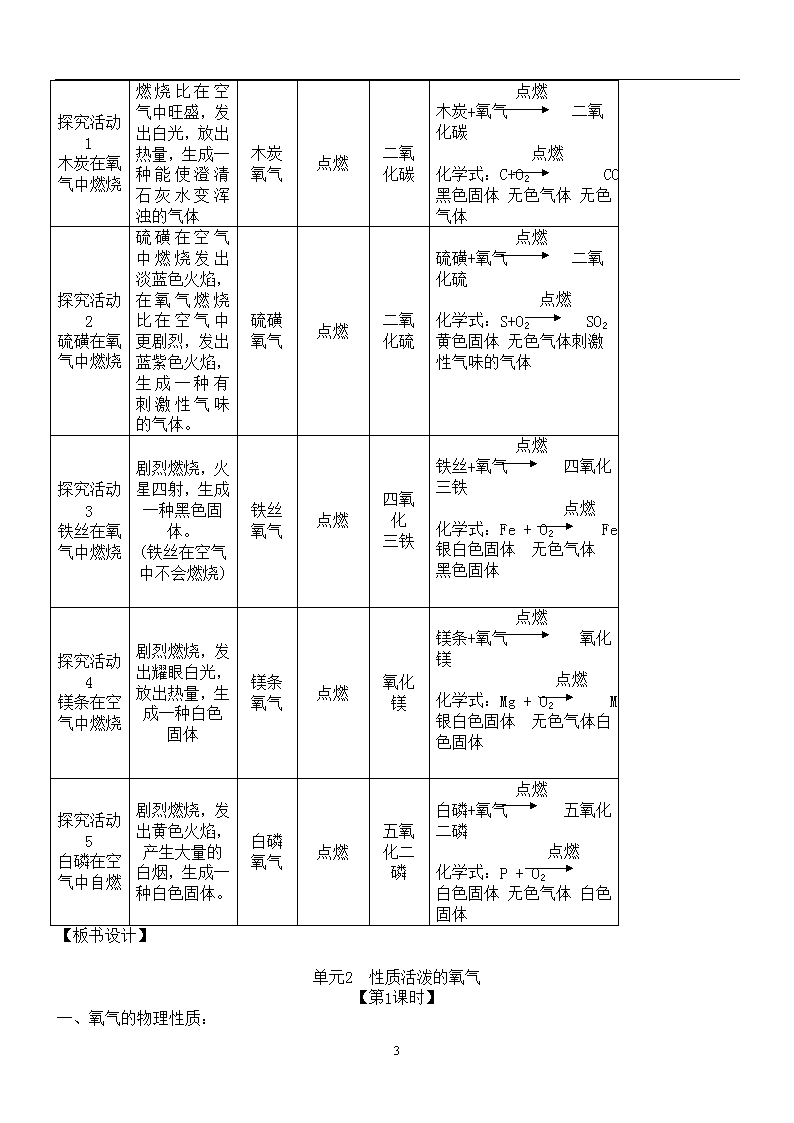
单元2 性质活泼的氧气(1) 【学习目标】 1.知道氧气的主要性质和用途,认识氧气能和多种物质发生氧化反应,初步了解氧气在实际生活中的广泛应用。 2.初步学习在实验室制取并收集氧气,了解工业上如何制取氧气。 3.认识自然界氧气的产生和消耗的途径。 【教学重点】氧气的化学性质和实验室制法。 【教学难点】氧化反应与化合反应、分解反应的区别。 【教学手段】实验为主,讨论分析 【教学课时】2课时 【教学用具】铁架台、试管、三角瓶、带导管的橡皮塞、水槽、集气瓶、药匙、长颈漏斗、酒精灯、玻璃片、火柴、双氧水、二氧化锰、高锰酸钾、棉花。 【教学流程】前提测评→探究实验→学生讨论→教师讲解→尝试归纳和练习。 教 学 过 程 教学流程 教师活动 学生活动 设计意图 测 评 上节课我们探究了空气中氧气的含量。 1.空气中氧气的含量是多少? (强调体积分数) 2.观察到红磷在空气中燃烧的现象是什么?并写出有化学反应的文字表达式及相关物质的化学式。 1.空气中氧气体积分数为21%。 2.剧烈燃烧,放出热量,发出黄色的火焰,产生大量的白烟,生成一种白色固体。 燃烧 红磷+氧气 五氧化二磷 燃烧 化学式:P+O2 P2O5 从旧知识引出新知识。 导 入 新 课 今天我们就通过实验来探究氧气的性质。 1.观察一瓶氧气可得出氧气有哪些物理性质? 2.请举一个生活实例说明氧气能微量溶解于水。 在常温下氧气是无色、无气味的气体,密度比空气大,不易溶于水。 水中鱼类能从水中得到氧气。 揭示新课题。 达成学习目标1。 教师演示木炭、硫磺、铁丝在氧气中燃烧的实验。 1. 学生模仿老师的演示实验,来探究,木炭硫磺、铁丝在氧气中的燃烧。补充镁条在空气中燃烧的实验。 4 氧 气 的 性 质 在空气中点燃木炭,观察现象后再伸入氧气瓶中观察现象。待燃烧熄灭后取出,倒入适量澄清石灰水,观察现象。 2.在空气中点燃硫磺,并观察燃烧现象后,再伸入氧气瓶内,观察现象,燃烧熄灭后,闻燃烧后的瓶内气味。 3.在酒精灯上点燃缠绕着木条的弯曲铁丝,本条燃烧后将带余烬的铁丝伸入氧气瓶中,观察现象。 讨论:实验中有少数小组的集气瓶破裂,提出问题。 ①瓶底为什么会破裂? ②采取什么方法能防止瓶底破裂? 交流讨论得出结论 ①铁丝燃烧生成物溅落瓶底,使瓶受热不均匀而破裂。 ②在瓶底垫上一层沙或放入适量的水。 通过探究实验,培养学生的模仿能力,观察能力,分析能力,归纳、总结能力,应用知识解决相关问题。进行辩证唯物主义教育和科学精神的培养。 达成学习目标1。 化 学 反 应 的 类 型 1.分析课本第56页的表格中5个化学反应的共同点有哪些? 氧化反应:物质跟氧气发生的化学反应。 化合反应:由两种或两种以上的物质生成一种物质的化学反应,简称“多变一”的反应,反应简式:A+B C。表中5个反应,哪些是氧化反应?哪些是化合反应? 2.你还能列举与氧气反应的化学变化吗? 1.五个化学反应共同点是: ①反应条件都是点燃。 ②反应物中都有氧气参加。 ③都有两种反应物。 ④都生成一种物质。 五个反应都是氧化反应。五个反应都是化合反应。 2.纸、木材、煤、石油天然气等都能和氧气反应。 培养分析、归纳、总结能力。 找出规律,应用规律解答生产、生活中的实际问题。 达成学习目标1。 氧气的用途 1.通过本节学习,你认识到氧气的化学性质有哪些? 2.阅读教材57页至58页内容。总结氧气的主要用途? 3.列举生活中不需要氧气的事例。 3.说明氧气是一种化学性质比较活泼的物质。 支持燃烧 4. 供给呼吸 5.①食品真空保存。 ②蛋黄派袋内注入保护气。 ③钢管上镀锌。 ④钢窗上涂油漆。 培养学生的阅读能力,分析能力和从物质的利弊两方面培养学生辩证的思维能力。 达成学习目标1。 尝试归纳:重新设计表格,尝试重新归纳知识——氧化反应。 现 象 反应物 反应条件 生成物 化学反应文字表达式及相关化学式 4 探究活动1 木炭在氧气中燃烧 燃烧比在空气中旺盛,发出白光,放出热量,生成一种能使澄清石灰水变浑浊的气体 木炭 氧气 点燃 二氧 化碳 点燃 木炭+氧气 二氧化碳 点燃 化学式:C+O2 CO2 黑色固体 无色气体 无色气体 探究活动2 硫磺在氧气中燃烧 硫磺在空气中燃烧发出淡蓝色火焰,在氧气燃烧比在空气中更剧烈,发出蓝紫色火焰,生成一种有刺激性气味的气体。 硫磺 氧气 点燃 二氧 化硫 点燃 硫磺+氧气 二氧化硫 点燃 化学式:S+O2 SO2 黄色固体 无色气体刺激性气味的气体 探究活动3 铁丝在氧气中燃烧 剧烈燃烧,火星四射,生成一种黑色固体。 (铁丝在空气中不会燃烧) 铁丝 氧气 点燃 四氧化 三铁 点燃 铁丝+氧气 四氧化三铁 点燃 化学式:Fe + O2 Fe3O4 银白色固体 无色气体 黑色固体 探究活动4 镁条在空气中燃烧 剧烈燃烧,发出耀眼白光,放出热量,生成一种白色固体 镁条 氧气 点燃 氧化镁 点燃 镁条+氧气 氧化镁 点燃 化学式:Mg + O2 MgO 银白色固体 无色气体 白色固体 探究活动5 白磷在空气中自燃 剧烈燃烧,发出黄色火焰,产生大量的白烟,生成一种白色固体。 白磷 氧气 点燃 五氧化二磷 点燃 白磷+氧气 五氧化二磷 点燃 化学式:P + O2 P2O5 白色固体 无色气体 白色固体 【板书设计】 单元2 性质活泼的氧气 【第1课时】 一、氧气的物理性质: 4 无色、无气味的气体,不易溶于水,密度比空气大。 二、氧气的化学性质: 点燃 1.C+O2 CO2 点燃 2.S+O2 SO2 点燃 3.Mg+O2 MgO 点燃 4.Fe+O2 Fe3O4 点燃 5.Al+O2 Al2O3 点燃 6.P+O2 P2O5 点燃 7.石蜡+O2 CO2+H2O 三、化学反应的类型 1.化合反应 2.氧化反应 四、氧气用途: 1.支持燃烧 2.供给呼吸 4查看更多