全国版2021高考化学一轮复习课时作业31水的电离和溶液的酸碱性含解析
课时作业(三十一) 水的电离和溶液的酸碱性
1.(2019·福建厦门质检)下列微粒不会影响水的电离平衡的是( )
A. B.
C.Cl—O—H D.
A [代表Na+,是强碱NaOH对应的阳离子,不发生水解,故不影响水的电离,A正确;S2-易发生水解反应而促进水的电离,B错误;HClO属于弱酸,部分电离产生H+和ClO-,抑制水的电离,C错误;代表CH3COOH,部分电离产生H+和CH3COO-,抑制水的电离,D错误。]
2.(2019·天津河西区模拟)已知40 ℃时水的离子积常数为Kw。该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,该溶液呈中性时,下列叙述不正确的是( )
A.a=b,pH=7
B.混合溶液的c(H+)=c(OH-)
C.混合溶液中c(B+)=c(A-)
D.混合溶液中c(OH-)= mol·L-1
A [40 ℃时水的离子积常数Kw>1.0×10-14,溶液呈中性时,pH<7,故pH=7的溶液呈碱性,A错误;混合溶液的c(H+)=c(OH-),则该溶液呈中性,B正确;混合溶液呈电中性,据电荷守恒可得c(B+)+c(H+)=c(A-)+c(OH-),若溶液中c(B+)=c(A-),故c(H+)=c(OH-),则该溶液呈中性,C正确;在水溶液中,Kw=c(H+)·c(OH-),将c(H+)= mol·L-1代入可得c(OH-)= mol·L-1,此时c(H+)=c(OH-),则该溶液呈中性,D正确。]
3.(2019·湖南双峰模拟)某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的c(H+)为1.0×10-10 mol·L-1
C.加入NaHSO4晶体,抑制了水的电离
D.该温度下加入等体积pH=12的NaOH溶液,可使该溶液恰好呈中性
D [该温度下蒸馏水呈中性,其pH=6,则有Kw=c(H+)·c(OH-)=1×10-12,温度越高,Kw越大,故该温度高于25 ℃,A正确;加入NaHSO4晶体后,溶液的pH=2,则水电离出的c(H+)水=c(OH-)水=1.0×10-10 mol·L-1,B正确;加入NaHSO4晶体后,电离产生H+,使溶液呈酸性,抑制水的电离,C正确;该温度下,pH=12的NaOH溶液中c(OH-)=1
8
mol·L-1,若加入等体积pH=12的NaOH溶液,充分反应后NaOH剩余,所得溶液呈碱性,D错误。]
4.(2019·黑龙江大庆模拟)下列叙述正确的是( )
A.95 ℃时纯水的pH<7,说明加热可导致水呈酸性
B.室温下,pH=5的盐酸溶液,加水稀释至溶液的体积为原溶液体积的103倍后pH=8
C.pH=1的盐酸与等体积pH=3的盐酸混合后pH=2
D.25 ℃时,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH<7
D [升高温度,水的电离程度增大,水电离产生的c(H+)增大,溶液的pH减小,但水仍呈中性,A错误;室温下,pH=5的盐酸加水稀释至原溶液体积的103倍,溶液仍呈酸性,则pH<7,B错误;pH=1的盐酸与pH=3的盐酸等体积混合后,所得混合液的pH<2,C错误;醋酸是弱电解质,pH=3的醋酸溶液中c(CH3COOH)>1×10-3 mol·L-1,pH=11的NaOH溶液中c(NaOH)=1×10-3mol·L-1,二者等体积混合后,醋酸剩余,所得混合液呈酸性,则有pH<7,D正确。]
5.(2019·福建四校联考)常温下,0.1 mol·L-1某一元酸(HA)溶液中=1.0×10-8,则下列叙述中正确的是( )
A.该一元酸溶液的pH=1
B.该溶液中由水电离出的c(H+)=1.0×10-3 mol·L-1
C.该溶液中水的离子积常数为1.0×10-22
D.用0.1 mol·L-1NaOH溶液V1 L与V2 L 0.1 mol·L-1该一元酸(HA)溶液混合,若混合溶液的pH=7,则V1
7,故A错误;醋酸溶液中存在CH3COOHCH3COO-+H+,加NaOH溶液消耗氢离子,醋酸的电离平衡正向移动,所以从a到c,醋酸的电离始终受到促进,故B错误;e点所示溶液中,加入的NaOH的物质的量是醋酸的物质的量的2倍,反应后溶液中醋酸钠和NaOH物质的量相等,根据物料守恒得c(Na+)=2c(CH3COO-)+2c(CH3COOH)=0.01 mol·L-1×,故C错误;c点,醋酸与氢氧化钠恰好反应生成醋酸钠,溶液显碱性,氢氧化钠溶液体积小于20 mL时的某一个值恰好使溶液显中性,所以从a→c的过程中,存在着pH=7的点,故D正确。]
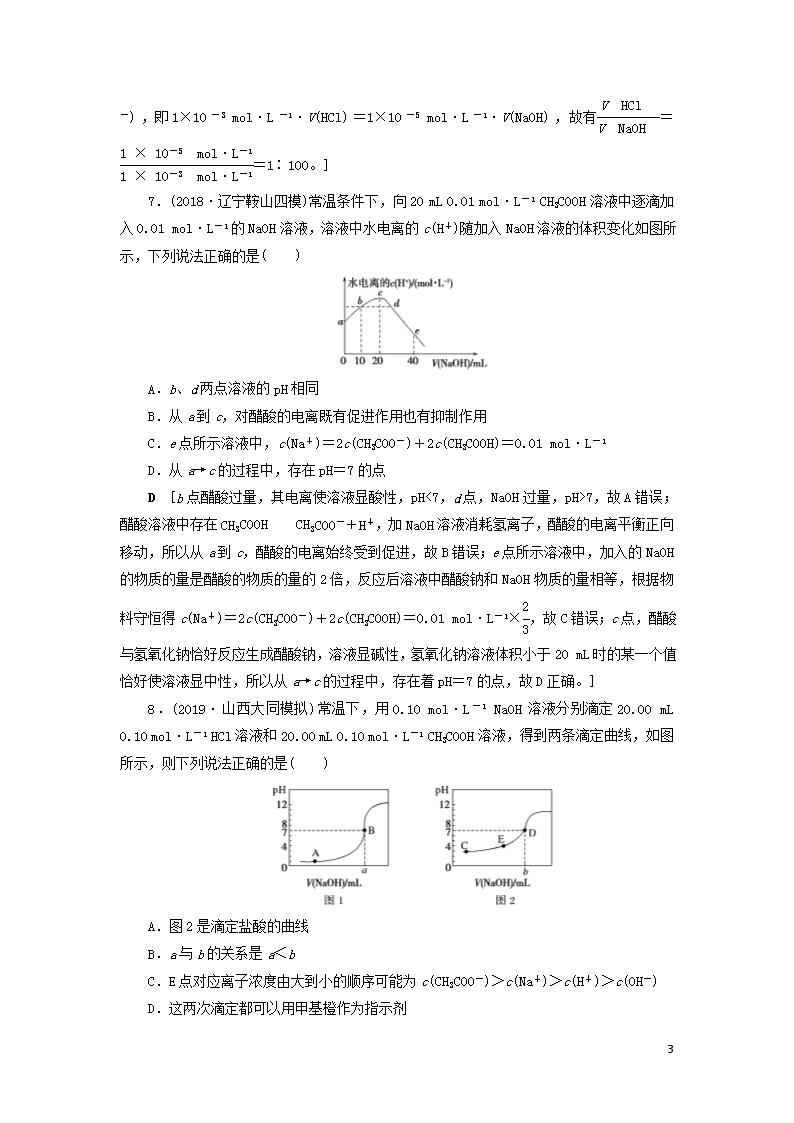
8.(2019·山西大同模拟)常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到两条滴定曲线,如图所示,则下列说法正确的是( )
A.图2是滴定盐酸的曲线
B.a与b的关系是a<b
C.E点对应离子浓度由大到小的顺序可能为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.这两次滴定都可以用甲基橙作为指示剂
8
C [如果酸为强酸,则0.10 mol·L-1酸的pH为1,根据酸的初始pH知,图1为盐酸的滴定曲线,故A错误;根据图1知,a点氢氧化钠溶液的体积是20.00 mL,酸和碱的物质的量相等,二者恰好反应生成强酸强碱盐,其溶液呈中性;醋酸溶液中滴入氢氧化钠溶液,醋酸钠溶液呈碱性,所以氢氧化钠溶液的体积小于20.00 mL,a>b,故B错误;E点溶液的成分为醋酸钠和醋酸,溶液呈酸性,说明醋酸的电离程度大于醋酸钠的水解程度,盐类水解程度较小,则溶液中离子浓度可能为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C正确;氢氧化钠和盐酸恰好反应呈中性,可以选择甲基橙或酚酞;氢氧化钠和醋酸恰好反应生成醋酸钠溶液呈碱性,只能选择酚酞,故D错误。]
9.(2019·河南中原名校联考)已知100 ℃时,水的离子积常数为Kw=1×10-12,对于该温度下pH=11的氨水,下列叙述正确的是( )
A.向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B.温度降低至25 ℃,该氨水溶液中H2O电离出的c(H+)小于10-11 mol·L-1
C.该氨水溶液中加入少量NH4Cl固体,NH3·H2O的电离程度增大
D.滴加等浓度、等体积的硫酸,所得溶液中存在电离平衡:NH4HSO4(aq)NH(aq)+H+(aq)+SO(aq)
B [100 ℃时,Kw=1×10-12,pH=11的氨水中c(OH-)=0.1 mol·L-1,则c(NH3·H2O)>0.1 mol·L-1,与同温同体积pH=1的盐酸混合,反应后氨水剩余,所得溶液呈碱性,A错误。100 ℃时,该氨水中水电离出的c(H+)水=c(OH-)水=1×10-11 mol·L-1;温度降低至25 ℃,水的离子积Kw减小,水的电离程度减小,则H2O电离出的c(H+)小于10-11 mol·L-1,B正确。氨水中存在电离平衡:NH3·H2ONH+OH-,加入少量NH4Cl固体,c(NH)增大,NH3·H2O的电离平衡逆向移动,电离程度减小,C错误。NH4HSO4是强电解质,在水溶液中完全电离,不存在电离平衡,D错误。]
10.(2018·四川南充二诊)25 ℃时,0.1 mol·L-1的3种溶液:①盐酸、②氨水、③CH3COONa溶液。下列说法中,不正确的是( )
A.3种溶液中pH最小的是①
B.3种溶液中水的电离程度最大的是③
C.①与②等体积混合后溶液显酸性
D.①与③等体积混合后:c(Na+)>c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
D [盐酸呈酸性,氨水和CH3COONa溶液呈碱性,则pH最小的是盐酸,A正确;盐酸和氨水抑制水的电离,CH3COONa因发生水解而促进水的电离,故水的电离程度最大的是CH3COONa,B正确;等浓度、等体积的盐酸和氨水混合,二者恰好完全反应生成NH4Cl,由于NH发生水解而使溶液呈酸性,C正确;等浓度、等体积的盐酸和CH3COONa溶液混合,二者恰好完全反应生成CH3COOH和NaCl,由于Na+、Cl-均不发生水解,则有c(Na+)=c(Cl-),D错误。]
8
11.(2019·广西钦州质检)常温下,浓度均为1.0 mol·L-1的HX溶液、HY溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )
A.HX是强酸,溶液每稀释10倍,pH始终增大1
B.常温下HY的电离常数约为1.0×10-4
C.溶液中水的电离程度:a点大于b点
D.消耗同浓度的NaOH溶液体积:a点大于b点
B [由图可知,常温下1.0 mol·L-1 HX和HY溶液的pH分别为0、2.0,则HX是强酸,HY是弱酸,稀释HX溶液,开始阶段每稀释10倍pH增大1,溶液较稀时,再稀释10倍pH增大小于1,pH始终小于7,A错误。由图可知,c(HY)=10-2 mol·L-1时溶液的pH=3.0,则HY的电离平衡常数为Ka(HY)==≈1.0×10-4,B正确。a点溶液的pH小于b点,则a点溶液的酸性强于b点,而酸性越强,水的电离程度越小,故水的电离程度:ac(A2-)>c(HA-)>c(OH-)>c(H+)
D.若溶液中加NaOH至=100时,c(OH-)>100 c(H+)
D [初始时,0.1 mol·L-1H2A溶液的pH=3.8,根据氢离子浓度的近似计算公式c(H+)===10-3.8 mol·L-1,所以Kal=10-6.6,其数量级为10-7,A错误。初始时,0.1 mol·L-1H2A溶液对于水的电离一定是抑制,随着H2
8
A逐渐被中和,转化为盐,则变成对水的电离产生促进,最后氢氧化钠过量,再对水的电离产生抑制,B错误。加入的氢氧化钠为0.6 g(0.015 mol)时,溶液为浓度相等的Na2A和NaHA混合溶液,由表中数据得到此时溶液一定显碱性,因为A2-的水解能力强于HA-,且A2-水解得到HA-,所以c(A2-)8时,一定有c(OH-)>100 c(H+),D正确。]
13.(2019·江苏扬州调研)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO)。饮用水中的ClO2、ClO含量可用连续碘量法进行测定。ClO2被I-还原为ClO、Cl-的转化率与溶液pH的关系如图所示。当pH≤2.0时,ClO也能被I-完全还原为Cl-。反应生成的I2用标准Na2S2O3溶液滴定:2Na2S2O3+I2===Na2S4O6+2NaI。
(1)请写出pH≤2.0时ClO与I-反应的离子方程式:
________________________________________________________________________。
(2)请完成相应的实验步骤:
步骤1:准确量取V mL水样加入到锥形瓶中;
步骤2:调节水样的pH为7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1 mL;
步骤5:________________________________________________________________________;
步骤6:再用c mol·L-1Na2S2O3溶液滴定至终点,又消耗Na2S2O3溶液V2 mL。
(3)根据上述分析数据,测得该饮用水中ClO的浓度为________mol·L-1(用含字母的代数式表示)。
解析 (3)根据电子守恒可得pH为7.0~8.0时反应的关系式:
ClO2 ~I2~ Na2S2O3
8
cV1×10-3mol cV1×10-3mol
pH≤2.0时,反应的关系式:
ClO ~2I2~ 4Na2S2O3
×10-3mol cV2×10-3mol
故原水样中含有n(ClO)=×10-3mol
c(ClO)=mol·L-1。
答案 (1)ClO+4H++4I-===Cl-+2I2+2H2O
(2)调节溶液的pH≤2.0 (3)
14.六氨氯化镁 (MgCl2·6NH3)具有极好的可逆性、放氨特性,是一种优良的储氨材料。某研究小组在实验室以菱镁矿(主要成分 MgCO3,含少量 FeCO3等杂质)为原料制备了六氨氯化镁,现在对产品的成分进行测定,其中氯离子含量检测方法如下:
A.称取1.420 g样品,加足量硫酸溶解,配制成250 mL溶液;
B.量取25.00 mL待测液于锥形瓶中;
C.用0.200 0 mol/L AgNO3标准溶液滴定至终点,记录消耗AgNO3标准溶液的体积;
D.重复b、c操作2~3次,平均消耗AgNO3标准溶液10.00 mL 。
(1)配制样品溶液时加硝酸的原因________________________________________________________________________
______________。
(2)该样品中氯离子百分含量为________。
(3)将氯离子百分含量实验值与理论值 (36.04%)相比较,请分析造成此结果的可能原因有________________________________(已知滴定操作正确、硫酸根离子对检测无影响)。
解析 (1)检验Cl-需要用AgNO3,而Ag+能与NH3络合生成[Ag(NH3)2]+,所以加入硝酸除去NH3;(2)由实验数据可得n(AgNO3)=10.00×10-3L×0.200 0 mol·L-1=0.002 000 mol,所以Cl-的百分含量=×100%=50.00%;(3)根据MgCl2·6NH3的组成可得,其中Cl-的百分含量=×100%=36.04%,但实验结果偏高,可能是MgCl2没有完全氨化,也可能是产品在称量时已有部分氨气逸出。
答案 (1)除去NH3,避免 NH3与Ag+发生络合,干扰检测 (2)50.00% (3)氨化过程不完全或晶体称量时已有部分氨气逸出
8
8