- 2021-08-24 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高考化学第一轮复习课件第3讲 铁及其重要化合物-3真题演练·部分真题解读
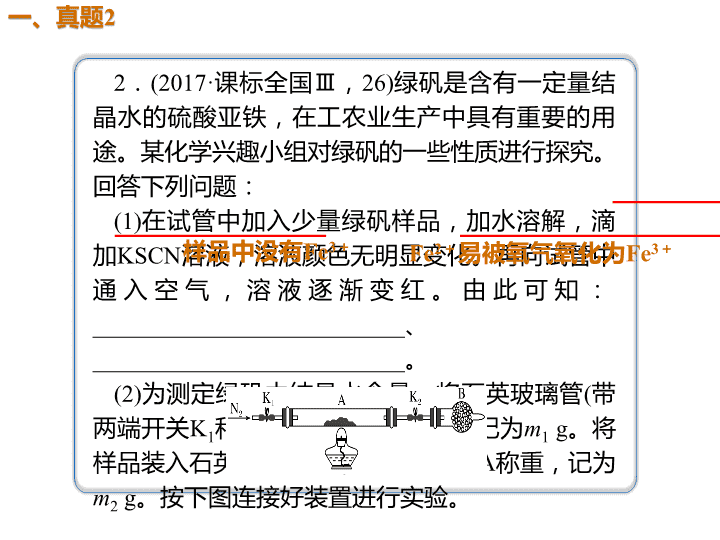
04 2.(2017·课标全国Ⅲ,26)绿矾是含有一定量结 晶水的硫酸亚铁,在工农业生产中具有重要的用 途。某化学兴趣小组对绿矾的一些性质进行探究。 回答下列问题: (1)在试管中加入少量绿矾样品,加水溶解,滴 加KSCN溶液,溶液颜色无明显变化。再向试管中 通 入 空 气 , 溶 液 逐 渐 变 红 。 由 此 可 知 : _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 、 __________________________。 (2)为测定绿矾中结晶水含量,将石英玻璃管(带 两端开关K1和K2)(设为装置A)称重,记为m1 g。将 样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。 样品中没有Fe3+ Fe2+易被氧气氧化为Fe3+ ①仪器B的名称是________。 ② 将 下 列 实 验 操 作 步 骤 正 确 排 序 ___________________________ (填标号);重复上述操作步骤,直至A恒重,记 为m3 g。 a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温 ③根据实验记录,计算绿矾化学式中结晶水数目 x=________(列式表示)。若实验时按a、d次序操作, 则使x________(填“偏大”“偏小”或“无影响”)。 干燥管 d、a、b、f、c、e 偏小 注意绿矾中Fe2+的保护 (3)为探究硫酸亚铁的分解产物,将(2)中已恒重 的装置A接入下图所示的装置中,打开K1和K2, 缓缓通入N2,加热。实验后反应管中残留固体为 红色粉末。 ①C、D中的溶液依次为________(填标号)。C、 D 中 有 气 泡 冒 出 , 并 可 观 察 到 的 现 象 分 别 为 ____________________________________。 a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4 ②写出硫酸亚铁高温分解反应的化学方程式 _________________________________________ c、a 生成白色沉淀、褪色 2FeSO4 Fe2O3+SO2↑+SO3↑ (3)①实验后反应管中残留的红色粉末为Fe2O3,根据得失电 子守恒可知必然有SO2产生,根据元素守恒可知还会生成SO3, 检验的试剂应选择品红溶液、BaCl2溶液,不能选择Ba(NO3)2 溶液,因为SO2会与Ba(NO3)2溶液产生白色沉淀,干扰SO3 的 检验,由于SO3可与水反应生成硫酸,故应先检验SO3,再利 用SO2能使品红褪色的原理检验SO2;②由题意可以得到硫酸 亚铁分解的方程式为2FeSO4 Fe2O3+SO2↑+SO3↑。 D Mg2+水解 解析 A项,NaOH浓溶液滴加到饱和FeCl3溶液中生 成Fe(OH)3沉淀,而Fe(OH)3胶体的制备是向沸水中 滴入饱和氯化铁溶液,加热至溶液出现红褐色,错 误;B项,氯化镁是强酸弱碱盐,MgCl2水解产生的 HCl易挥发,将MgCl2溶液加热蒸干生成Mg(OH)2, 故由MgCl2溶液制备无水MgCl2要在HCl气流中加热 蒸干,错误;C项,铜与稀硝酸反应,应该用稀盐酸 或稀硫酸除去Cu粉中混有的CuO,错误;D项,分 别将少量钠投入到盛有水和乙醇的烧杯中,利用反 应的现象:反应剧烈的是水,反应平缓的是乙醇, 可比较水和乙醇中氢的活泼性,正确。查看更多