- 2021-08-24 发布 |
- 37.5 KB |
- 30页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019届一轮复习人教版化学常用仪器和实验基本操作学案
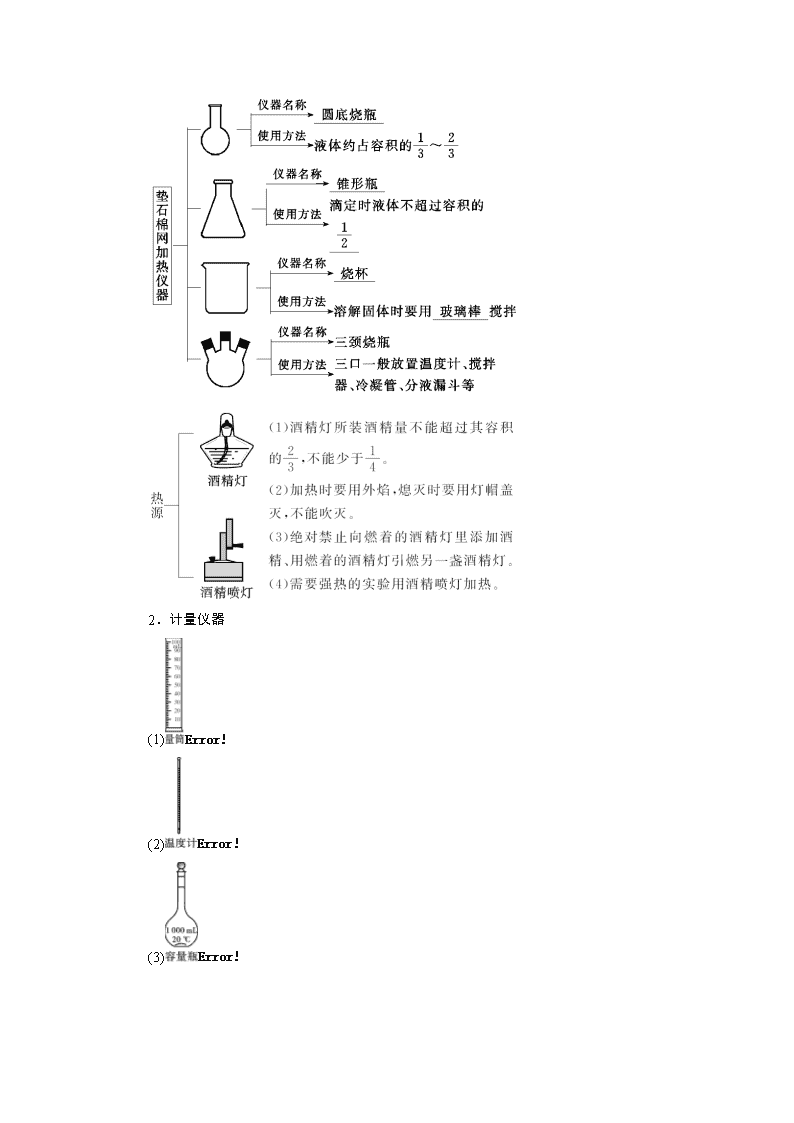
第十章 化学实验 第39讲 化学常用仪器和实验基本操作 考纲要求 考情分析 命题趋势 1.了解化学实验是科学探究过程中的一种重要方法。了解化学实验室常用仪器的主要用途和使用方法。 2.掌握化学实验的基本操作,能识别化学品标志,了解实验室一般事故的预防和处理方法。 2017,全国卷Ⅲ,9T 2017,海南卷,5T,12T 2016,全国卷丙,9T 2016,天津卷,5T 从近几年的高考实验题的考查来看,考点主要有四个:一是考查实验常用仪器的结构及使用方法;二是考查化学实验的安全知识;三是考查化学实验的基本操作知识与技能;四是考查检查装置的气密性。 分值:2~6分 考点一 常用化学仪器的识别与使用(见学用讲义P188) 1.加热仪器 2.计量仪器 (1) (2) (3) (4) (5) 3.分离提纯仪器 仪器 主要用途 使用方法和注意事项 __普通漏斗__ (1)向小口容器中转移液体 (2)加滤纸后,可过滤液体 (1)制作过滤器时,滤纸__紧贴__漏斗内壁,用水润湿,注意不得留有__气泡__ (2)滤纸边缘低于__漏斗__边缘,液体低于__滤纸__边缘 __分液漏斗__ (1)用于随时添加液体 (2)__萃取、分液__ (1)注意活塞不得渗漏 (2)分离液体时,下层液体由__下口放出__,上层液体由__上口倒出__ __蒸发皿__ 蒸发或浓缩溶液 可直接加热,加热时液体体积不超过其容积的2/3,快蒸干时停止加热 __蒸馏烧瓶__ 蒸馏或分馏 (1)加热时要垫石棉网 (2)加热时液体的量不超过其容积的__1/2__ __直形冷凝管__ 冷凝或冷凝回流 冷却水的流向应“b进a出” __洗气瓶__ 除去气体中的杂质,其中广口瓶可换作大试管或锥形瓶 (1)一般选择能与杂质气体反应的试剂作吸收剂 (2)装入液体量不宜超过容积的2/3 (3)气体的流向为__A进B出__ 用于干燥或吸收某些气体,干燥剂为粒状,常用无水CaCl2、碱石灰 (1)注意干燥剂或吸收剂的选择 (2)一般为__大口__进气,__小口__出气 4.其他常用仪器 仪器 主要用途 使用方法和注意事项 (1)滴瓶用于盛放少量液体药品 (2)胶头滴管用于吸取和滴加液体 (1)胶头滴管使用时不要将液体吸入胶头内,不能平置和倒置;滴液时不可接触器壁;用后立即洗净,再去吸取其他药品 (2)滴瓶上的滴管与滴瓶配套使用 (3)见光分解的物质要用棕色瓶盛装 (1)用于贮存固体药品,瓶口内壁磨砂,并配有磨砂的玻璃塞。其瓶口上表面磨砂的叫集气瓶,集气瓶配有毛玻璃片 (2)用于贮存液体药品。有无色和棕色之分,棕色的常用于存放见光易分解的药品 (1)不宜盛放易挥发物,盛碱性物质时应改用__橡胶塞__ (2)盛放氧化性药品时一定要用玻璃塞 制取气体的发生器(用于固体+液体―→气体) (1)固体为块状 (2)该气体溶解度小 (3)反应无强热放出 装配反应器 下端应插入液面下,否则气体会从漏斗口逸出 1.判断正误,正确的划“√”,错误的划“×”。 (1)容量瓶、分液漏斗、酸(碱)式滴定管使用前都要检漏、洗涤,酸(碱)式滴定管还需用待盛液体润洗。 ( √ ) (2)烧瓶、锥形瓶、量筒加热时均需要垫石棉网。( × ) (3)计量仪器中,滴定管、量筒、容量瓶、托盘天平、温度计的“0”刻度都在仪器的底部。( × ) (4)在灼烧固体物质时需用到的仪器是坩埚、泥三角。( √ ) (5)(2016·全国卷乙)用长颈漏斗分离出乙酸与乙醇反应的产物。( × ) 2.下列仪器对应的名称正确的是( B ) A.三脚架 B.表面皿 C.长颈漏斗 D.瓷钳锅 规避计量仪器使用时的四个易失分点 (1)托盘天平的精确度为0.1 g。 (2)10 mL量筒的精确度为0.1 mL,无“0”刻度,小刻度在下方。 (3)滴定管的精确度为0.01 mL,“0”刻度在接近上口处。 (4)容量瓶只有一条刻度线,只能读取一个值,该数值为容量瓶的容量值。 常用计量仪器的读数及误差分析 1.平视读数(如图1):实验室中用量筒、移液管或滴定管量取一定体积的液体,读取液体体积时,视线应与凹液面最低点保持水平,视线与刻度的交点即为读数(即凹液面定视线,视线定读数)。 2.俯视读数(如图2):当用量筒测量液体的体积时,由于俯视视线向下倾斜,寻找切点的位置在凹液面的上侧,读数高于正确的刻度线位置,即读数偏大。 3.仰视读数(如图3):读数时,由于视线向上倾斜,寻找切点的位置在液面的下侧,因滴定管刻度标法与量筒不同,这样仰视读数偏大。 至于俯视和仰视的误差,还要结合具体仪器进行分析,因为量筒刻度从下到上逐渐增大;而滴定管刻度从下到上逐渐减小,并且滴定管中液体的体积是两次体积读数之差,在分析时还要看滴定前读数是否正确,然后才能判断实际量取的液体体积是偏大还是偏小。 [例1]用0.102 6 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为( B ) A.22.30 mL B.22.35 mL C.23.65 mL D.23.70 mL 解析 滴定管的“0”刻度在上方,滴定时液体消耗,液面逐渐下降,故题图中的正确读数为22.35 mL。 [例1](2016·天津卷)下列选用的仪器和药品能达到实验目的的是( ) A B C D 制乙炔的发生装置 蒸馏时的接收装置 除去SO2中的少量HCl 准确量取一定体积K2Cr2O7标准溶液 [答题送检]来自阅卷名师报告 错误 致错原因 扣分 A 对电石与水反应的情况不清楚,实际上,电石与水能剧烈反应且放热量大,不安全 -6 B 对蒸馏装置中各部分仪器的连接含混不清 -6 D 根据溶液的酸碱性、氧化性等性质来选择合适的滴定管 -6 [解析] 制备乙炔时常用饱和食盐水代替水以减缓反应速率,长颈漏斗改为分液漏斗,A项错误;牛角管与锥形瓶之间是直接相连的,不必用橡皮塞,B项错误;HCl可以与NaHSO3反应放出SO2,而SO2不能与NaHSO3反应,C项正确;K2Cr2O7具有强氧化性,会氧化碱式滴定管下端的橡皮管,K2Cr2O7应盛放于酸性滴定管中,D项错误。 [答案] C 1.利用实验器材(规格和数量不限)能完成相应实验的一项是( D ) 选项 实验器材(省略夹持装置) 相应实验 A 烧杯、玻璃棒、蒸发皿 CuSO4溶液的浓缩结晶 B 烧杯、玻璃棒、胶头滴管、滤纸 用盐酸除去BaSO4中少量BaCO3 C 烧杯、玻璃棒、胶头滴管、容量瓶 用固体NaCl配制0.5 mol·L-1的溶液 D 烧杯、玻璃棒、胶头滴管、分液漏斗 用溴水和CCl4除去NaBr溶液中少量NaI 1.完成下列填空。 (1)(2016·四川卷)实验室过滤所需的玻璃仪器是__漏斗、烧杯、玻璃棒__。 (2)(2016·海南卷)浓缩硫酸锌、硫酸铜溶液使用的器皿名称是__蒸发皿__。 2.下列有关实验的选项正确的是( B ) A.配制0.10 mol·L-1 NaOH溶液 B.除去CO中的CO2 C.苯萃取碘水中I2,分出水层后的操作 D.记录滴定终点读数为12.20 mL 考点二 实验基本操作(见学用讲义P191) 1.药品的取用 (1)根据药品的状态和用量选择取用方法。 取用药品 固体药品 液体药品 粉末 块状 一定量 少量 多量 一定量 使用仪器 药匙(或纸槽) __镊子__ 用__托盘天平__称量 __胶头滴管__ 用试剂瓶倾倒 量筒、滴定管(或移液管) (2)向仪器内加入药品的操作方法。 ①向容器内加固体药品 ②向容器内加液体药品 2.仪器的洗涤 (1)洗净的标准:玻璃仪器内壁附着均匀水膜,不__凝聚成水滴__,也不成股流下。 (2)常见残留物的洗涤 待清洗仪器 污物 清洗试剂 做过KMnO4分解实验的试管 MnO2 __热浓盐酸__ 做过碘升华的烧杯 碘 __酒精__ 长期存放FeCl3溶液的试剂瓶 Fe(OH)3 __稀盐酸__ 长期存放澄清石灰水的试剂瓶 CaCO3 __稀盐酸__ 做过银镜实验的试管 银 __稀硝酸__ 做过油脂实验的试管 油污 __NaOH或热纯碱溶液__ 做过硫实验的试管 硫 热的NaOH溶液 做过苯酚实验的烧瓶 苯酚 __NaOH或酒精__ 3.试纸的使用 (1)类型及作用 ——定性检验碱性溶液 ——定性检验酸性溶液 ——定量、定性检验溶液__酸碱__性的强弱 ——检验Cl2等具有__强氧化__性的物质 ——检验SO2等具有__漂白__性的物质 (2)使用方法 ①检验液体:取一小块试纸放在表面皿或玻璃片上,用蘸有__待测液__的玻璃棒点在__ 试纸中部__,观察试纸颜色的变化。 ②检验气体:一般先将试纸__润湿__,粘在玻璃棒的一端,并使其接近出气口,观察颜色的变化。 (3)注意事项 4.物质的加热 (1)固体的加热 ①试管口要略__向下__倾斜,防止生成的水倒流,引起试管__炸裂__。 ②先给试管__均匀__加热,受热均匀后再__固定__在药品部位加热。 (2)液体的加热 ①加热前,先把玻璃容器外壁的水__擦干__,以免炸裂试管;用试管夹夹住试管__中上__部,管口__向上__倾斜,不得对人,以防液体沸腾时溅出烫伤人。 ②试管内液体的体积不超过试管容积的____。 (3)加热的方式 加热方式 适用范围 直接加热 瓷质、金属质或小而薄的玻璃仪器(如试管)等 隔石棉网加热 较大的玻璃反应器(如烧杯、烧瓶等) 浴热(水浴、油浴、沙浴等) ①需严格控制温度的(如硝基苯的制备) ②需反应混合液静止的(如银镜反应) ③蒸馏沸点差较小的混合液 5.物质的溶解 (1)固体的溶解 一般在烧杯或试管里进行,为了加速溶解,常采用__研细__、__搅拌__、振荡或__加热__等措施,但FeCl3、AlCl3等易水解的固体溶解时不能__加热__。 (2)液体的稀释 用量筒分别量取一定体积被溶解的液体和溶剂,然后先后加入烧杯中搅拌而稀释。但对于稀释放热较多的液体,往往先加入密度__较小__的液体,再沿烧杯内壁缓缓加入密度__较大__的液体,边加入边搅拌。如浓H2SO4稀释时是把__浓H2SO4__慢慢加入到__水中__,并用玻璃棒不断搅拌。 (3)气体的溶解 ①对溶解度较小的气体(如__Cl2__等),为了增大气体分子与水分子的接触机会,应将气体导管插入水中(如图中A)。 ②对极易溶于水的气体(如NH3、HCl等),气体导管口只能靠近液面,最好在导管口连接一倒置的漏斗,并使漏斗边缘刚好贴在液面上,这样可以增大气体的吸收率,减少气体的逸出,同时也避免出现液体__倒吸__的现象(如图中B和C)。 1.判断正误,正确的划“√”,错误的划“×”。 (1)用氢氟酸清洗做过硅酸分解实验的瓷坩埚。( × ) (2)做钠盐溶液的焰色反应时,用玻璃棒蘸取待测液放在酒精灯火焰上灼烧。 ( × ) (3)向试管中滴加液体时,胶头滴管紧贴试管内壁。 ( × ) (4)配制氯化铁溶液,是将FeCl3溶于蒸馏水,再加入一定量的铁粉。 ( × ) (5)用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中。 ( × ) 2.下列实验操作正确的是( D ) A.可用氨水除去试管内壁上的银镜 B.硅酸钠溶液应保存在带玻璃塞的试剂瓶中 C.将三氯化铁溶液蒸干,可制得无水三氯化铁 D.锌与稀硫酸反应时,要加大反应速率可滴加少量硫酸铜 化学实验中的几个重要数据 (1)酸碱指示剂的用量一般在2~3滴。不宜多加,否则会造成较大误差。 (2)配制一定物质的量浓度溶液时,烧杯、玻璃棒要洗涤2~3次;往容量瓶中加水时,一般加到距离刻度线1~2 cm处,再改用胶头滴管定容。 (3)水浴加热的温度不超过100 ℃。 (4)实验室制取硝基苯应控制反应温度为50~60 ℃,用水浴加热,且控制水浴温度为50~60 ℃。 装置气密性的检查方法 方法 微热法 液差法 外压法 原理 升高装置中气体的温度,使气体膨胀 缩小装置中气体的体积,增大压强 增大或减小装置中气体的物质的量 图例 具体操作 塞紧橡胶塞,将导气管末端伸入盛水的烧杯中,用手捂热(或用酒精灯微热)烧瓶 塞紧橡胶塞,用止水夹夹住导气管的橡胶管部分,从长颈漏斗向试管中注水 塞紧橡胶塞,打开止水夹,推动或拉动注射器活塞 现象说明 导管口有气泡产生,停止微热,冷却后导气管末端形成一段水柱,且保持一段时间不下降 停止加水后,长颈漏斗中的液面高于试管中的液面,且液面差不再改变 推动注射器活塞之后导管中出现一段液柱,且液面差不改变;拉动注射器活塞试管中产生气泡 [例1]下列装置操作图不能用于检查气密性的是( A ) [例1](2016·海南卷)下列有关实验操作的叙述错误的是( ) A.过滤操作中,漏斗的尖端应接触烧杯内壁 B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 D.向容量瓶转移液体时,引流用玻璃棒可以接触容量瓶内壁 [答题送检]来自阅卷名师报告 错误 致错原因 扣分 C 对滴定操作要求不清晰,滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁,目的是使尖嘴上的残余液体进入锥形瓶 -3 [解析] 从滴瓶中取用试剂时,如果滴管的尖嘴接触试管内壁,容易造成试剂的污染,B项错误。 [答案] B 1.下列实验操作正确且能达到相应实验目的的是( C ) 选项 实验目的 实验操作 A 称取2.0 g NaOH固体 先在托盘上各放1张滤纸,然后在右盘上添加2 g砝码,左盘上添加NaOH固体 B 配制FeCl3溶液 将FeCl3固体溶于适量蒸馏水 C 检验溶液中是否含NH 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 D 验证铁的吸氧腐蚀 将铁钉放入试管中,用盐酸浸没 1.(2016·江苏卷)根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤。下列图示装置和原理能达到实验目的的是( C ) A.制取氨气 B.制取NaHCO3 C.分离NaHCO3 D.干燥NaHCO3 解析 A项,制NH3需要用NH4Cl固体和Ca(OH)2固体加热进行反应,错误;B项,CO2应从长导管进、短导管出,错误;C项,制得的NaHCO3为固体,用过滤法分离,正确;D项,加热时NaHCO3会分解,错误。 2.(2017·全国卷Ⅲ)下列实验操作规范且能达到目的的是( B ) 选项 目的 操作 A 取20.00 mL盐酸 在50 mL酸式滴定管中装入盐酸,调整初始读数为30. 00 mL后,将剩余盐酸放入锥形瓶 B 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗 C 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上 D 配制浓度为0.010 mol·L-1的KMnO4溶液 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 解析 A项,滴定管的0刻度在上,刻度线以下有盐酸,所以滴定管中剩余盐酸的体积大于20.00 mL,错误;B项,碘易溶于酒精,可用酒精洗涤,又由于酒精与水互溶,再用水洗净即可,正确;C项,用pH试纸测定溶液的pH时试纸不能湿润,错误;D项,配制溶液时,高锰酸钾需在烧杯中溶解,不能在容量瓶中溶解,错误。 考点三 化学试剂的存放及实验安全(见学用讲义P193) 1.常见危险化学药品的标志 2.常见意外事故的处理 意外事故 处理方法 金属钠、钾起火 用__沙土__盖灭 酒精灯不慎碰倒起火 用__湿抹布__盖灭 浓碱液溅到皮肤上 用较多水冲洗,然后涂上__硼酸__溶液 浓硫酸溅到皮肤上 用大量__水__冲洗,最后涂上3%~5%的__NaHCO3__溶液 不慎将酸溅到眼中 用大量水冲洗,边洗边眨眼睛,切不可用手揉眼睛 温度计水银球不慎碰破 先用胶头滴管吸取,滴入试剂瓶,再用__硫粉__覆盖 液溴、苯酚沾到皮肤上 用酒精擦洗 重金属盐中毒 喝大量豆浆、牛奶,并及时送医院 3.化学试剂的保存 (1)试剂瓶选用的四个要素 ①瓶口:固体药品存放于__广口瓶__,液体药品存放于__细口瓶__。 ②瓶质:与玻璃强烈反应的试剂(如__氢氟酸__)不能用玻璃试剂瓶盛装。 ③瓶塞:强碱性溶液不可用__玻璃__塞的玻璃试剂瓶来盛装,可用__橡胶__塞。强氧化性试剂不可用__橡胶__塞的试剂瓶。 ④瓶色:见光易分解的试剂应保存在__棕__色试剂瓶里。 (2)特殊试剂存放的“十防范” 保存依据 保存方法 典型实例 防氧化 ①密封或用后立即盖好 ②加入还原剂 ③隔绝空气 ①Na2SO3固体、Na2S、KI溶液等用后立即盖好 ②FeSO4溶液中加少量铁屑 ③K、Na保存在煤油里,白磷保存在冷水中,Li保存在__石蜡__里 防潮解(或与水反应或吸水) 密封保存 NaOH、CaCl2、CuSO4、P2O5等固体,浓硫酸等密封保存 防与CO2反应 密封保存,减少露置时间 NaOH、Na2CO3溶液、石灰水、Na2O2固体等密封保存 防挥发 ①密封,置于阴凉处 ②液封 ①浓盐酸、浓氨水等置于阴凉处 ②液溴加水封 防燃烧 置于阴凉处,不与氧化剂混合贮存,严禁火种 苯、汽油、酒精等 防分解 保存在__棕__色瓶中,置于阴凉处 浓硝酸、KMnO4、AgNO3溶液、氯水等 防水解 加入酸(碱)抑制水解 FeCl3溶液中加__HCl__ 防腐蚀 ①能腐蚀橡胶的物质用__玻璃__ ①浓硝酸、KMnO4溶液、氯水、溴水等腐蚀橡胶,汽油、苯、CCl4等能使橡胶溶胀 塞或塑料盖 ②能腐蚀玻璃的物质用塑料容器 ②氢氟酸保存在__塑料__瓶中 防黏结 碱性溶液用橡胶塞 NaOH、Na2CO3、Na2SiO3溶液等 防变质 现配现用 银氨溶液等 常见化学药品保存方法口诀 药品状态定口径,瓶塞取决酸碱性; 硝酸固碘硝酸银,低温避光棕色瓶; 液溴氨水易挥发,阴凉保存要密封; 白磷存放需冷水,钾钠钙钡煤油中; 碱瓶须用橡胶塞,塑料存放氟化氢; 易变质药放时短,易燃易爆避火源; 特殊试剂特殊放,互不反应要记清。 1.判断正误,正确的划“√”,错误的划“×”。 (1)实验室装有白磷的试剂瓶应贴上标签:。( × ) (2)稀释浓硫酸时,将浓硫酸慢慢倒入水中,并不断搅拌。( √ ) (3)实验室制取氯气时,没设计尾气吸收装置。 ( × ) (4)做金属钠实验时,剩余的钠放回原试剂瓶。 ( √ ) (5)白磷保存在冷水中。 ( √ ) 2.化学实验设计和操作中必须十分重视安全和环境保护问题。下列实验问题处理方法不正确的是__②③⑥⑦⑧__。 ①在制取氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡胶塞;②在气体发生装置上直接点燃一氧化碳气体时,必须先检验一氧化碳气体的纯度。最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声;③实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室;④给试管中的液体加热时不时移动试管或加入碎瓷片,以免暴沸伤人;⑤配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;⑥用酒精灯直接去燃着的酒精灯上引燃;⑦浓NaOH溶液沾在皮肤上,立即用稀硫酸清洗;⑧实验室制备Cl2时,用饱和食盐水吸收尾气 实验安全操作(“十防”) 1.防倒吸:用试管加热固体时,试管口应略向下倾斜;如实验室制O2、NH3等,加热法制取并用排水法收集气体或吸收溶解度较大的气体时,容易发生倒吸,要注意熄灯顺序或加装安全瓶。 2.防爆炸:点燃可燃气体(如H2、CO、CH4、C2H2、C2H4)或用CO、H2还原Fe2O3、CuO之前,要检验气体纯度。 3.防暴沸:稀释浓硫酸或将浓硫酸与酒精混合时,要将密度大的浓硫酸缓慢倒入水或酒精中;加热液体混合物时要加沸石。 4.防失火:实验室中的可燃物质一定要远离火源。 5.防中毒:制取有毒气体(如Cl2、CO、SO2、H2S、NO2、NO)时,应在通风橱中进行。 6.防堵塞:常有以下装置——防止堵塞导管,使液体顺利流入或气体流出或使内外压强相等。 7.防炸裂:普通玻璃制品都有受热不均匀易炸裂的特性,因此(1)试管加热时先要预热;(2)做固体在气体中燃烧实验时要在集气瓶底预留少量水或铺一层细沙;(3)注意防止倒吸;(4)热的烧瓶、烧杯、试管等要避免骤冷。 8.防泄漏:检查装置的气密性、长颈漏斗下端插入液面下以防止气体泄漏;检查滴定管、分液漏斗、容量瓶是否漏水以防止液体泄漏。 9.防污染:(1)已取出的未用完的试剂一般不放回原瓶(块状固体、钠、钾等除外);(2)用胶头滴管滴加液体时,不伸入瓶内,不接触试管壁[向FeSO4溶液中加NaOH溶液制Fe(OH)2除外];(3)取用试剂时试剂瓶盖倒放于桌面上;(4)药匙和胶头滴管尽可能专用(或洗净、擦干后再取其他药品);(5)废液及时处理;(6)凡有污染性气体(如Cl2、SO2、CO、NOx等)产生的均须对尾气进行吸收(碱液吸收Cl2、NOx,蘸Na2CO3溶液的棉花吸收SO2)或处理(用酒精灯点燃CO或将CO收集在气球中)。 10.防意外:应设有良好的通风设备,使空气畅通。使用、制备有毒气体和做有烟雾的实验应在密闭系统或通风橱中进行,外加尾气吸收处理装置;不可尝药品的味道;误食重金属盐应立即服用生蛋白或鲜牛奶。 [例1](2016·全国卷丙)下列有关实验的操作正确的是( D ) 选项 实验 操作 A 配制稀硫酸 先将浓硫酸加入烧杯中,后倒入蒸馏水 B 排水法收集KMnO4分解产生的O2 先熄灭酒精灯,后移出导管 C 浓盐酸与MnO2反应制备纯净Cl2 气体产物先通过浓硫酸,后通过饱和食盐水 D CCl4萃取碘水中的I2 先从分液漏斗下口放出有机层,后从上口倒出水层 解析 稀释浓H2SO4需要将浓H2SO4沿着玻璃棒缓慢注入盛有蒸馏水的烧杯中,并不断搅拌,A项错误;为防止倒吸,收集满O2后应该先移出导管,再熄灭酒精灯,B项错误;应该把含有H2O、HCl杂质的Cl2依次通过饱和食盐水、浓H2SO4才能得到干燥纯净的Cl2,C项错误;I2能溶解在CCl4中,振荡静置分层后CCl4层在下层,水层在上层,应该先从分液漏斗下口放出CCl4层,后从上口倒出水层,D项正确。 [例1]进行化学实验时应强化安全意识。下列做法正确的是( ) A.金属钠着火时使用泡沫灭火器灭火 B.用试管加热碳酸氢钠固体时使试管口竖直向上 C.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 D.制备乙烯时向乙醇和浓硫酸的混合液中加入碎瓷片 [答题送检]来自阅卷名师报告 错误 致错原因 扣分 A - 定势思维,不同类型物质引起的火灾,处理方法大不相同 5 [解析] 金属钠能与泡沫灭火器中的水反应,而且钠在燃烧时与氧气反应生成过氧化钠,过氧化钠会与泡沫灭火器中的CO2、H2O反应生成氧气助燃,因而金属钠着火时不能用泡沫灭火器灭火,A项错误;加热固体时为了防止水蒸气冷凝回流到热的试管底部,从而使试管炸裂,试管口应该略向下倾斜,B项错误;浓硫酸溅到皮肤上应立即用大量水冲洗,然后再涂上3%~5%的NaHCO3溶液,C项错误;制备乙烯时加入碎瓷片可防止液体暴沸,D项正确。 [答案] D 1.下列说法正确的是( A ) A.在“镀锌铁皮的镀层厚度的测定”实验中,将镀锌铁皮放入稀硫酸,待产生氢气的速率突然减小,可以判断锌镀层已反应完全 B.在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在 C.在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热 D.受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况做进一步处理 解析 Zn比Fe活泼,与H+反应时Zn比Fe反应快,且Zn与Fe构成原电池,使Zn反应更快,所以当Zn反应完时,产生氢气的速率会明显变慢,A项正确;火柴头中氯元素的存在形式是KClO3,ClO与Ag+不反应,B项错误;加热时,铵盐易分解,Fe2+易被空气中的O2氧化,所以制备硫酸亚铁铵不宜用蒸发结晶法,宜用降温结晶的方法,即先制成热饱和溶液,然后冷却结晶,C项错误;受强碱腐蚀时,应先水冲,再涂硼酸(不宜用醋酸);受强酸腐蚀时,应先水冲,再涂碳酸氢钠溶液,D项错误。 1.(2016·浙江卷)下列叙述不正确的是( B ) A.钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火 B.探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏高 C.蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置 D.为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线 解析 B 项,若先将硫代硫酸钠与硫酸混合并计时,则两者发生反应,再用水浴加热至设定温度,在未达到设定温度前,因反应速率慢而使测得的反应速率偏低,错误。 2.(2017·海南卷)下列危险化学品标志中表示腐蚀品的是( A ) A B C D 解析 A项,为腐蚀品标志,正确;B项,是易燃固体标志,错误;C项,是放射性物质标志,错误;D项,是氧化剂标志,错误。 考点四 仪器的组合与创新使用(见学用讲义P196) 1.广口瓶的“一材多用” (1)A装置可作集气瓶和洗气瓶 例如,利用A装置收集或干燥以下三种气体: ①Cl2 ②NH3 ③NO Ⅰ.若集气瓶是干燥的,则由b口进气可收集的气体有__②__。 Ⅱ.若集气瓶是干燥的,则由a口进气可收集的气体有__①__。 Ⅲ.若集气瓶充满水,则由b口进气可收集的气体有__③__。 Ⅳ.若集气瓶内装入浓硫酸进行气体干燥,可用此装置干燥的气体是__①③__,这时气体由__a__口进入。 (2)A装置用于监控气体流速 例如:给病人输氧气时,可在广口瓶中加入少量水,从a端通入氧气,b端接入呼吸罩,则可从广口瓶中产生气泡的速率来监控所通氧气的速率(如图所示)。 (3)B装置用于测量气体的体积 长导管与另一弯管连接伸入量筒底部,广口瓶中盛满水,气体“短进”,将广口瓶中的水排到量筒中来测量难溶于水的气体的体积。 (4)安全防倒吸装置 ①C装置中长导管与另一弯管连接伸入溶液中,气体“短进长出”。 ②D装置中,两短导管间加一长直玻璃管,气体从两短导管其中一个进,另一个出。 1.广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成具有各种功能的装置。下列各图中能用作安全瓶防倒吸的是( B ) A B C D 2.如图所示装置有多种用途。回答下列问题: (1)洗气:除去CO2中的水蒸气,装置内应盛的物质是__浓硫酸__;除去CO中的CO2,装置内应盛的物质是__氢氧化钠溶液__,气体应从__A__端通入。 (2)检验:证明CO中含CO2,装置内应盛__澄清石灰水__。 (3)贮气:若用排空气法收集H2(装置放置方向不变),气体应从装置的__B__端通入。若用排水法收集O2时,瓶内先装满水,气体从__B__端通入。若用水将装置中的O2排出进行实验时,水应从__A__端通入。 (4)测量气体体积:瓶内先装满水,气体从__B__端通入,还需要用到的一种仪器是__量筒__。该方法适用于测量__难溶于水__的气体的体积。 (5)用作安全瓶:将它连接在气体发生装置之后,以防止液体倒吸流入气体发生装置而损坏仪器。此时瓶中无液体,气体从__B__端通入。 一 装置连接时注意操作的先与后 1.装配仪器时:先下后上,先左后右。 2.加入试剂时:先固后液。 3.实验开始时:先查仪器的气密性,再加药品,后点酒精灯。 4.有些实验为防倒吸:往往最后停止加热或最后停止通气。 5.有些实验为防氧化:往往最后停止通气。 6.仪器拆卸的一般过程:从右到左,自上而下,先拆主体,后拆部件。 7.净化气体时:一般先除去杂质气体,后除去水蒸气。 [例1]为了探究碱式碳酸镁[mMgCO3·nMg(OH)2·xH2O]的组成,某化学小组仅利用如图所示的仪器组装一套完整装置进行实验(夹持仪器省略)。 回答下列问题: (1)实验时应向装置中通入空气,若空气流从左向右,装置连接顺序为(装置不重复使用,填入仪器接口字母编号):空气→(__d__)(__c__)→(__a__)(__b__)→(__i__)(__j(或j__i)__)→(__e__)(__f__)→g。 (2)连接好装置,检查装置气密性,装好药品后,加热前应进行的操作是__关闭K1,打开K2,通入足量空气后,再打开K1,关闭K2__。 (3)装置B的作用是__吸收空气中的CO2__,装置A的作用是__除去空气中的水蒸气__。 (4)有同学认为(1)中的整套实验装置有缺陷,其不妥之处为__D可能会吸收空气中的水蒸气与二氧化碳气体__; 改进方案是__D后再接一个装有碱石灰的干燥管__。 (5)将装置改进后进行实验,称取一定量的碱式碳酸镁样品,充分反应后得到1.6 g残留物,生成1.32 g二氧化碳和0.72 g水。则此碱式碳酸镁的化学式为__3MgCO3·Mg(OH)2·3H2O__。 二 球形干燥管的多种用途 1.干燥管可作干燥、吸收及检验装置 (1)干燥管内盛无水硫酸铜时,可用于水的检验。 (2)可用于有毒气体的尾气吸收,如内盛碱石灰可吸收HCl、Cl2、SO2等。 (3)可用于定量测定气体的质量。定量测定时,有时需要考虑空气中的成分对测定结果的影响,所以吸收气体的装置后还要另接一个干燥管,目的是防止空气中的水或二氧化碳等对定量测定产生干扰。 2.球形干燥管的创新用途 (1)A装置为尾气吸收装置,原理类似于倒置在水中的漏斗。 (2)B装置为简易的过滤器,可净化天然水。如果去掉上边两层,可用于活性炭对液体中色素的吸附实验。 (3)C装置是一微型反应器,体现了绿色化学思想,是高考化学试题命题的方向,该装置既可节约药品,又可防止污染。铜在该装置中燃烧时,Cl2封闭在干燥管内,实验后剩余的Cl2也能用水吸收,并观察CuCl2溶液的颜色。 (4)D装置为一简易的启普发生器,可用于H2、CO2的制取,也可用于铜与硝酸的反应。 [例2]如图中的装置D是实验室制备CO2的简易装置图,用该装置制备CO2可起到随时使反应发生,也可以随时使反应停止的效果。图中的装置A、B、C也可起到相同效果的有( B ) [例1]如下图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( ) 选项 X 收集气体 Y A 碱石灰 氯化氢 水 B 碱石灰 氨气 水 C 氯化钙 二氧化硫 氢氧化钠 D 氯化钙 一氧化氮 氢氧化钠 [答题送检]来自阅卷名师报告 错误 致错原因 扣分 B NH3密度比空气小,收集时应采用向下排空气法 -2 D NO不能用排空气法收集 -2 [解析] A项,HCl通过碱石灰时被碱石灰吸收而导致无法收集到HCl,错误;B项,NH3的密度小于空气,收集时需采用向下排空气法,错误;C项,SO2的密度大于空气,可采用向上排空气法收集,同时剩余SO2可用NaOH溶液吸收,正确;D项,NO遇空气中的氧气发生反应生成NO2,且NO也不与NaOH溶液反应,可见收集、尾气处理装置均不对,错误。 [答案] C 1.(2018·太原模拟)用如图装置(加热及夹持仪器已略去)进行的实验,不能达到相应实验目的的是( D ) A.利用装置①可以验证Na2O2与水的反应是放热反应 B.装置②可用于收集H2、CO2、Cl2、HCl、NO2 C.利用装置③制取SO2,并验证其还原性 D.利用装置④验证KHCO3和K2CO3的热稳定性,X中应放的物质是K2CO3 解析 若右边烧杯中有气泡产生,则说明Na2O2与水的反应为放热反应,A项能达到实验目的;收集气体时若气体密度大于空气密度,则b口进a口出,若气体密度小于空气密度,则a口进b口出,B项能达到实验目的;大试管中Cu与浓硫酸反应生成SO2气体,若小试管中酸性KMnO4溶液褪色,则证明SO2具有还原性,C项能达到实验目的;X中应放的物质是KHCO3,D项不能达到实验目的。 1.下列实验操作正确的是( B ) A.用玻璃棒蘸取CH3COOH溶液点在水润湿的pH试纸上,测定该溶液的pH B.中和滴定时,滴定管用所盛装的反应液润洗2~3次 C.用装置甲分液,放出水相后再从分液漏斗下口放出有机相 D.用装置乙加热分解NaHCO3固体 解析 测定溶液的pH时,不可将pH试纸用水润湿,A项错误;滴定管要经过水洗和润洗,B项正确;分液漏斗中下层液体从下口放出,上层液体从上口倒出,C项错误;若用装置乙,NaHCO3加热分解有H2O生成,会倒流到试管底部,可能引起试管炸裂,所以试管口应略向下倾斜,D项错误。 2.某研究小组采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。 装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。 装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为__d__(填字母)。 解析 装置Ⅲ是吸收过量SO2的尾气处理装置,故可利用碱性溶液吸收。装置a是密闭装置有危险,且气体不容易吸收,b、c中试剂均不与SO2反应,不能用于SO2尾气的处理,d可充分吸收SO2同时具有防倒吸作用。 课时达标 第37讲(见课时达标P61) 1.在盛放浓硫酸的试剂瓶标签上印有下列警示标记中的( D ) 解析 浓硫酸是有强氧化性的腐蚀性酸,D项正确。 2.实验室中保存下列化学药品的方法不妥当的是( C ) A.将AgNO3晶体放在棕色试剂瓶中 B.NaOH溶液保存在带橡胶塞的细口试剂瓶中 C.金属钾、钠和非金属白磷保存在煤油中 D.浓硝酸溶液保存在棕色试剂瓶中 解析 白磷易自燃,须存放在水中,C项错误。 3.在进行化学实验时必须注意安全,下列说法不正确的是( D ) A.如果苯酚浓溶液沾在皮肤上应立即用酒精清洗 B.不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛 C.不慎将浓碱液沾到皮肤上,应立即用抹布拭去,再用大量水冲洗,然后涂上稀硼酸溶液 D.如果酸流到实验台上,立即用适量的氢氧化钠溶液中和,然后用水冲洗,再用抹布擦干 4.完成下列实验,所选装置正确的是( A ) 选项 A B C D 实验目的 检查装置气密性 实验室用纯碱和稀硫酸制备二氧化碳 用已知浓度的氢氧化钠溶液测定未知浓度的盐酸 从碘的CCl4溶液中分离出碘 实验装置 5.下列有关实验现象的预测或装置的选用正确的是( B ) A.用装置(Ⅰ)加热草酸晶体获取某些气体(草酸晶体的熔点为101.5 ℃,分解温度约为150 ℃) B.用装置(Ⅱ)进行实验时,酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 C.用装置(Ⅲ)进行实验时,广口瓶内先有浅红棕色气体出现后又变为无色,且不会产生空气污染 D.用装置(Ⅳ)分离溴苯和苯的混合物 解析 草酸晶体熔点(101.5 ℃)低于分解温度(150 ℃),未分解就先熔化,试管口应向上倾斜,A项错误;浓硫酸与蔗糖(含少量水)作用,有CO2、SO2生成,SO2能还原高锰酸钾,从而使酸性高锰酸钾溶液褪色,B项正确;产生的NO污染空气,C项错误;装置中缺少温度计,D项错误。 6.下列操作完全正确的一组是( A ) ①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部 ②给盛有液体的体积超过容积的试管加热 ③把鼻孔靠近容器口去闻气体的气味 ④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管 ⑤取用放在细口瓶中的液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上的标签对着地面 ⑥将烧瓶放在桌上,用力塞紧塞子 ⑦用坩埚钳夹取加热后的蒸发皿 ⑧将胶头滴管垂直伸进试管内滴加液体 ⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中 ⑩检查装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热 A.①④⑦⑩ B.①④⑤⑦⑩ C.①④⑤⑦⑧⑩ D.④⑤⑦⑩ 解析 ②给试管中液体加热时,液体的体积不能超过试管容积的,错误;③闻气体的气味时,不能把鼻孔靠近容器口,错误;⑤取用放在细口瓶中的液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上的标签应对着手心,防止标签被腐蚀,错误;⑥将烧瓶放在桌上,用力塞紧塞子,容易使烧瓶破裂,错误;⑧滴加液体时,胶头滴管应垂直在试管口上方,错误;⑨稀释浓硫酸时,应将浓硫酸沿着烧杯内壁慢慢注入水中,且不断用玻璃棒搅拌,错误。 7.下列有关实验操作的说法中,正确的是( C ) A.配制1 L 0.1 mol·L-1 NaCl溶液的实验中,用托盘天平称取5.85 g NaCl B.用广范pH试纸测得橙汁的pH为3.50 C.用酸式滴定管量取25.00 mL高锰酸钾溶液 D.可用过滤的方法除去淀粉溶液中混有的少量NaCl杂质 解析 托盘天平的准确度为0.1 g,不能用托盘天平称取5.85 g NaCl,A项错误;pH试纸测定结果为整数,不能用广范pH试纸测得橙汁的pH为3.50,可选pH计测定,B项错误;高锰酸钾可氧化橡胶,滴定管的准确度为0.01 mL,则用酸式滴定管量取25.00 mL高锰酸钾溶液,C 项正确;淀粉胶粒与离子均可透过滤纸,不能用过滤的方法除去淀粉溶液中混有的少量NaCl杂质,可选渗析法,D项错误。 8.根据下列实验或实验操作和现象,所得结论正确的是( C ) 选项 实验或实验操作 现象 实验结论 A 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 出现白色沉淀 H2CO3的酸性比H2SiO3的酸性强 B 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 有白色沉淀生成 原溶液中含有SO、SO、HSO中的一种或几种 C 试管b比试管a中溶液的红色深 增大反应物浓度,平衡向正反应方向移动 D 左边棉球变为橙色,右边棉球变为蓝色 氧化性:Cl2>Br2>I2 解析 盐酸有一定的挥发性,制取的二氧化碳中可能含有挥发的氯化氢,立即通入硅酸钠溶液中产生白色沉淀,不能证明是二氧化碳与硅酸钠反应,则不能证明碳酸的酸性大于硅酸,A项错误;与硝酸酸化的氯化钡溶液反应产生白色沉淀,不一定证明溶液中含有SO、SO、HSO中的一种或几种,可能含有Ag+,B项错误;氯气与NaBr反应生成溴单质,左边棉球变为橙色,因为氯气也与KI反应生成单质碘,则右边棉球变为蓝色,不能证明溴的氧化性大于碘,D项错误。 9.下列实验操作中,仪器一定要插到液面以下的是( C ) ①制备Fe(OH)2时,将NaOH溶液滴入FeSO4溶液中所用的胶头滴管 ②制备氢气的简易装置中的长颈漏斗 ③石油分馏时控制温度的温度计 ④用乙醇制备乙烯时所用的温度计 ⑤向BaCl2溶液中滴加稀硫酸所用的胶头滴管 A.③⑤ B.②⑤ C.①②④ D.①②③④⑤ 解析 ①Fe(OH)2易被空气中的氧气氧化,制备时,要将盛装NaOH溶液的胶头滴管插入FeSO4溶液中,再挤出NaOH溶液;②制备氢气的简易装置中,为防止生成的H2从长颈漏斗口逸出,要将长颈漏斗下端插入稀酸中;③ 石油分馏时,控制温度的温度计的水银球要置于蒸馏烧瓶的支管口处;④用乙醇制备乙烯时,要在170 ℃时进行反应,温度计要插入反应混合液中;⑤向BaCl2溶液中滴加稀硫酸,胶头滴管不能插到液面以下。 10.用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到的是( C ) 选项 实验步骤 实验用品 A 步骤1:将海带灼烧灰化 B 步骤2:将海带灰溶解、过滤 C 步骤3:氧化滤液中的I- D 步骤4:检验碘元素 11.下列实验操作完全正确的是( C ) 选项 实验 操作 A 钠与水反应 用镊子从煤油中取出金属钠,切下绿豆粒大小的钠,小心放入装满水的烧杯中 B 配制一定浓度的氯化钾溶液1 000 mL 准确称量氯化钾固体,放入1 000 mL的容量瓶中,加水溶解,振荡摇匀,定容 C 排除碱式滴定管尖嘴部分的气泡 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 D 取出分液漏斗中所需的上层液体 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 12.下列实验能达到实验目的且符合安全要求的是( B ) A.制备氢氧化亚铁并观察其颜色 B.收集氧气 C.制备并检验氢气的可燃性 D.浓硫酸的稀释 13.安全是顺利进行实验及避免伤害的保障。下列实验操作正确但不是从实验安全角度考虑的是( D ) A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度 B.操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出 C.操作③:吸收氨气或氯化氢气体并防止倒吸 D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水 解析 A项,由于连通氢气发生装置的导管在液面以下,燃烧的氢气在液面上,所以该装置可以防止点燃不纯氢气时发生爆炸,该操作是从安全角度考虑,不符合题意;B项,打开活塞使漏斗内气体放出,防止分液漏斗内压强过大而引起危险,该操作是从安全角度考虑,不符合题意;C项,水层在下层,不能防止倒吸,应该使用四氯化碳和水,该操作不正确,不符合题意;D项,检查容量瓶是否漏水操作正确,但这不是从实验安全角度考虑,符合题意。 14.如图为常用玻璃仪器组成的七种实验装置,根据需要可在其中加入液体或固体试剂。下列说法错误的是( B ) A.装置A、B既能用于收集Cl2,又能用于收集NO B.装有浓硫酸的装置F可用于干燥CO2气体 C.装置C、E可用于尾气吸收,能防止液体倒吸到气体发生装置中 D.装置G可用于合成氨实验中,可干燥、混合气体并能大致观察H2和N2的体积比 解析 装置A可用排空气法收集Cl2,若装置A装满水,则可用于收集NO,装置B可用排饱和食盐水法收集Cl2,也能用于收集NO,A项正确;装置F为U形干燥管装置,该装置只能盛装固体干燥剂,B项错误;装置C中的烧杯可吸收尾气,洗气瓶起到缓冲作用,防止烧杯中的液体倒吸入气体发生装置中,装置E中间膨大部分可防止液体倒吸,C 项正确;装置G中装入浓硫酸,可干燥H2和N2的混合气体,通过气泡多少可大致观察H2和N2的体积比,D项正确。查看更多