2020学年高一化学下学期期末考试试题 理 新版 新人教版(1)
小二黑体
2019学年度第二学期期末考试
高一化学(理科班)试题
(时间:90分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Al-27 S-32
第Ⅰ卷 选择题(共48分)
一、选择题(每小题2分,共48分。每小题只有一个选项符合题意)
1.下列化学用语正确的是( )
A.甲烷分子的比例模型:
B.苯的最简式:CH
C.乙烯的分子式:CH2=CH2
D.乙醇的结构简式:C2H6O
2.标准状况下,44.8L CH4与一定量Cl2在光照条件下发生取代反应,待反应完全后,测得四种有机取代产物的物质的量相等,则消耗的Cl2为( )
A.1mol
B.2 mol
C.4mol
D.5 mol
3.下列反应中,不属于取代反应的是( )
A.
B.
C.
D.
4.乙烯直接水合法制乙醇因污染小而应用于工业合成,下列有关说法错误的是( )
A.该反应属于加成反应
B.乙烯能使酸性KMnO4溶液褪色
C.乙烷中含有少量乙烯,可用H2除去
D.等物质的量的乙烯与乙醇充分燃烧,耗氧量相同
5.下列物质与水混合后静置,不出现分层的是( )
9
A.三氯甲烷 B.乙醇 C.苯 D.四氯化碳
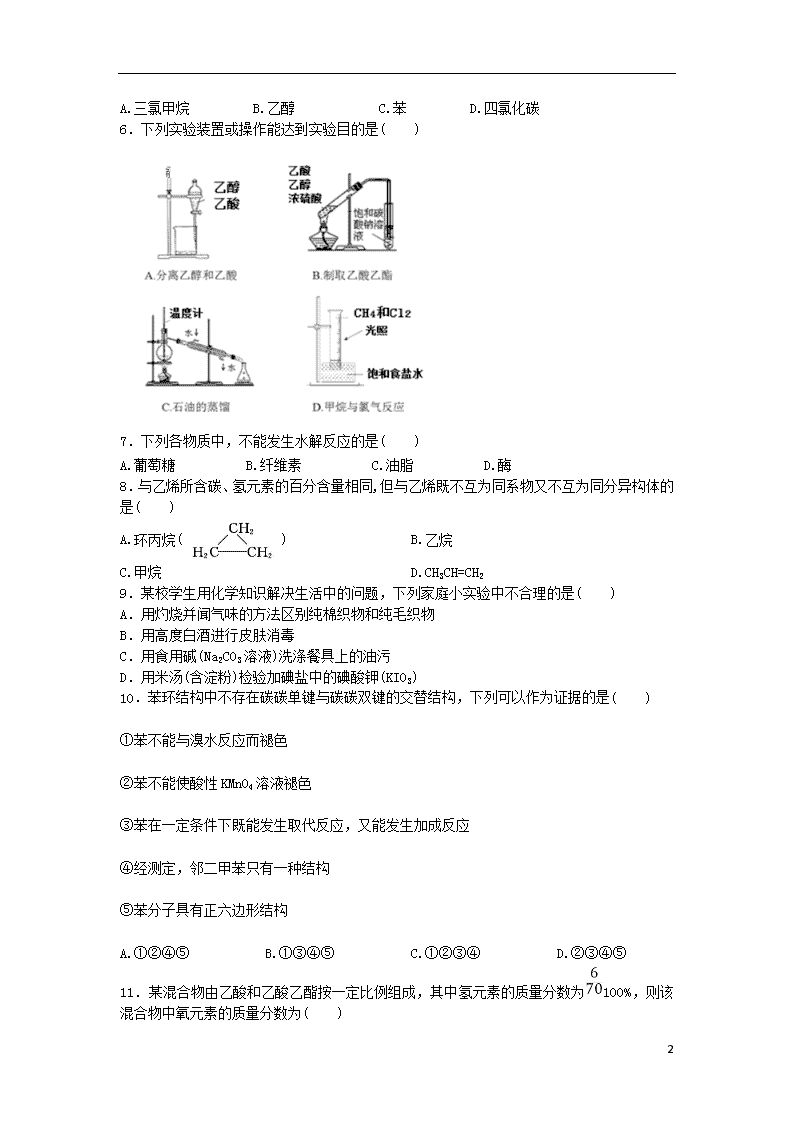
6.下列实验装置或操作能达到实验目的是( )
7.下列各物质中,不能发生水解反应的是( )
A.葡萄糖 B.纤维素 C.油脂 D.酶
8.与乙烯所含碳、氢元素的百分含量相同,但与乙烯既不互为同系物又不互为同分异构体的是( )
A.环丙烷()
B.乙烷
C.甲烷
D.CH3CH=CH2
9.某校学生用化学知识解决生活中的问题,下列家庭小实验中不合理的是( )
A.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
B.用高度白酒进行皮肤消毒
C.用食用碱(Na2CO3溶液)洗涤餐具上的油污
D.用米汤(含淀粉)检验加碘盐中的碘酸钾(KIO3)
10.苯环结构中不存在碳碳单键与碳碳双键的交替结构,下列可以作为证据的是( )
①苯不能与溴水反应而褪色
②苯不能使酸性KMnO4溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤苯分子具有正六边形结构
A.①②④⑤
B.①③④⑤
C.①②③④
D.②③④⑤
11.某混合物由乙酸和乙酸乙酯按一定比例组成,其中氢元素的质量分数为100%,则该混合物中氧元素的质量分数为( )
9
A.40%
B.60%
C.64%
D.72%
12.下列各类烷烃中,一氯代物只有一种的是( )
A.(CH3)2CHCH3
B.CH3CH2CH3
C.CH3CH2CH2CH3
D.C(CH3)4
13.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻铜片质量减小的是( )
A.水
B.无水乙醇
C.石灰水
D.盐酸
14.相同物质的量浓度的下列物质的稀溶液中,pH最小的是( )
A.乙醇 B.乙酸 C.碳酸钠 D.碳酸
15.下列金属冶炼的反应原理,错误的是( )
A.2Ag2O 4Ag+O2↑
B.火法炼铜:Cu2S+O2 2Cu+SO2
C.Al2O3+3H2 2Al+3H2O
D.MgCl2(熔融) Mg+Cl2↑
16.工业上以浓缩海水为原料提取溴的部分流程如下:
下列说法正确的是( )
A.海水需要浓缩,是因为海水中的Br2含量较低
B.热空气的作用是将多余的Cl2吹出
C.吸收塔中发生的反应是3Br2+3=5Br-++3CO2
D.反应釜2中发生的反应是5Br-++3H2O=3Br2+6OH-
17.石油裂化的目的是( )
A.使直链烃转化为芳香烃 B.使长链烃分子断裂为短链烃分子
C.除去石油中的杂质 D.提高重油的产量和质量
18.在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%。下列反应类型能体现“原子经济”原则的是( )
①置换反应 ②化合反应 ③分解反应 ④取代反应 ⑤加成反应
⑥复分解反应 ⑦加聚反应
A.①②⑤ B.②⑤⑦ C.⑥⑦ D.只有⑦
19.已知:
9
①H2 (g)+O2(g)H2O(g);ΔH1=akJ·mol-1
②2H2 (g)+O2(g)2H2O(g);ΔH2=bkJ·mol-1
③H2(g)+O2(g)H2O(l);ΔH3=ckJ·mol-1
④2H2(g)+O2(g)2H2O(l);ΔH4=dkJ·mol-1
下列关系正确的是( )
A.c
a>0
C.2a=d<0
D.2c=d>0
20.ht#tp://wln100.com 未来脑教学云平台|+在36g碳不完全燃烧所得气体中,CO占1/3体积,CO2占2/3体积。且有:C(s)+1/2O2(g)=CO(g);△H=-110.5kJ/mol,CO(g)+1/2O2 (g)=CO2(g) △H=-283kJ/mol
与这些碳完全燃烧相比,损失的热量是( )
A.172.5 kJ
B.1149 kJ
C.283kJ
D.517.5 kJ
21.相同质量的氢气、一氧化碳、乙醇、甲烷完全燃烧时,放出热量最少的是(已知这些物质的燃烧热分别为285. 8 kJ•mol−1、283.0.kJ•mol−1、1 366. 8 kJ•mol−1、890.3 kJ•mol−1) ( )
A.H2(g)
B.CO(g)
C.C2H5OH(l)
D.CH4(g)
22.下列分别是利用不同能源发电的实例图形,其中不属于新能源开发利用的是( )
23.已知:H2O(g)=H2O(l)△H1=-Q1kJ•mol-1(Q1>0)
C2H5OH(g)=C2H5OH(l)△H2=-Q2kJ•mol-1(Q2>0)
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=-Q3kJ•mol-1(Q3>0)
若使18.4g液态乙醇完全燃烧,最后恢复到室温,则放出的热量为( )kJ
A.0.4Q1+Q2+Q3 B.0.5(Q1+Q2+Q3)
C.1.2Q1-0.4Q2+0.4Q3 D.1.5Q1-0.5Q2+0.5Q3
24.已知A(g)+C(g)D(g) ΔH=-Q1kJ/mol,B(g)+C(g)E(g) ΔH=-Q2kJ/mol,Q1、Q2均大于0,且Q1>Q2,若A、B组成的混合气体1 mol与足量的C反应,放热为Q3kJ。则原混合气体中A与B的物质的量之比为( )
9
A.
B.
C.
D.
第Ⅱ卷 非选择题(共52分)
二、非选择题(共52分)
25.(10分)现有下列几组物质:
①35Cl和37Cl ②石墨与C60
③CH4和CH3CH2CH3
④和
⑤CH3CH2=CH2和CH2=CH—CH=CH2
⑥(CH3)2CHCH3和
⑦和
(1)互为同位素的是 (填序号,下同)。
(2)互为同分异构体的是 。
(3)互为同系物的是 。
(4)互为同素异形体的是 。
(5)属于同一种物质的是 。
26.(11分)(1)煤的气化是将其转化为可燃性气体的过程,主要化学反应方程式为 。煤也可以直接液化,属于
(填“化学变化”或“物理变化”)。
(2)由乙烯合成聚乙烯的化学方程式为 该高分子化合物的链节为 ;若该高分子化合物的相对分子质量为42 000,则其聚合度为 。
9
(3)一种甲烷水合物晶体中,平均每46个水分子构成8个分子笼,每个分子笼可容纳1个甲烷分子或水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,这种可燃冰的平均组成可表示为 。
(11分) I. 为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
试回答下列问题:
(1)该反应为_______反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)反应物化学键断裂吸收的能量_______(填“高”或“低”)于生成物化学键形成放出的能量。
Ⅱ. 用如图所示的装置做铝热反应实验,回答下列问题:
(4)写出该反应的化学方程式:____________________________,
在该反应中________是氧化剂,氯酸钾的作用是 。
(5)选出该实验的实验现象(把序号填写在横线上):________。
①镁带剧烈燃烧;②放出大量的热,并发出耀眼的白光;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
28.(9分)某同学为了验证海带中含有碘,拟进行如下实验,请完成相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的硅酸盐质实验仪器有________(填代号,限填3项)。
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三脚架 E.泥三角 F.酒精灯 G.烧杯 H.量筒
(2)第2步:I-溶液的获取。主要操作为______________________。
9
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用________(填代号),离子方程式为___________________________________________。
A.浓硫酸 B.新制氯水 C.KMnO4溶液 D.H2O2
(4)第4步:碘单质的检验。操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显 色,则证明海带中含碘。
29.(11分)在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)C装置的作用是 。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是 ,
B装置中的现象是 。
分离A装置中产物的操作名称是 ,分离B装置中产物需要的玻璃仪器名称是 。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为 。
(4)写出A装置中发生反应的化学方程式 ,反应类型为 E装置的作用是 。
9
小二黑体
2019学年度第二学期期末考试
高一化学(理科班)试题
参考答案
选择题(每小题2分,共48分。每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
B
D
B
C
B
D
A
A
D
A
A
D
题号
13
14
15
16
17
18
19
20
21
22
23
24
答案
D
B
C
C
B
B
A
C
B
C
C
A
二、非选择题(共52分)
25. (10分)(每问2分)(1)① (2)⑦ (3)③ (4)② (5)④⑥
26. (11分)
(1)C(S)+H2O(g) CO(g)+H2(g) (2分)化学变化(1分)
(2)nCH2=CH2(2分) —CH2CH2— (2分)
1 500(2分)
(3)CH4·8H2O(2分)
27.(11分)
(1)放热 (1分)
(2)高(1分)
(3)低(1分)
(4)2Al+Fe2O32Fe+Al2O3 (2分) Fe2O3 (2分) 助燃剂,引发铝热反应。(2分)
(5)①②③④(2分)
28. (9分)
(1)BEF(2分)
(2)将灰烬转移到烧杯中,加适量蒸馏水,用玻璃棒充分搅拌,煮沸,过滤(2分)
9
(3)D(2分) 2I-+H2O2+2H+===I2+2H2O(2分)
(4)蓝(1分)
29. (11分)
(1)检验B装置中是否有溴挥发出来(1分)
(2)橙色褪去,液体不分层(1分) 橙黄色褪去,液体分层 (1分) 蒸馏(1分) 分液漏斗、烧杯、玻璃棒(1分)
(3)氧化反应 (1分)
(4) (2分)加成反应 (1分)检验乙烯与酸性KMnO4溶液反应的产物二氧化碳 (2分)
9