- 2021-08-07 发布 |
- 37.5 KB |
- 10页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018-2019学年山东省莒县第二中学高二下学期第一次月考化学试题 Word版
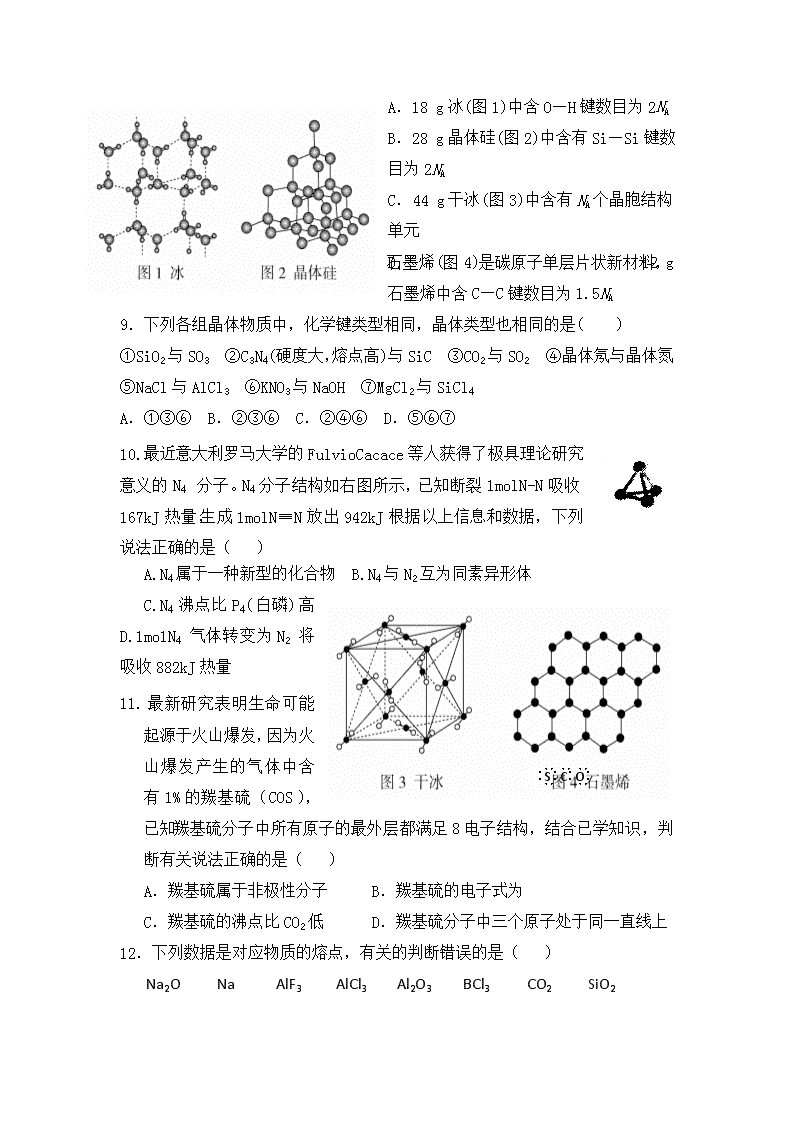
2018-2019学年山东省莒县第二中学高二下学期第一次月考化学试题 2019.03 请注意:时间60分钟 满分100分 相对原子质量:H 1 C 12 N 14 S 32 Cl 35.5 Ca40 Mn 55 Fe 56 Cu 64 Zn 65 O 16 Li 7 Ni 28 一、选择题(本题包括16小题,每小题只有一个选项符合题意,每小题3分,共48分) 1.X、Y两元素可形成XY3型共价化合物,则X、Y最外层的电子排布可能是( ) A.X:3s23p1 Y:3s23p5 B.X:2s22p3 Y:2s22p4 C.X:3s23p1 Y:2s22p5 D.X:2s22p3 Y:1s1 2.下列各组原子中,彼此化学性质一定相似的是( ) A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子 D.最外层都只有一个电子的X、Y原子 3.下列关于电离能和电负性的说法不正确的是( ) A.第一电离能的大小:Mg>Al B.锗的第一电离能高于碳而电负性低于碳 C.Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是碳 D.F、K、Fe、Ni四种元素中电负性最大的是F 4.以下有关元素性质的说法不正确的是( ) A.具有下列电子排布式的原子中,①1s22s22p63s23p2;②1s22s22p3;③1s22s22p2;④1s22s22p63s23p4,原子半径最大的是① B.下列原子的外围电子排布中,①3s23p1;②3s23p2;③3s23p3;④3s23p4,对应的第一电离能最大的是③ C.①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl,元素的电负性随原子序数的增加而递增的是④ D.某元素的逐级电离能(kJ/mol)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时最可能生成的阳离子是③ ①X+ ②X2+ ③X3+ ④X4+ 5.下列常见分子中σ键、π键判断正确的是( ) A.CN-与N2结构相似,CH2===CHCN分子中σ键与π键数目之比为1∶1 B.CO与N2结构相似,CO分子中σ键与π键数目之比为2∶1 C.C与O互为等电子体,1 mol O中含有的π键数目为2NA D.已知反应N2O4(l)+2N2H4(l)===3N2(g)+4H2O(l),若该反应中有4 mol N—H键断裂,则形成的π键数目为6NA 6.下列说法错误的是( ) A.在NH和[Cu(NH3)4]2+中都存在配位键 B.H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央 C.SO2、SO3、BF3、NCl3都是极性分子 D.向含有0.1 mol [Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1 mol AgCl 7.S2Cl2是橙黄色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发,并产生酸性悬浊液。其分子结构如图所示。下列关于S2Cl2的说法中错误的是( ) A.S2Cl2为非极性分子 B.分子中既含有极性键又含有非极性键 C.与S2Br2结构相似,熔、沸点S2Br2>S2Cl2 D.与水反应的化学方程式可能为 2S2Cl2+2H2O===SO2↑+3S↓+4HCl 8. 以NA表示阿伏加德罗常数的值,下列说法错误的是( ) A.18 g冰(图1)中含O—H键数目为2NA B.28 g晶体硅(图2)中含有Si—Si键数目为2NA C.44 g干冰(图3)中含有NA个晶胞结构单元 D.石墨烯(图4)是碳原子单层片状新材料,12 g石墨烯中含C—C键数目为1.5NA 9.下列各组晶体物质中,化学键类型相同,晶体类型也相同的是( ) ①SiO2与SO3 ②C3N4(硬度大,熔点高)与SiC ③CO2与SO2 ④晶体氖与晶体氮 ⑤NaCl与AlCl3 ⑥KNO3与NaOH ⑦MgCl2与SiCl4 A.①③⑥ B.②③⑥ C.②④⑥ D.⑤⑥⑦ 10.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4 分子。N4分子结构如右图所示,已知断裂1molN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是( ) A.N4属于一种新型的化合物 B.N4与N2互为同素异形体 C.N4沸点比P4(白磷)高 D.1mo1N4气体转变为N2将吸收882kJ热量 ∶S∶C∶O∶ ¨ ¨ ¨ ¨O C O ¨ 11.最新研究表明生命可能起源于火山爆发,因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( ) A.羰基硫属于非极性分子 B.羰基硫的电子式为 C.羰基硫的沸点比CO2低 D.羰基硫分子中三个原子处于同一直线上 12.下列数据是对应物质的熔点,有关的判断错误的是( ) Na2O Na AlF3 AlCl3 Al2O3 BCl3 CO2 SiO2 920℃ 97.8℃ 1291℃ 190℃ 2073℃ -107℃ -57℃ 1723℃ A.只要含阴离子的晶体就一定是离子晶体 B.在共价化合物分子中各原子都形成8电子结构 C.同族元素的氧化物可形成不同类型的晶体 D.金属晶体的熔点不一定比分子晶体的高 13.石墨能与熔融金属钾作用,形成石墨间隙化合物,钾原子填充在石墨各层谈原子中。比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面图形见下图,则x值为 ( ) A.8 B.12 C.24 D.60 14.科学家最近发现一种由钛原子和碳原子构成的气态团簇分子,如图1所示:图中顶角和面心的原子都是钛原子,棱的中心和体心的原子都是碳原子该分子的化学式是 ( ) A.Til3C14 B.Ti14C13 C.Ti4C5 D.TiC 15.下列说法正确的是(NA为阿伏加德罗常数)( ) A.124 g P4含有P—P键的个数为4NA B.12 g石墨中含有C—C键的个数为1.5NA C.12 g金刚石中含有C—C键的个数为4NA D.60gSi02中含Si—O键的个数为2NA 16.下列说法中正确的是 ( ) A.NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 B.P4和CH4都是正四面体形分子且键角都为109°28′ C.NH离子呈平面正方形结构 D.NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 莒县二中2017级第一次月考化学试题 2019.03 第Ⅱ卷(非选择题 共52分) 二、非选择题(本题包括4小题,共52分) 17.(8分)人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测为钛(22Ti),它被誉为“未来世纪的金属”。 试回答下列问题: (1)22Ti元素基态原子的价电子层排布为 ; (2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定; ① 偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如右图,它的化学式是 ; ②已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验: a.分别取等质量的两种配合物晶体的样品配成待测溶液; b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀; c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的,则绿色晶体配合物的化学式为 ,绿色晶体中含有化学键类型是 。 18.(14分)X、Y、Z、M、R、Q为元素周期表中前四周期元素,且原子序数之和为105。X位于周期表的s区,有两种氧化物;Y是良好的半导体材料,晶体Y结构与金刚石类似;Z原子价电子层的p轨道半充满,核外电子总数是最外层电子数的3倍;X+与M-相差一个电子层;M原子得到一个电子后3p轨道全充满;R有“生物金属”之称,R4+离子和氩原子的核外电子排布相同。 请填写下列空白: (1)六种元素中电负性最大的是____________(填元素符号);其中Q的基态原子核外电子排布式为__________;化合物XM的电子式为____________。 (2)X、Y、Z、M的第一电离能由小到大的顺序是____________(填元素符号)。 (3)Q元素可形成两种常见的离子Q2+与Q3+,其中化学性质较稳定的是________(填离子符号),其原因是_____________________。 (4)与R位于同周期的元素中,基态原子的电子排布中4s轨道上只有1个电子的元素有____________(填元素名称)。 19.(15分)下图1是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。回答下列问题(需要用到元素符号或分子式的,请用相应元素的元素符号或分子式作答): 图1 (1)a与b对应的元素可形成10电子中性分子X,写出带一个单位正电荷的1个X的等电子体________。将X溶于水后的溶液滴入到CuSO4溶液中至过量,再加入适量乙醇,可析出一种深蓝色晶体,其化学式为__________________________________。 (2)元素c位于元素周期表的____________区,d原子次外层有____________对自旋相反的电子,c、d单质的晶体堆积方式类型分别是________、________。 A.简单立方堆积 B.体心立方堆积 C.六方最密堆积 D.面心立方最密堆积 (3)d的一种氯化物为白色立方结晶,熔点430 ℃,沸点1490 ℃,其熔融态导电性差,晶胞结构如图2所示:该氯化物固体属于______晶体,其中氯原子的配位数为________。 图2 (4)e元素与氧可形成如图3中A所示的正四面体离子eO ,其中e在正四面体的体心,eO四面体通过共用顶角氧离子可形成B,则B的化学式为________。 图3 (5)单质a、f对应的元素以1∶1的原子个数比形成的分子(相同条件下对H2的相对密度为39)中含__________个σ键和____________个π键,其中f原子的杂化轨道类型为____________________。 20.(15分)硫及其化合物有许多用途,相关物质的物理常数如下表所示: H2S S8 FeS2 SO2 SO3 H2SO4 熔点/℃ −85.5 115.2 >600(分解) −75.5 16.8 10.3 沸点/℃ −60.3 444.6 −10.0 45.0 337.0 回答下列问题: (1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。 (2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。 (3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。 (4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____ 形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。 (5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为________g·cm−3;晶胞中Fe2+位于所形成的正八面体的体心,该正八面体的边长为______nm。 莒县二中2017级第一次月考化学试题 2019.03 参考答案 1-5 ACBDC 6-10 CACBB 11-15 DBABB 16D 17.(8分 每空2分)(1)3d24s2(2)①BaTiO3②[TiCl(H2O)5]Cl2·H2O 离子键、配位键、极性共价键 18.答案 (1)Cl 1s22s22p63s23p63d64s2(或[Ar]3d64s2) Na+[]- (2)Na查看更多
相关文章
- 当前文档收益归属上传用户