- 2021-08-06 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018-2019学年湖北省宜昌市葛洲坝中学高一上学期12月月考化学试题
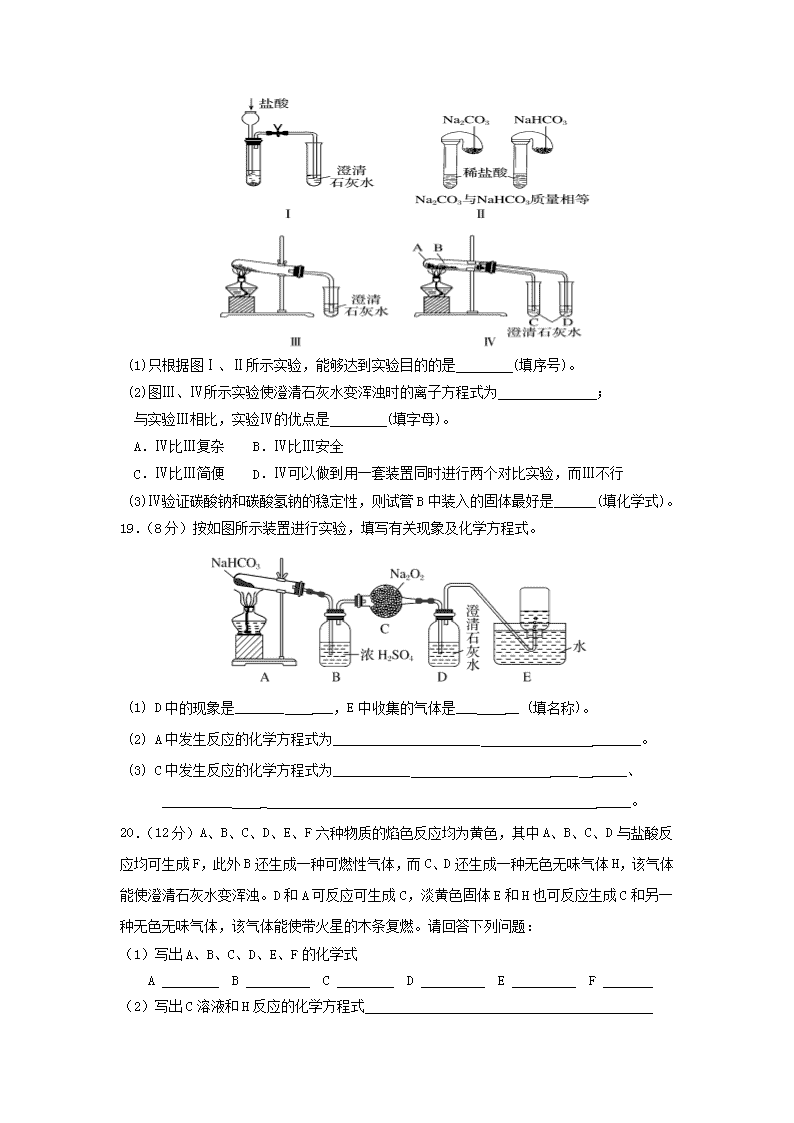
2018-2019学年湖北省宜昌市葛洲坝中学高一上学期12月月考化学试题 考试时间:2018年12月 有关相对原子质量:H—1 C—12 N—14 O—16 Na—23 Al—27 S—32 一、选择题(本题包括17小题,每小题3分,共51分) 1.将饱和FeCl3溶液加入沸水中能制得Fe(OH)3胶体,下列有关说法正确的是 A.溶液和胶体的本质区别是能否发生丁达尔效应 B.含0.1 mol FeCl3溶质的溶液形成胶体后,胶体粒子为0.1 mol C.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 D.可通过观察液体是否澄清透明,来区别溶液和胶体 2.下列离子方程式书写正确的是 A.氢氧化钡与稀硫酸反应:Ba2++OH-+H++SO===BaSO4↓+H2O B.Al2O3溶于盐酸中:O2-+2H+===H2O C.铜和硝酸银溶液反应:Cu+Ag+===Cu2++Ag D.Cu(OH)2中加入硝酸:Cu(OH)2+2H+===Cu2++2H2O 3.下列有关氧化还原反应的叙述正确的是 A.在一定条件下能发生反应:3O2===2O3,该反应不属于氧化还原反应 B.氧化反应一定先于还原反应发生 C.氧化还原反应中一种物质被氧化,另一种物质一定被还原 D.氧化性强的物质与还原性强的物质接触一定能发生反应 4.溶液中含Na+、SO、CO、HCO四种离子,加入过氧化钠固体后,假设反应前后溶液的体积不变,则离子浓度不变的是 A.HCO B.Na+ C.CO D.SO 5.除去碳酸氢钠溶液中混有的少量碳酸钠,采用的方法是 A.通入过量二氧化碳气体 B.加氢氧化钡溶液 C.加澄清石灰水 D.加稀盐酸 6.下列有关焰色反应实验的叙述正确的是 A.可用铜丝代替铂丝进行实验 B.观察钾的焰色反应要透过蓝色钴玻璃 C.实验结束后用碳酸钠溶液洗净铂丝 D.焰色反应是物质的化学性质 7.已知水和苯不互相溶,苯不与钠反应,在烧杯中加水和苯,观察到的现象可能是 A.钠在水层中反应并四处游动 B.钠停留在苯层中不发生反应 C.钠在苯的液面上反应并四处游动 D.钠在苯与水的界面处反应,可能做上下跳动 8.分别将一小块钠投入下列溶液中,只有气体放出没有沉淀生成的是 A.饱和NaCl溶液 B.稀NaHSO4溶液 C.MgCl2溶液 D.CuSO4溶液 9.下列各组离子中能大量共存,溶液呈现无色,且加入一小块钠后仍然能大量共存的是 A.K+、MnO4—、SO42—、H+ B.Ba2+、Na+、HCO3—、NO3— C.Na+、NO3—、K+、Cl− D.Ca2+、NO3—、Cl−、CO32— 10.PbO2与Cr3+反应生成Cr2O和Pb2+,则与1.5 mol PbO2反应所需的Cr3+物质的量为 A.3.0 mol B.1.5 mol C.1.0 mol D.0.75 mol 11.过量的NaHCO3与Na2O2混合,在密闭容器中充分加热后排出气体,残留的物质应是 A.Na2O和Na2O2 B.Na2O2和Na2CO3 C.Na2CO3 D.Na2O 12.下列对于Na2O、Na2O2的比较正确的一项是 A.Na2O、Na2O2都是碱性氧化物 B.Na2O、Na2O2都是易溶于水的白色固体 C.Na2O2在反应中只作氧化剂 D.1 mol Na2O2与水反应时转移1 mol电子 13.常温下,在水溶液中发生如下反应:①16H++10C-+2XO===2X2++5C2+8H2O ②2A2++B2===2A3++2B-;③2B-+C2===B2+2C-。下列说法错误的是 A.反应C2+2A2+===2A3++2C-可以进行 B.反应③是置换反应 C.氧化性由强到弱的顺序是XO>C2>B2>A3+ D.还原性由强到弱的顺序是C->A2+>B->X2+ 14.在2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O反应中,下列说法正确的是 A.氧化产物与还原产物物质的量之比5∶2 B.2mol KMnO4完全反应,转移的电子数为16NA C.该反应中HCl做还原剂,KCl、MnCl2是氧化产物 D.氧化剂与还原剂的物质的量之比5∶1 15.Mg、Al混合物与足量盐酸反应,产生标况下的氢气4.48 L,下列说法不正确的是 A.参加反应的Mg、Al共0.2 mol B.参加反应的HCl为0.4 mol C.Mg、Al在反应中共失去0.4 mol电子 D.若与足量的稀硫酸反应能产生0.2 mol H2 16.关于Na2CO3和NaHCO3性质的说法错误的是 A.热稳定性:NaHCO3<Na2CO3 B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3 C.溶解性NaHCO3<Na2CO3 D.等物质的量Na2CO3、NaHCO3与足量酸反应产生CO2质量相同 17.下列关于Na2CO3和NaHCO3的叙述中错误的是 A.等质量的两种盐分别与足量盐酸反应,在相同情况下,NaHCO3产生的二氧化碳多 B.等物质的量Na2CO3和NaHCO3分别与足量盐酸反应,相同条件下产生二氧化碳体积相等 C.等物质的量的Na2CO3和NaHCO3分别与相同浓度足量盐酸反应,消耗盐酸体积前者是后者的2倍 D.将澄清石灰水加入NaHCO3溶液中不产生沉淀,而加入Na2CO3溶液中则产生沉淀 二、非选择题(本题包括5小题,共49分) 18.(5分)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。 (1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是 (填序号)。 (2)图Ⅲ、Ⅳ所示实验使澄清石灰水变浑浊时的离子方程式为 ; 与实验Ⅲ相比,实验Ⅳ的优点是 (填字母)。 A.Ⅳ比Ⅲ复杂 B.Ⅳ比Ⅲ安全 C.Ⅳ比Ⅲ简便 D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行 (3)Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是______(填化学式)。19.(8分)按如图所示装置进行实验,填写有关现象及化学方程式。 (1) D中的现象是_______ ___,E中收集的气体是___ __ (填名称)。 (2) A中发生反应的化学方程式为_____________________ _______。 (3) C中发生反应的化学方程式为___________ ____ _____、 __________ _ _____。 20.(12分)A、B、C、D、E、F六种物质的焰色反应均为黄色,其中A、B、C、D与盐酸反应均可生成F,此外B还生成一种可燃性气体,而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应可生成C,淡黄色固体E和H也可反应生成C和另一种无色无味气体,该气体能使带火星的木条复燃。请回答下列问题: (1)写出A、B、C、D、E、F的化学式 A B C D E F (2)写出C溶液和H反应的化学方程式 (3)写出下列反应的离子方程式: ① D+A: ② B+水: 21.(14分)(1)按如图所示操作,充分反应后: ①Ⅰ中发生反应的离子方程式为___________________________________; ②Ⅱ中铜丝上观察到的现象是______________________________________ ③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为__________。 (2)将少量Cl2通入FeCl2的溶液中,反应的离子方程式为2Fe2++Cl2===2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱为___________________ (3) NaHCO3溶液与足量澄清石灰水反应的离子方程式 (4)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。 写出反应方程式并标出电子转移方向及数目 若反应方程式中转移了0.3 mol电子,则氧化产物的质量是___ _ 22.(10分)过氧化钠与铝粉混合物共18.3g,加入1L水,充分反应后混合物完全溶解,并收集到5.6L气体(标准状况下)(1)计算生成的气体的总质量;(2)计算反应后溶液中各溶质的物质的量浓度(该溶液体积不变)。 宜昌市葛洲坝中学2018—2019学年第一学期 高一年级12月月考试题答案 1—5:CDADA 6—10:BDBCC 11—15:CDDAA 16—17:BD 18、(1)Ⅱ (2)CO2+Ca2++2OH-==CaCO3+H2O D (3)NaHCO3 19、(1)澄清石灰水变浑浊 氧气 (2)2NaHCO3=△=Na2CO3+H2O+CO2↑ (3)2Na2O2+2H2O==4NaOH+O2↑ 2Na2O2+2CO2==2Na2CO3+O2 20、(1)NaOH、Na、Na2CO3、NaHCO3、Na2O2、NaCl (2) Na2CO3+H2O+CO2==2NaHCO3 (3) HCO3-+OH-==H2O+CO32- 2Na+2H2O==2Na++2OH-+H2↑ 21、(1)Fe+Cu2+==Fe2++Cu 变成银白色 Ag+>Cu2+>Fe2+ (2)Fe2+>Cl- (3)HCO3-+OH-+Ca2+== H2O+CaCO3↓ (4)3H2S+2HNO3 ==3S+2NO↑+4H2O 4.8g 22、(1)3.5g (2)0.3 mol/L 0.1 mol/L查看更多