- 2021-08-06 发布 |
- 37.5 KB |
- 11页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019-2020学年安徽省黄山市屯溪第一中学高二上学期期中考试化学试题 word版
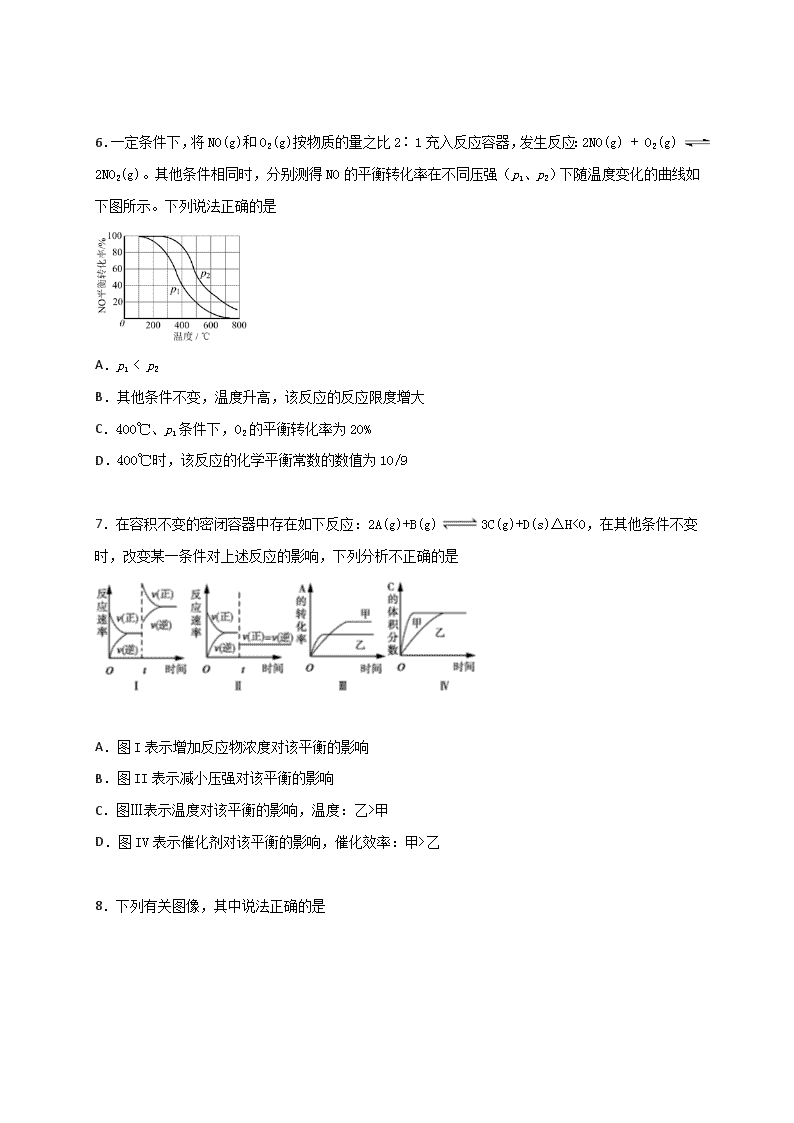
屯溪一中2019-2020学年上学期期中考试试卷 高二化学 (考试时间:90分钟 试卷满分:100分) 注意事项: 1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。 2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。 3.回答第Ⅱ卷时,用0.5mm的黑色中性笔将答案写在答题卡上。写在本试卷上无效。 第Ⅰ卷(选择题 共48分) 一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题目要求的。 1.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生,下列属于未来新能源标准的是 ①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能 A. ⑤⑥⑦ B. ⑤⑥⑦⑧ C. ③⑤⑥⑦⑧ D. ③④⑤⑥⑦⑧ 2.下列关于纯净物、混合物、电解质、非电解质的正确组合为 纯净物 混合物 电解质 非电解质 A 磷酸 冰水混合物 硫酸 干冰 B 蒸馏水 蔗糖溶液 氧化铝 二氧化硫 C 胆矾 氨水 盐酸 铜 D 胆矾 食盐水 氯化铜 石墨 A. A B. B C. C D. D 3.已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1 2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1 根据以上热化学方程式判断,下列说法正确的是 A.1molCO 完全燃烧,放出热量为283 J B.Na2O2(s)+CO2(s)=Na2CO3(s)+ O2(g) △H=-226 kJ·mol-l C.CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024 D.CO 的燃烧热为566 kJ·mol-1 4.可逆反应mA(s)+n D(g)pX(g)+qY(g)在反应过程中,其他条件不变,D的转化率和温度T或压强p关系如图所示(D﹪为D的转化率),下列叙述中正确的是 A.正反应为放热反应 B.使用催化剂,D的物质的量减小 C.化学方程式系数m+n=p+q D.增加物质A或D的用量,平衡均向右移动 5.目前工业上处理有机废水的一种方法是:在调节好pH和Mn2+浓度的废水中加入H2O2,使有机物氧化降解。现设计如下对比实验(实验条件见下左表),实验测得有机物R浓度随时间变化的关系如下图所示。下列说法正确的是 A.313K时,在0~100s内有机物R降解的平均速率为:0.014 mol·L-1·s-1 B.对比①②实验,可以得出温度越高越有利于有机物R的降解 C.对比①②实验,可以发现在两次实验中有机物R的降解百分率不同 D.通过以上三组实验,若想使反应停止,可以向反应体系中加入一定量的NaOH溶液 6.一定条件下,将NO(g)和O2(g)按物质的量之比2∶1充入反应容器,发生反应:2NO(g) + O2(g) 2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如下图所示。下列说法正确的是 A.p1 < p2 B.其他条件不变,温度升高,该反应的反应限度增大 C.400℃、p1条件下,O2的平衡转化率为20% D.400℃时,该反应的化学平衡常数的数值为10/9 7.在容积不变的密闭容器中存在如下反应:2A(g)+B(g)3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是 A.图I表示增加反应物浓度对该平衡的影响 B.图II表示减小压强对该平衡的影响 C.图Ⅲ表示温度对该平衡的影响,温度:乙>甲 D.图IV表示催化剂对该平衡的影响,催化效率:甲>乙 8.下列有关图像,其中说法正确的是 A.由图Ⅰ知,反应在 T1、T3 处达到平衡 B.由图Ⅰ知,该反应的△H<0 C.由图Ⅱ知,t3时采取降低反应温度的措施 D.由图Ⅱ知,反应在 t6时,NH3 体积分数最大 9.一定条件下,在密闭容器中充入CO2与H2进行反应:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):下列叙述正确的是 A.该可逆反应的ΔH>0 B.催化剂甲作用下反应的活化能比催化剂乙作用下反应的活化能大 C.500K下达到平衡时,反应在催化剂甲作用下的转化率比在催化剂乙作用下的转化率高 D.d、e两点反应已经达到平衡 10.稀氨水中存在着下列平衡:NH3·H2ONH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( ) ①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥少量MgSO4固体 A.①②③⑤ B.③ C.③④⑥ D.③⑤ 11.数据:7.2×10﹣4、4.6×10﹣4、4.9×10﹣10分别是三种酸的电离平衡常数,若已知这些酸可发生如下反应:①NaCN+HNO2===HCN+NaNO2,②NaCN+HF====HCN+NaF,③NaNO2+HF===HNO2+NaF。由此可判断下列叙述中,不正确的是( ) A.HF的电离平衡常数为7.2×10﹣4 B.HNO2的电离平衡常数为4.9×10﹣10 C.根据①③两个反应即可知三种酸的相对强弱 D.HNO2的电离平衡常数比HCN大,比HF小 12.把1 L 0.1 mol·L-1醋酸溶液用蒸馏水稀释至10 L,下列叙述正确的是( ) A.c(CH3COOH)变为原来的 B.c(H+)变为原来的 C.的比值增大 D.溶液的导电性增强 13.下列关于热化学反应的描述中正确的是( ) A.HCl和NaOH反应的中和热△H=-57.3 kJ·mol-1,则1 mol硫酸与足量氢氧化钡溶液反应放热为114.6 kJ B.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(1)=2H2(g)+O2(g)反应的△H=+571.6kJ·mol-1 C.反应物的热效应与是否使用催化剂有关 D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g) + 3H2(g) ⇌ 2NH3(g) △H= -38.6 kJ·mol-1 14.钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是 A.盐酸的浓度越大,腐蚀速率越快 B.钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小 C.碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比 D.对比盐酸和硫酸两条曲线,可知Cl—也会影响碳素钢的腐蚀速率 15.下列事实不能用勒夏特列原理解释的是 A.开启啤酒瓶后,瓶中马上泛起大量泡沫 B.合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 C.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 D.对于2HI(g)H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 16.温度为T时,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO2(g)+O2(g)2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是 容器 编号 容器类型 起始物质的量 / mol 平衡时SO3的物质的量 / mol SO2 O2 SO3 I 恒温恒容 2 1 0 1.8 II 恒温恒压 2 1 0 a III 绝热恒容 0 0 2 b A.容器I中SO2的转化率小于容器II中SO2的转化率 B.容器II的平衡常数大于容器III中的平衡常数 C.平衡时SO3的物质的量:a>1.8、b>1.8 D.若起始时向容器I中充入0.10 mol SO2(g)、0.20mol O2(g)和2.0 mol SO3(g), 则此时v正<v逆 第II卷(非选择题) 二、非选择题:包括第题17-20题四个大题,共52分。 17.(14分)节能减排措施是我国“十一五”期间提出的政策措施。 (1)煤的燃烧,会产生大量有害气体。将煤转化为水煤气,可有效降低排放。 C(s)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1 H2(g)+ O2(g)=H2O(g) △H=-242.0kJ·mol-1 CO(g)+O2(g)=CO2(g) △H=-283.0kJ·mol-1 根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式___________。 (2)汽车尾气的排放是大气污染物的重要来源,其中含有NO气体。根据资料显示用活性炭还原法可以处理氮氧化物,某硏究小组向固定容积的密闭容器中加入一定量的活性炭和NO发生反应C(s)+2NO(g)CO2(g)+N2(g) △H=-574kJ·mol-1,并在温度T时将所测反应数据制成下表: ①0到10min内,NO的平均反应速率v(NO)=___________mol·L-1·min-1。 ②下列数据不再变化可表示该反应达到平衡的是___________。 a.容器内压强 b.混合气体的平均摩尔质量 c.混合气体的密度 ③若容器改为可变容积容器,达平衡后,再充入少量NO气体,再次达到平衡时N2的浓度 (填“增大”,“减小”,或“不变”) (3)在某温度T时能同时发生反应: 2N2O5(g)2N2O4(g)+O2(g) K1 N2O4(g)2NO2(g) K2 若向一体积固定为2L的密闭容器内加入N2O5 2mol,一段时间后,容器内的反应达到平衡,此时n(NO2)=0.4mol,已知K2=0.1,请计算出K1=___________。 (4)在一定温度下,有a、硫酸氢钠b、硫酸c、醋酸三种溶液,若三者c(H+)相同时,物质的量浓度由大到小的顺序是_________________,当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是_________________________。 18.(12分)以甲醇为原料制取高纯H2是重要的研究方向。回答下列问题: (1)甲醇水蒸气重整制氢主要发生以下两个反应。 主反应:CH3OH(g)+H2O(g)CO2(g)+3H2(g) △H=+49kJ·mol-1 副反应:H2(g)+CO2(g) CO(g)+H2O(g) △H=+41kJ·mol-1 ①甲醇在催化剂作用下裂解可得到H2和CO,反应的热化学方程式为__________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是_________________________。 ②适当增大水醇比[n(H2O):n(CH3OH)],有利于甲醇水蒸气重整制氢,理由是 ___________。 ③某温度下,将n(H2O):n(CH3OH)=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为________________(忽略副反应)。 (2)工业上常用CH4与水蒸气在一定条件下来制取H2,其反应原理为:CH4(g)+H2O(g)CO(g)+3H2(g) △H=+203kJ·mol-1,在容积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测 得平衡时H2的体积分数与温度及压强的关系如图所示。 ① 压强为p1时,在N点:v正_______v逆(填“大于”“小于”或“等于”), ② N点对应温度下该反应的平衡常数K=________mol2·L-2。 19.(12分) 某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题: 实验 序号 反应温 度/℃ 参加反应的物质 Na2S2O3 H2SO4 H2O V/mL c/mol·L-1 V/mL c/mol·L-1 V/mL A 20 10 0.1 10 0.1 0 B 20 5 0.1 10 0.1 5 C 20 10 0.1 5 0. 1 5 D 40 10 0.1 10 0.1 0 (1)写出反应的离子方程式______________________________。 (2)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是______(填实验序号)。 (3)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中: ①能说明温度对该反应速率影响的组合是__________(填实验序号); ②A和B、A和C的组合比较,所研究的问题是________________________________; ③B和C组合比较,所研究的问题是________________________________________。 (4)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:______________________________。 20.(14分)部分弱酸的电离平衡常数如表: 弱酸 HCOOH HNO2 H2S H2SO3 H2C2O4 H2CO3 电离平衡常数25℃) K=1.8×10-4 K=5.1×10-4 K1=9.1×10-8 K2=1.1×10-12 K1=1.23×10-2 K2=6.6×10-8 K1=5.4×10-2 K2=5.4×10-5 K1=4.3×10-7 K2=5.6×10-11 (1)上表的6种酸进行比较,酸性最弱的是:__________;HCOO-、S2-、HSO3- 三种离子中,最难结合H+的是______________________。 (2)在浓度均为0.1mol/L的HCOOH和H2C2O4混合溶液中,逐渐滴入0.1mol/L的NaOH溶液,被OH-先后消耗的酸及酸式酸根依次是:_______________________。 (3)已知HNO2具有强氧化性,弱还原性。将HNO2溶液滴加到H2S溶液中,同时有沉淀和无色气体生成,该气体遇空气立即变为红棕色,试写出两酸之间的化学反应方程式:_______________________。 (4)下列离子方程式书写正确的是 A.HNO2+HS- == NO2-+ H2S↑ B.2HCOOH+SO32-== 2HCOO-+H2O+SO2↑ C.H2SO3+2HCOO-== 2HCOOH+SO32- D.H2SO3+SO32-== 2HSO3- E.H 2C2O4+ NO2-=HC2O4-+HNO2 (5)将少量SO2通入Na2C2O4溶液,写出离子方程式____________________________。 (6)已知HX为一元弱酸。HX的电离常数为5.5×10-8。某混合溶液中含有4molNaX、2molNa2CO3和1molNaHCO3。往溶液中通入3molCO2气体,充分反应后,气体全部被吸收,计算NaHCO3的物质的量 屯溪一中2019-2020学年上学期期中考试试卷 高二化学参考答案 一、 选择题48分 1. B 2. B 3. C 4.A 5. D 6.A 7. A 8. B 9. D 10. B 11. B 12. C 13. B 14. C 15. D 16. B 二、综合题52分 17.(14分) (1)C(s)+H2O(g)=CO(g)+H2(g) △H=+131.5kJ·mol-1 (2) ① 0.048 ② bc ③ 不变 (3) 0.16 (4) c>a>b . c>a=b 18. 12分 (1) ① CH3OH(g)⇌CO(g)+2H2(g) △H=+90kJ/mol 升高温度 ② 提高甲醇的转化率,并有利于抑制CO的生成 ③ (p2/p1-1)×100% (2) ①大于 ② 48 19.(12分) (1). S2O32-+2H+=S↓+SO2↑+H2O (2). D (3). ①A和D ② 相同温度条件下浓度对该反应速率的影响 ③. 相同温度条件下,该反应速率更大程度上取决于哪种反应物的 (4). SO2易溶于水,测定不精确或实验装置较复杂,不易控制 20.(14分) (1). H2S HSO3- (2). H2C2O4、HCOOH、HC2O4- (3). 2HNO2+H2S=2H2O+2NO↑+S↓ (4). DE (5). SO2+H2O+C2O42-=HC2O4-+HSO3- (6). 6mol 查看更多